P1100309
Próbkę analizowanej mieszaniny substancji wprowadza się za pomocą kranu dawkującego między elektrolit wiodący i terminujący.
Do anody i katody przykłada się napięcie i przez układ zaczyna przepływać prąd dektryc/ny. W wyniku jednokierunkowego pola elektrycznego wszystkie jony zaczną poruszać się do odpowiednich elektrod.
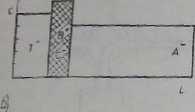
Przebieg opisanego procesu przedstawiono na rys. 36.4. Na pierwszym rysunku widać elektrolit wiodący, próbkę i elektrolit terminujący. Dalsze rysunki (poniżej)
i
|
1 1 |
i |
|
T~ |
li |
|
U |

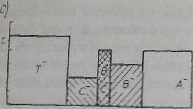
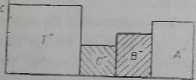
Rys. 36.4. Schemat rozdzielania substancji metodą izofąchoforezy: a) początkowe »U-dium rozdzielania (elektrolit wiodący, próbka i elektrolit terminujący, b. c) stan rozdzielania w określonych przedziałach , czasu, d) równowagowy stan rozdzielania
przedstawiają stan rozdzielania w określonych przedziałach czasu. Czwarty rysunek przedstawia stan równowagi. Każdą strefę w kapilarze tworzy jeden rodzaj jonów, a stężenia substancji w tych strefach są w równowadze ze stężeniem elektrolitu wiodącego. Przy stałej średnicy kapilury i składzie elektrolitu wiodącego długości poszczególnych stref już dalej się nic zmieniają. Po osiągnięciu stanu równowagi i przy stałym prąd/ic elektrycznym wszystkie strefy rozdzielanych substancji poruszają się z jednakową prędkością, z czym wiąże się nazwa metody.
Ponieważ wszystkie strefy poruszają się z jednakową prędkością, a jednocześnie poszczególne rodzaje jonów mają różne efektywne ruchliwości, każda strefa
pia swój własny gradient potencjału, który jej nadaje jednakową prędkość. Gradient potencjału w każdej poszczególnej strefie jest stały, ale wzrasta od jednej strefy do drugiej- Wszystkie strefy są uszeregowane zgodnie ze swoimi efektywnymi ruchlr->voścur«mi. Przyrost gradientu potencjału wiąże się jsutcmatycccie z obniżeniem śtę-i«i:a właściwego rodzaju jonów' w rozpatrywanej strefie. Granice stref między poszczególnymi substancjami rozdzielanymi są w tej technice bardzo ostre.
Jeżeli podczas analizy utrzymuje się stały prąd, poszczególne strefy maja różne temperatury w wyniku różnych gradientów potencjałów. Jeżeli do kapi!n> jest przyłączone odpowiednio skonstruowane termoogniwo. sygnały dostarczane przez to termoogniwo charakteryzują poszczególne strefy. Przez różniczkowanie tych sygnałów albo przez zastosowanie term o ogniwa różniczkującego bardzo łatwo można uzyskać granice poszczególnych stref. Graficzny zapis isouschoforctcgramu wygląda podobnie jak zwykły graficznie przedstawiony chrcn.Hogram, ale jego interpretacja jest zupełnie odmienna. Wysokości fal są tu źródłem informacji o rodzaju jonów (informacja jakościowa), podczas gdy odległość między falami pedaje długości strefy, a więc tym samym informację o ilości określonego jonu w układzie (informacja ilościowa). Detekcja substancji za pomocą tennoogniwa jest więc metodą uniwersalną, ale jej zdolność rozdzielcza jest względnie mała z uwagi na porównanie profilu stężeniowego i temperaturowego na granicy strefy.
Technika izotachoforezy umożliwia wykonanie rozdzielania mieszanin słabych kwasów i zasad oraz jonów metali. Bardzo perspektywiczne jest zastosowanie izo-lachoforezy do analizy mieszanin aminokwasów i protein, czemu obecnie poświęca się wicie uwagi. Można także analizować związki jonowe nierozpuszczalne w wodzie przez zastosowanie odpowiednich rozpuszczalników organicznych. W perspektywie można przewidzieć rozwój odpowiednich detektorów, które umożliwiałyby detekcję stref krótszych niż 0,3 mm, a tym samym analizę mieszanin v icłodcładnfkowycfc-
36.3.5. Kombinacja elektroforezy z chromatografią bibułową 1 z przepływem rozpuszczalnik a
Zasadę elektroforezy można połączyć z zasadą chromatografii bibułowej, przez co bardzo zwiększa się selektywność rozdzielania, lub tez z przepływem rozpuszczalnika, przez co osiąga się ciągłość operacji i podwyższa pojemność prcpar&tywną całego procesu.
Pierwszy sposób jest ważny w analizie złożonych mieszanin (w mikroskali) i jc?t odpowiednikiem dwuwymiarowej chromatografii bibułowej. Drugi sposób jest pre-paratywnym rozwiązaniem elektroforezy. Teoretycznie tym sposobem można rozdzielić dowolne ilości substancji. W praktycznych rozwiązaniach konstrukcyjnych napotkano na duże przeszkody.
36.3.6. Źródła prądu
Głównym elementem przy zestawianiu układu do elektroforezy jest odpowiednie źródło prądu stałego. Do elektroforezy na bibule jest potrzebne źródło napięciu i zmieniające się w zakresie 200-600 V i natężenia roboczego 50-100 roA. Do elektro- ’
Wyszukiwarka