P1050446
KONDUKTOM Emu KLASYCZNA 51
Hiys. 2.7b). Prawa część krzywej jest bardziej nachylona w stosunku do [osi X, co jest spowodowane mniejszą ruchliwością jonów OH niż H+ ■rys. 2.7a).
Krzywa miareczkowania mocnego kwasu mocną zasadą podawana jest na ogół w podręcznikach w postaci dwóch przecinających się [prostych.
Miareczkowanie mocnego kwasu słabą zasadą. Podczas miareczkowania mocnego kwasu słabą zasadą, np. kwasu solnego amoniakiem. liczba jonów wodorowych maleje aż do punktu równoważności (rys. 2.8 — odcinek AB). Następnie, ze względu na bardzo słabą dysocjację amoniaku w obecności chlorku amonu, przewodnictwo po przekroczeniu PK pozostaje prawie stałe (rys. 2.8 — odcinek BC).
i
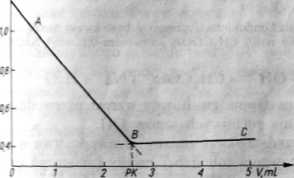
Rys, UL Krzywa miareczkowania konduktometrycznego mocnego kwasu słabą zasadą; roztwór 0.001 mol/l HC1 miareczkowano roztworem 0,1 mol/1 NH,
W bezpośrednim sąsiedztwie PR linie proste ulegają zakrzywieniu wskutek niecałkowitego przebiegu reakcji Produkt końcowy wyznacza się z przecięcia stycznych do tych linii.
• Miareczkowanie słabego kwasu mocną zasadą lub słabej zasady mocnym kwasem. Krzywą miareczkowania kwasu octowego wodorotlenkiem sodu przedstawiono na rys. 2.9. Początkowo nieznaczne zmniejszenie przewodnictwa jest spowodowane wiązaniem niewielkiej ilości jonów wodorowych, pochodzących z dysocjacji kwasu octowego, w cząsteczki wody. Następnie stopniowy wzrost przewodnictwa jest związany z zastępowaniem słabo zdysocjowanego kwąsu octowego przez dobrze zdysocjowany octan sodu
Wyszukiwarka