P1050727
II. POLAROGRAFIA 319
równe. Wtedy ostatni człon równania jest równy zeru i wartość potencjału elektrody jest funkcją stężeń utleniacza i reduktora
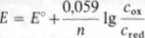
(5.7)
gdzie: c„, crcd — stężenia zarówno w masie roztworu, jak i na powierzchni elektrody. Jeżeli jednak doprowadzi się napięcie i elektroda kroplowa będzie się polaryzować, to na jej powierzchni ustali się stosunek stężeń formy utlenionej i zredukowanej, różny od stosunku stężeń w głębi roztworu. Jeżeli przebiegająca pod wpływem doprowadzonego napięcia reakcja jest odwracalna, tzn. przebiega z małym nadnapięciem lub bez niego, to potencjał elektrody można określić równaniem Nernsta. Potencjał ten będzie zależał od stosunku stężeń formy utlenionej do zredukowanej na powierzchni kroplowej elektrody rtęciowej
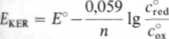
(5.8)
gdzie: c° — stężenie substancji na powierzchni kropli rtęci.
Prąd dyfuzyjny zależy od różnicy stężeń postaci utlenionej » w roztworze i na powierzchni rtęci
(5.9)
fd — Kox(Cox C-ox)
gdzie Jd oznacza prąd dyfuzyjny odpowiadający określonemu potencjałowi niższemu od potencjału, przy którym występuje graniczny prąd dyfuzyjny. Natężenie prądu można rozważać albo jako wielkość chwilową (por. 5.1.3) w danej chwili trwania kropli, albo jako wielkość średnią w przedziale czasu, który odpowiada istnieniu tej kropli. Symbol Jd oznacza średni prąd dyfuzyjny.
Ze wzrostem doprowadzonego napięcia, stężenie postaci utlenionej na powierzchni rtęci maleje i gdy natężenie prądu dj&gyjpego osiągnie wartość graniczną /di/ stężenie postaci utlenionej będzie tak małe w porównaniu ze stężeniem w głębi roztworurże' można je przyrównać do zera
(5.10)
ufi “ fQix&
■
Wyszukiwarka