P1050760
5J. OSCYLOPOLAROGRAFIA 351
Przedstawione zależności są słuszne wówczas, gdy w roztworze nie znajduje się depolaryzator. Jeżeli w roztworze znajduje się substancja ulegająca reakcji elektrodowej, to na wykresie pojawia się stopień zarówno na katodowej, jak i anodowej części krzywej (rys. 5.29). Symetria tych stopni świadczy o odwracalności reakcji zachodzących na elektrodzie (rys. 5.29a) lub o ich nieodwracalności (rys. 5.29b). Gdy reakcja elektrodowa jest reakcją odwracalną, potencjały stopnia katodowego i anodowego pokrywają się, a dla reakcji nieodwracalnych potencjały stopnia katodowego i anodowego są różne. Przykładem układu odwracalnego jest układ T1+/T1, a nieodwracalnego Zn2+/Zn (rys. 5.29).
5J. OSCYLOPOLAROGRAFIA 351
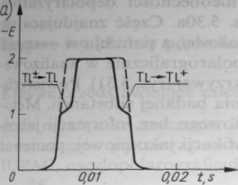
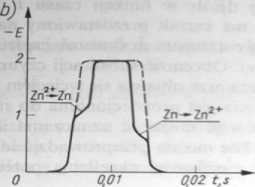
Rys. 5.29. Krzywe E = f(t) w obecności depolaryzatorów: a) dla odwracalnej reakcji elektrodowej talu(I), b) dla nieodwracalnej reakcji elektrodowej cynku(II), Szyszko [2.4]
Pojawienie się stopni na krzywej jest wynikiem powstawania prądu dyfuzyjnego. W obecności depolaryzatora natężenie prądu płynącego w układzie jest sumą [5.11].
/-/dl + /„ (5-35)
gdzie: JDL — prąd pojemnościowy; /d — prąd dyfuzyjny.
Ponieważ w danej fazie prąd przechodzący przez naczynko musi być stały, więc suma prądów pojemnościowego i dyfuzyjnego jest stała. W obecności depolaryzatora wartość natężenia prądu pojemnościowego jest mniejsza, co powoduje spadek wartości potencjału elektrody czynnej w danym czasie i pojawienie się stopni na krzywej. Obecność depolaryzatora powoduje hamowanie ładowania się podwójnej warstwy elektrycznej przy takiej wartości potencjału, przy której ulega on reakcji, ponieważ reakcja elektrodowa umożliwia
Wyszukiwarka