DSC02072
Zadanie 20. Ile poszczególnych rodzajów wiązań (sigma i pi) występuje w cząsteczce.o poniższym wzorze?
COOH
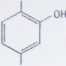
NH.
Zadanie 21. Hybrydyzacja orbitali atomowych to:
a) egzoenergetyczny proces uwspólniania pary elektronowej
b) mieszanie funkcji falowych tworzących wiązanie
@ zabieg czysto matematyczny prowadzący do obliczania rozkładu przestrzennego elektronów w cząsteczkach
d) delokalizacja elektronów na całą cząsteczkę, jak np. w cząsteczce benzenu
Zadanie 22. W której z podanych cząsteczek kąt pomiędzy dwoma wiązaniami kowalencyjnymi jest najmniejszy?
a) BF3
b) BeFj
c) CH4 0)H2O
Zadanie 23. W cząsteczkach CH4, NH3, H20 występuje ten sam typ hybrydyzacji atomu centralnego, a różne są kąty między wiązaniami: CH4109°, NH3107°, H20 105°. Czym spowodowane są te różnice?
Zadanie 24. Wskaż (podkreśl) wzory cząsteczek, w których wszystkie atomy leżą w jednej płaszczyźnie:
c2h2
h2o, co2, nh3,
BF3,
Wyszukiwarka
Podobne podstrony:
DSC02076 ,<? /i Zadanie 9. Określ: a) ile wiązań
DSC02076 ,<? /i Zadanie 9. Określ: a) ile wiązań
Zadanie 20 Ile jest permutacji/zbioru siedmioelementowego, dla których /(4) = 4 ? Zadanie 21 Na ile
Zadanie 20. (2pkt) Na mapie zaznaczono główne obszary występowania wybranych surowców’ energetycznyc
Segregator1 Strona 2 5 pkt Zadanie 20. Dane są trzy orbitale jednej powłoki: Oceń prawdziwość poniżs
Rodzaje wiązań między atomami występującymi w podstawowych grupach materiałów
Rysunek 2.5 Rodzaje wiązań między atomami występującymi w podstawowych grupach materiałów
Rodzaj zadania Polecenia i pomoce Ocena wykonania Wiązanie kokardka Zawiąż misiowi kokardkę na
CCF20090524�011 (2) Zadanie 20. Na podstawie danych z tabeli wskaż, jaki rodzaj urządzeń ochronnych
więcej podobnych podstron