skanuj0008 (2)

) 'Ovb<|^)rvj<s£.
''y.-w*.*!^
D
f*5r-> b
CA- J
Plik PA J 6
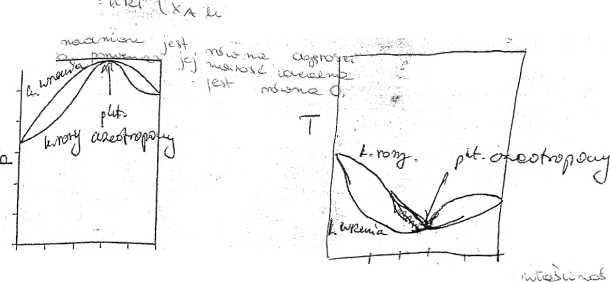
O 0,2 0,4 0,6 0,8 1 Układ ten ■wykazuje ........
b i OJ
0,L 1 Xa Jj
. odchylenia od prawa Raoulta:^SŁst
v
W^7v»vO!.łM fc‘
C CCC -ty->-0 1**£L
_ ppa^.^. VL, {u.***^ .-^CLdu^a
Podaj wzory definicyjng funkeji nadmiarowych mieszania i ich objaśnienia słowne: vr «*&&&*£ %*•$%•«<*•***
1 pkt możliwy do uzyskrnifa (po łA za wzÓr);:ńie ma punktów ujemnych. \*<v*
a) ..cf.^acc^tk.—.....
.............,(||(^......
M rrO^oy^Py........cyxsĄ.ŁCtaxi rlrs-o^.ri^ ^ę>j^n ęfo^j^tc&O^ęj ~ ,~C^/-<. ,s>#
J»gj
ViC_<-v{CL- Cs. .vtAc. ■ (UA-^y5 >OZ_Ko,
29. Jaki jest stosunek stałej równowagi reakcji w temperaturze 100ÓK dó stałej równowagi tej samej reakcji w temperaturze 500K, jeżeli jest to reakcja endotermiczna, a jej molowa entalpia (w tym zakresie temperatur stała) wynosi8314J/mpL •
■ -•
2 pkt możliwe dti użyskania; nie mapuńktówngemnyeh.
Cvv6( *"
?w.
IŹC;.
:foiA££. ■ *W '
ha k - §i^n ' -
l ^ ) -

, W
V2n^
w
Ki-
(r V^A " vOOp)j
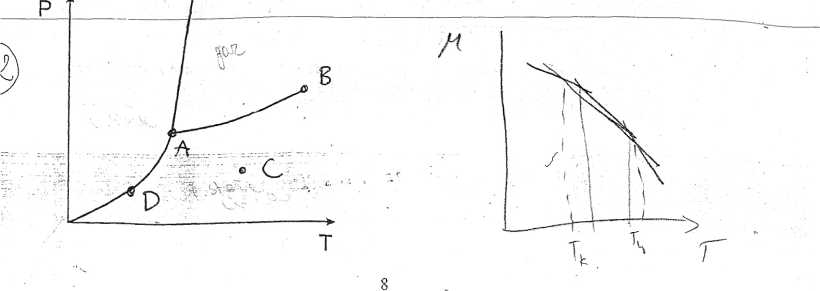
30. Na załączonym diagramie fazowym dla układu jednoskładnikowego zaznacz (wyraźnie* punkt + duża literały. A. punkt potrójny, B. punkt krytyczny, C. dowolny punkt o dWÓbłi stopniach swbbóily W óbszar^ fgy ok^tden sowanych, D. dowolny punkt o jednym stopniu swobody leżący poniżej temperatury punktu potrójnego.
2 pkf możliwe do uzyskania; nie ma punktów ujemnych, *
Wyszukiwarka
Podobne podstrony:
skanuj0015 (197) &L TlllMkro SŁ=L H> ! jUkuę* ’ ILwŁl Ml fcl 1: ~.__Li &
skanuj0017 (205) ^C-ULSCCUinO. lVencz.eLO.skxx c^ru.pa. FD 30- 03.2009 r FfiS ńHOkG WB/KE/TNW/401^ T
skanuj0017 (230) -Z2- 259 Tclbli ca 6.2ZZawlecz ki wg PN- 7S/M- 82001 Dopuszczalne ku tal ty zakończ
skanuj0030 (131) I s/Ło^a ^ Sł^fwCLo ^® fcoav»^ s ftb! Wf^eLu
skanuj0047 (65) CS 2) k. rr •iWdCi Cą^CCiiwrnaną ftf
skanuj0056 (20) 00 D G RAM M ATI CA Leggiamo e scriviamo: completiamo le frasi eon il verbo giusto.
więcej podobnych podstron