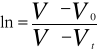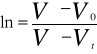CH3COOC2H5 + H2O ![]()
CH3COOH + C2H5OH (1)
Marzena Chmielecka 1
Biotechnologia numer studenta
Wydział Biotechnologii i Nauk o Żywności
Politechniki Łódzkiej
Środa 1215 - 1600
Ćwiczenie nr 21
Hydroliza estru w środowisku kwaśnym
Data wykonania ćwiczenia: 17. 10. 2007 r.
Data oddania sprawozdania: 24. 10. 2007 r.
Wstęp teoretyczny:
Reakcja hydrolizy estru polega na przyłączeniu cząsteczki H2O do atomu węgla C w grupie karboksylowej. W środowisku obojętnym reakcja zachodzi bardzo wolno, natomiast dodanie kwasu, który jest katalizatorem, znacznie przyśpiesza reakcję. Równanie reakcji hydrolizy estru w obecności jonów H+ możemy zapisać w postaci:
CH3COOC2H5 + H2O ![]()
CH3COOH + C2H5OH (1)
Zgodnie ze schematem (1) szybkość reakcji hydrolizy, wyrażona przez zmianę stężenia estru, powinna zależeć od stężeń obu substratów, estru i wody, i można ją opisać równaniem reakcji II rzędu:
![]()
(2)
W roztworach wodnych stężenie wody (cwody ok. 55![]()
) jest bardzo duże, znacznie większe od stężenia estru, i podczas reakcji praktycznie nie ulega zmianie (cwody= const.), dlatego równanie wyrażające szybkość reakcji hydrolizy można zapisać jak dla reakcji I- rzędu:
![]()
(3)
Rozwiązanie równania różniczkowego (3) prowadzi do wzoru, który umożliwia wyznaczenie eksperymentalnej stałej szybkości kexp z zależności logarytmu stężenia substratu ct od czasu rekcji t:
lnct = lnc0 - kexp t (4)
gdzie c0 oznacza początkowe stężenie estru (dla t= t0).
Szybkość reakcji zależy od stężenia jonów H+, cH, na szybkosć reakcji hydrolizy, opisuje równanie (5), w którym k0 jest szybkością reakcji niekatalizowanej (w środowisku obojętnym), natomiast kH stałą szybkości reakcji katalitycznej:
![]()
(5)
Pomiary:
SERIA I |
SERIA II |
||||
CHCl= 0,5 M |
CHCl= 0,2 M |
||||
t (min.) |
Vt (ml) |
ln |
t (min.) |
Vt (ml) |
ln |
0 |
20,2 |
0 |
0 |
11,8 |
0 |
15 |
21,3 |
0,0293 |
15 |
12,2 |
0,0185 |
30 |
21,5 |
0,0623 |
30 |
12,8 |
0,0470 |
45 |
23,6 |
0,0935 |
45 |
13,2 |
0,0664 |
60 |
24,3 |
0,1139 |
60 |
13,8 |
0,0962 |
75 |
25,4 |
0,2095 |
75 |
14,5 |
0,1322 |
90 |
29,6 |
0,2833 |
90 |
14,8 |
0,1481 |
105 |
30,8 |
0,3260 |
105 |
15,5 |
0,1860 |
∞ |
58,3 |
|
∞ |
33,6 |
|
Stałą szybkości reakcji obliczam z równania: ![]()
poprzez badanie nachylenia prostej w układzie współrzędnych ![]()
.
Wykres dla 0,5 M kwasu HCl:
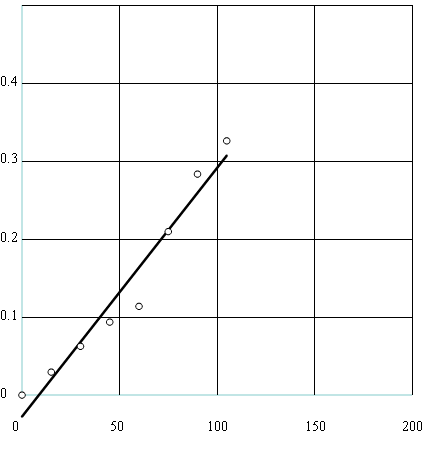
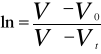
t [s]
Współczynnik kierunkowy prostej: ![]()
, ![]()
współczynnik korelacji: 0,98593
a= -k
Szybkość reakcji: ![]()
![]()
Wykres dla 0,2 M kwasu HCl:

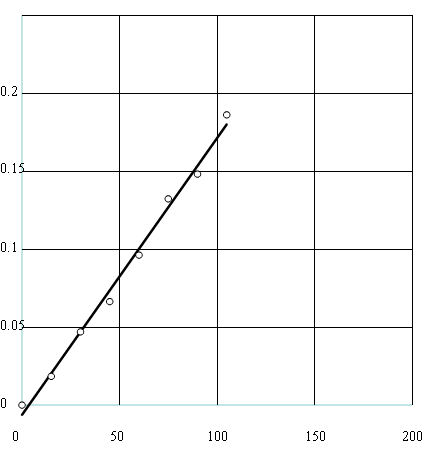
t [s]
Współczynnik kierunkowy prostej: ![]()
, ![]()
współczynnik korelacji: 0,9966
a= -k
Szybkość reakcji: ![]()
![]()
Wnioski:
Stała hydrolizy w przypadku użycia kwasu HCl o stężeniu 0,5 M wynosi ![]()
![]()
, a dla kwasu o stężeniu 0,2 M ![]()
![]()
. Z wyznaczonych stałych widać, że na jej wpływ ma stężenie kwasu, gdyż tam gdzie było większe stężenie stała jest większa. Wyniki obarczone są optycznym błędem odczytu.
6