35031 skan0008 (10)
1. Jednostki i nomenklatura w chemii fizycznej
Zarówno wykład, jak i obliczenia w chemii fizycznej powinny być prowadzone w międzynarodowym układzie jednostek SI. Układ ten oparty jest na siedmiu podstawowych niezależnych jednostkach fizycznych oraz na dwóch uzupełniających jednostkach kątów.
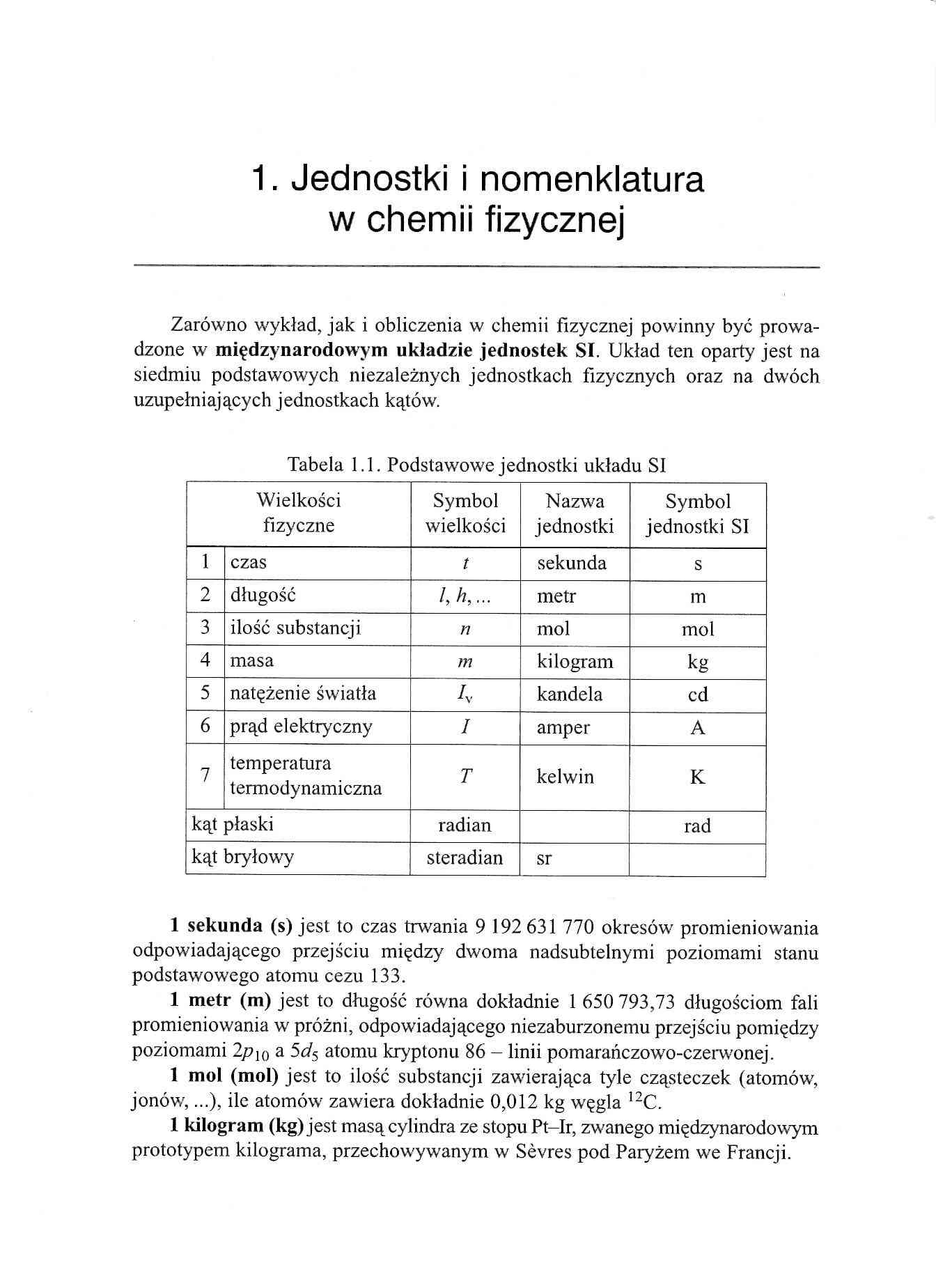
Tabela 1.1. Podstawowe jednostki układu SI
|
Wielkości fizyczne |
Symbol wielkości |
Nazw-a jednostki |
Symbol jednostki SI | |
|
1 |
czas |
t |
sekunda |
s |
|
2 |
długość |
/, h,... |
metr |
m |
|
3 |
ilość substancji |
n |
mol |
mol |
|
4 |
masa |
m |
ki logram |
kg |
|
5 |
natężenie światła |
K |
kandela |
cd |
|
6 |
prąd elektryczny |
i |
amper |
A |
|
7 |
temperatura termodynamiczna |
T |
kelwin |
K |
|
kąt płaski |
radian |
rad | ||
|
kąt bryłowy |
steradian |
sr | ||
1 sekunda (s) jest to czas trwania 9 192 631 770 okresów' promieniowania odpowiadającego przejściu między dwoma nadsubtelnymi poziomami stanu podstawowego atomu cezu 133.
1 metr (m) jest to długość równa dokładnie 1 650 793,73 długościom fali promieniowania w' próżni, odpowiadającego niezaburzonemu przejściu pomiędzy poziomami 2p[0 a 5d5 atomu kryptonu 86 - linii pomarańczowo-czerwonej.
1 mol (mol) jest to ilość substancji zawierająca tyle cząsteczek (atomów', jonów',...), ile atomów' zawiera dokładnie 0,012 kg w'ęgla 12C.
1 kilogram (kg) jest masą cylindra ze stopu Pt-Ir, zwanego międzynarodowym prototypem kilograma, przechowywanym w Sevres pod Paryżem we Francji.
Wyszukiwarka
Podobne podstrony:
13696 skan0010 (10) Jednostki i nomenklatura w chemii fizycznej 13 W wielu dostępnych tabelach, zbio
skan0012 (10) Jednostki i nomenklatura w chemii fizycznej
skan0011 (9) 14 Jednostki i nomenklatura w chemii fizycznej Tabela 1.4. Wartości stałych fizycznych
72195 skan0013 (6) 16 Jednostki i nomenklatura w chemii fizycznej (a) 1 mol czyste
50072 skan0015 (6) 18 Jednostki i nomenklatura w chemii fizycznej Cd. tab. 1.6. Nazwa wielkości
skan0017 (5) 20 Jednostki i nomenklatura w chemii fizycznej Cd. tab. 1.6. Nazwa wielkości
11117 skan0009 (10) 12 Jednostki i nomenklatura w chemii fizycznej 1 kandela (cd) jest natężeniem św
skan0009 (10) 12 Jednostki i nomenklatura w chemii fizycznej 1 kandela (cd) jest natężeniem światła
skan0009 (10) 12 Jednostki i nomenklatura w chemii fizycznej 1 kandela (cd) jest natężeniem światła
11117 skan0009 (10) 12 Jednostki i nomenklatura w chemii fizycznej 1 kandela (cd) jest natężeniem św
więcej podobnych podstron