
Chemiczne źródła prądu
Budowa i działanie ogniw galwanicznych i akumulatorów
Pomiar pojemności różnych baterii
Chemiczne źródła prądu możemy podzielić na:
•
•
•
•
•
•
•
•
•
•
Źródła pierwotne (ogniwa); które dostarczają energii w wyniku reakcji chemicznych zużywających
ich elementy i składniki chemiczne w sposób nieodwracalny
Źródła wtórne (akumulatory); które oddają energie dostarczoną im w czasie ładowania.
Najczęściej spotykanym źródłem pierwotnym są ogniwa kubkowe manganowo – cynkowe, tzw.
suche (ogniwo Leclanchego). Ogniwo takie składa się z kubka cynkowego, będącego jednocześnie jego
obudową i elektrodą ujemną, oraz z elektrody dodatniej w postaci pałeczki węglowej włożonej w wore-
czek z depolaryzatorem (MnO
2
) oraz elektrolitu. Depolaryzator ma za zadanie wiązanie wydzielającego
się w czasie rozładowywania ogniwa wodoru powodującego zmniejszenie SEM ogniwa. Elektrolitem jest
chlorek amonu (NH
4
Cl). Wyżej opisaną budowę mają ogniwa R1 – R20.
Nieco inną budowę mają ogniwa zasadowe manganowo – cynkowe (baterie alkaliczne). Ogniwo
zamknięte jest w obudowie stalowej stanowiącej elektrodę dodatnią. Elektrodą ujemną jest pręcik stalowy
włożony do woreczka z opiłkami cynkowymi. Pozostałą przestrzeń wypełnia depolaryzator z grafitem.
Elektrolitem jest zasada potasowa (KOH). Powyższą budowę mają wszystkie ogniwa oznaczone literą
„L”, np. LR6. Są znacznie wydajniejsze od ogniw suchych.
Z wtórnych źródeł zasilania stosuje się akumulatory kadmowo – niklowe (Ni Cd). Elektrolitem
jest wodorotlenek potasu z dodatkiem wodorotlenku litu. Nasycone są nim obie elektrody i separator.
Elektrody wykonane są ze sprasowanego proszku zamkniętego w woreczkach z niklowej siatki drucianej.
Pojemność tego typu akumulatora będącego odpowiednikiem „paluszka” (R6) nie przekracza 1000 mAh.
AKUMULATORY (Ni – MH) !!!!!!
Oznaczenia
Ogniwa oznaczane są kodem literowo cyfrowym składającym się z jednej lub dwóch liter i liczby jedno-
lub dwucyfrowej. Pierwsza litera oznacza rodzaj ogniwa:
A – ogniwo, w którym depolaryzatorem jest tlen z powietrza, a elektrolitem chlorek amonowy
M – ogniwo rtęciowe, w którym depolaryzatorem jest tlenek rtęci, a elektrolitem KOH
L – ogniwo alkaliczne, w którym depolaryzatorem jest dwutlenek manganu, a elektrolitem KOH.
S – ogniwo srebrowe, w którym elektrolitem jest KOH
C – ogniwo litowe
Brak pierwszej litery oznacza ogniwo, w którym depolaryzatorem jest dwutlenek manganu, a elektrolitem
jest chlorek amonowy.
Druga litera oznacza typ baterii i jej kształt:
R – ogniwo kubkowe, walcowe
F – ogniwo płytowe prostopadłościenne
S – ogniwo prostopadłościenne
Liczby występujące po tych literach oznaczają rozmiary ogniwa.

Ogniwa galwaniczne
Elektroda
Ogniwo
Dodatnia Ujemna
Elektrolit
Depolaryzator
SEM (V)
W (kJ / kg)
Reakcja
chemiczna
Daniella
Zn/ZnSO
4
//CuSO
4
/Cu
Cu
Zn
E: 10 – 20 % roztwór H
2
SO
4
D: roztwór CuSO
4
0,95 – 1,04 V
b.d.
Zn + CuSO
4
→ ZnSO
4
+ Cu
Zn + Cu
2+
→ Zn
2+
+ Cu
Leclanchego
Zn/NH
4
Cl/MnO
2
, C
Pałeczka
węglowa
Cylinder
Zn
E: roztwór salmiaku (NH
4
Cl)
D: MnO
2
(brausztyn)
1,53 V
150 – 420 kJ/kg
Zn + 2MnO
2
+ 2NH
4
Cl →
[Zn(NH
3
)
2
]Cl
2
+ Mn
2
O
3
+ H
2
O
Westona
Hg
Cd
ab
E: Nasycony roztwór KCl,
Hg
2
SO
4
i CdSO
4
D: pasta Hg
2
SO
4
i CdSO
4
1,0181 V
patrz przyp. D
3Cd + 3Hg
2
SO
4
+ 8H
2
O → 6Hg +
3CdSO
4
• 8H
2
O
Clarka
Hg
Zn
ae
E: Nasycony roztwór KCl,
Hg
2
SO
4
i ZnSO
4
D: pasta Hg
2
SO
4
i ZnSO
4
1,4198 V
patrz przyp. D
3Zn + 3Hg
2
SO
4
→ 3ZnSO
4
+ 6Hg
Rubena
Hg + HgO sprasowany
pył Zn
E: roztwór KOH
D: -
1,34 V
450 kJ/kg
HgO + Zn + 2KOH → Hg + K
2
[ZnO
2
] +
H
2
O
Litowo – siarkowe
Li/LiClO
4
/TiS
2
Siarka z
grafitem
Lit
E: sole litu (LiClO
4
) w rozpusz-
czalnikach organicznych.
D: -
2,48 V
2600 kJ/kg
Li
+
+ e
-
→ Li
Wytworzony lit wbudowuje się w sieć
krystaliczną TiS
2
2Li + (1 + x)S → Li
2
S
(1+x)
•
•
•
•
•
A: amalgamat
B: 4% Hg
C: 12,5% Hg
D: stosowane jako wzorzec napięcia, a nie jako źródło zasilania
E: 7% Hg
W – gęstość energii użytecznej
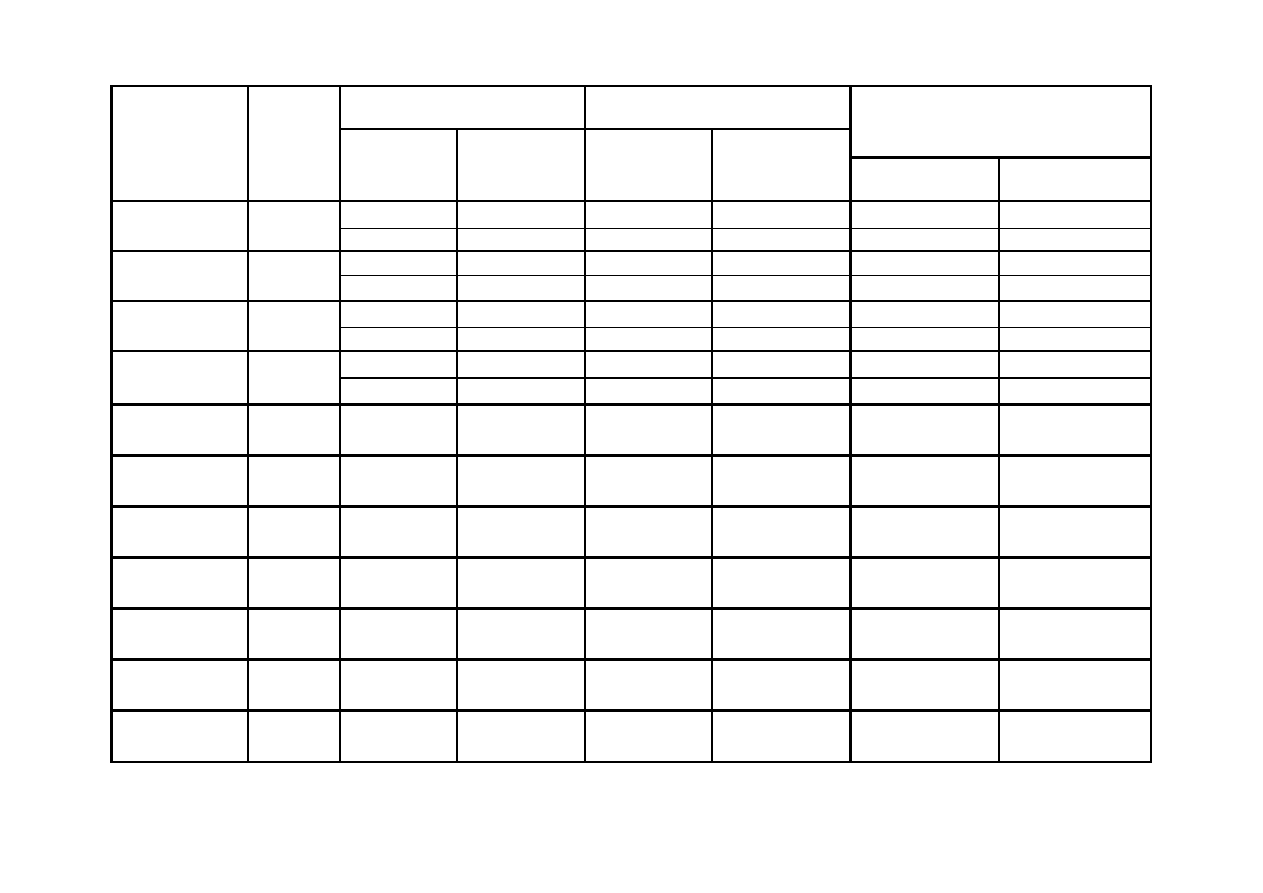
Baterie suche
Parametry przed
rozładowaniem
Czas pracy
Pojemność
(mAh)
Nazwa Cena
(zł)
Napięcie (V) Natężenie (A)
Rozładowanie
do 1 V
Rozładowanie
całkowite
Rozładowanie do
1 V
Rozładowanie
całkowite
1,63
2,89
5h
7h
1000 mAh
1400 mAh
Kodak R6
0,85
1,63
2,8
4,5
7,5h
900 mAh
1500 mAh
1,57
2,41
1,3h
2,3h
265 mAh
460 mAh
Cybercell
Duvacell
1
R6
0,4
1,58
2,35
1h
2,3h
200 mAh
460 mAh
1,65
3,3
3h
4h
600 mAh
800 mAh
Justa R6
0,5
1,66
3,15
3h
4h
600 mAh
800 mAh
1,65
3,05
5,5h
7,5h
1100 mAh
1500 mAh
Panasonic Spe-
cial R6
1
1,65
2,88
5h
7h
1000 mAh
1400 mAh
Wonder Ultra R6
(Energizer)
0,7
1,67
3,27
6,5h
8h
1300 mAh
1600 mAh
LongLife
Philips R6
0,8
1,57
2,83
5h
6,5h
1000 mAh
1300 mAh
Philips Super
R14
1,5
1,59
3,4
• 1 – wszystkie baterie suche (chińskie itp.) wyglądające jak baterie Duracell
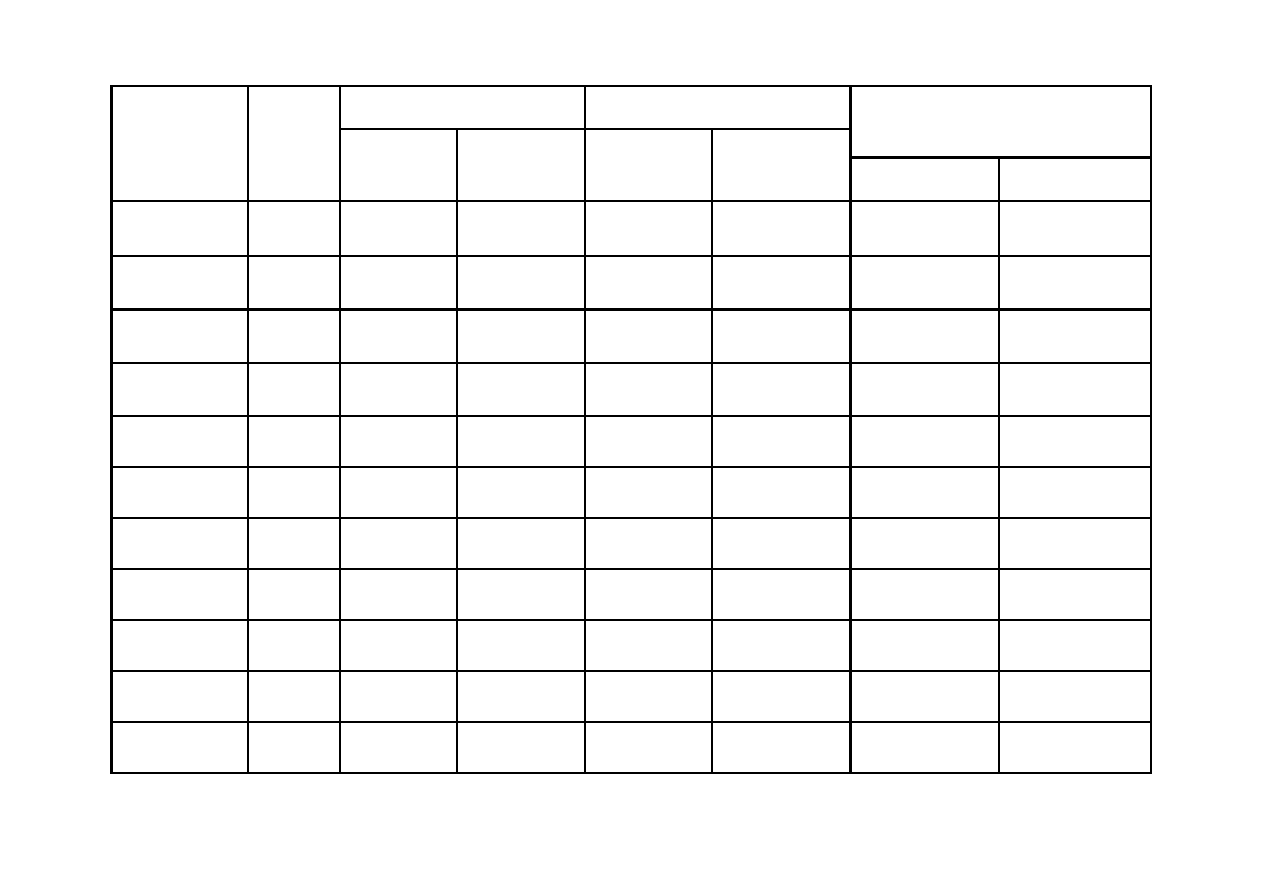
Baterie alkaliczne
Parametry przed
rozładowaniem
Czas pracy
Pojemność
(mAh)
Nazwa Cena
(zł)
Napięcie (V) Natężenie (A)
Rozładowanie
do 1 V
Rozładowanie
całkowite
Rozładowanie do
1 V
Rozładowanie
całkowite
Sony Alkaline
LR6
1,9
1,61
5,45
19h
22,5h
3800 mAh
4500 mAh
Duracell LR6
2,5
1,6
3,3
19h
20h
3800 mAh
4000 mAh
GP Alkaline LR6
1,8
1,55
4,8
19h
21h
3800 mAh
4200 mAh
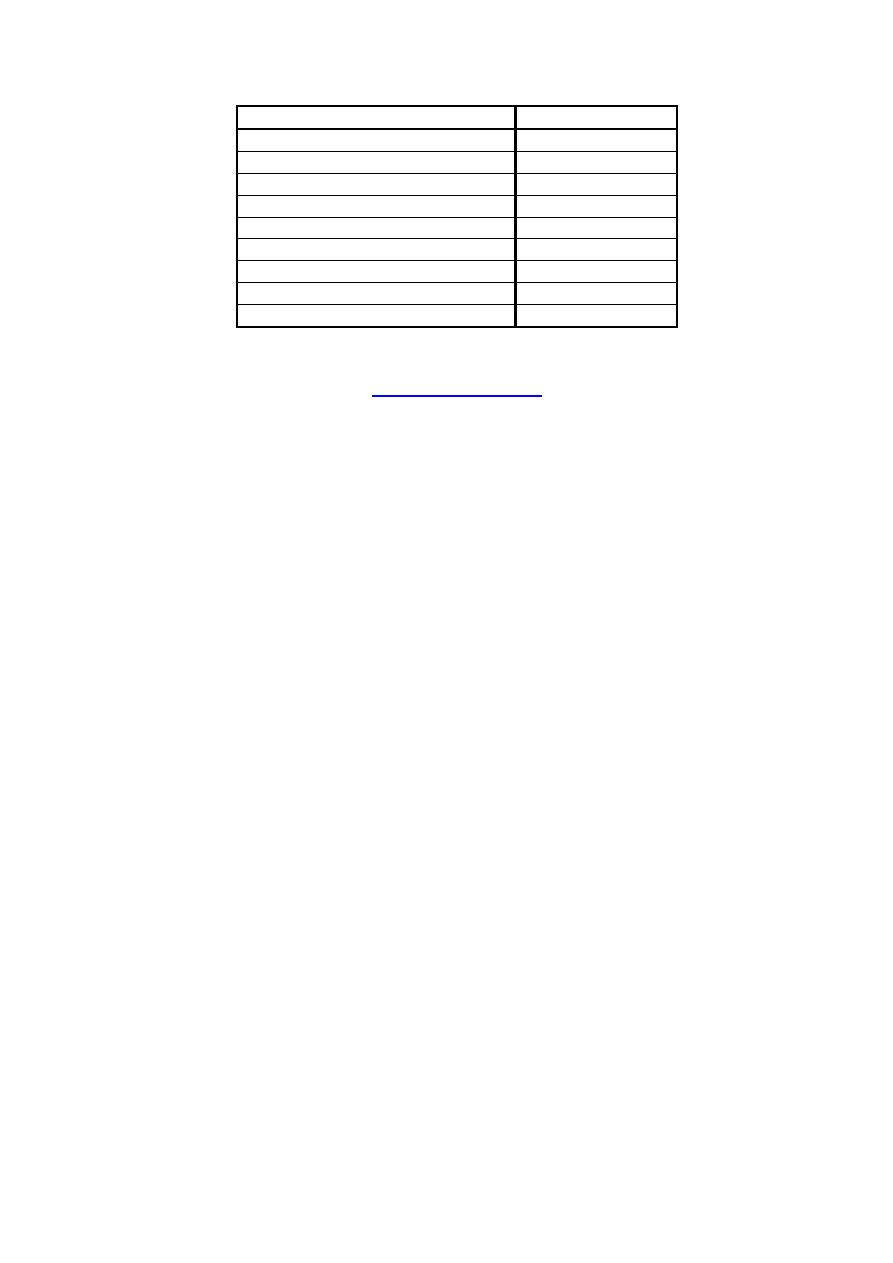
Cena baterii w przeliczeniu na 1000 mAh
Nazwa baterii
Cena 1000 mAh
GP Alkaline LR6
0,47
Sony Alkaline LR6
0,5
Wonder Ultra R6 (Energizer)
0,53
Duracell LR6
0,65
LongLife Philips R6
0,8
Justa R6
0,83
Kodak R6
0,85
Panasonic Special R6
0,95
Cybercell 1,6
Autor: Piotr Maliński
Wyszukiwarka
Podobne podstrony:
chemiczne żródła prądu
Łącznośc 6 Chemiczne źródła prądu elektrycznego, Konspekty, ŁĄCZNOŚĆ (marianoitalianooo)
Chemiczne źródła prądu
chemiczne zrodla pradu
ŹRÓDŁA PRĄDU ELEKTRYCZNEGO
lab zrodla pradu
źródła prądu i napięcia
sprawdzone, FIZ 50, Obwód wyidealizowany. Do biegunów A i B źródła prądu zmiennego przyłączony jest
Źródła prądu
Spawalnicze zrodla pradu - sprawko, Uczelnia, Technologia Spajania
Chemiczne źródła energii elektrycznej Ogniwa galwaniczne
Laboratoryjne źródła prądu
ŹRÓDŁA PRĄDU ELEKTRYCZNEGO
Chemiczne źródła energii elektrycznej
Źródła prądu stałego
więcej podobnych podstron