
Wyk
Wyk
ł
ł
ad 6
ad 6
Podstawy chemii organicznej
Rozmieszczenie elektronów w atomie
Elektrony walencyjne
Wi
ą
zania chemiczne
Teoria strukturalna
Orbitale molekularne
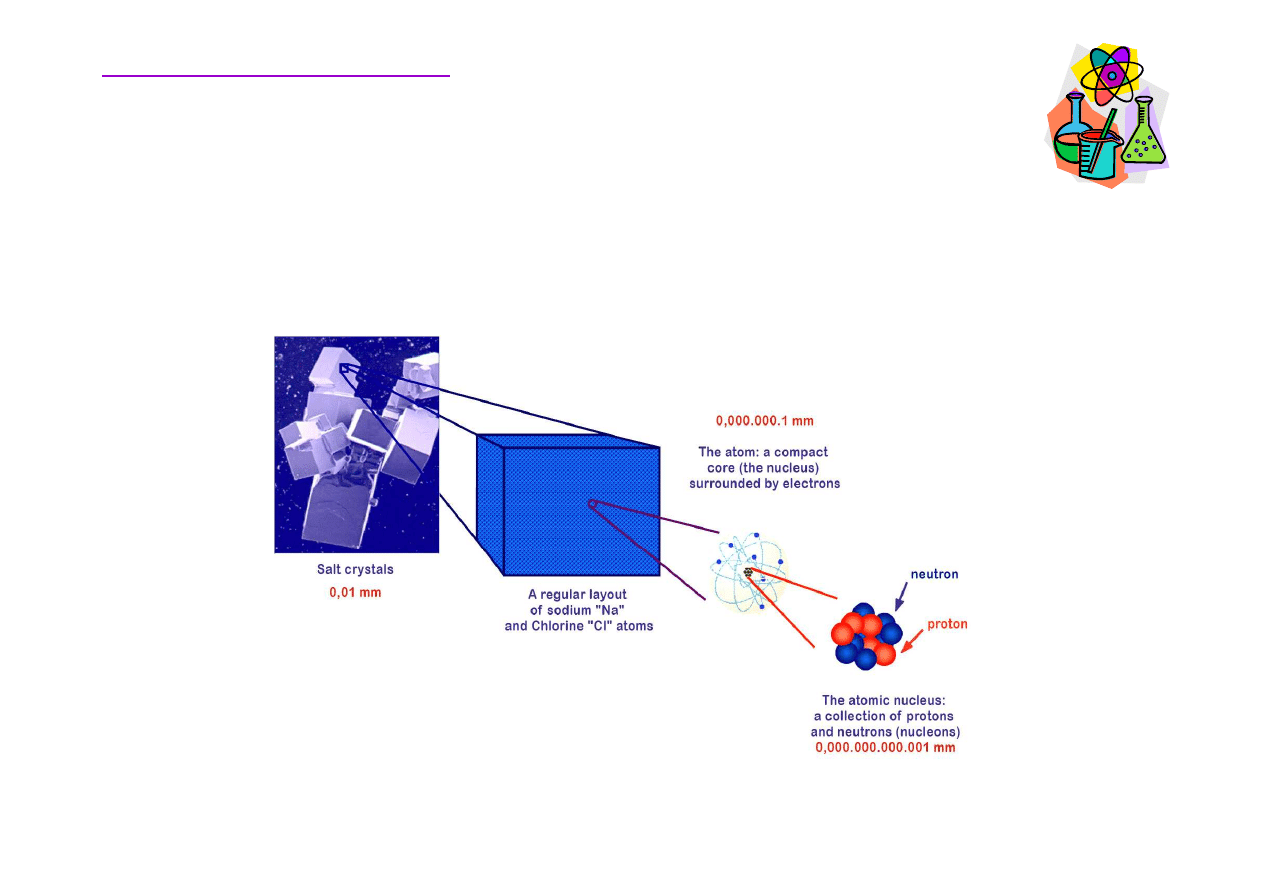
Atom – podstawowy składnik materii
http://www.ganil-spiral2.eu/science-us/understand-ganil/fundamental-principles
Podstawy chemii organicznej
Struktura atomu
John Dalton – twórca współczesnej
teorii atomów (1803)
http://en.wikipedia.org/wiki/John_Dalton
http://chemistry.tutorcircle.com/inorganic-chemistry/dalton-s-atomic-theory.html
Struktura atomu
Podstawy chemii organicznej
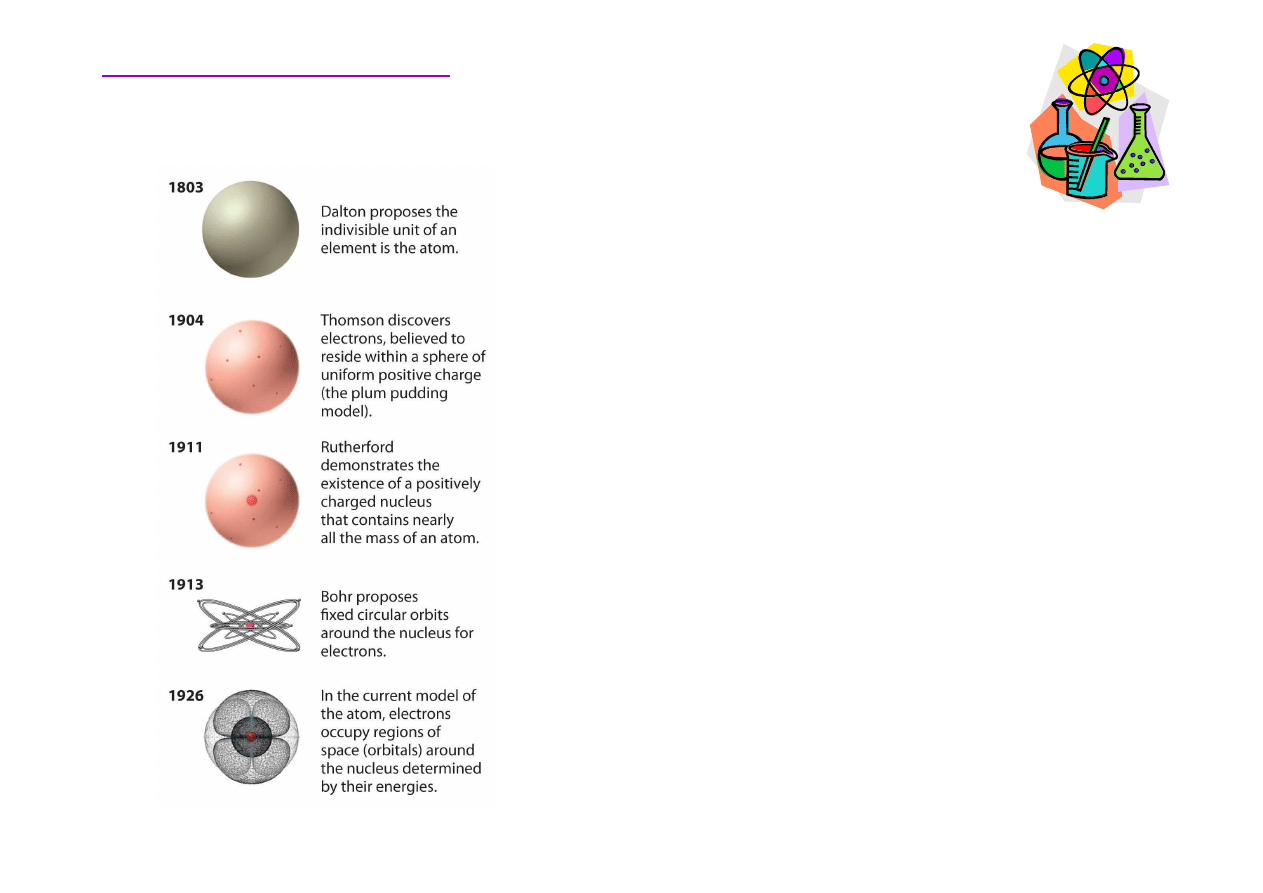
http://2012books.lardbucket.org/books/principles-of-general-chemistry-v1.0/s05-05-the-atom.html
Struktura atomu
Podstawy chemii organicznej
J. Dalton – najmniejsz
ą
, niepodzieln
ą
cz
ęś
ci
ą
pierwiastków chemicznych jest atom
J.J. Thomson – odkrycie elektronów, ujemnie
naładowane elektrony unosz
ą
si
ę
w jednorodnej,
dodatnio naładowanej kuli.
E. Rutheford – nowy model atomu, w którym dodatni
ładunek i wi
ę
kszo
ść
masy atomu s
ą
skupione
w niewielkim j
ą
drze w jego centrum, a ujemnie
naładowane elektrony kr
ążą
wokół j
ą
dra
N. Bohr - hipoteza istnienia zestawu dopuszczalnych
orbit, na których mog
ą
kr
ąż
y
ć
elektrony wokół j
ą
dra
atomowego
Obowi
ą
zuj
ą
cy model atomu, elektrony
s
ą
jednocze
ś
nie cz
ą
stkami i falami.
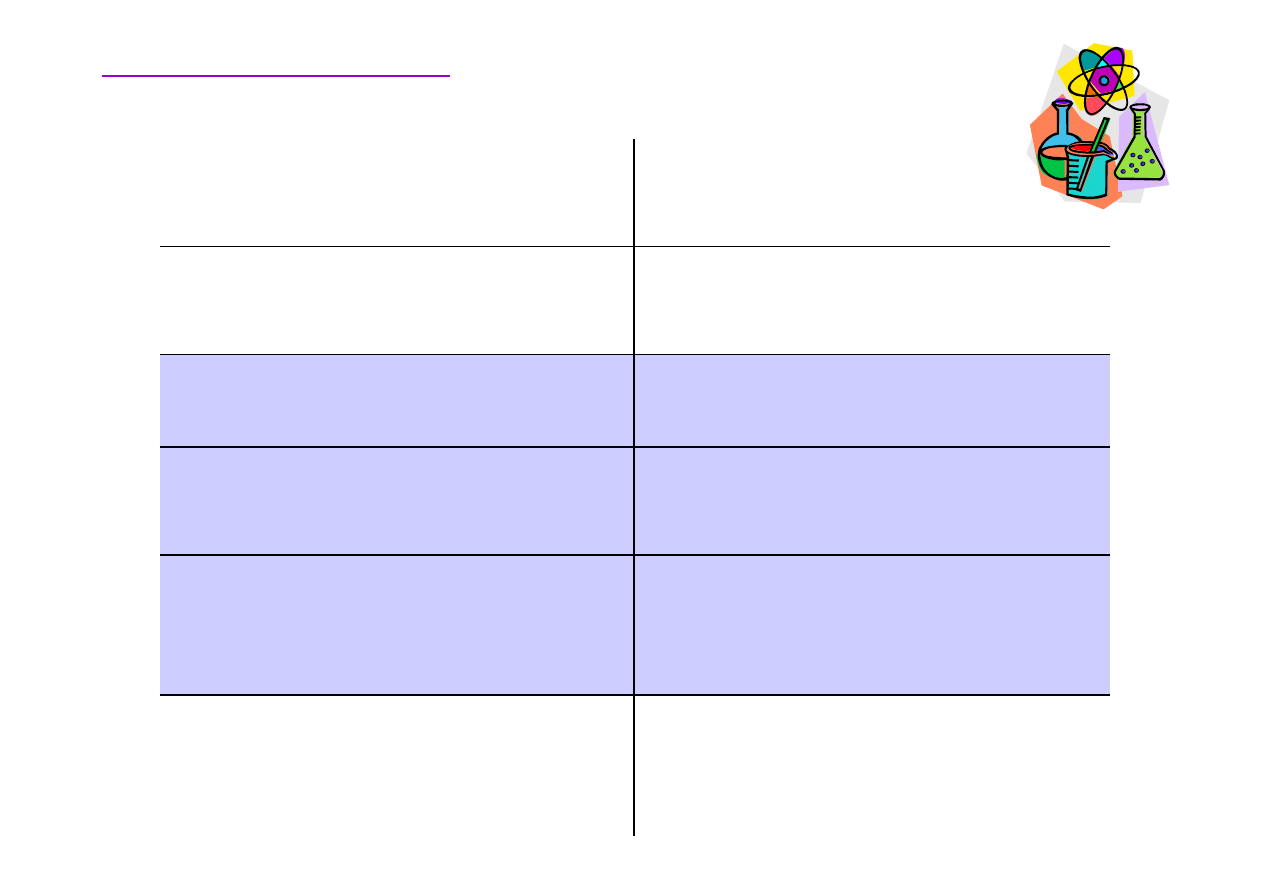
Atomy bior
ą
udział w reakcjach
chemicznych. Budowa zwi
ą
zku
chemicznych (rodzaj i ilo
ść
atomów) jest stała.
Atomy bior
ą
udział w reakcjach
chemicznych. Budowa zwi
ą
zku
chemicznych (rodzaj i ilo
ść
atomów) jest stała.
5
Atomy danego pierwiastka mog
ą
si
ę
ró
ż
ni
ć
masami.
Wszystkie atomy danego pierwiastka
s
ą
identyczne.
4
Atom zawiera mniejsze cz
ą
steczki,
takie jak protony, neutrony i
elektrony.
Atom jest najmniejsz
ą
cz
ą
stk
ą
pierwiastków chemicznych.
3
Atomy s
ą
podzielne i mo
ż
na je
zniszczy
ć
.
Atomy s
ą
niepodzielne i
niezniszczalne.
2
Pierwiastek chemiczny jest
zbudowany z z niezwykle małych
cz
ą
steczek nazywanych atomami
Materia jest zbudowana z niezwykle
małych cz
ą
steczek nazywanych
atomami
1
Współczesna teoria
Teoria Daltona
N
o
Struktura atomu
Podstawy chemii organicznej

Skaningowy mikroskop tunelowy (STM od ang. Scanning
Tunneling Microscope) – rodzaj mikroskopu ze skanuj
ą
c
ą
sond
ą
(ang. Scanning Probe Microscope) – umo
ż
liwia
uzyskanie obrazu powierzchni materiałów przewodz
ą
cych
ze zdolno
ś
ci
ą
rozdzielcz
ą
rz
ę
du pojedynczego atomu.
Obraz atomów niklu – skaningowy mikroskop tunelowy
(scanning tunneling microscope, STM).
http://researcher.watson.ibm.com/researcher/view_group.php?id=4245
Podstawy chemii organicznej
Struktura atomu

•
Ś
rednica atomu wynosi 10
-10
m
•
Ś
rednica j
ą
dra atomu to 10
-14
m, zatem obj
ę
to
ść
j
ą
dra
atomowego jest mniejsza 10 000 razy od obj
ę
to
ś
ci atomu.
http://www.getchemistryhelp.com/chemistry-lesson-structure-of-the-atom/
atom
J
ą
dro
atomowe
Podstawy chemii organicznej
Struktura atomu

• Pierwiastek o najwy
ż
szej g
ę
sto
ś
ci to osm - 22.59 g/cm
3
.
• Gdyby
ś
cisn
ąć
99.9% masy atomu w 1/10 000 obj
ę
to
ś
ci,
g
ę
sto
ść
j
ą
dra atomowego wynosiłaby około 100 000 000
000 000 g/cm
3
!
• Kostka o wymiarach 1 cm x 1 cm x 1 cm zbudowana z j
ą
der
atomowych miałaby mas
ę
tryliona gramów!
• Gdyby pudełko od zapałek wypełni
ć
j
ą
drami atomowymi,
wa
ż
yłoby ponad 2.5 biliona ton!
http://www.getchemistryhelp.com/chemistry-lesson-structure-of-the-atom/
Podstawy chemii organicznej
Struktura atomu
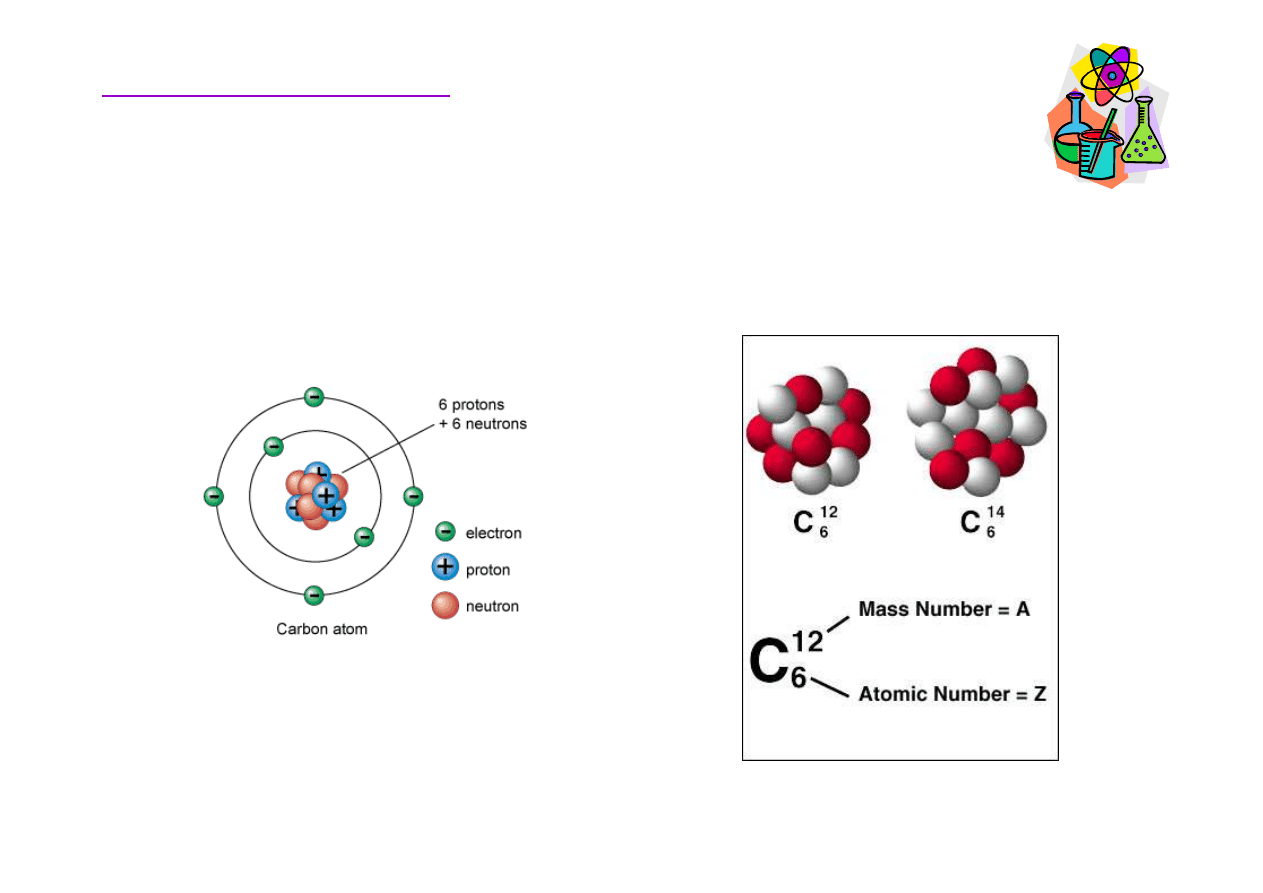
Struktura atomu
Podstawy chemii organicznej
Liczba atomowa (Z) = ilo
ść
protonów (i jednocze
ś
nie elektronów) w atomie
Liczba masowa (A) = ilo
ść
protonów + ilo
ść
neutronów w j
ą
drze
http://www.universetoday.com/56747/atom-structure/
http://www.atomicarchive.com/Physics/Physics3.shtml
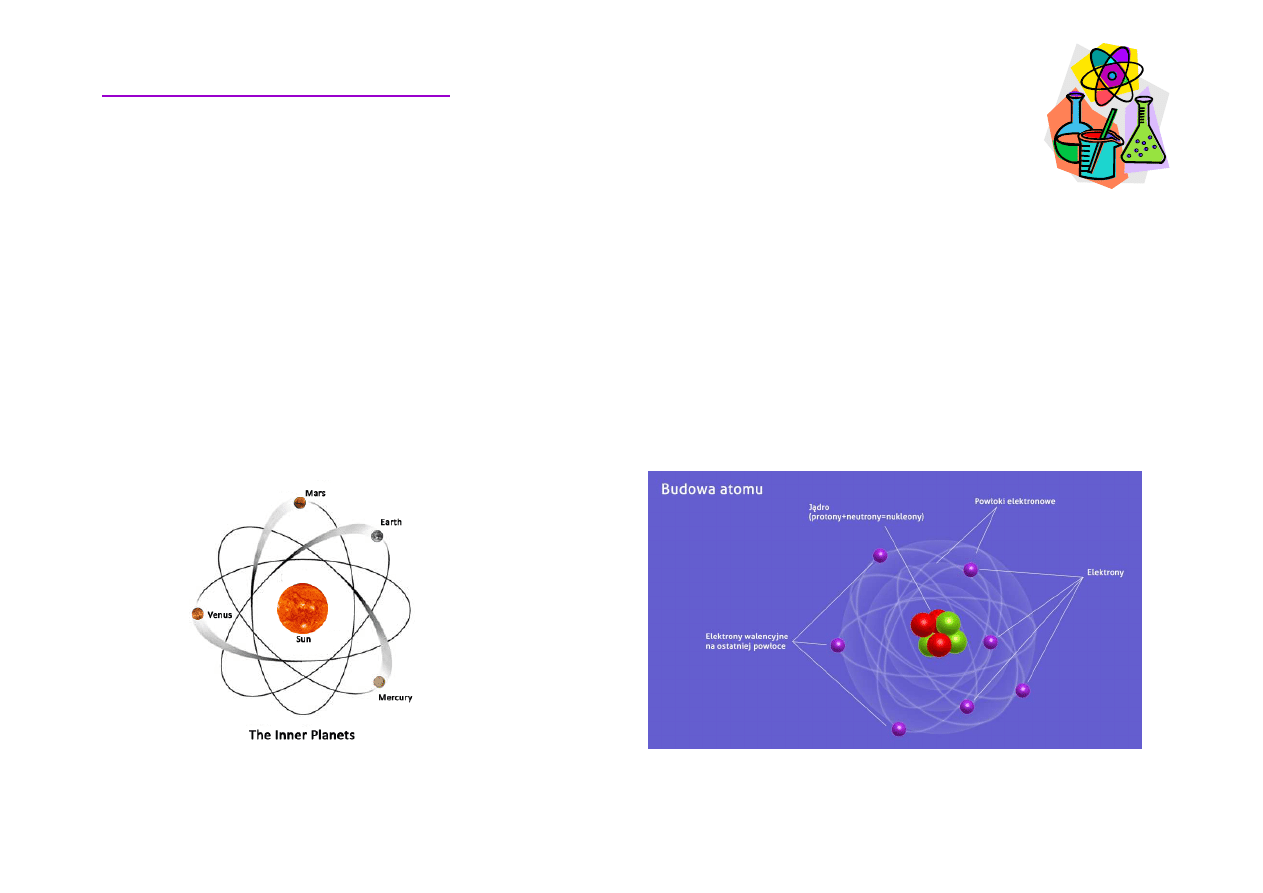
Struktura atomu
http://edudu.pl/sciaga-budowa-atomu,521b28495f2886ca0977
Podstawy chemii organicznej
Elektrony wykazuj
ą
jednocze
ś
nie wła
ś
ciwo
ś
ci cz
ą
stek i
wła
ś
ciwo
ś
ci falowe. Dlatego mo
ż
emy tylko okre
ś
li
ć
prawdopodobie
ń
stwo znajdowania si
ę
elektronu w
konkretnym miejscu.
http://teedee.myweb.uga.edu/imd/ssatom.html
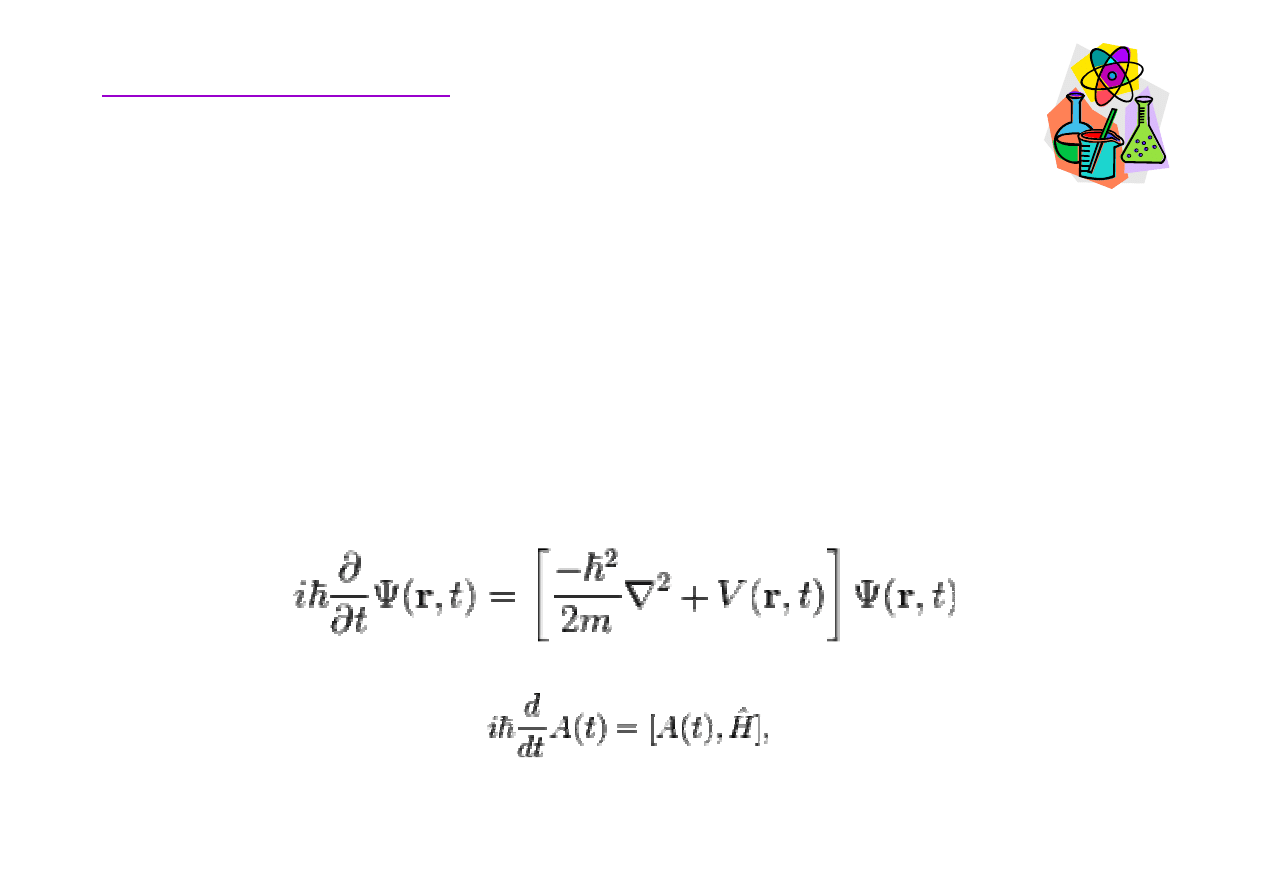
Struktura atomu
Mechanika falowa Schrödingera i mechanika kwantowa
Heisenberga stworzyły podstawy nowoczesnego
rozumienia struktury atomu.
Podstawy chemii organicznej
http://en.wikipedia.org/wiki/Schr%C3%B6dinger_equation

Struktura atomu
Najlepszym opisem poło
ż
enia elektronów w atomie jest
chmura prawdopodobnych poło
ż
e
ń
– orbital.
Podstawy chemii organicznej
http://www.goldenrosycross.org.mt/wp-content/uploads/2011/11/electron_cloud_by_theemerald.jpg

Rozmieszczenie elektronów w atomie
Ka
ż
dy orbital atomowy jest okre
ś
lony przez trzy liczby
kwantowe:
•
główn
ą
liczb
ę
kwantow
ą
(n)
•
orbitaln
ą
(poboczn
ą
) liczb
ę
kwantow
ą
(l)
•
magnetyczn
ą
liczb
ę
kwantow
ą
(m)
Do jednoznacznego zidentyfikowania orbitalu niezb
ę
dne jest
podanie warto
ś
ci wszystkich trzech liczb kwantowych (
n
,
l
,
m
).
Podstawy chemii organicznej

Rozmieszczenie elektronów w atomie
Główna liczba kwantowa (n) okre
ś
la energi
ę
elektronu i
jego odległo
ść
od j
ą
dra. Wszystkie orbitale o danej
warto
ś
ci n nale
żą
do tej samej powłoki atomu.
n=1 (K), n=2 (L), n=3 (M), n=4 (N)
Podstawy chemii organicznej
http://pradeep-vcp.blogspot.com/2011_05_01_archive.html

Rozmieszczenie elektronów w atomie
Ka
ż
da powłoka mo
ż
e przyj
ąć
okre
ś
lon
ą
liczb
ę
elektronów
→
2n
2
.
n
1
2
3
4
...
powłoka
K(2e)
L (8e) M (18e)
N(32e)
...
Podstawy chemii organicznej
http://chemistry.tutorcircle.com/inorganic-chemistry/electron-shells.html
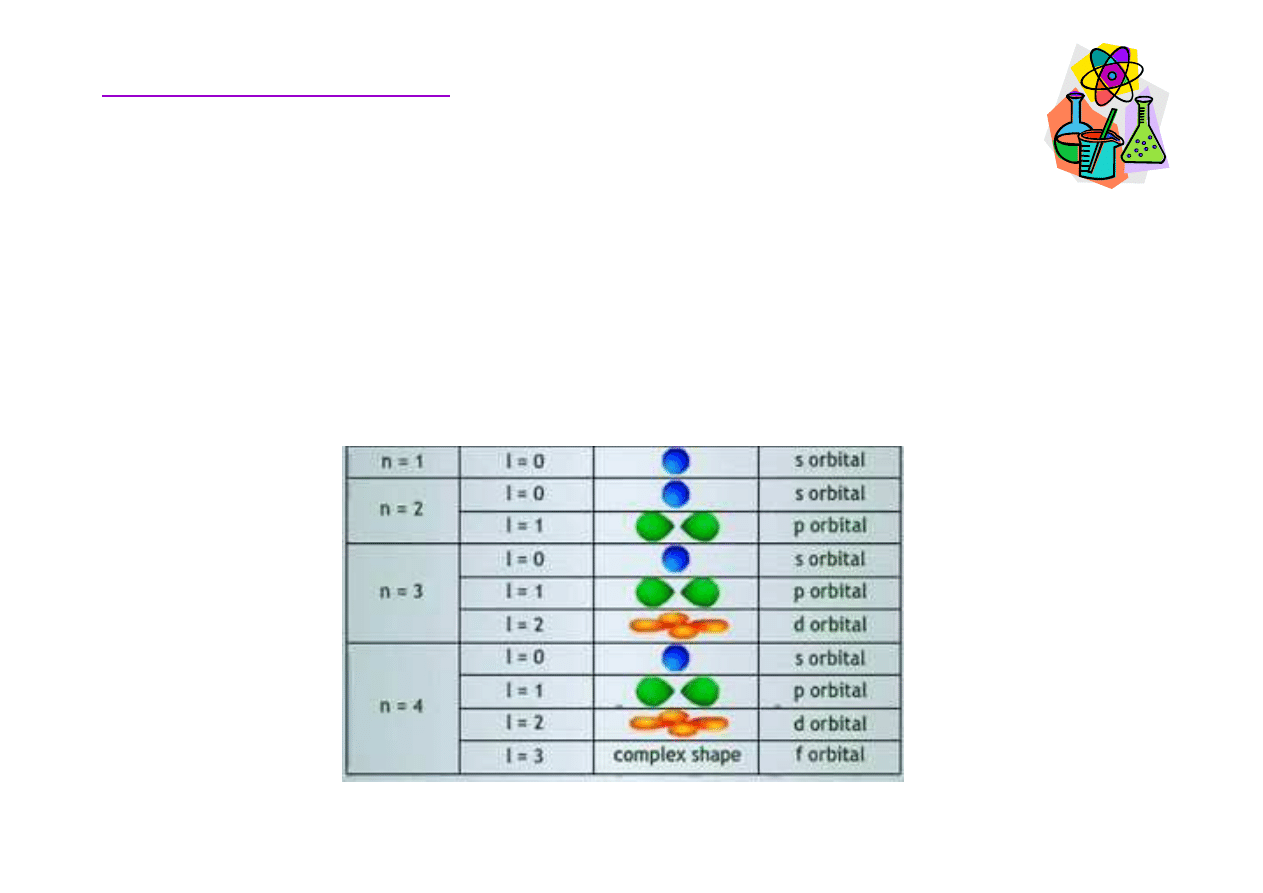
Rozmieszczenie elektronów w atomie
Orbitalna (poboczna) liczba kwantowa (l) okre
ś
la kształt
orbitalu, dla ka
ż
dej liczby n jej warto
ść
wynosi od 0 do n-1.
Podstawy chemii organicznej
http://pradeep-vcp.blogspot.com/2011_05_01_archive.html
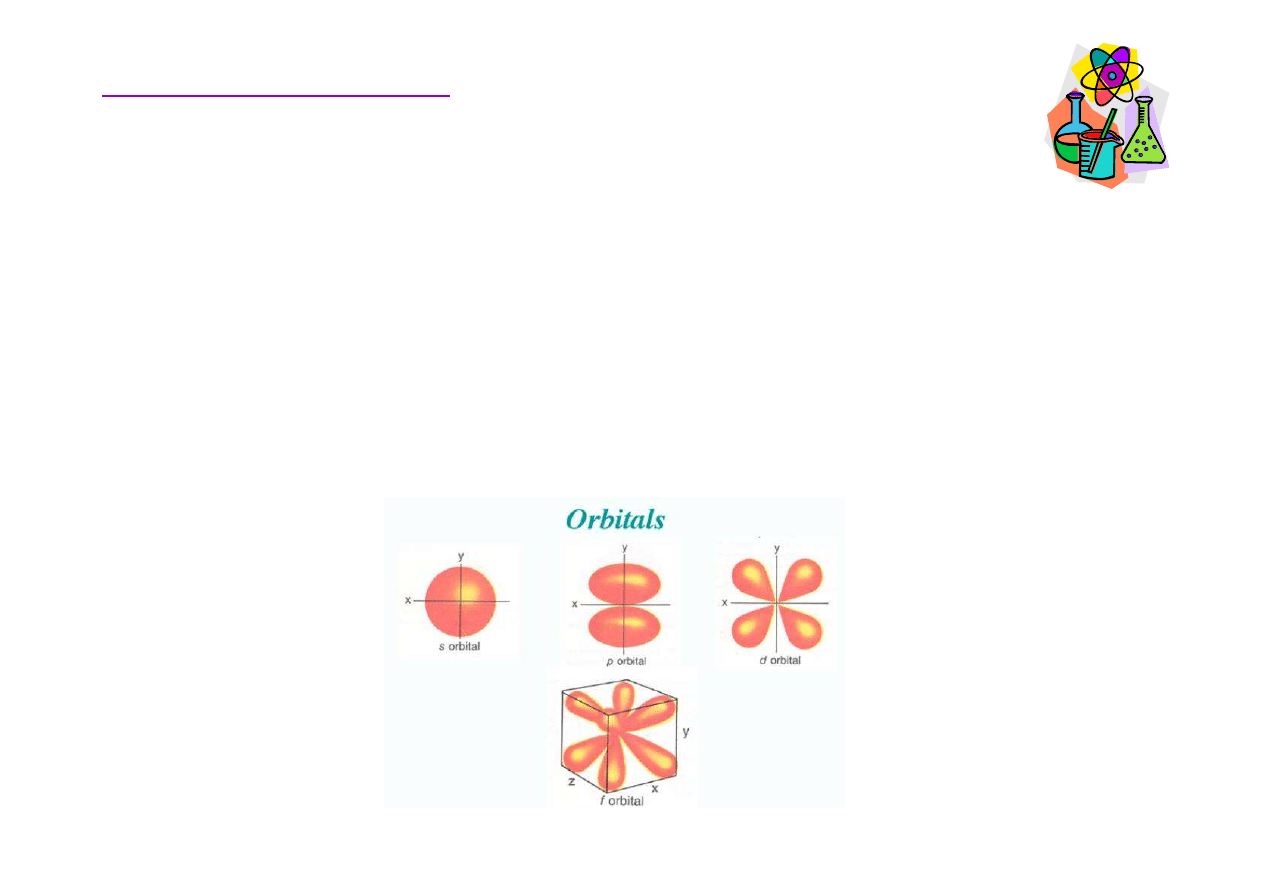
Rozmieszczenie elektronów w atomie
warto
ść
l
0
1 2 3 4 .....
okre
ś
lenie literowe s
p d f
g .....
Ka
ż
dy typ orbitalu (s, p, d, f) posiada swój własny
kształt.
Podstawy chemii organicznej
http://plim14.wordpress.com/2012/07/10/orbitals/

Rozmieszczenie elektronów w atomie
Zbiór stanów kwantowych (czyli elektronów) o tej samej
warto
ś
ci głównej i pobocznej to podpowłoka elektronowa.
Ka
ż
da powłoka zawiera 1 (n=1) lub wi
ę
cej (n>1) podpowłok.
Wszystkie orbitale o tej samej liczbie l w danej powłoce nale
żą
do tej samej podpowłoki i maj
ą
tak
ą
sam
ą
energi
ę
.
n=1
→
1s
n=2
→
2s 2p
n=3
→
3s 3p 3d
n=4
→
4s 4p 4d 4f
Podstawy chemii organicznej
Rozmieszczenie elektronów w atomie
Magnetyczna liczba kwantowa (m) okre
ś
la orientacj
ę
przestrzenn
ą
orbitalu. Przyjmuje warto
ś
ci od –l do +l.
Podstawy chemii organicznej
http://pl.wikibooks.org/wiki/Chemia/Liczby_kwantowe
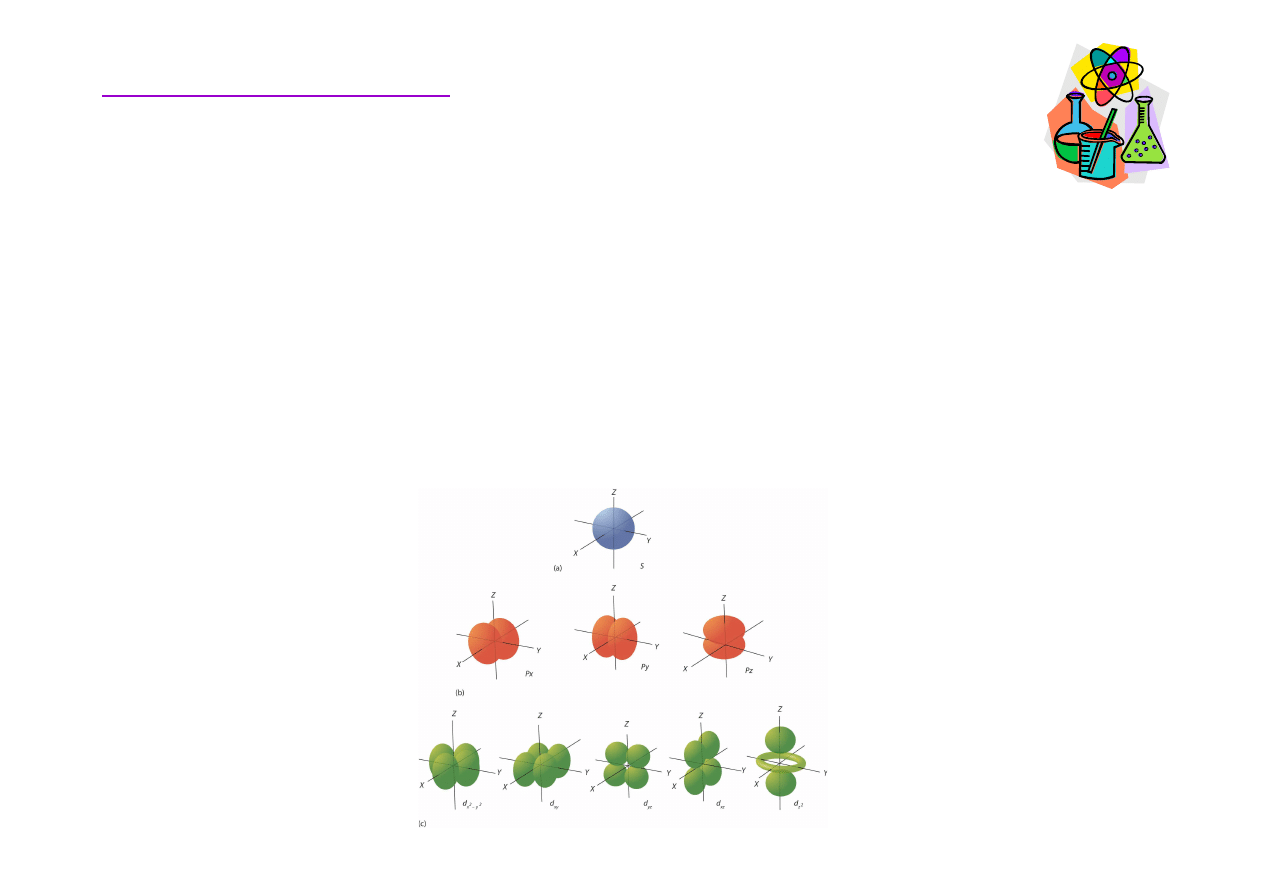
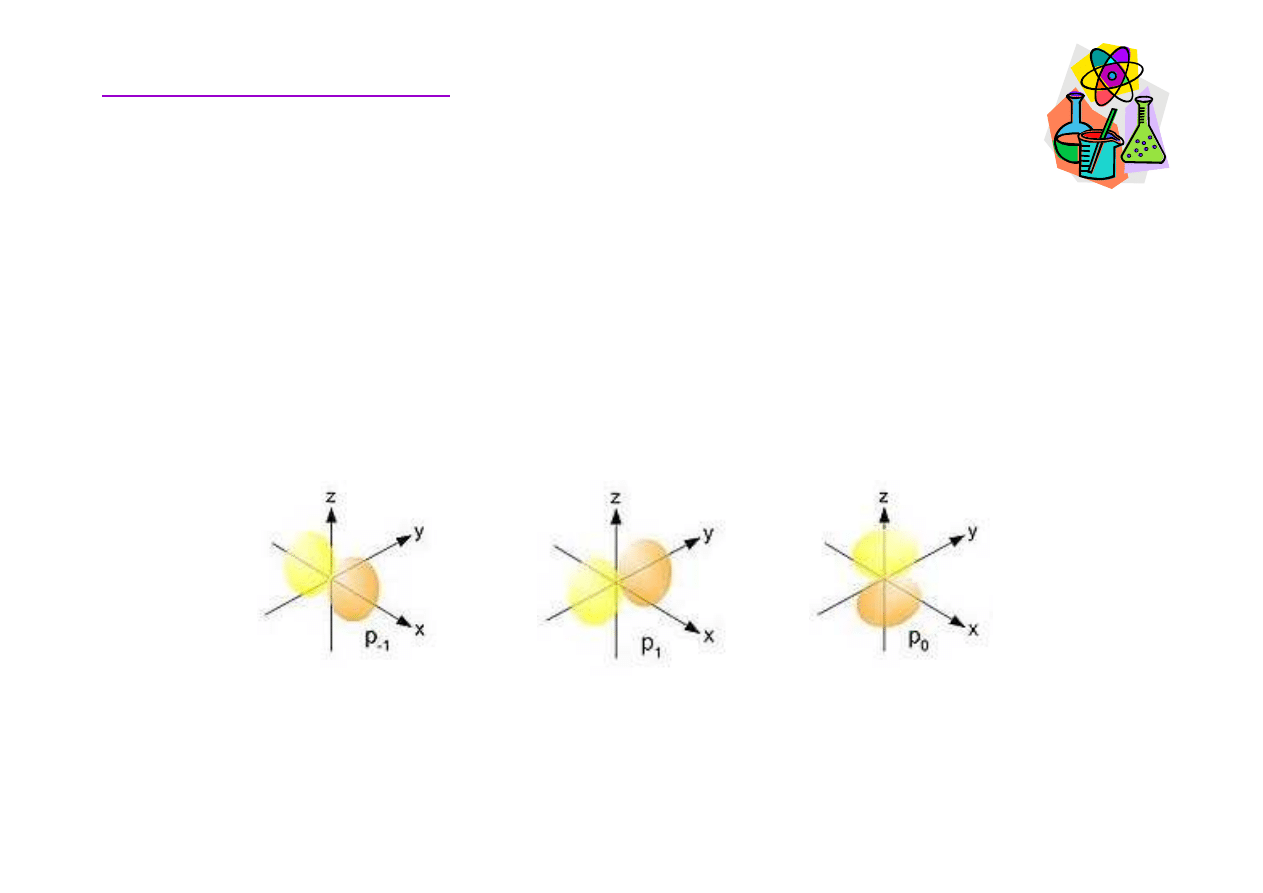
Rozmieszczenie elektronów w atomie
• Dla orbitalu s
→
m=0
→
mo
ż
liwa jest tylko jedna orientacja
• Dla orbitalu p
→
m= -1,0,+1
→
trzy mo
ż
liwe orientacje - px,
py, pz
• Dla orbitalu d
→
m = -2,-1,0, +1,+2
→
pi
ęć
mo
ż
liwych
orientacji - dxy,dyz,dxz,dx2y2,dz2
Podstawy chemii organicznej
http://2012books.lardbucket.org/books/beginning-chemistry/s12-02-quantum-numbers-for-electrons.html
Rozmieszczenie elektronów w atomie
Ka
ż
dy orbital mo
ż
e by
ć
zaj
ę
ty przez co najwy
ż
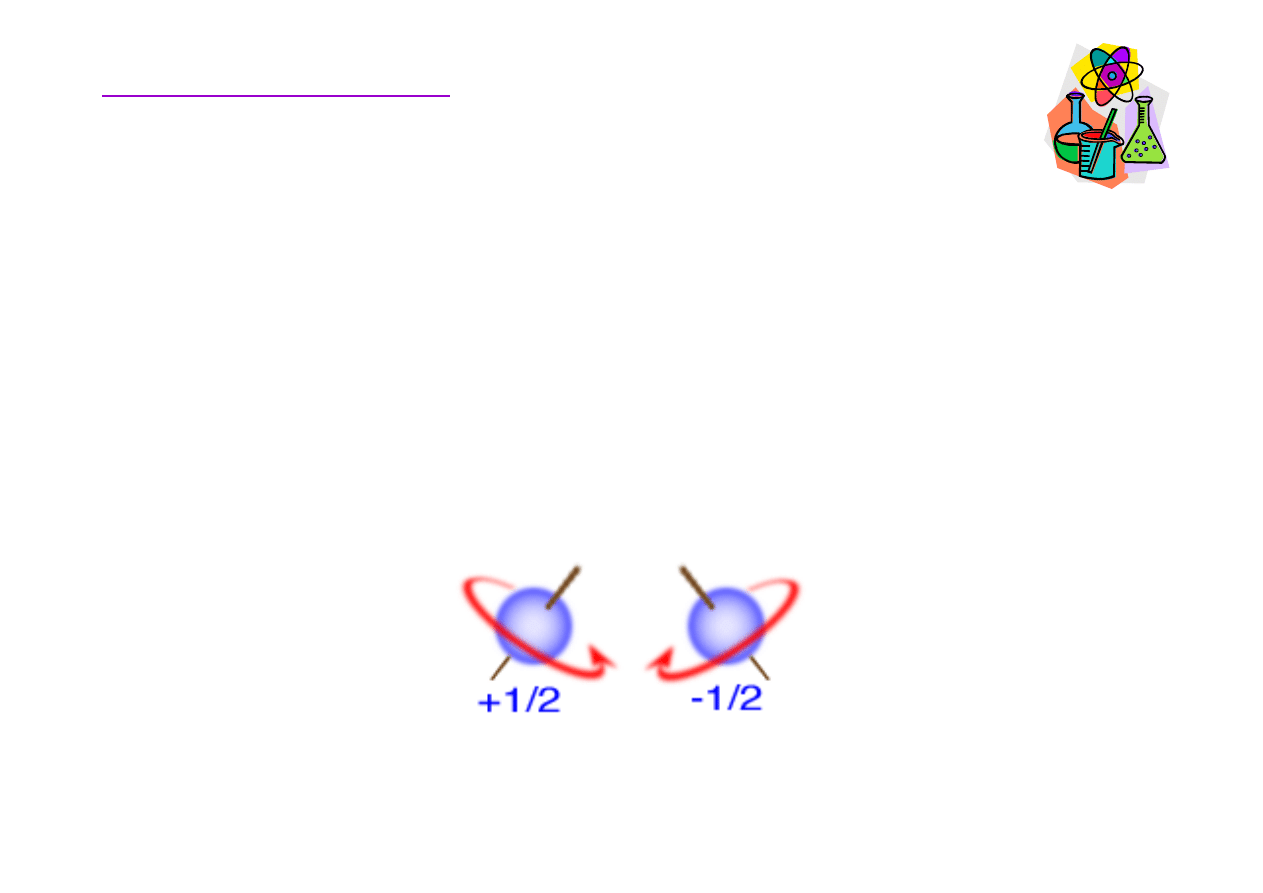
ej dwa elektrony.
Spinowa liczba kwantowa (s) - informuje o spinie (ruchu
obrotowym) elektronu, zgodnym z ruchem wskazówek zegara
(+1/2,
↑
) lub przeciwnym do ruchu wskazówek zegara (-1/2,
↓
).
Podstawy chemii organicznej
http://chemwiki.ucdavis.edu/Wikitexts/UC_Davis/UCD_Chem_124A%3A_Kauzlarich/ChemWiki_Module_Topics/Spin_Quantum_Number
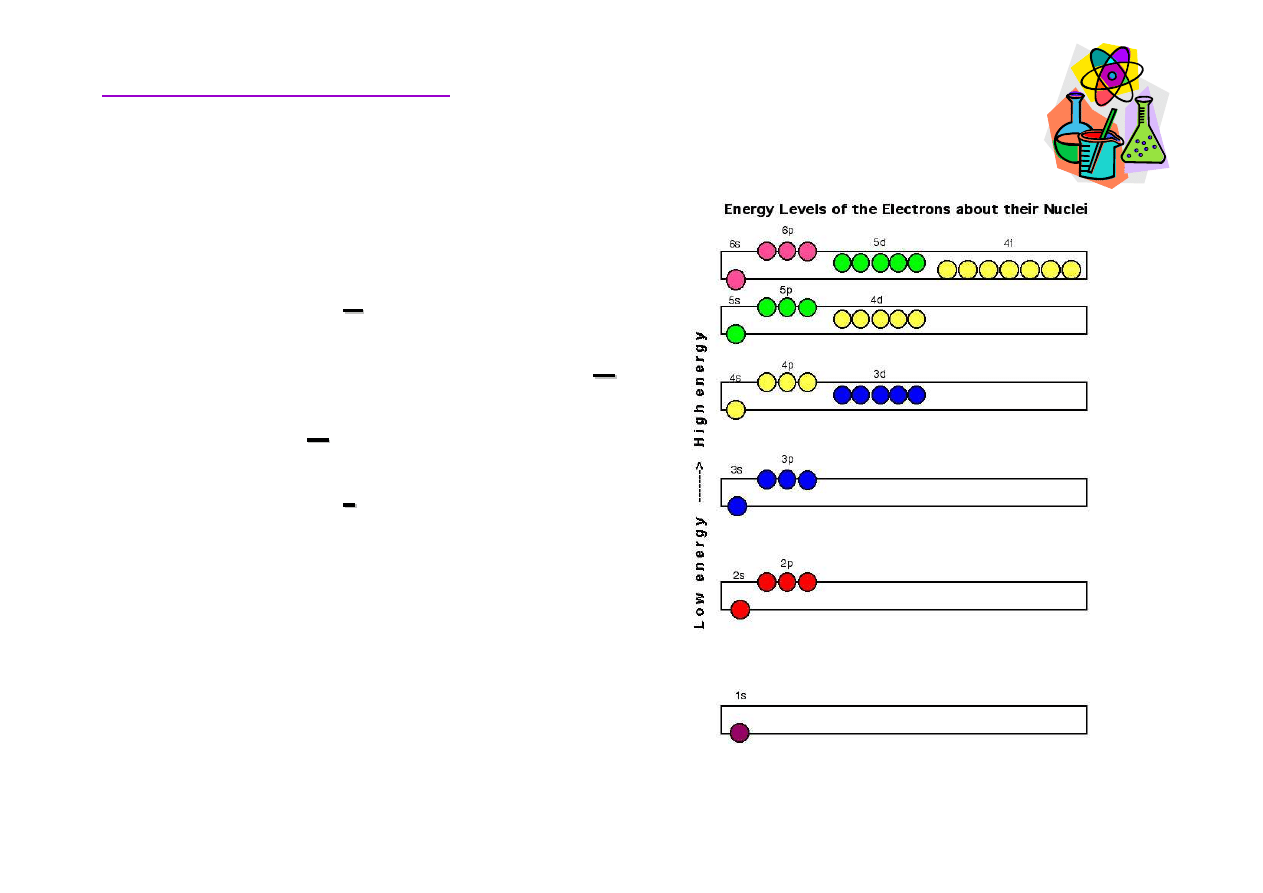
Rozmieszczenie elektronów w atomie
W obr
ę
bie ka
ż
dej powłoki,
podpowłoka
s
s ma najni
ż
sz
ą
energi
ę
, potem podpowłoka
p
p,
nast
ę
pnie
d
d i ostatecznie
podpowłoka
f
f. Podpowłoki o
ró
ż
nych warto
ś
ciach n mog
ą
mie
ć
nachodz
ą
ce na siebie
warto
ś
ci energii.
Podstawy chemii organicznej
boomeria.org

Rozmieszczenie elektronów w atomie
Główna liczba kwantowa (n) –
nazwa miasta w adresie.
Orbitalna (poboczna) liczba kwantowa (l) –
nazwa ulicy w
adresie
Magnetyczna liczba kwantowa (m)
– numer domu w adresie
Spinowa liczba kwantowa –
imi
ę
i nazwisko w adresie
Podstawy chemii organicznej
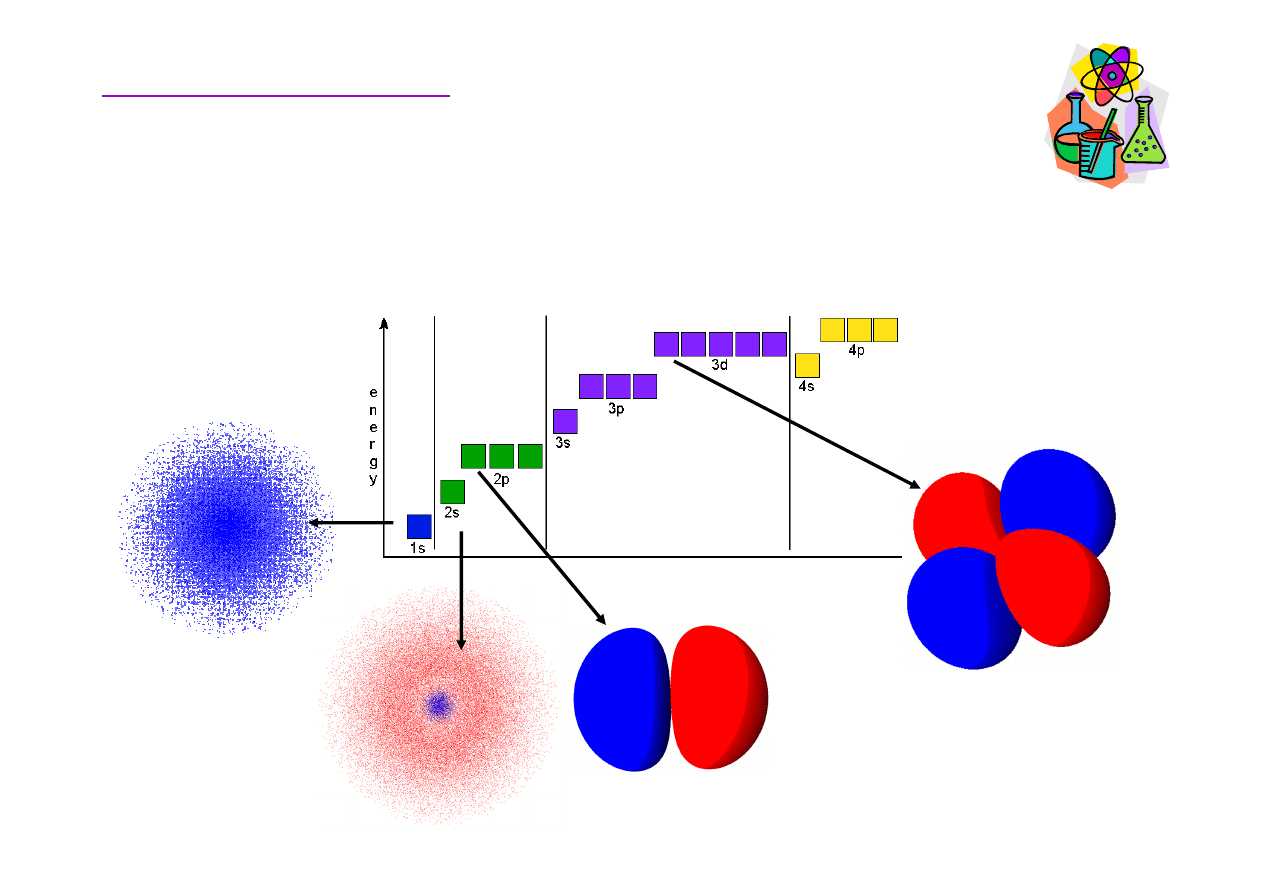
Rozmieszczenie elektronów w atomie
Podstawy chemii organicznej
Konfiguracja elektronów okre
ś
la ich rozmieszczenie na
powłokach według rosn
ą
cej energii.
http://kaffee.50webs.com/Science/activities/Chem/Activity.Electron.Configuration.html
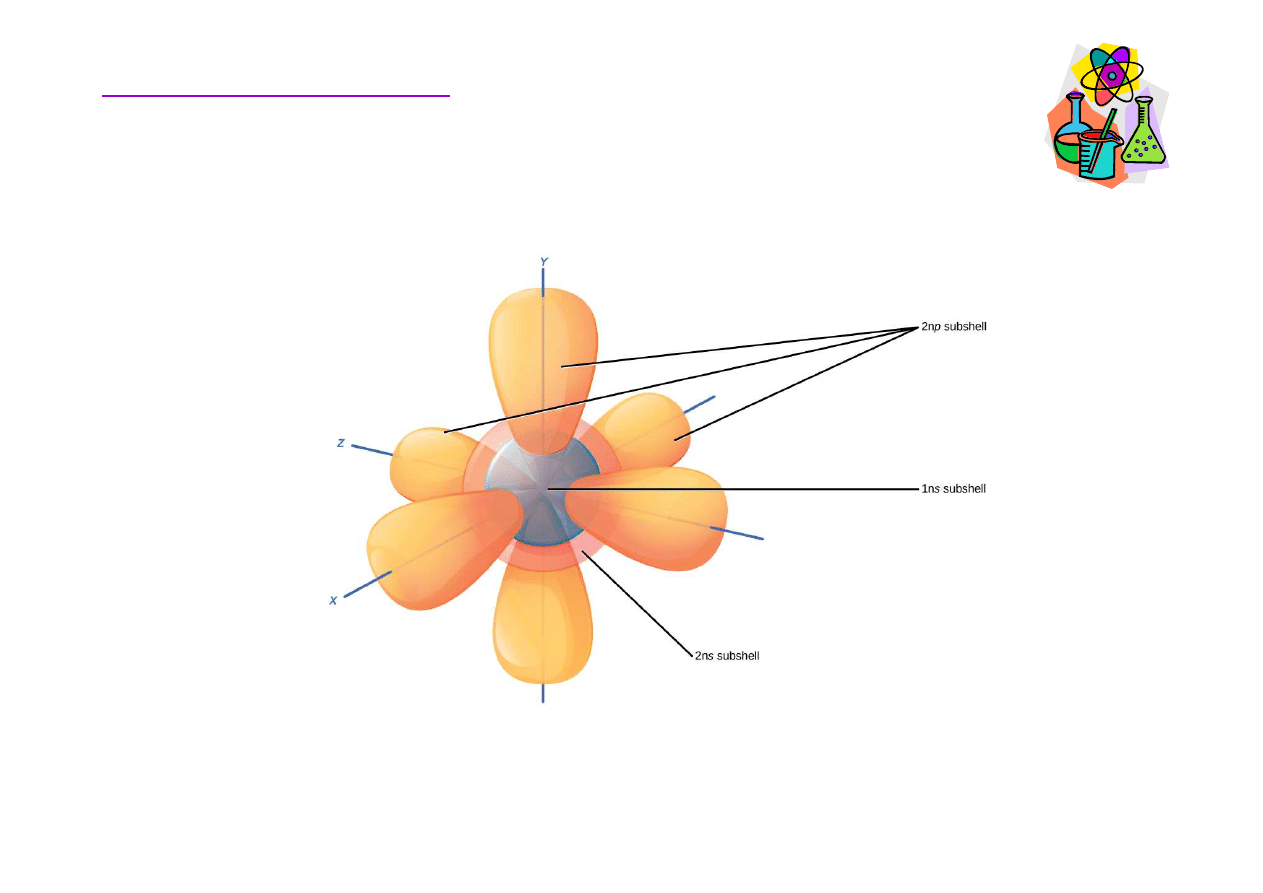
Rozmieszczenie elektronów w atomie
Podstawy chemii organicznej
http://www.forum.biolog.pl/pow-oki-podpow-oki-chmura-elektronowa-vt53686.htm
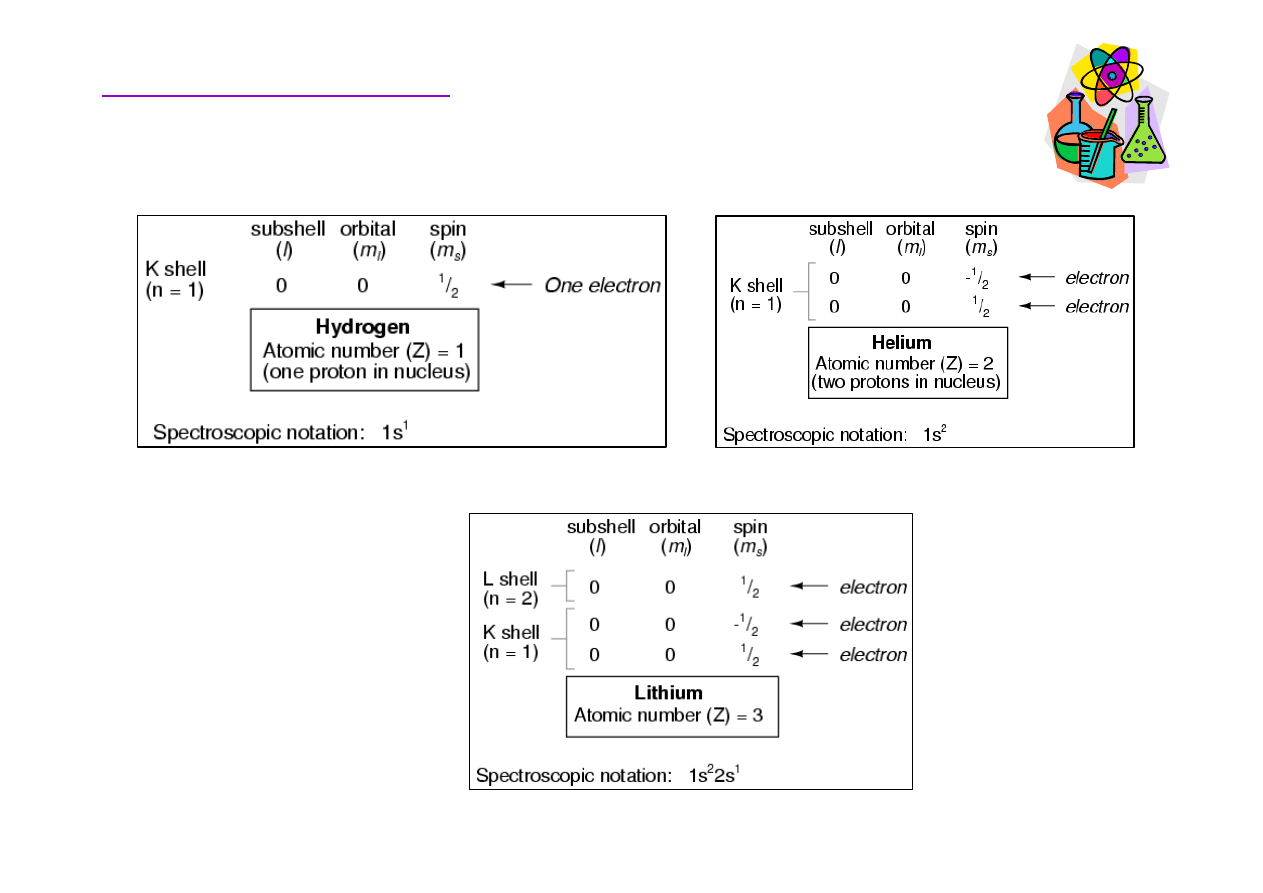
Rozmieszczenie elektronów w atomie
Podstawy chemii organicznej
http://www.faqs.org/docs/electric/Semi/SEMI_2.html

Rozmieszczenie elektronów w atomie
Podstawy chemii organicznej
http://mrcauseysworld.com/chemistry/configurations.html
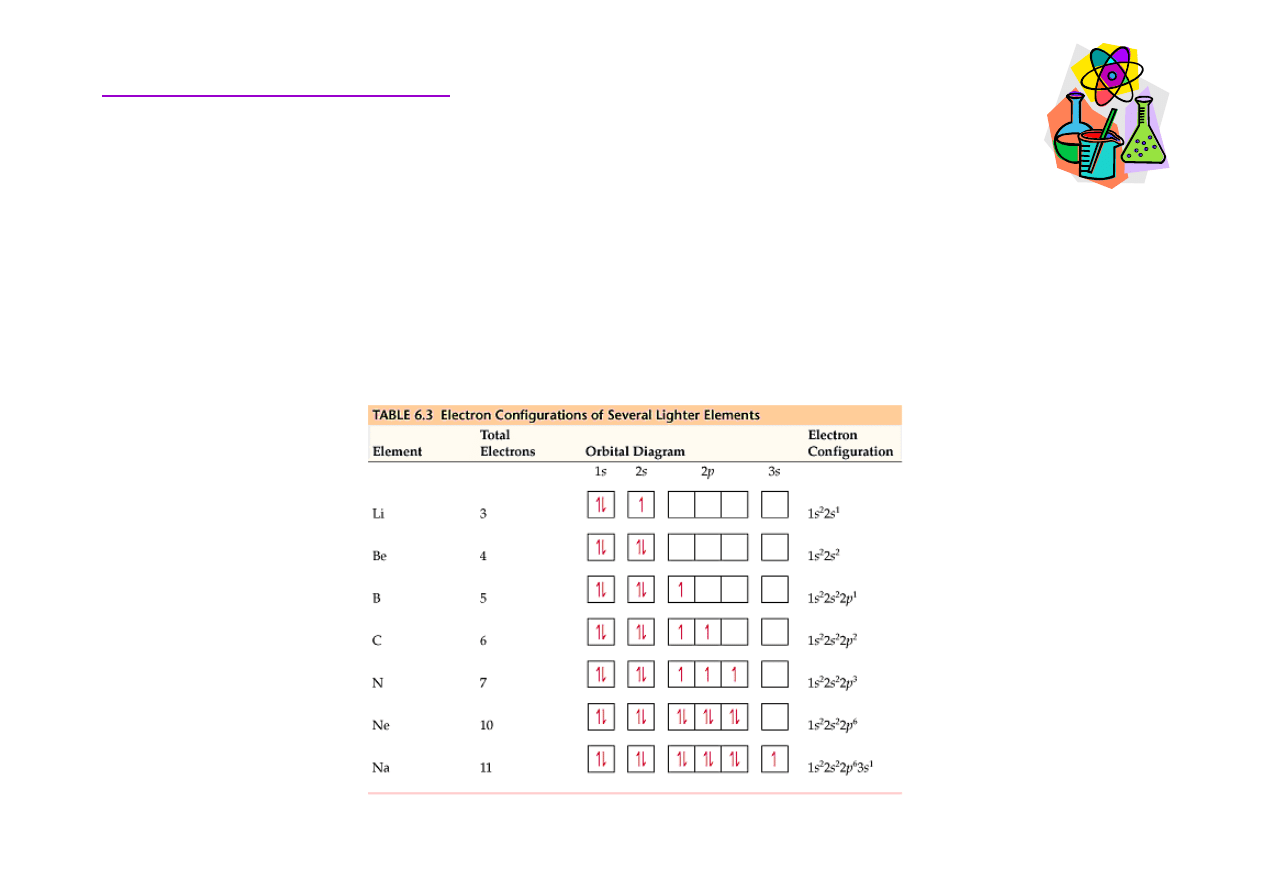
Rozmieszczenie elektronów w atomie
Elektrony walencyjne – elektrony zewn
ę
trznych powłok.
Elektrony walencyjne zajmuj
ą
orbitale s i p w obr
ę
bie powłoki o najwy
ż
szej
głównej liczbie kwantowej dla danego atomu.
Podstawy chemii organicznej
http://wps.prenhall.com/wps/media/objects/3311/3390683/blb0608.html

Rozmieszczenie elektronów w atomie
• Symbole Lewisa – elektrony walencyjne s
ą
pokazane jako
kropki umiejscowione obok symbolu danego pierwiastka
• 1-4 elektrony
→
pojedyncze kropki
• 5-8 elektronów
→
jeden lub wi
ę
cej sparowanych elektronów
Podstawy chemii organicznej
http://www.iun.edu/~cpanhd/C101webnotes/chemical-bond/lewis-electron-dot.html
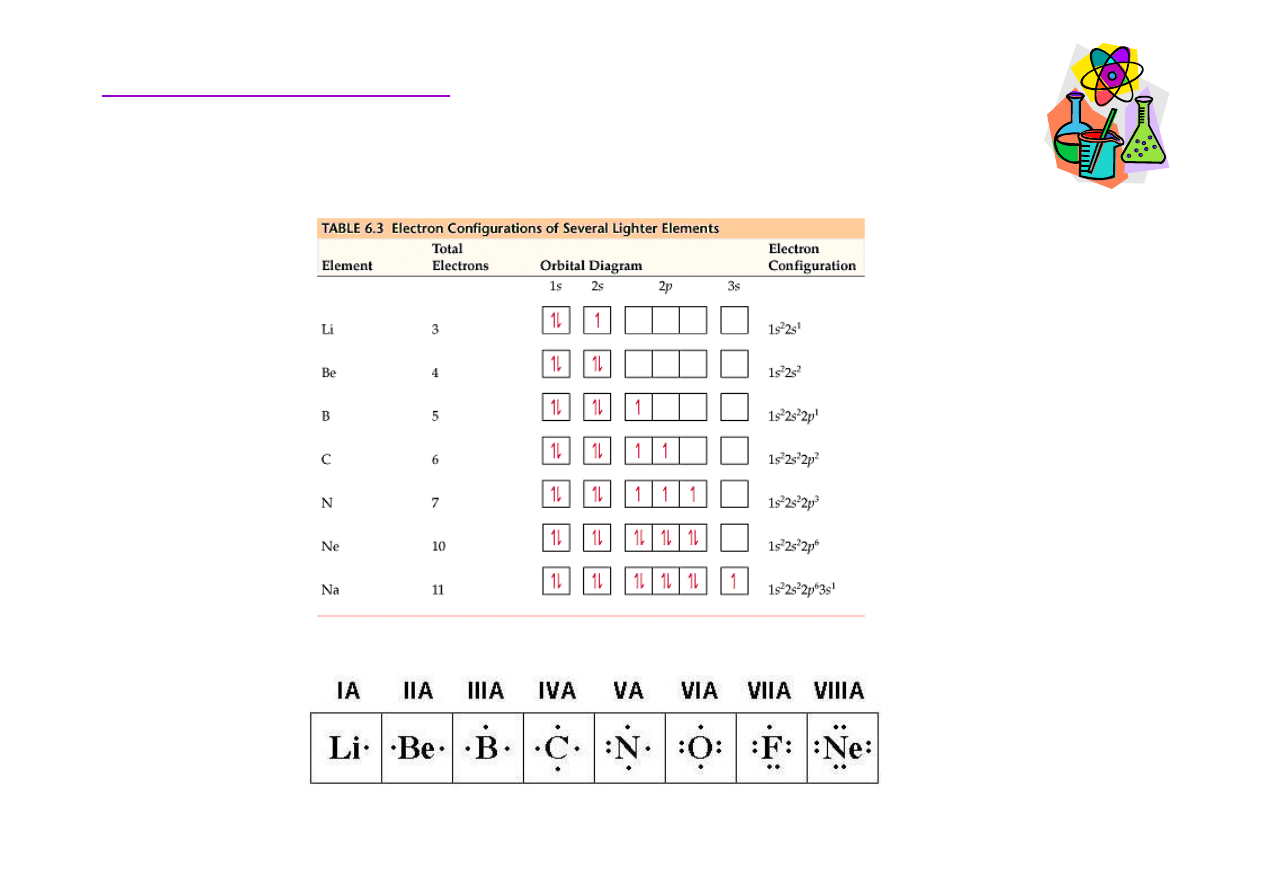
Rozmieszczenie elektronów w atomie
Podstawy chemii organicznej
http://edtech2.boisestate.edu/lindabennett1/502/Compounds%20and%20Naming/Lewis%20Dot.html
http://wps.prenhall.com/wps/media/objects/3311/3390683/blb0608.html
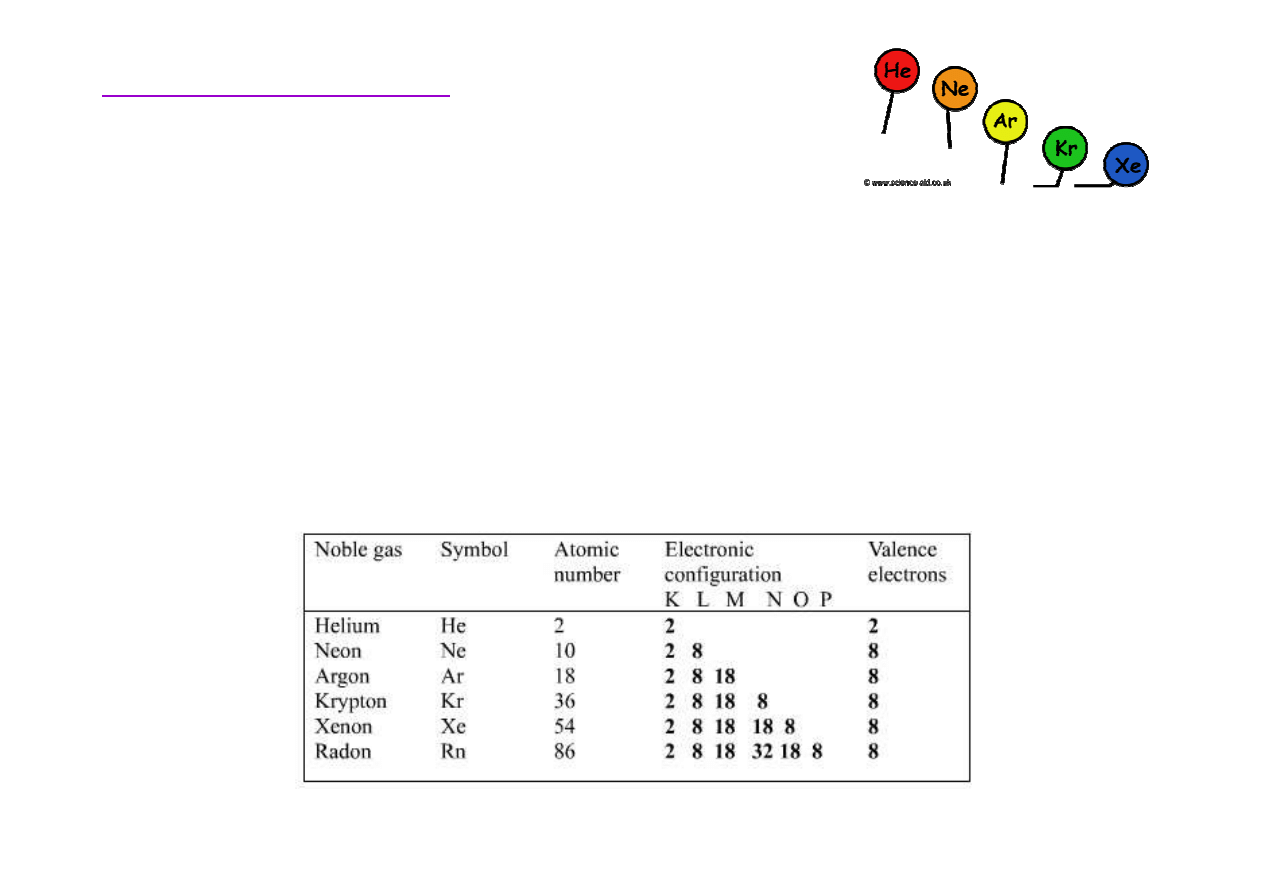
Rozmieszczenie elektronów w atomie –
gazy szlachetne
Gazy szlachetne maj
ą
wypełnion
ą
powłok
ę
walencyjn
ą
.
Posiadaj
ą
one (z wyj
ą
tkiem He) osiem elektronów
walencyjnych (2 elektrony na orbitalu s, 6 elektronów na
orbitalu p)
→
oktet.
Podstawy chemii organicznej
my-lyceum.net
Rozmieszczenie elektronów w atomie –
gazy szlachetne
Gazy szlachetne charakteryzuj
ą
si
ę
stabiln
ą
konfiguracj
ą
elektronow
ą
(oktet) i nie wchodz
ą
w oddziaływania z
innymi atomami.
Podstawy chemii organicznej
http://www.hopaj.pl/63094
Rozmieszczenie elektronów w atomie –
wi
ą
zania chemiczne
W przyrodzie atomy niemal wszystkich pierwiastków
wchodz
ą
w oddziaływania ze sob
ą
tworz
ą
c zwi
ą
zki
chemiczne. W ten proces zaanga
ż
owane s
ą
elektrony
walencyjne, które tworz
ą
wi
ą
zania chemiczne.
Podstawy chemii organicznej
http://wirdou.com/

Rozmieszczenie elektronów w atomie –
wi
ą
zania chemiczne
Atomy ulegaj
ą
jonizacji i przemieszczenie elektronów
(wi
ą
zania jonowe) lub dziel
ą
si
ę
elektronami (wi
ą
zania
kowalencyjne) tak, aby osi
ą
gn
ąć
konfiguracj
ę
elektronow
ą
gazów szlachetnych. Według reguły oktetu
magiczn
ą
cyfr
ą
stabilno
ś
ci jest "8" (2 elektrony na orbitalu
s
s, 6 elektronów na orbitalu
p
p).
Podstawy chemii organicznej
chemistryunderstood.com
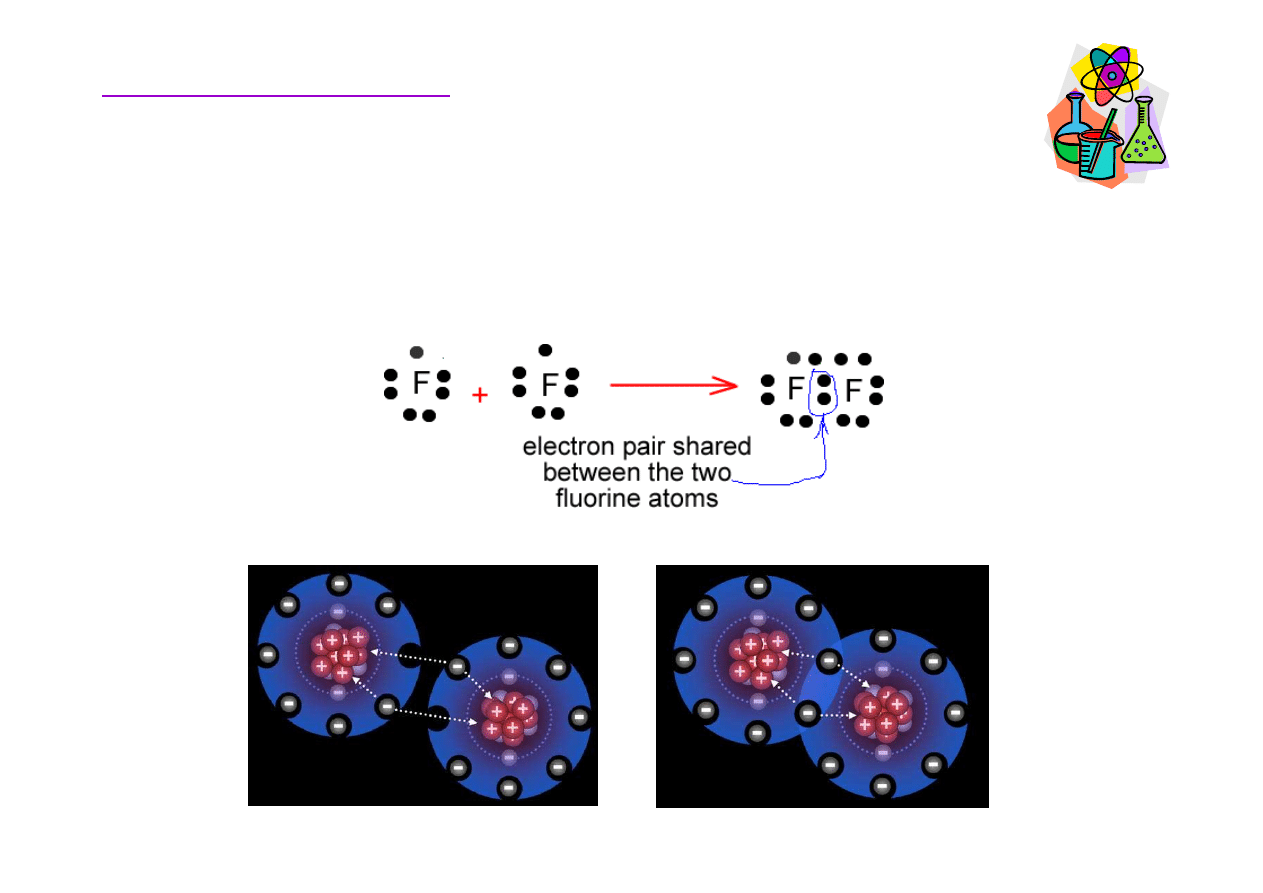
Wi
ą
zanie kowalencyjne
Podstawy chemii organicznej
Wi
ą
zanie kowalencyjne powstaje, gdy dwa atomy dziel
ą
si
ę
elektronami walencyjnymi.
http://www.chemistryland.com/CHM130W/11-Bonds/bonds.html
http://www.clickandlearn.org/gr9_sci/atoms/bonding.htm

Wi
ą
zanie kowalencyjne spolaryzowane
Wi
ą
zanie kowalencyjne spolaryzowane powstaje, gdy
dwa atomy dziel
ą
si
ę
elektronami w nierówny sposób.
Jeden z ko
ń
ców wi
ą
zania ma wtedy cz
ą
stkowy ładunek
dodatni, drugi cz
ą
stkowy ładunek ujemny.
Podstawy chemii organicznej
employees.csbsju.edu
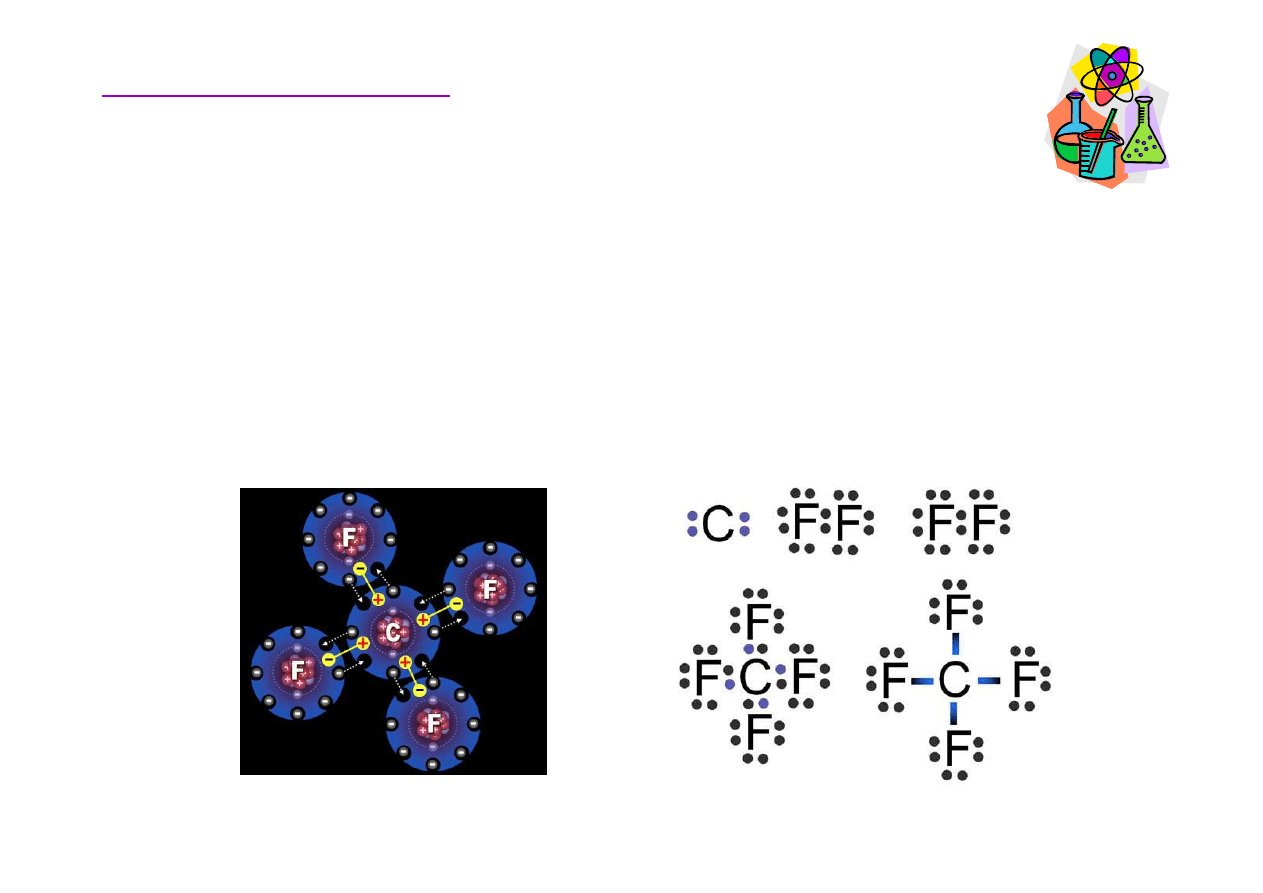
Wi
ą
zanie kowalencyjne spolaryzowane
Podstawy chemii organicznej
http://www.chemistryland.com/CHM130W/11-Bonds/bonds.html
Fluor „potrzebuje" 1 elektronu aby dopełni
ć
swoj
ą
zewn
ę
trzn
ą
powłok
ę
do oktetu. W
ę
giel dostarcza tego elektronu, zyskuj
ą
c
elektrony od fluoru (po 1 od ka
ż
dego atomu), tak,
ż
e mo
ż
e
uzyska
ć
oktet.
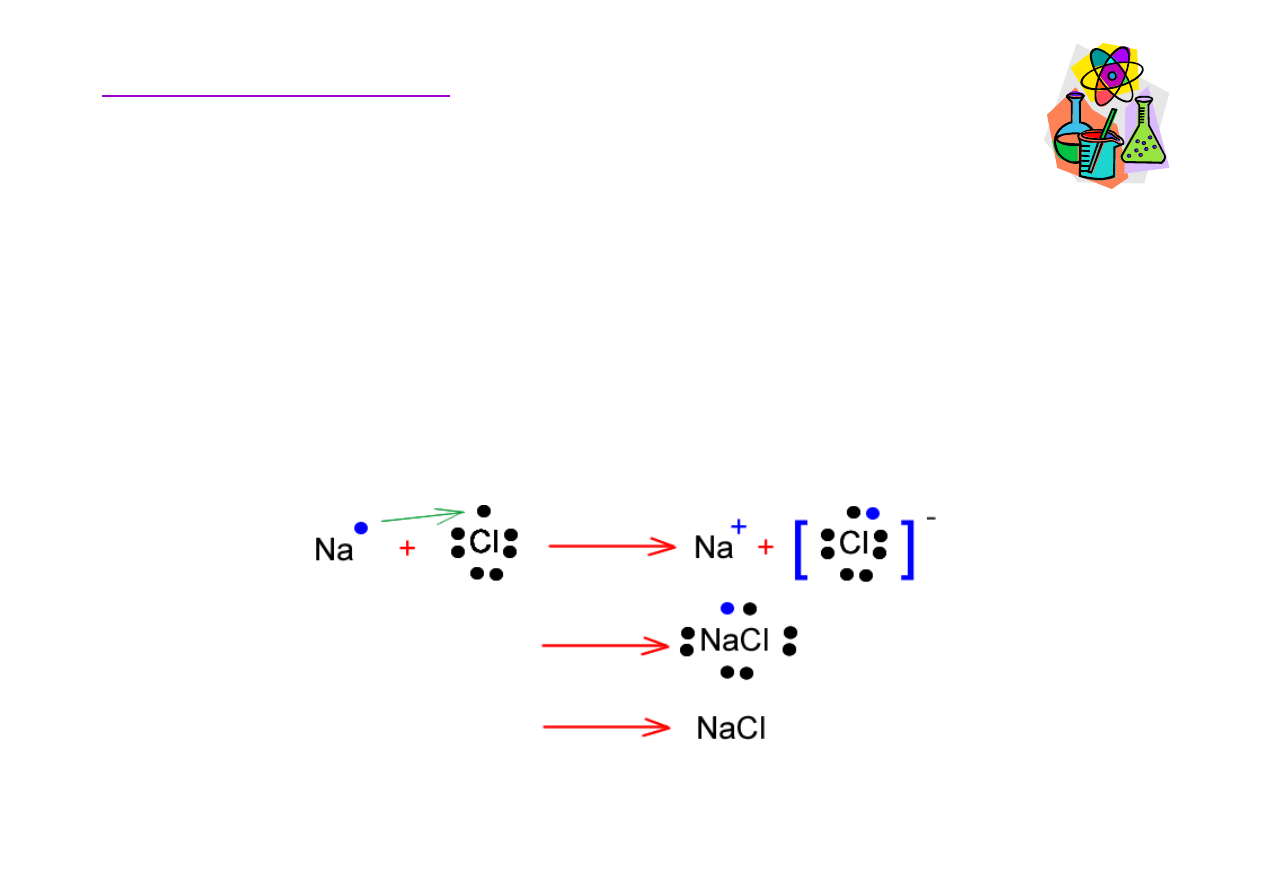
Wi
ą
zanie jonowe
Wi
ą
zanie jonowe powstaje, gdy jeden z atomów przekazuje elektron do
innego atomu.
Atom sodu ma jeden elektron na zewn
ę
trznej powłoce (orbital s). Je
ż
eli
go straci, uzyska stabiln
ą
konfiguracj
ę
oktetu. Chlor posiada 7
elektronów walencyjnych, posiada zatem jeden „wakat”.
Podstawy chemii organicznej
http://www.clickandlearn.org/gr9_sci/atoms/bonding.htm
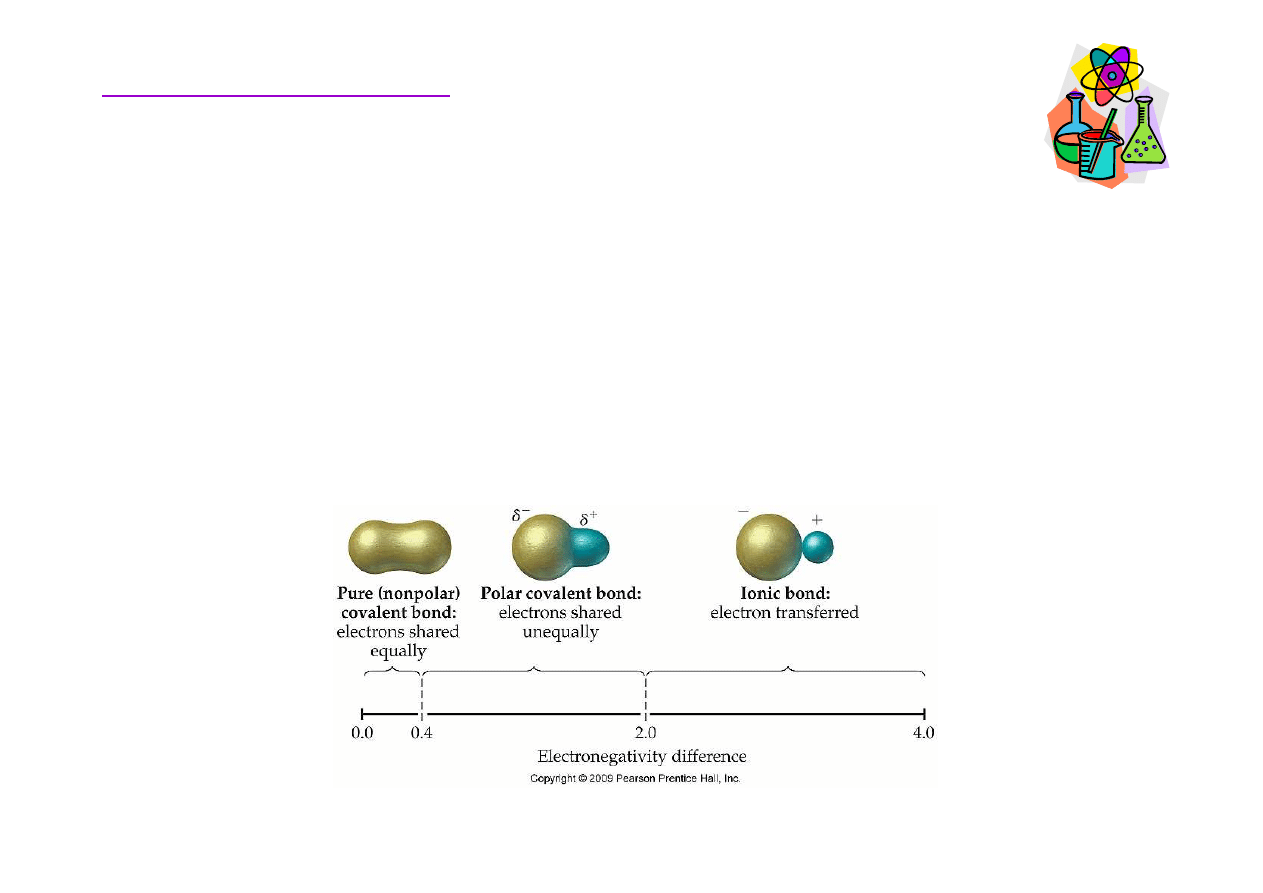
Elektroujemno
ść
Elektroujemno
ść
– zdolno
ść
przyci
ą
gania elektronów
przez jeden z atomów wi
ą
zania. Atom pierwiastka o
wi
ę
kszej elektroujemno
ś
ci odci
ą
ga elektrony wi
ą
zania od
pierwiastka o mniejszej elektroujemno
ś
ci.
Podstawy chemii organicznej
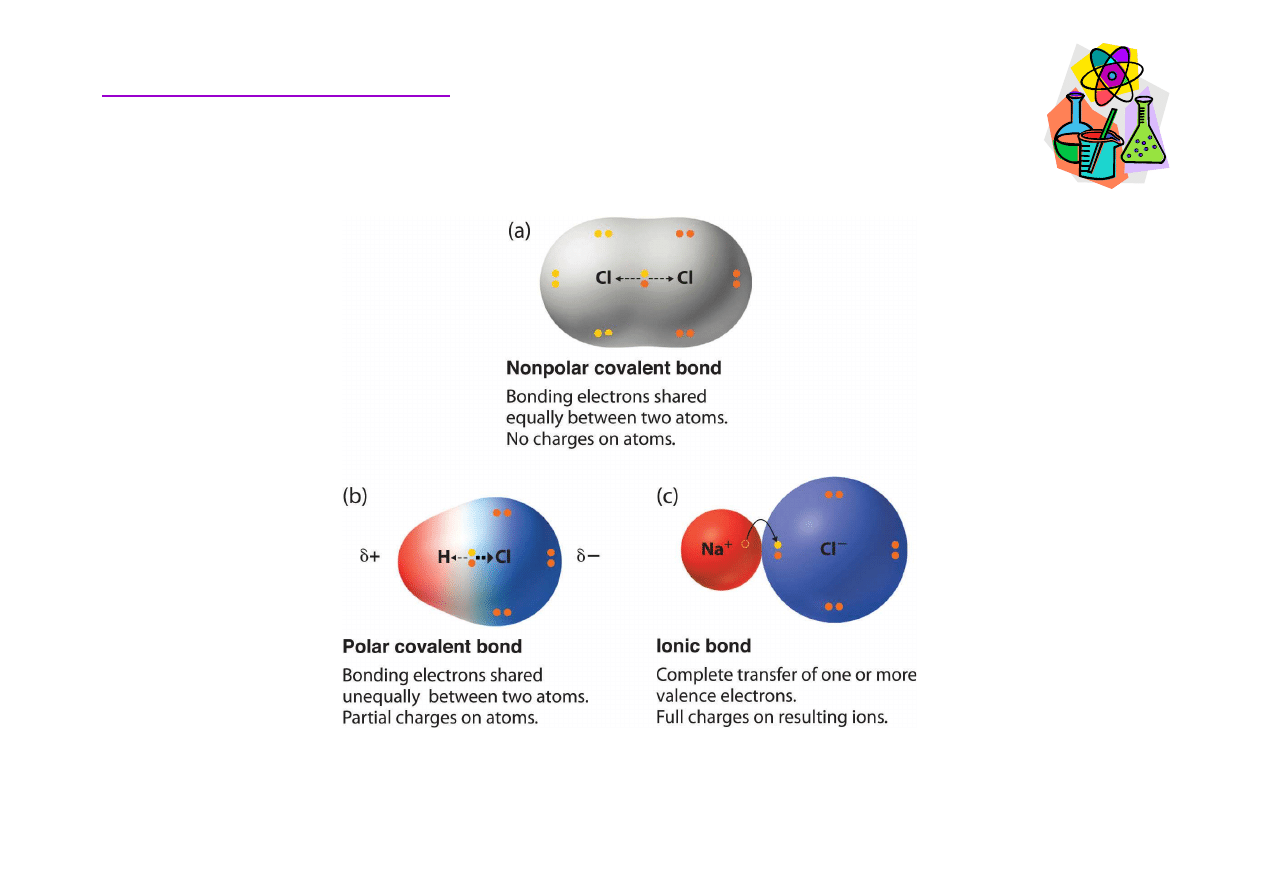
Wi
ą
zania chemiczne - podsumowanie
Podstawy chemii organicznej
http://2012books.lardbucket.org/books/principles-of-general-chemistry-v1.0m/s12-09-polar-covalent-bonds.html
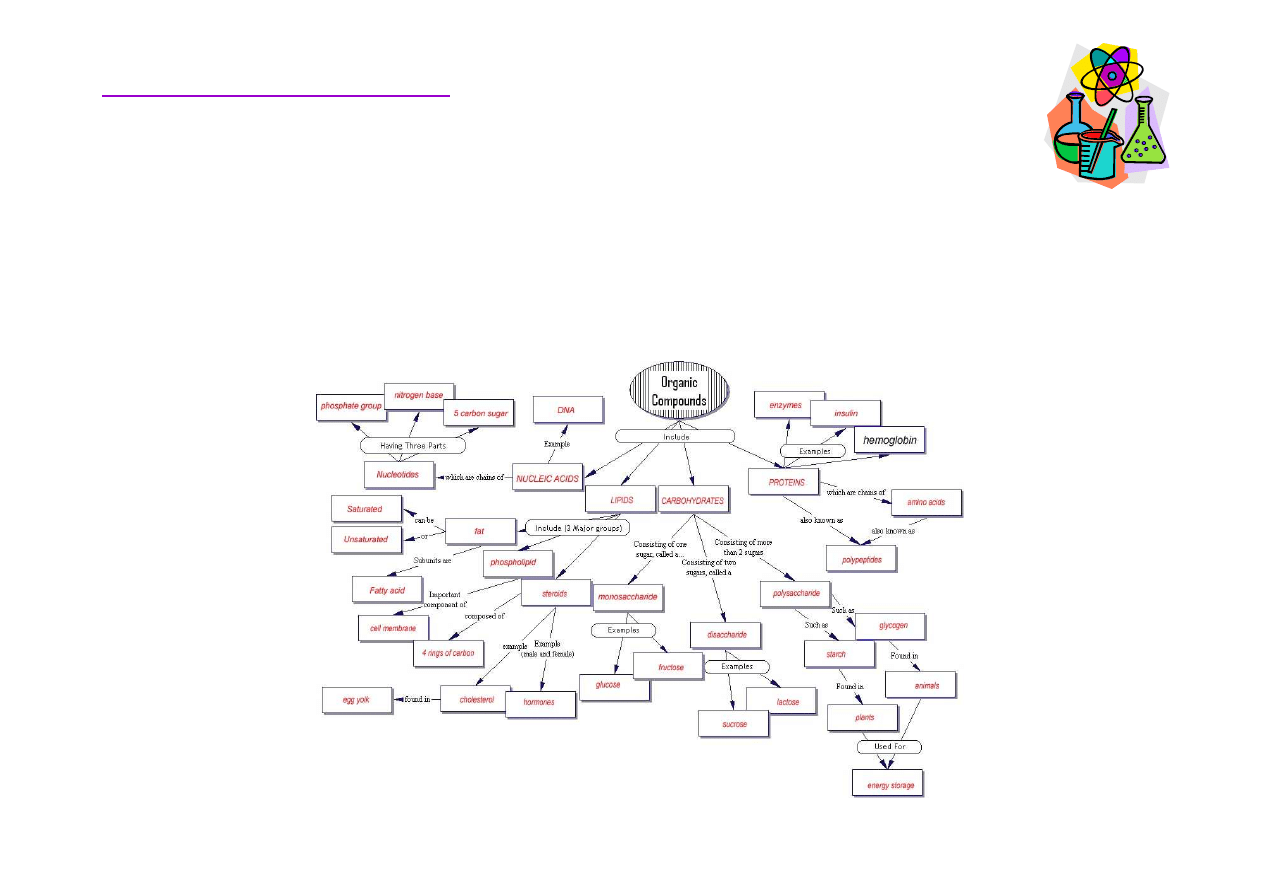
Chemia organiczna
Chemia organiczna to chemia zwi
ą
zków w
ę
gla. Około 90%
poznanych zwi
ą
zków to zwi
ą
zki organiczne.
Podstawy chemii organicznej
http://www.biologycorner.com/worksheets/conceptmap-organic_key.html
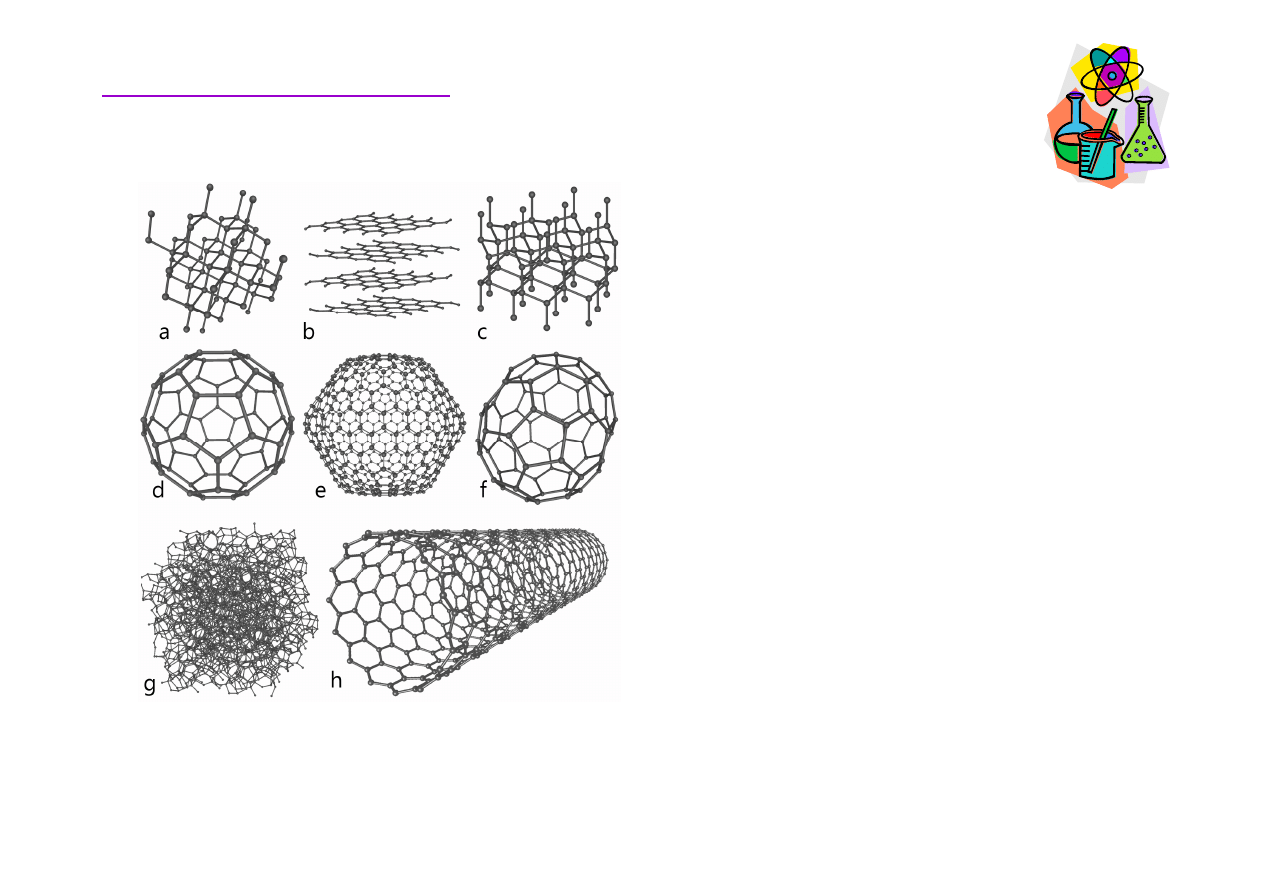
Chemia organiczna
Podstawy chemii organicznej
W
ę
giel atomowy jest bardzo
nietrwały, dlatego jest
stabilizowany w ró
ż
nego
rodzaju wieloatomowych
strukturach nazywanych
odmianami alotropowymi.
http://upload.wikimedia.org/wikipedia/commons/f/f8/Eight_Allotropes_of_Carbon.png
Odmiany alotropowe w
ę
gla: a) diament; b) grafit; c) lonsdaleit;
d–f) fulereny (C60, C540, C70); g) w
ę
giel amorficzny; h) nanorurka w
ę
glowa.
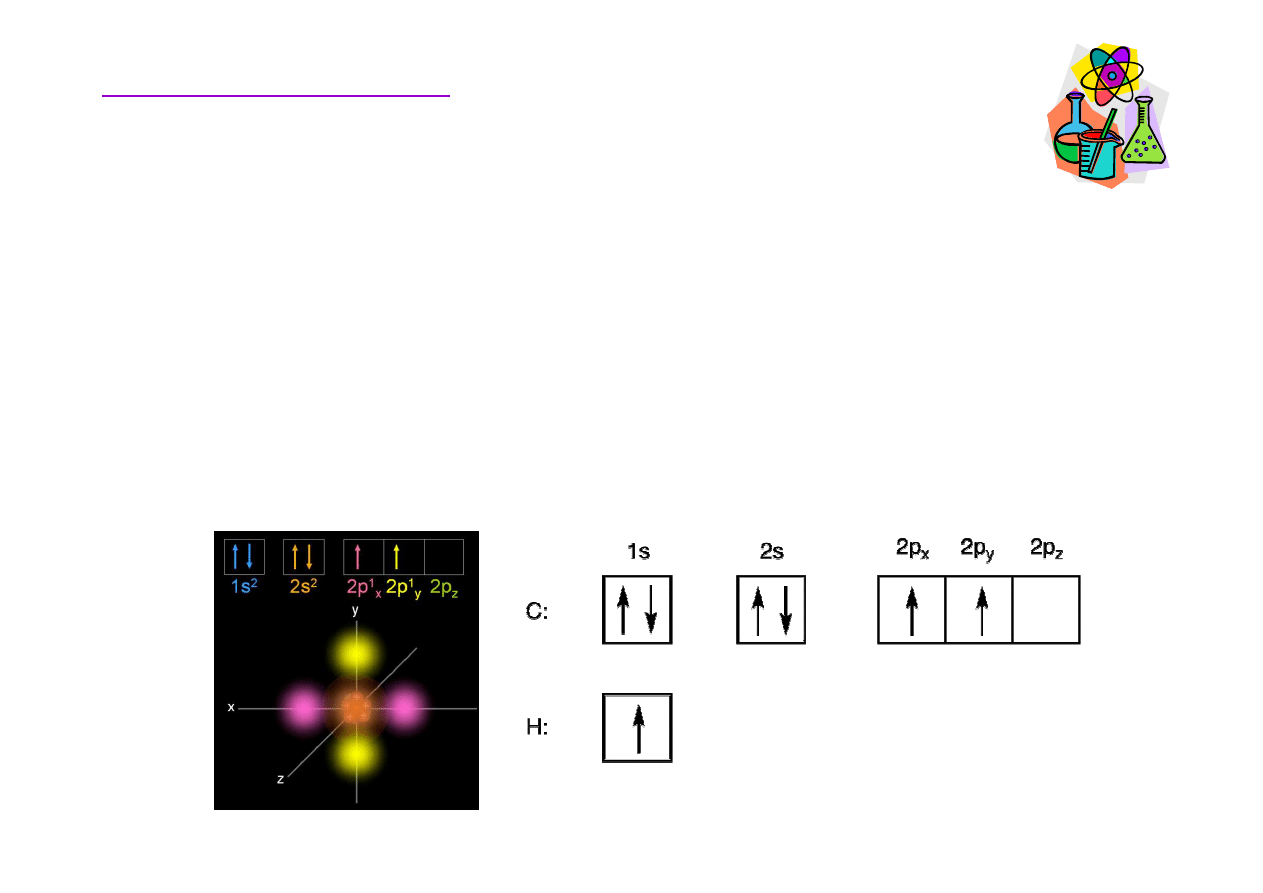
Zwi
ą
zki organiczne
Podstawy chemii organicznej
Zwi
ą
zki organiczne zawsze zawieraj
ą
atomy w
ę
gla (C) i
wodoru (H) oraz niektóre z nich atomy tlenu (O), siarki (S),
azotu (N), fosforu (P) lub chlorowca (F, Cl, Br lub I).
http://www.chemistryland.com/CHM151S/07-Atomic%20Structure/ElectronConfig/ElectronConfiguration.html
http://science.uvu.edu/ochem/index.php/alphabetical/g-h/hybridization
/

Teoria strukturalna
Pomi
ę
dzy latami 1858 i 1861 August Kekule, Archibald
Scott Cooper i Alexander M. Butlerow, pracuj
ą
c
niezale
ż
nie, stworzyli podstawy jednej z najwa
ż
niejszych
teorii w chemii: teorii strukturalnej.
Podstawy chemii organicznej
August Kekule
http://pl.wikipedia.org/wiki/Plik:Frkekul%C3%A9.jpg
Archibald Scott Cooper
http://en.wikipedia.org/wiki/File:Couper_Archibald_Scott.jpg
Alexander M. Butlerow
http://en.wikipedia.org/wiki/File:Butlerov_A.png
Teoria strukturalna
Podstawy chemii organicznej
http://ochembyamin.blogspot.com/
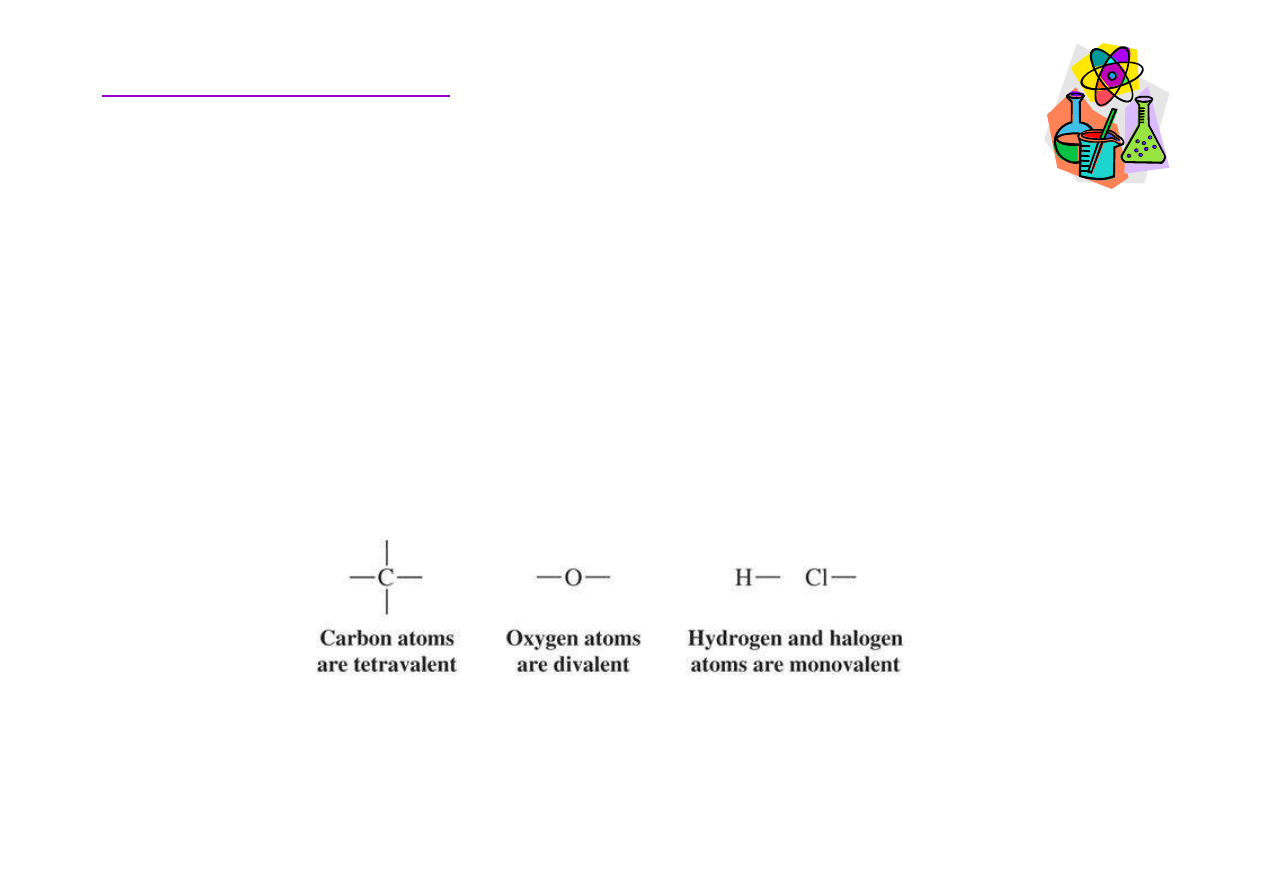
• Atomy w zwi
ą
zkach organicznych mog
ą
tworzy
ć
okre
ś
lon
ą
liczb
ę
wi
ą
za
ń
wykorzystuj
ą
c swoje elektrony
walencyjne.
Teoria strukturalna
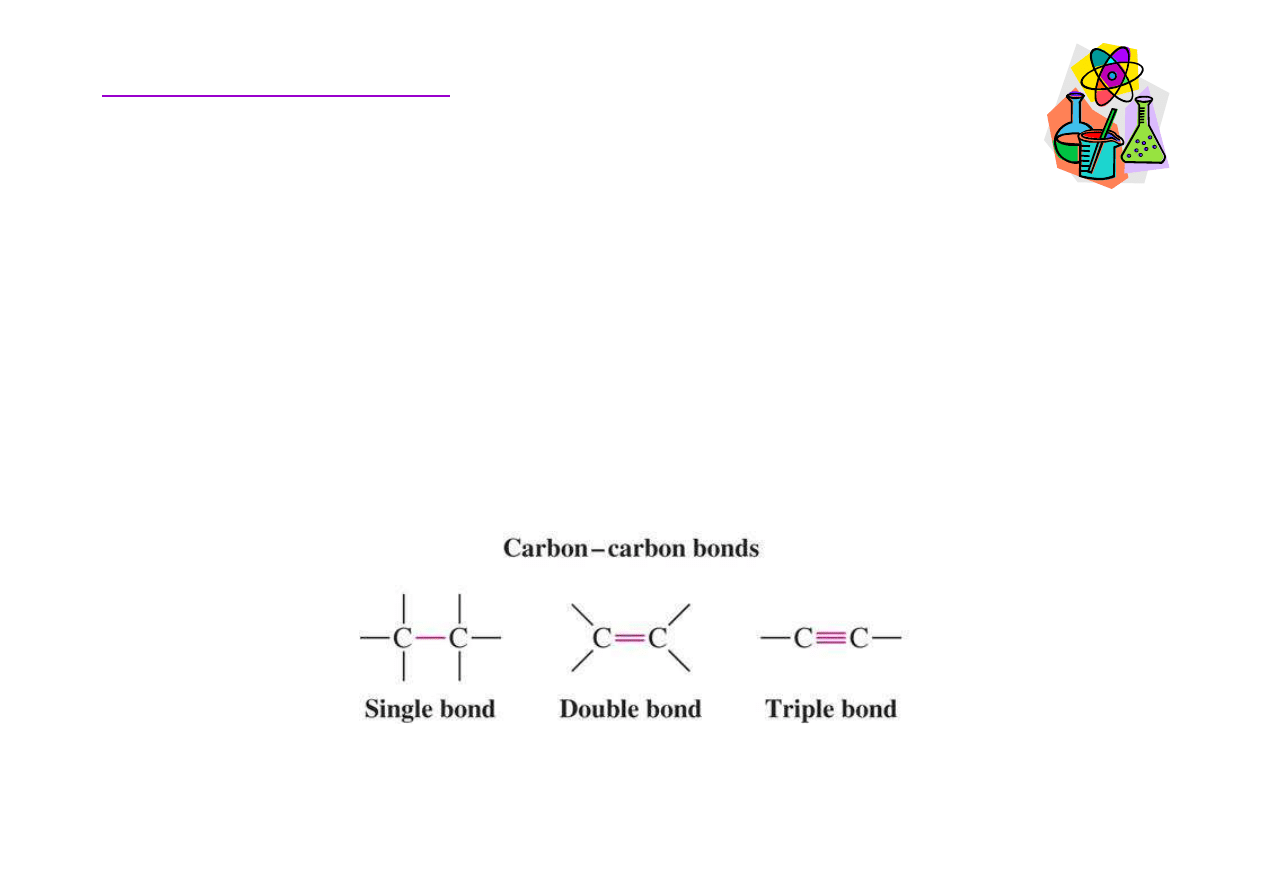
• Atomy w
ę
gla mog
ą
ł
ą
czy
ć
si
ę
ze sob
ą
lub z atomami
innych pierwiastków wi
ą
zaniami pojedynczymi,
podwójnymi lub potrójnymi.
Podstawy chemii organicznej
http://ochembyamin.blogspot.com/

Orbitale molekularne
Orbital molekularny (inaczej cz
ą
steczkowy, skrót MO) –
matematyczna funkcja opisuj
ą
ca stan elektronu jako fali
w cz
ą
steczce. Funkcja ta jest u
ż
ywana do obliczania
fizycznych i chemicznych wła
ś
ciwo
ś
ci elektronu, takich
jak prawdopodobie
ń
stwo znalezienia go w dowolnym
rejonie cz
ą
steczki.
Podstawy chemii organicznej
Orbitale molekularne
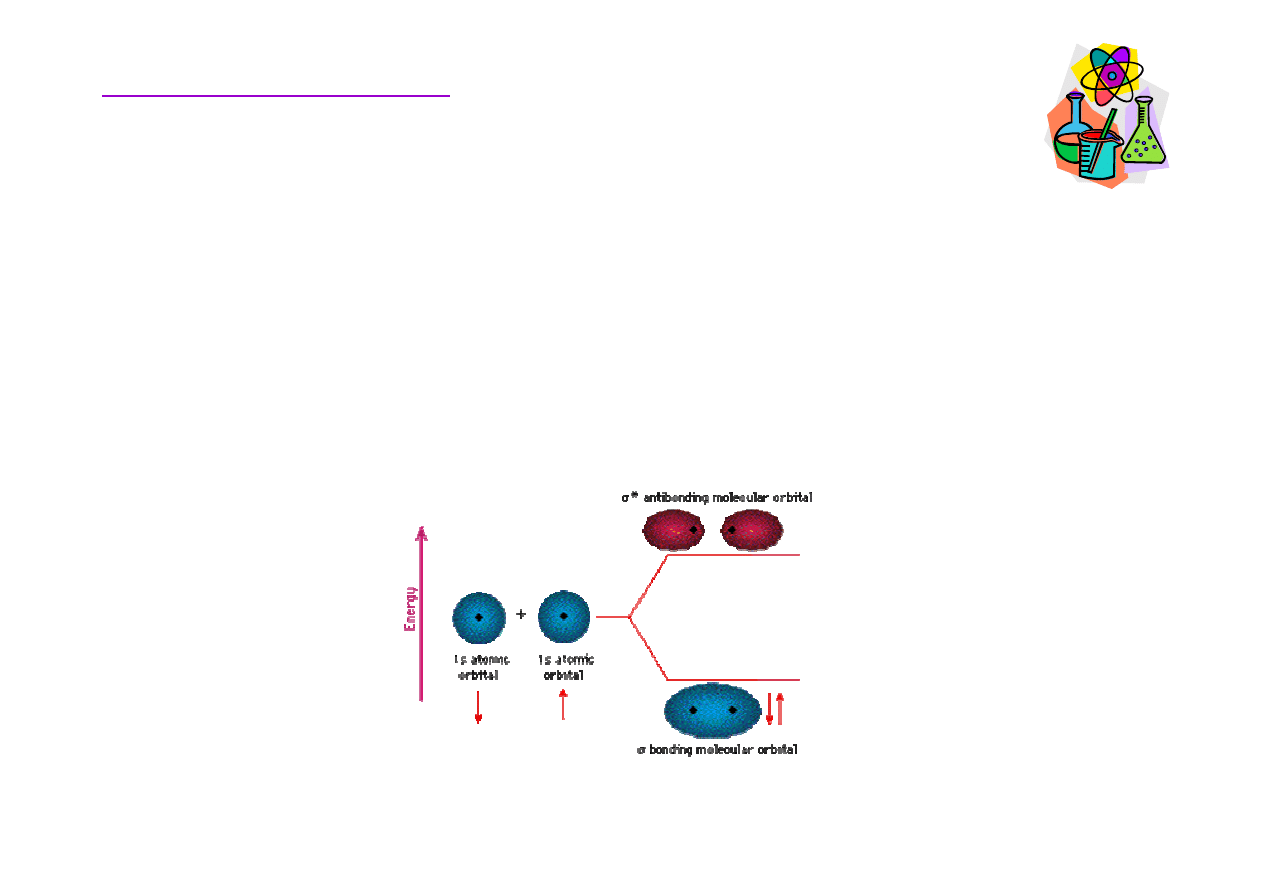
• orbital molekularny powstaje w wyniku nakładania si
ę
orbitali atomowych atomów tworz
ą
cych wi
ą
zanie
• liczba powstaj
ą
cych orbitali molekularnych = liczba
nakładaj
ą
cych si
ę
orbitali atomowych
Podstawy chemii organicznej
http://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/intro3.html
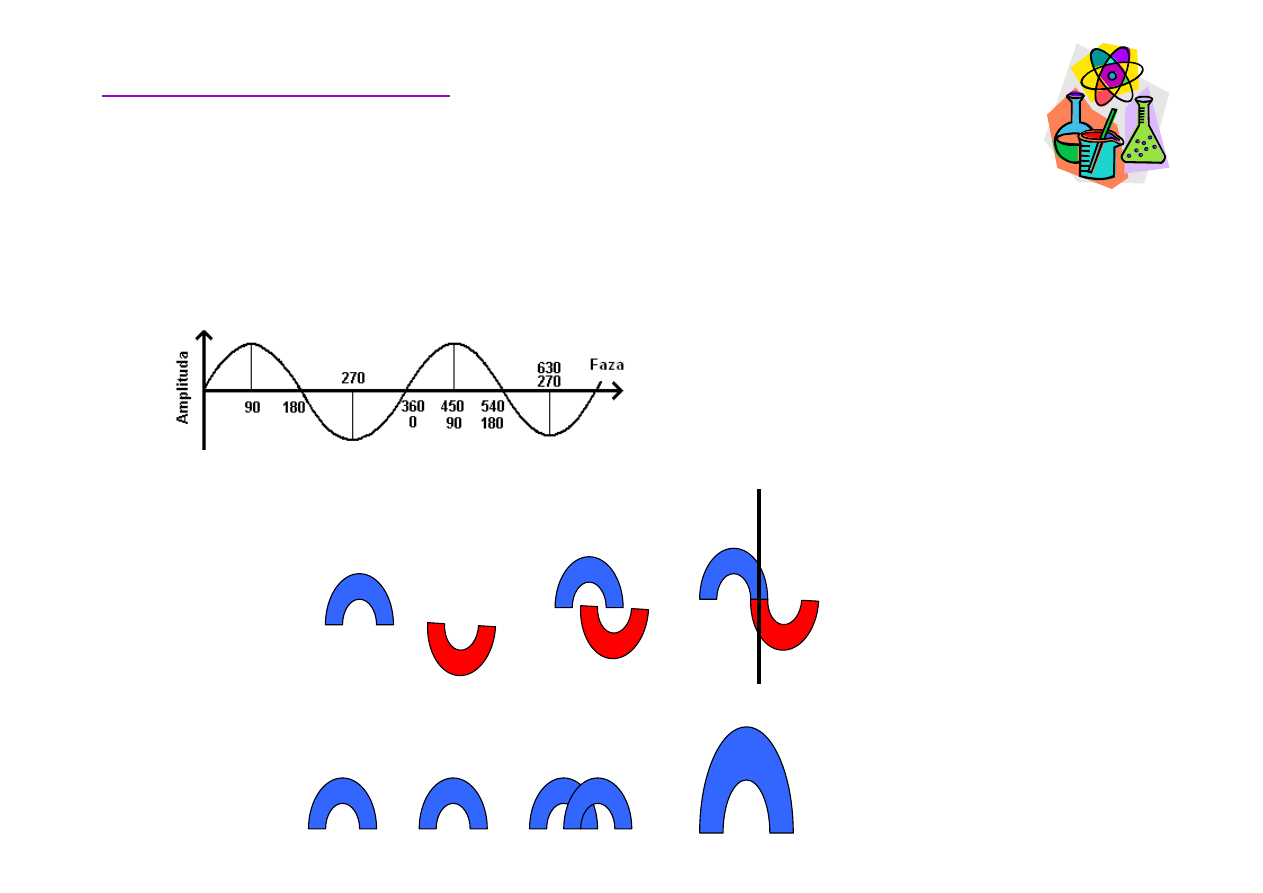
Orbitale molekularne
Elektron mo
ż
e by
ć
rozpatrywany jako oscyluj
ą
ca fala, która
jako taka mo
ż
e posiada
ć
faz
ę
.
Podstawy chemii organicznej
+
→
=
+
→
=
Płaszczyzna
w
ę
złowa
Fale o zgodnych fazach
Fale o przeciwnych fazach
http://edu.pjwstk.edu.pl/wyklady/wspmu/scb/index04.html
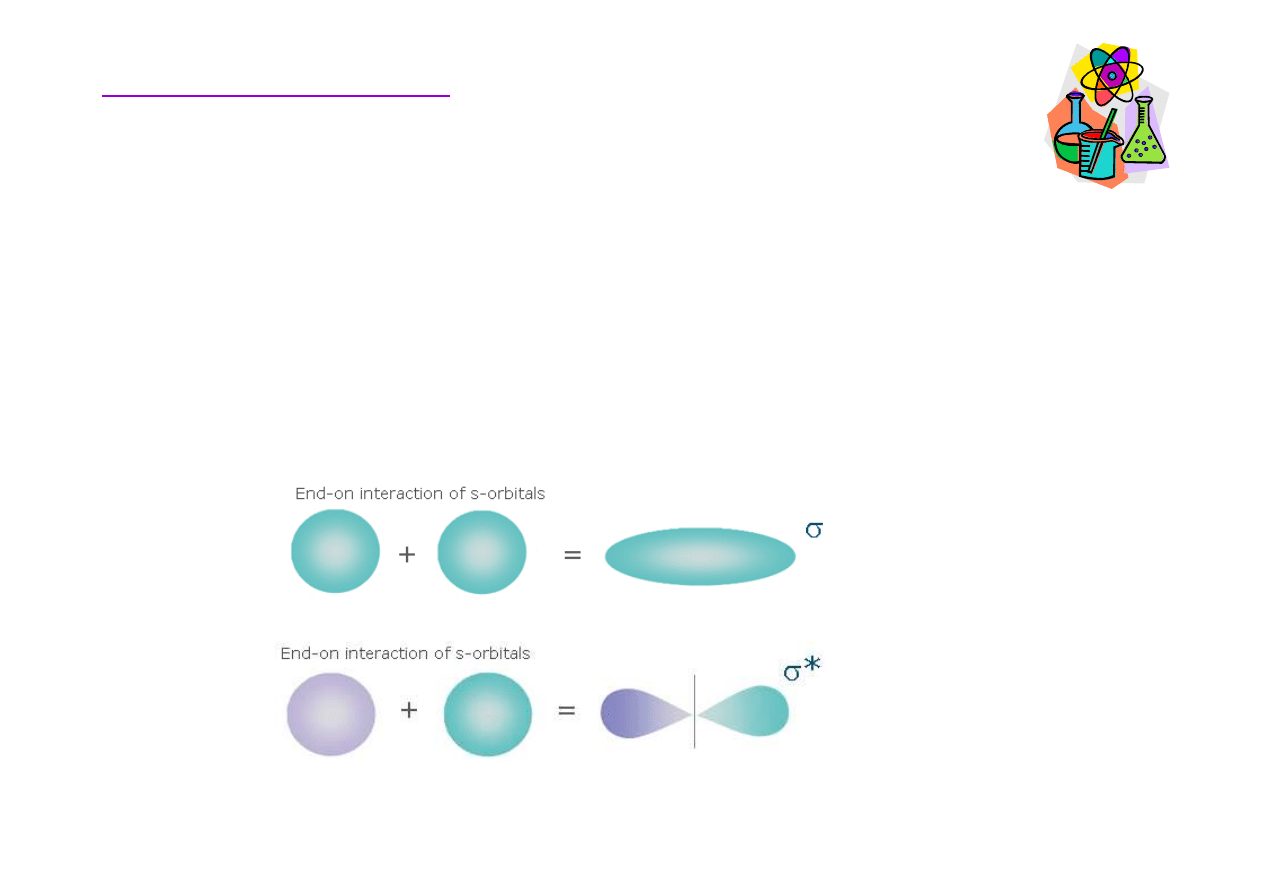
Orbitale molekularne
Graficznie faza orbitalu jest przedstawiana znakiem + lub –
(znaki te nie maj
ą
nic wspólnego z ładunkiem
elektrycznym) albo poprzez cieniowanie.
Podstawy chemii organicznej
http://www.ntu.ac.uk/cels/molecular_geometry/mo_theory/Sigma_MOs/index.html
Te same fazy
Przeciwne fazy
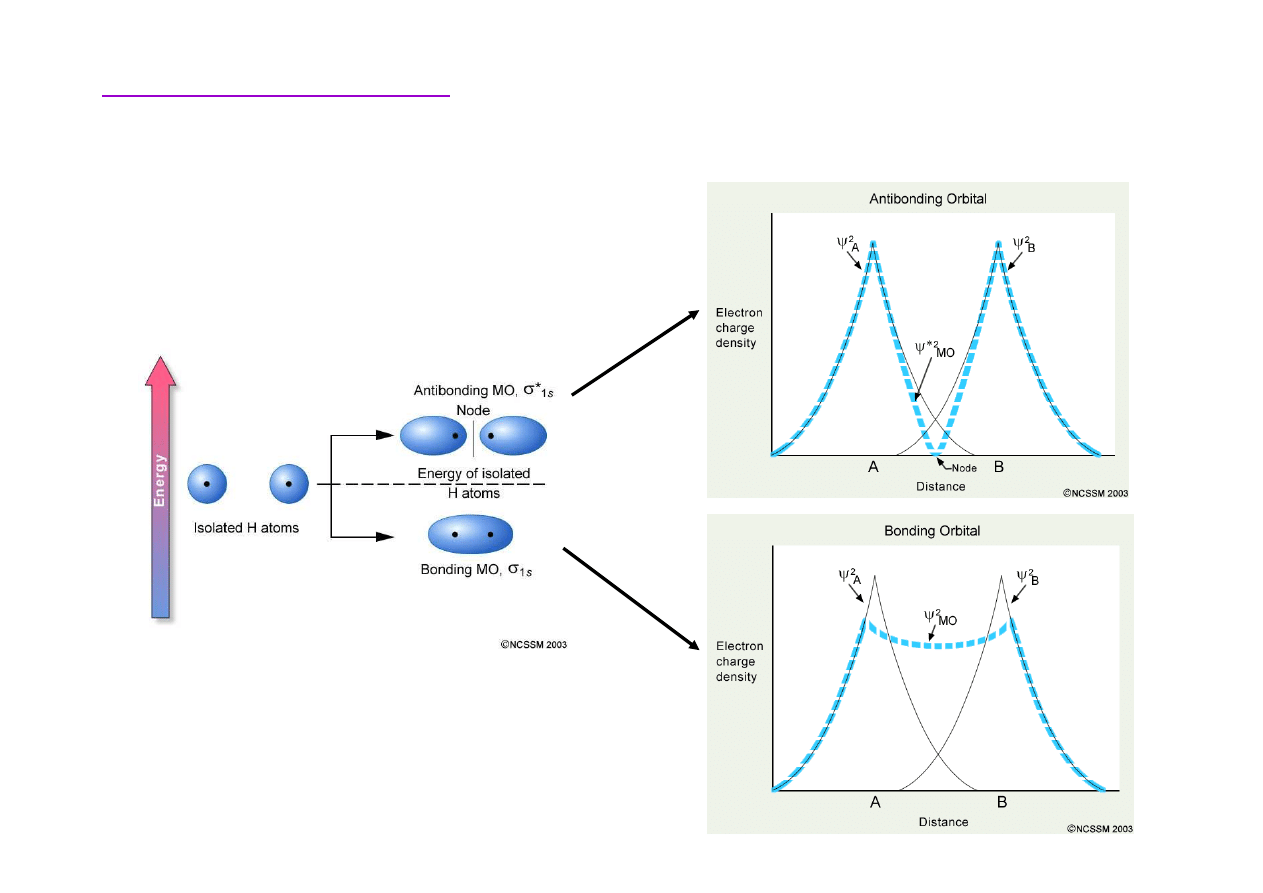
Orbitale molekularne
Podstawy chemii organicznej
http://www.dlt.ncssm.edu/tiger/chem3.html
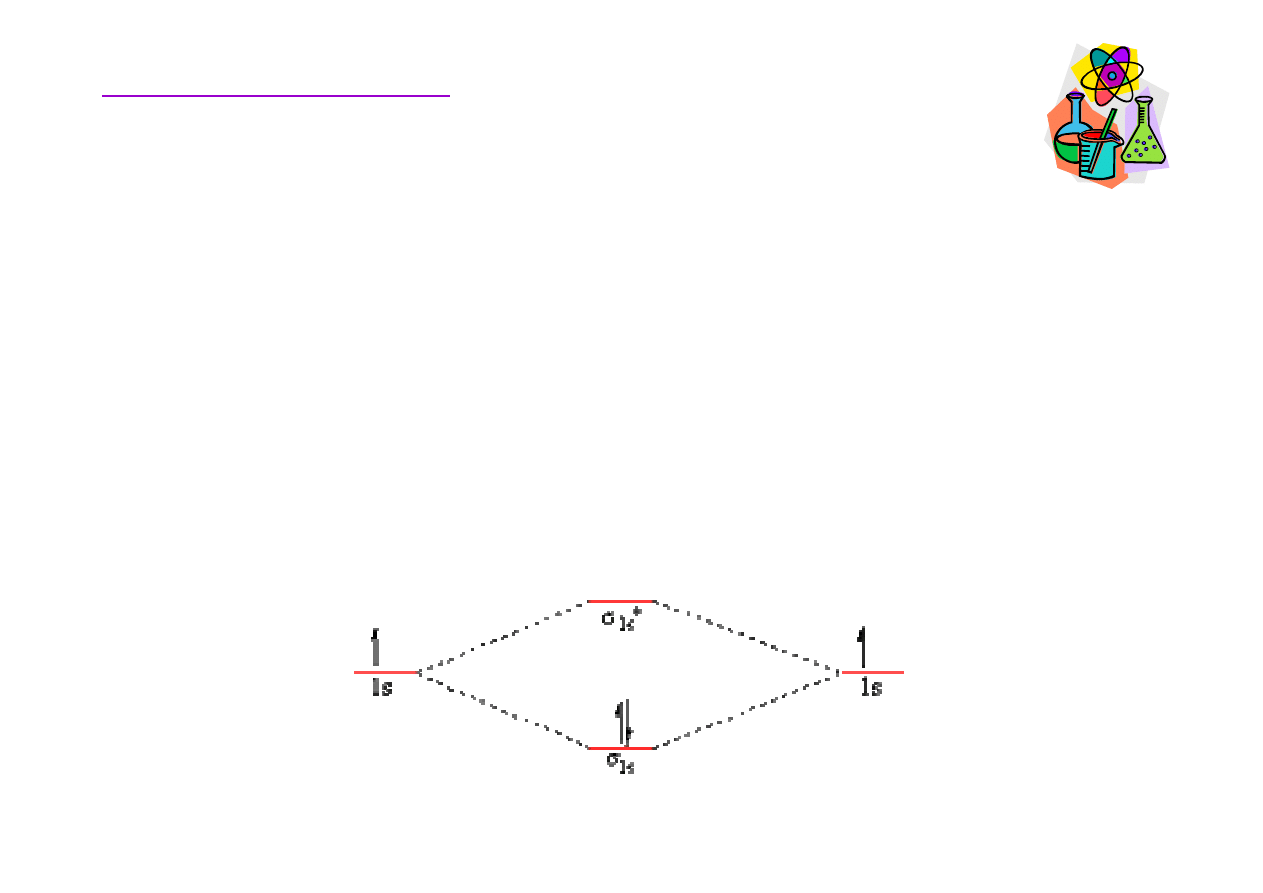
Orbitale molekularne –wi
ą
zanie
σ
• molekularny orbital wi
ąż
acy (
σ
MO)- elektrony znajduj
ą
si
ę
przez wi
ę
kszo
ść
czasu w rejonie pomi
ę
dzy dwoma
j
ą
drami.
• molekularny orbital antywi
ąż
acy (
σ
* MO)- elektrony
znajduj
ą
si
ę
przez wi
ę
kszo
ść
czasu w rejonie poza
przestrzeni
ą
pomi
ę
dzy dwoma j
ą
drami
Podstawy chemii organicznej
http://chemed.chem.purdue.edu/genchem/topicreview/bp/ch8/mo.html
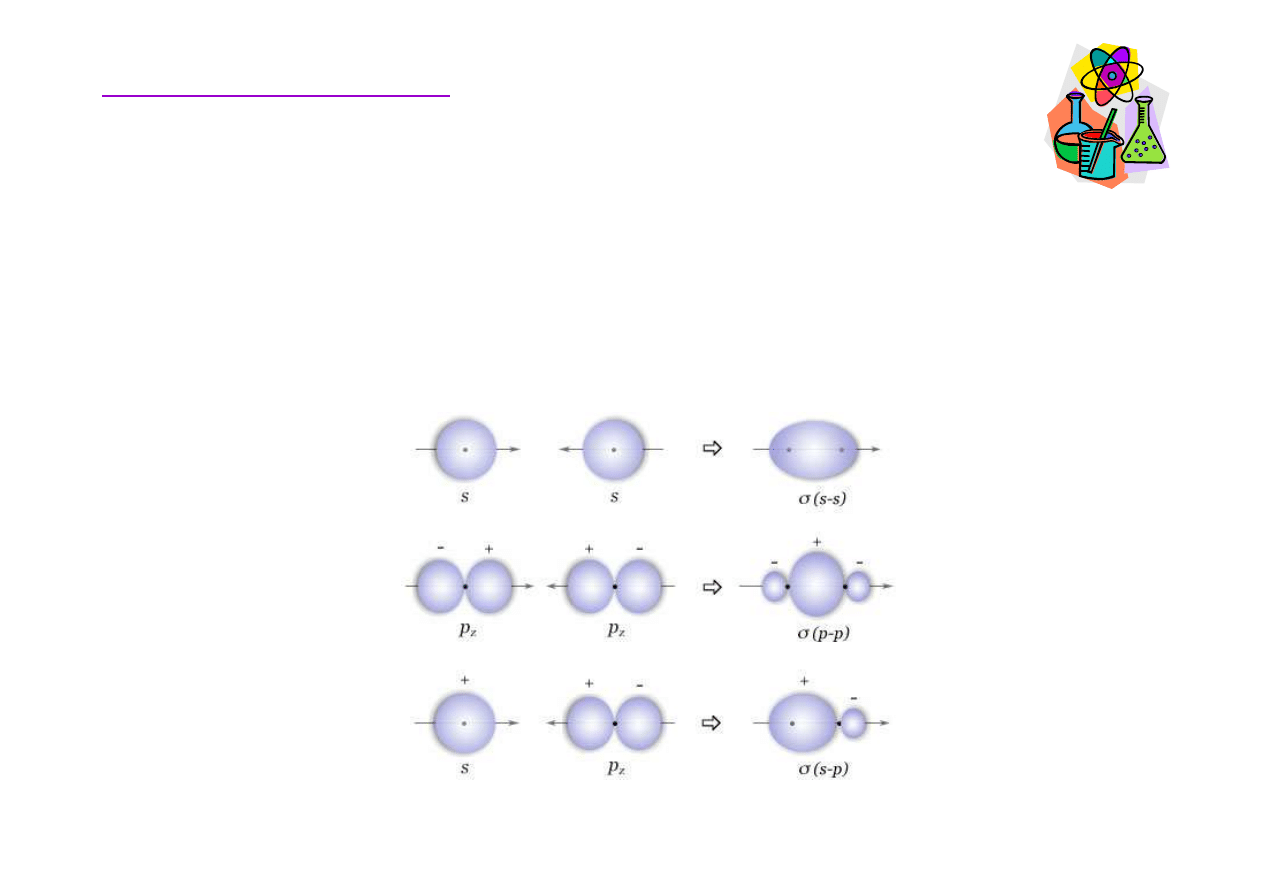
Orbitale molekularne –wi
ą
zanie
σ
Wi
ą
zania sigma (
σ
) to najsilniejszy typ wi
ą
zania
kowalencyjnego. Powstaj
ą
przez współosiowe nakładanie si
ę
orbitali atomowych typu s i p.
Podstawy chemii organicznej
http://en.wikipedia.org/wiki/Sigma_bond
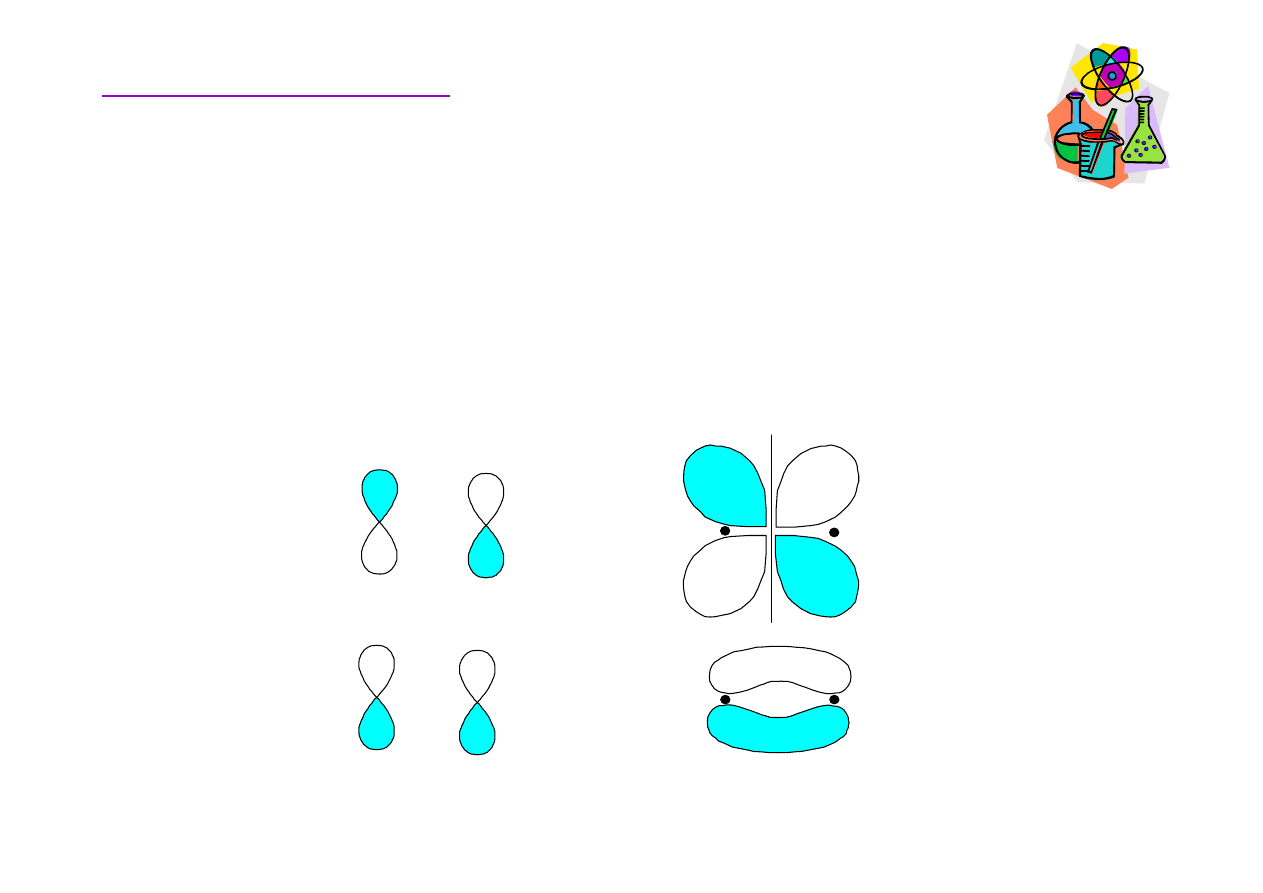
Orbitale molekularne –wi
ą
zanie
π
Wi
ą
zania Pi (
π
) powstaj
ą
poprzez boczne nakładanie si
ę
atomowych orbitali p.
Podstawy chemii organicznej
*
π
π
+
+
+
+
+
+
+
-
-
-
-
-
-
-
http://www.tch-pg.cba.pl/files/Isem/chemnieorg/5-OrbitalemolekTECH.doc

Orbitale molekularne –wi
ą
zania
π
i
σ
Wi
ą
zania
π
s
ą
słabsze od wi
ą
za
ń σ
. Wi
ą
zanie
π
pomi
ę
dzy
dwoma atomami pojawia si
ę
dopiero wtedy, gdy powstanie
wi
ą
zanie
σ
(wi
ą
zania podwójne i potrójne).
Podstawy chemii organicznej
E
n
e
rg
ia
σ
MO
σ
*MO
π
MO
π
* MO
wi
ążą
cy
antywi
ążą
cy

W
ę
giel
Ka
ż
dy atom w
ę
gla posiada 4 elektrony walencyjne, które
mo
ż
e dzieli
ć
z czterema innymi atomami, które go otaczaj
ą
→
atom w
ę
gla jest czterowarto
ś
ciowy.
http://www.chemistryland.com/CHM130W/11-Bonds/bonds.html
Podstawy chemii organicznej
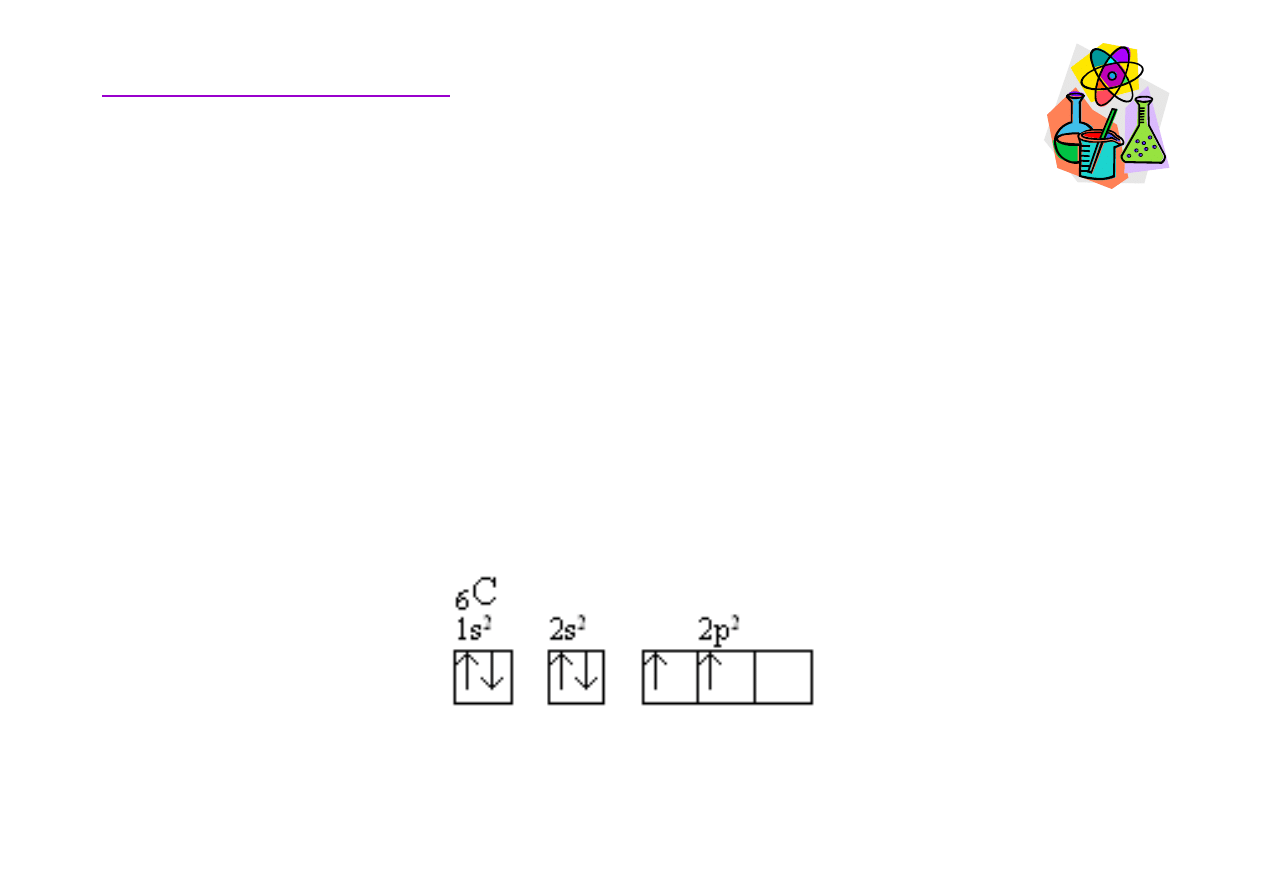
W
ę
giel
Atom w
ę
gla posiada cztery elektrony walencyjne, dwa na
orbitalu 2s i po jednym na orbitalach 2p
x
i 2p
y
, orbital 2p
z
jest pusty. Taka konfiguracja elektronowa wskazuje,
ż
e do
tworzenia wi
ą
za
ń
dost
ę
pne s
ą
tylko 2 elektrony.
Podstawy chemii organicznej
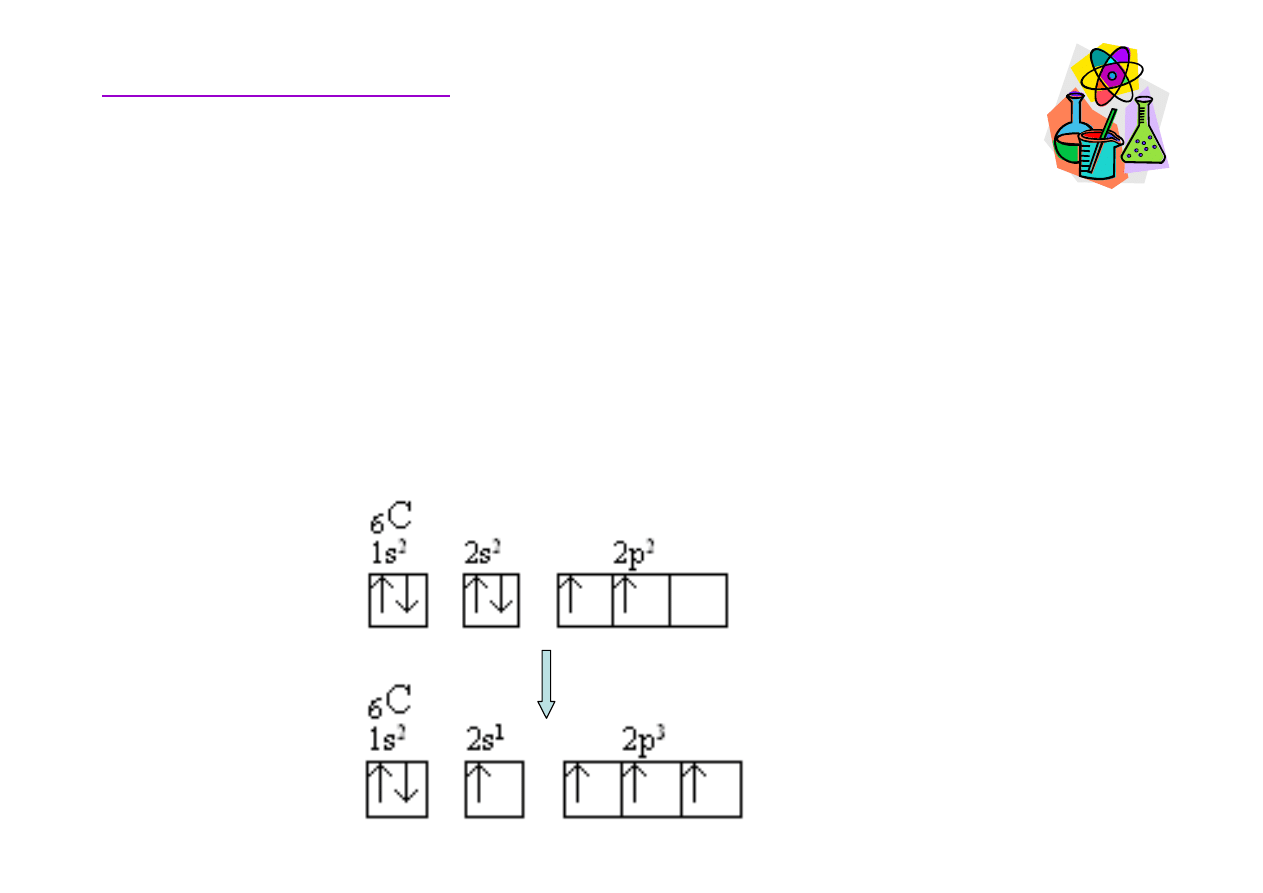
W
ę
giel
Jeden z elektronów z orbitalu 2s podczas tworzenia
wi
ą
zania jest przenoszony na pusty orbital 2p
z
(promocja
elektronu – wzbudzenie go na wy
ż
szy poziom
energetyczny), co powoduje,
ż
e w
ę
giel zyskuje cztery
niesparowane elektrony i mo
ż
e utworzy
ć
cztery wi
ą
zania.
Podstawy chemii organicznej
Konfiguracja elektronowa w
stanie podstawowym
Konfiguracja elektronowa w
stanie wzbudzonym
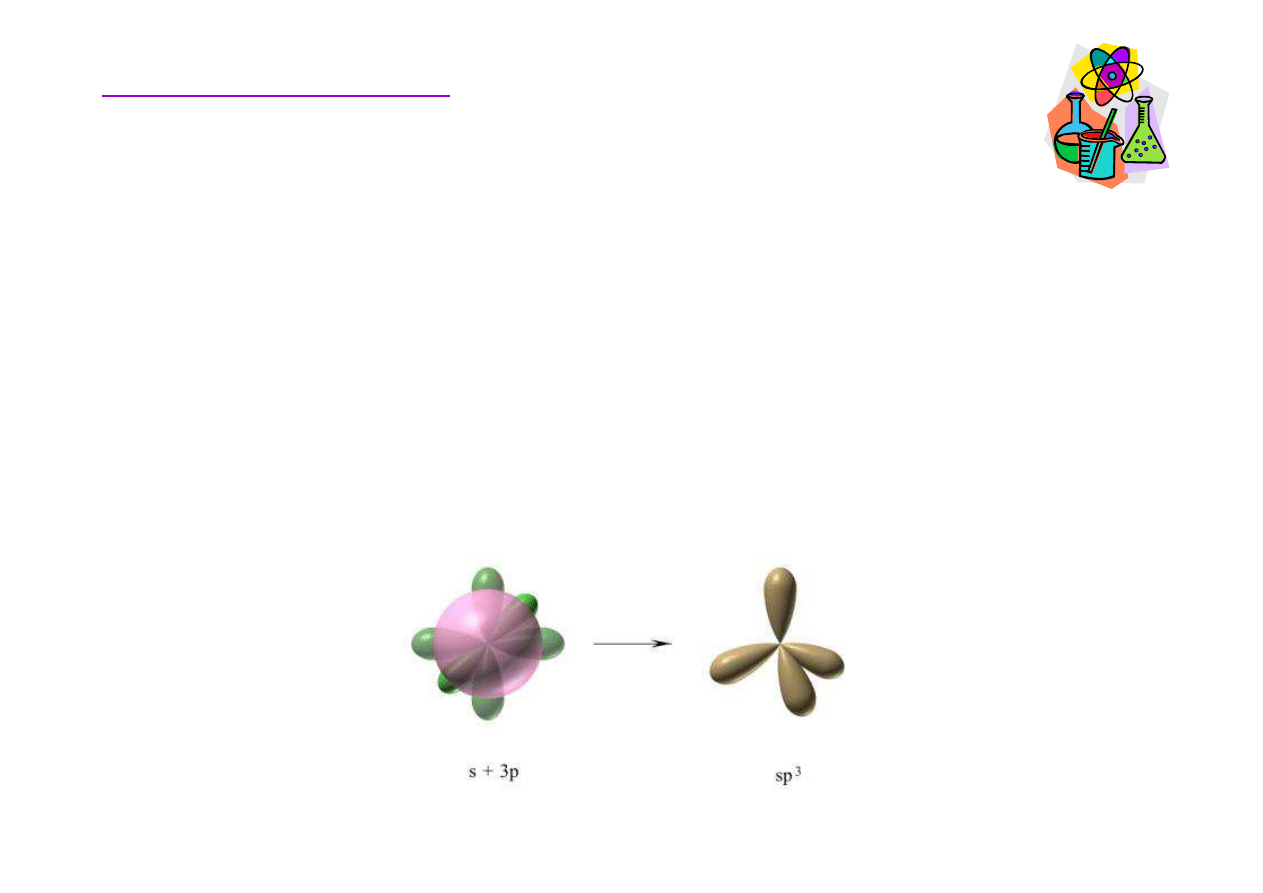
W
ę
giel - hybrydyzacja orbitali
W stanie wzbudzonym orbital 2s i trzy orbitale 2p (2p
x
, 2p
y
, 2p
z
)
nakładaj
ą
si
ę
na siebie (hybrydyzuj
ą
). W efekcie powstaj
ą
cztery równocenne energetycznie orbitale zhybrydyzowane
sp
3
. Proces ten ma miejsce tylko podczas tworzenia wi
ą
za
ń
i
jest nazywany hybrydyzacj
ą
orbitali.
Podstawy chemii organicznej
http://zasoby1.open.agh.edu.pl/dydaktyka/chemia/a_e_chemia/1_3_budowa_materii/01_04_03_2b.html
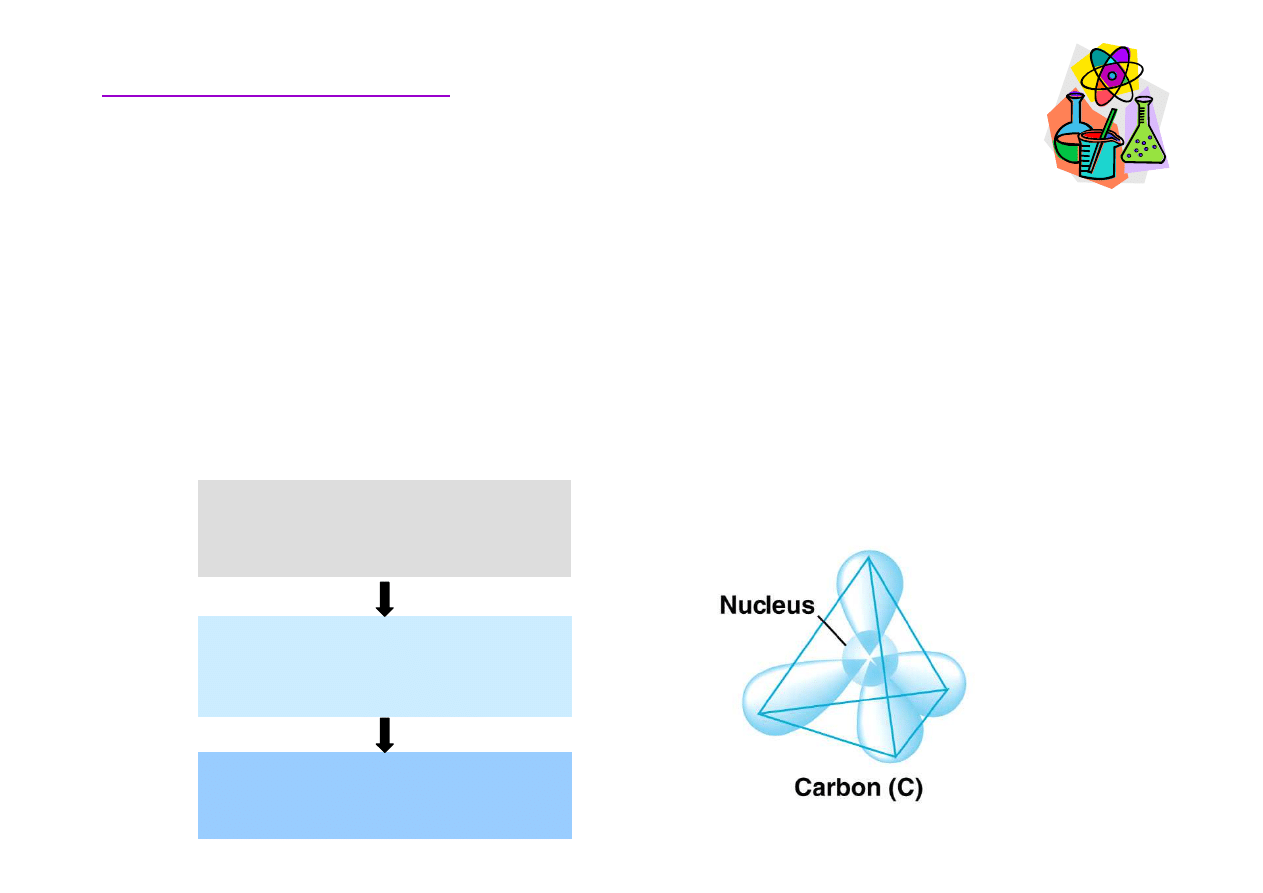
W
ę
giel - hybrydyzacja orbitali
Hybrydyzacja
→
nakładanie si
ę
(mieszanie) orbitali
atomowych podczas tworzenia si
ę
wi
ą
za
ń
, w wyniku czego
powstaj
ą
orbitale zhybrydyzowane (ró
ż
ni
ą
ce si
ę
kształtem i
energi
ą
od wyj
ś
ciowych orbitali atomowych).
Podstawy chemii organicznej
2p
z
2p
y
2p
x
2s
1s
↑
↑
↑↓
↑↓
C
sp
3
sp
3
sp
3
sp
3
1s
↑
↑
↑
↑
↑↓
C*
2p
z
2p
y
2p
x
2s
1s
↑
↑
↑
↑
↑↓
C*
http://iws.collin.edu/biopage/faculty/mcculloch/1406/outlines/chapter%204/Ma2-6.JPG

Dzi
ę
kuj
ę
za uwag
ę
Wyszukiwarka
Podobne podstrony:
chemia 2014 odp
Arkusz CKU Chemia 2014
chemia 2014 kolos, lekarski, I rok, chemia, kolos - teoria
Chemia 3 2014
Zagadnienia chemia 2014, żcioż, III semestr, Chemia żywności
chemia 7 2014
chemia 2 2014
chemia 2014
chemia 2014 odp
Arkusz CKU Chemia 2014
chemia 2014 operon probna rozszerzona odpowiedzi
chemia 2014 maj matura rozszerzona
Pytania z wejściówek, analityka medyczna UMP 2014, chemia fizyczna, ćwiczenia
arkusz 2 opm chemia z tutorem 12 06 2014 klasy przedmaturalne
WF-Zagadnienia Egz-22.05.2014, rok numero uno, chemia nieorganiczna
Rzeczy których nie ma u piegusa wykład chemia( 02 2014
Sprawozdanie 2 Badanie właściwości i analiza jakościowa anionów, Politechika Białostocka, budownictw
więcej podobnych podstron