Badanie wyników nauczania z chemii. Poziom r
ozszerzony
Copyright by ZamKor spółka z ograniczoną odpowiedzialnością S.K.A., Kraków 2014
Z
K
am
or
1
MODEL
ODPOWIEDZI I SCHEMA
T PUNKT
OW
ANIA
W
ażne doświadczenia – poziom r
ozszerzony
Zadanie
Odpowiedzi
Uwagi
Punktacja
za czynność
za
zadanie
1
– za poprawnie wskazaną obserwację:
Obserwacja:
Zawartość zlewki uległa r
ozdzieleniu na dwie warstwy
/
Otrzymano klar
owny
roztwór
.
1.1
1
1
2
– za poprawnie uzupełniony wniosek i poprawne uzasadnienie:
Wniosek: Metanol
bardzo dobrze r
ozpuszcza się
/
praktycznie nie r
ozpuszcza się
w wodzie.
Uzasadnienie:
Cząsteczka metanolu ma budowę polarną, dlatego metanol dobrze
rozpuszcza się w r
ozpuszczalniku polarnym
.
lub Między cząsteczkami metanolu i cząsteczkami wody tworzą się wiązania wodor
owe.
lub inne poprawnie sformułowane uzasadnienie odnoszące się do budowy cząsteczki metanolu
2.1
1
1
3
– za wybór odpowiedniej metody rozdziału:
destylacja
3.1
1
1
4
– za poprawnie sformułowane obserwacje:
W
ydziela się (bezbarwny) gaz o charakterystycznym zapachu
.
4.1
1
1
Dokument pobrany przez: 25087af0d481e50d7a52e9c006498b9824f8a75b
Badanie wyników nauczania z chemii. Poziom r
ozszerzony
Copyright by ZamKor spółka z ograniczoną odpowiedzialnością S.K.A., Kraków 2014
Z
K
am
or
2
5
– za poprawną metodę rozwiązania – za obliczenia i wynik z jednostką:
6,9 cm
3
Przykładowe r
ozwiązanie
:
n = 0,5 ∙ 0,2 = 0,1 mol
1 mol — 63 g
0,1 mol —
m
s
=>
m
s
= 6,3 g
C
p
= 65%
czyli
65 g — 100 g roztw
.
6,3 g —
m
r
=>
m
r
= 9,7 g
V
r
=
=
97
14
,
,
g g cm
3
6,
9c
m
3
lub inny prawidłowy sposób rozwiązania
5.1
1 1
3
– za poprawnie uzupełniony opis czynności:
Kolbę miarową o objętości 500 cm
3
napełnić do połow
y wodą destylowaną. Za pomocą
pipety odmierzyć i dodać
6,9
cm
3
65-proc. kwasu azotowego(V). Zawartość kolby
wymieszać, a następnie
dodawać (por
cjami) wodę ze zlewki. Ostatnie kr
ople wody dodać
za pomocą pipety aż do kr
eski (menisk dolny)
. Kolbę zamknąć korkiem i wymieszać jej
zawartość.
lub inaczej poprawnie sformułowane czynności; uczniom należy zwrócić uwagę na celowość użytego sprzętu laboratoryjnego
5.2
1
6
a) za poprawne uzupełnienie obu zdań:
Wskazanie wagi, na której znajdował się sód, (
wzr
osło
,
zmalało ,
nie uległo zmianie ).
Wskazanie wagi, na której znajdował się jod, ( wzrosło ,
zmalało
,
nie uległo zmianie ).
6.1
1
2
b) za poprawnie sformułowane uzasadnienie:
Sód jest bardzo aktywny – r
eaguje z zawartym w powietrzu tlenem (tworząc nadtlenek
sodu), dlatego wskazanie wagi wzr
osło.
Jod ulega sublimacji, dlatego wskazanie wagi zmalało.
lub inaczej poprawnie sformułowane uzasadnienie
6.2
1
Dokument pobrany przez: 25087af0d481e50d7a52e9c006498b9824f8a75b
Badanie wyników nauczania z chemii. Poziom r
ozszerzony
Copyright by ZamKor spółka z ograniczoną odpowiedzialnością S.K.A., Kraków 2014
Z
K
am
or
3
7
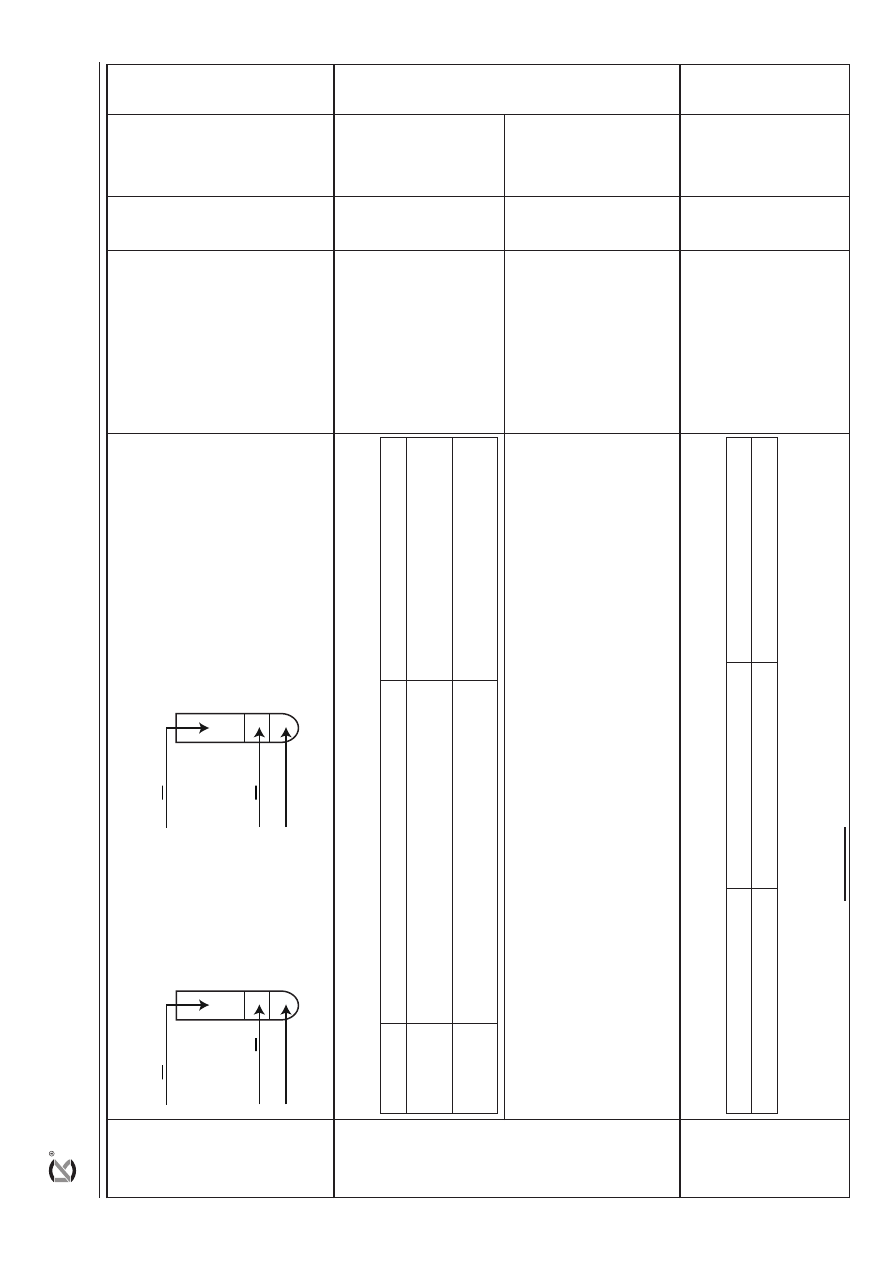
– za poprawne uzupełnienie schematu doświadczenia:
C
/ D
C
/ D
A /
B
1.
2.
A
/ B
CHCl
3
CHCl
3
7.1
1
1
8
a) za poprawne uzupełnienie wiersza tabeli:
Probówka
Sposób identyfikacji wydzielającego się gazu
Równanie reakcji/zapis procesu
1
Do wylotu pr
obówki przyłożyć palące się
łuczywko.
2H
2
+ O
2
→ 2H
2
O
2
Do wylotu pr
obówki zbliżyć zwilżony wodą
uniwersalny papier
ek wskaźnikowy
.
SO
2
+ H
2
O
→ ←
HSO
3
–
+ H
+
lub zapis: SO
2
+ H
2
O
→ ←
H
2
SO
3
H
2
SO
3
→ ←
HSO
3
–
+ H
+
HSO
3
–
→ ←
SO
3
2–
+ H+
8.1
2 × 1
3
b) za poprawne określenie barw otrzymanych roztworów:
Probówka 1:
jasnozielona (zielona) przechodząca w żółtobrunatną
Probówka 2:
bezbarwna
– za wyłączne określenie barwy jako „jasnozielona” uczeń otrzymuje punkt – za wyłączne określenie barwy jako „żółtobrunatna” uczeń nie otrzymuje punktu
8.2
1
9
– za poprawne uzupełnienie tabeli i uzupełnienie zdania:
Probówka 1
Probówka 2
Probówka 3
Reakcja nie zachodzi.
MnO + 2H
+
→ Mn
2+
+ H
2
O
Reakcja nie zachodzi.
Charakter chemiczny tlenku manganu(II):
kwasowy
/
amfoteryczny
/
zasadowy
/
obojętny
.
9.1
1
1
Dokument pobrany przez: 25087af0d481e50d7a52e9c006498b9824f8a75b
Badanie wyników nauczania z chemii. Poziom r
ozszerzony
Copyright by ZamKor spółka z ograniczoną odpowiedzialnością S.K.A., Kraków 2014
Z
K
am
or
4
10
a) za poprawne określenie barwy i poprawne uzasadnienie obserwacji:
Barwa wskaźnika:
czerwona (pomarańczowoczerwona)
Uzasadnienie:
Mn
2+
+ 2H
2
O
→ ←
Mn(OH)
2
+ 2H
+
10.1
1
3
b) za poprawne uzupełnienie wiersza tabeli:
Obserwacja
Równanie reakcji
Bezpośrednio po
dodaniu NaOH
(aq)
W
ytrącił się biały osad.
MnCl
2
+ 2NaOH → Mn(OH)
2
+ 2NaCl
Po upływie kilku godzin
(Przy powierzchni) biały osad zmienił barwę na brunatną.
2Mn(OH)
2
+ O
2
→ 2MnO
2
+ 2H
2
O
lub zapis:
2Mn(OH)
2
+ O
2
→
→
2MnO(OH)
2
2Mn(OH)
2
+ O
2
→
→
2(MnO
2
∙ H
2
O)
10.2
2 × 1
11
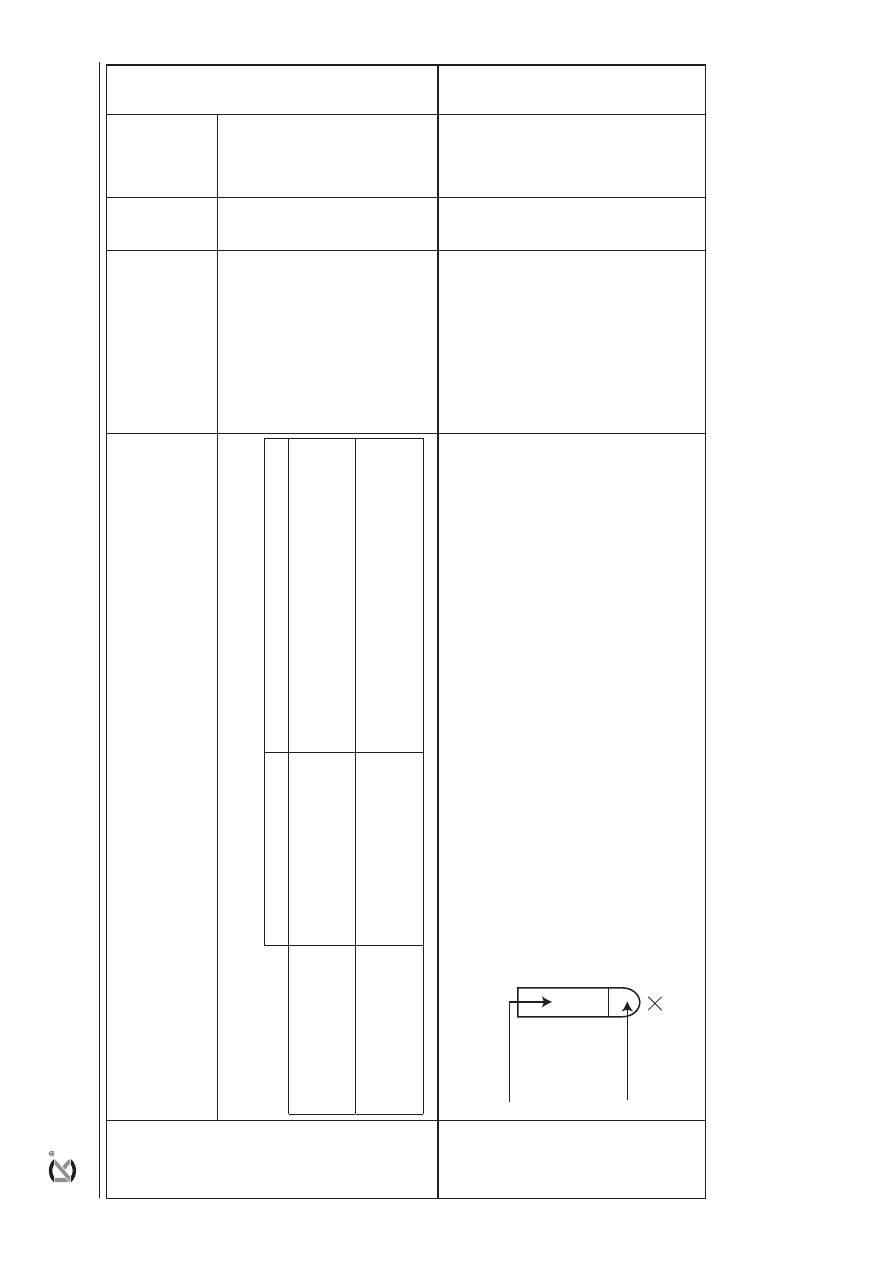
– za poprawne uzupełnienie schematu i podanie nazwy jonów:
Cr
3+
H
2
O
2
,
O
H
–
Nazwa jonów:
(aniony) chr
omianowe(VI)
11.1
1
1
Dokument pobrany przez: 25087af0d481e50d7a52e9c006498b9824f8a75b
Badanie wyników nauczania z chemii. Poziom r
ozszerzony
Copyright by ZamKor spółka z ograniczoną odpowiedzialnością S.K.A., Kraków 2014
Z
K
am
or
5
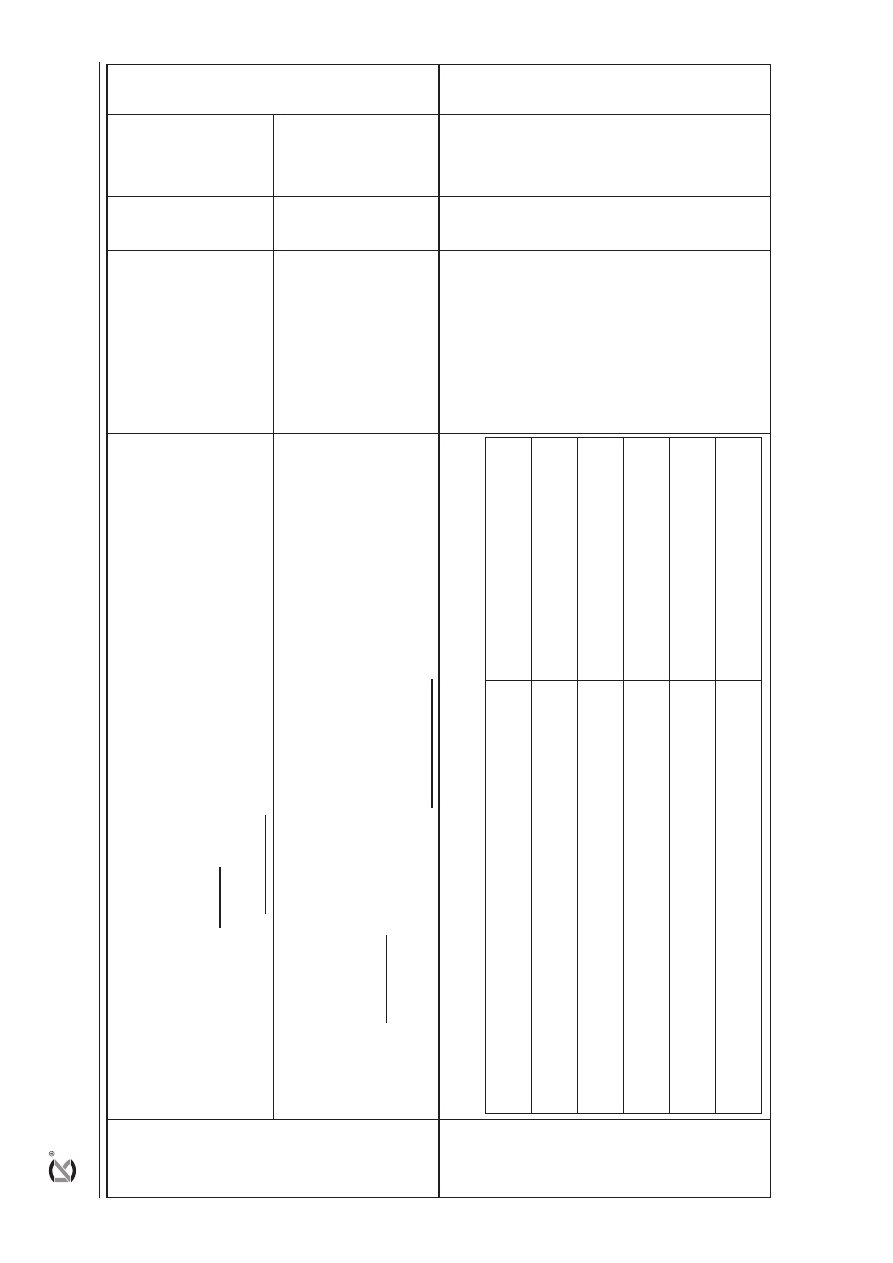
12
a) za wskazanie odpowiednich numerów zlewek oraz określenie typu i mechanizmu reakcji:
Numer / numery zlewek:
2,
5
Typ reakcji:
substytucja
/
addycja
Mechanizm:
nukleofilowy
/
elektr
ofilowy
/
wolnor
odnikowy
12.1
1
2
b) za wskazanie odpowiednich numerów zlewek oraz określenie typu i mechanizmu reakcji:
Numer / numery zlewek:
1,
4
Typ reakcji:
substytucja
/
addycja
Mechanizm:
nukleofilowy
/
elektr
ofilowy
/
wolnor
odnikowy
12.2
1
13
– za poprawne uzupełnienie tabeli:
Charakterystyka
Oznaczenie literowe związku
spełniającego warunek
W
odny roztwór tej substancji przewodzi prąd elektryczny
.
C, E
W
odny roztwór tej substancji wykazuje odczyn obojętny
.
A, B, D
Po dodaniu zawiesiny Cu(OH)
2
do roztworu tej substa
ncji
i wymieszaniu powstaje klarowny
, szafirowy roztwór
.
B, D
Po dodaniu zawiesiny Cu(OH)
2
do roztworu tej substa
ncji
i ogrzaniu powstaje pomarańczowoczerwony osad.
D
Reaguje z zasadą sodową.
C, E
13.1
za 5
poprawnych uzupełnień
– 2 pkt
za 3–4 poprawne
uzupełnienia
– 1 pkt
za 0–2 poprawne
uzupełnienia
– 0 pkt
2
Dokument pobrany przez: 25087af0d481e50d7a52e9c006498b9824f8a75b
Badanie wyników nauczania z chemii. Poziom r
ozszerzony
Copyright by ZamKor spółka z ograniczoną odpowiedzialnością S.K.A., Kraków 2014
Z
K
am
or
6
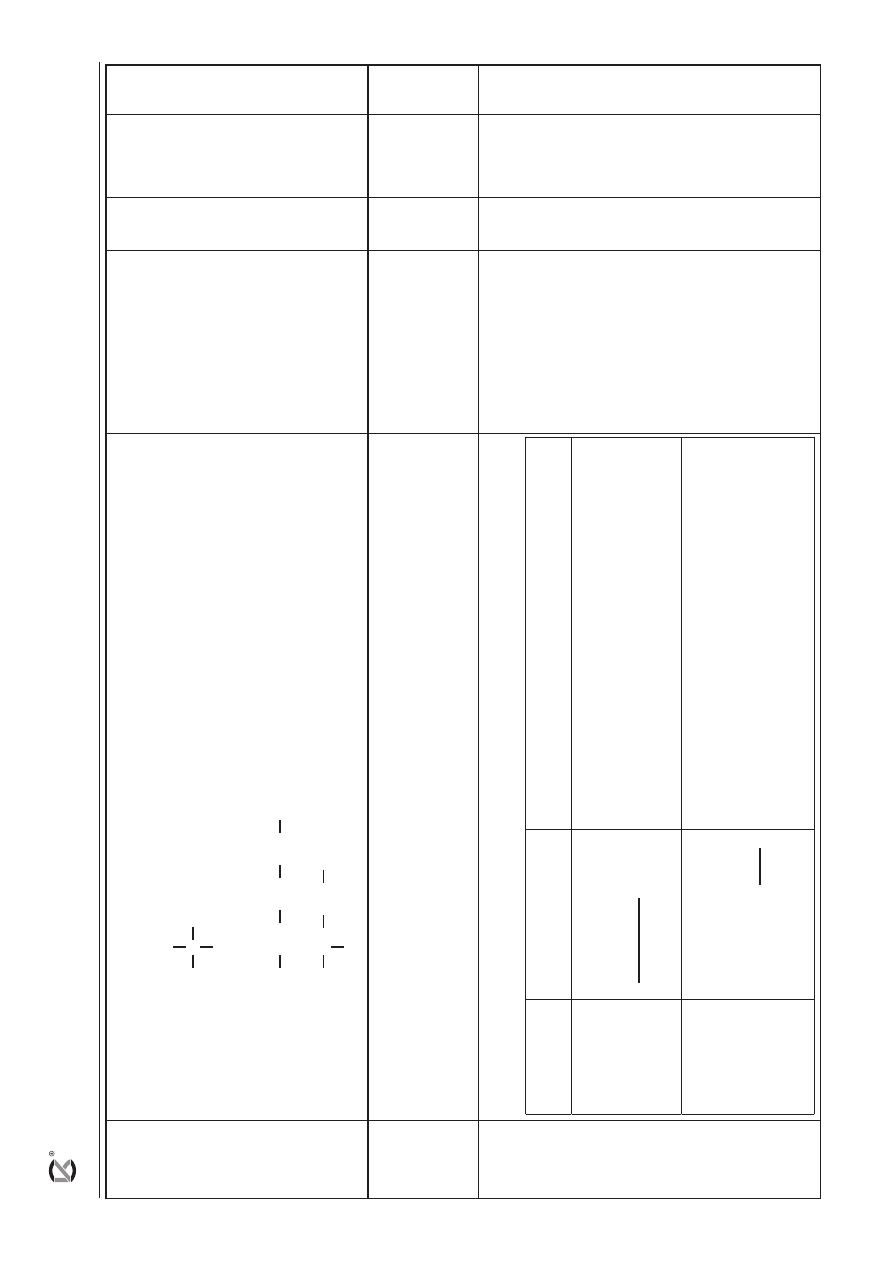
14
– za poprawnie narysowane wzory półstrukturalne (grupowe) zidentyfikowanych alkoholi:
Alkohol nr 1:
CH
3
CH
3
CH
3
OH
C
Alkohol nr 2:
CH
3
CH
2
OH
CH
2
CH
2
Alkohol nr 3:
CH
3
CH
OH
CH
2
CH
3
14.1
1
1
15
– za poprawne uzupełnienie obserwacji:
Obserwacje:
W
obu pr
obówkach wydziela się (bezbarwny
, bezwonny) gaz.
Intensywniejsze wydzielanie gazu widać w pr
obówce, do któr
ej wlano kwas mrówkowy
.
lub inaczej poprawnie sformułowane obserwacje umożliwiające odróżnienie kwasów
15.1
1
1
16
– za poprawne uzupełnienie wiersza tabeli:
Zlewka
z
roztworem
Barwa wskaźnika
Uzasadnienie
HCl
bezbarwny
,
żółty
(W
r
oztworze kwasu stężenie jonów H
+
jest
duże) zgodnie z
r
egułą przekory układ dąży do
zmniejszenia
stężenia
jonów H
+
–
stan równowagi
reakcji przesuwa się w
lewo – w
str
onę formy
niezdysocjowanej.
NaOH
bezbarwny
,
żółty
(W
r
oztworze zasady stężenie jonów OH
–
jest
duże → łączą się one z
jonami H
+
, zmniejszając
ich stężenie) zgodnie z
r
egułą przekory układ
dąży do zwiększenia stężenia jonów H
+
– stan
równowagi r
eakcji przesuwa się w
prawo
–
w
str
onę formy zdysocjowanej.
lub inne poprawnie sformułowane uzasadnienie odnoszące się do reguły przekory
16.1
2 × 1
2
Dokument pobrany przez: 25087af0d481e50d7a52e9c006498b9824f8a75b
Badanie wyników nauczania z chemii. Poziom r
ozszerzony
Copyright by ZamKor spółka z ograniczoną odpowiedzialnością S.K.A., Kraków 2014
Z
K
am
or
7
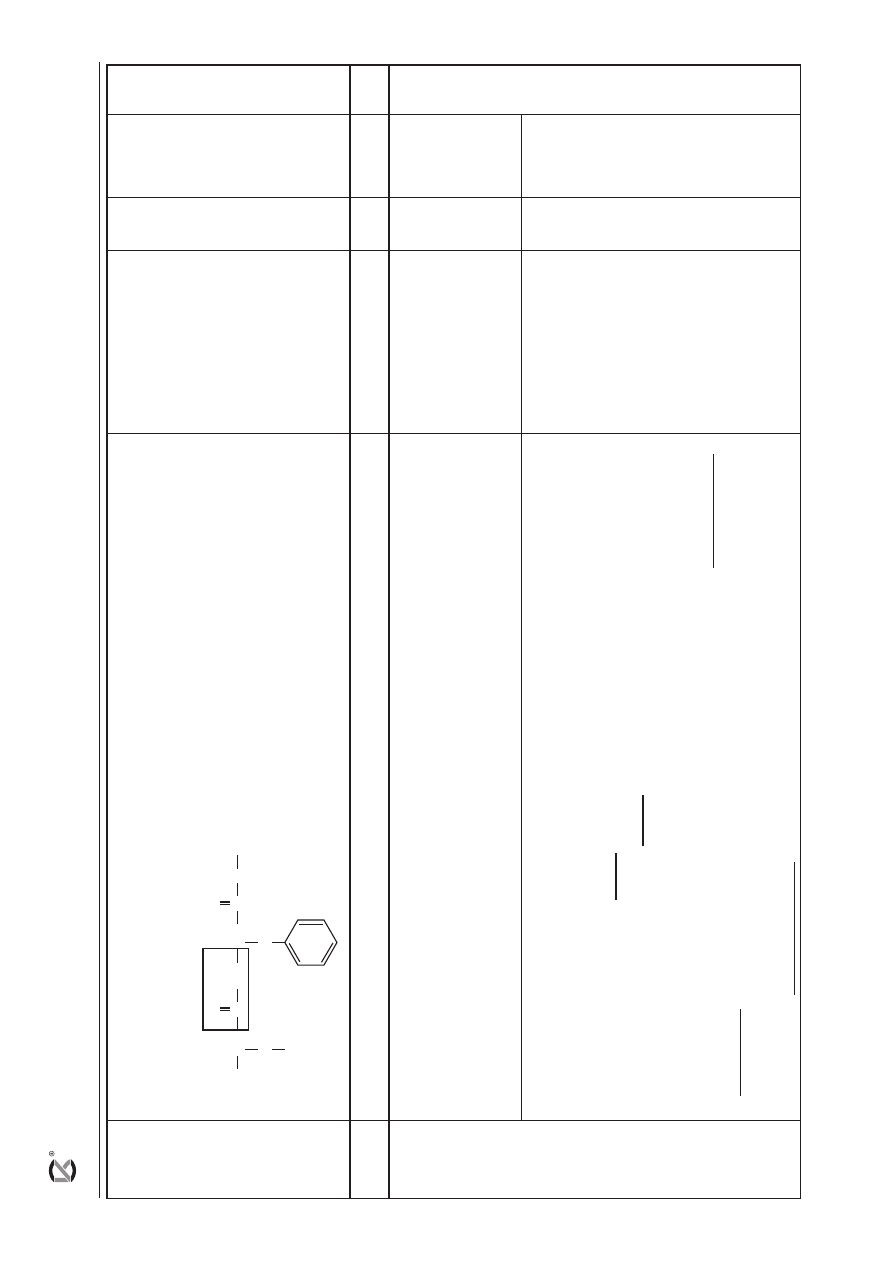
17
– za wybór odpowiedniego odczynnika oraz zaznaczenie odpowiedniego fragmentu w
cząsteczce związku:
Odczynnik:
świeżo strącony wodor
otlenek miedzi(II)
H
2
N
O
CH
COOH
CH
2
NH
C
O
CH
CH
2
C
O
CH
3
17.1
1
1
18
– za wybór wzoru odpowiedniej substancji:
KOH
18.1
1
1
19
a) za obliczenia prowadzące do wskazania odpowiedniego półogniwa i poprawny zapis schematu ogniwa:
SEM = E
K
– E
A
=>
E
A
= E
K
– SEM = –0,26 – 1,43 = –1,69V
=>
elektrodę ujemną
stanowi
glin
Schemat ogniwa:
Al |
Al
3+
|| Ni
2+
| Ni
19.1
1
2
b) za poprawnie uzupełnione obserwacje:
1. Podczas pracy tego ogniwa:
a) masa elektrody dodatniej (
rośnie
,
maleje ,
nie ulega zmianie ).
b) masa elektrody ujemnej ( rośnie ,
maleje
,
nie ulega zmianie ).
2. Podczas pracy tego ogniwa:
a)
w półogniwie dodatnim barwa roztworu ( staje się bardziej intensywna
,
staje się mniej
intensywna
,
nie ulega zmianie ).
b)
w półogniwie ujemnym barwa roztworu ( staje się bardziej intensywna
,
staje się mniej
intensywna
,
nie ulega zmianie
).
19.2
1
Dokument pobrany przez: 25087af0d481e50d7a52e9c006498b9824f8a75b
Wyszukiwarka
Podobne podstrony:
doswiadczenia model rs 6 1392900786
doswiadczenia arkusz rs 6 1392900606
obliczenia model rs 5 1392900934
organiczna 2 model rs 4 1392901170
organiczna 1 model rs 3 1392901271
nieorganiczna 2 model rs 2 1392901381
doswiadczenia arkusz rs 6 1392900606
obliczenia model rs 5 1392900934
organiczna 2 model rs 4 1392901170
nieorganiczna 2 model rs 2 1392901381
doswiadczenia arkusz rs 6 1392900606
obliczenia model rs 5 1392900934
obliczenia arkusz rs 5 1392900864
nieorganiczna 2 arkusz rs 2 1392901336
organiczna 2 arkusz rs 4 1392901126
obliczenia arkusz rs 5 1392900864
więcej podobnych podstron