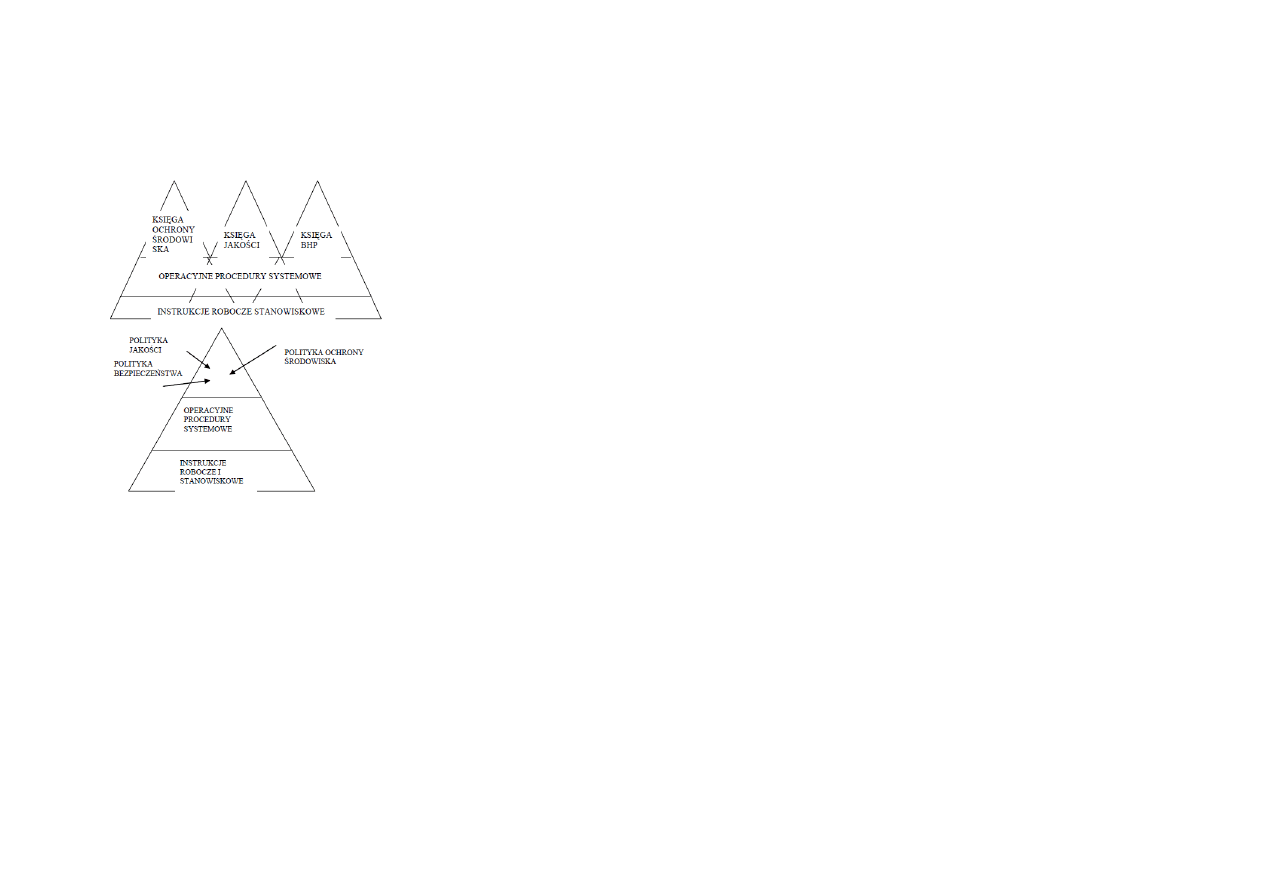
CZĘŚD I – ZINTEGROWANY SYSTEM ZARZĄDZANI
Elementy :
1.
System Zarządzania Jakością (ISO 9000:2001)
2.
System Zarządzania Środowiskiem (ISO 14001:1998)
3.
System Zarządzania BHP (ISO 18001:2004)
TPM – Total Productive Maintenance
Eliminacja 6 dużych strat poprzez prace w wielofunkcyjnych zespołach – Focused Improvement
1.
Formalne włączenie pracowników produkcji w pomoc przy utrzymaniu ruchu
2.
Zbudowanie systemu planowanych przeglądów, konserwacji i prewencji
3.
Podnoszenie wiedzy i umiejętności operatorów i pracowników Działu Utrzymania Ruchu
poprzez szkolenia
4.
Zbudowanie systemu zapewniającego projektowanie/zakup/produkcję łatwego w obsłudze
i utrzymaniu sprzętu
CZĘŚD II – NORMA ISO 18001:2004
Oparta na rozporządzeniu Ministra Pracy i Polityki Socjalnej w sprawie ogólnych przepisów BHP.
Nowelizacja z 2007 regulowała zawartości dokumentacji oceny ryzyka zawodowego.
Regulacje normy ISO 18001
1.
Ocenianie i dokumentowanie ryzyka zawodowego związanego z pracą
2.
Stosowanie niezbędnych środków profilaktycznych zmniejszających ryzyko zawodowe
(organizacja bezpiecznego miejsca pracy oraz oddziaływaniem środowiska pracy)
3.
Likwidacja zagrożeo dla zdrowia i życia pracownika (zmiana technologii, maszyn itd.)
4.
Informowanie pracowników o ryzyku zawodowym i zasadami ochrony
5.
Konsultowanie z pracownikami działao związanych z BHP (ryzyko przy pracach)
Ryzyko zawodowe:
Prawdopodobieostwo z jakim ktoś może zostad poszkodowany w związku z istniejącym zagrożeniem w
środowisku pracy(czynniki chemiczne, hałas i drgania mechaniczne, ręczne prace transportowe,
czynniki biologiczne)
Czynniki chemiczne (wymagania zawarte w rozporządzeniu MZ z 2004 r.)
1.
Listy wszystkich substancji znajdujących się na stanowisku pracy i sąsiednich
2.
Identyfikacja (informacje)
a.
Właściwości niebezpieczne
b.
Zagrożeo związanych z występowaniem czynnika chemicznego (karta
charakterystyki od dostawcy) dotyczących :
Scenariuszy narażenia, rodzaju, poziomu i czasu jego trwania
Wartości najwyższych dopuszczalnych stężeo w środowisku pracy i materiale
biologicznym
Efektów działao zapobiegawczych, wyników oceny stanu zdrowia pracowników
Warunków pracy przy odczynnikach z uwzględnieniem ich ilości
Szacowanie poziomu ryzyka zawodowego:
NDS/NDS (najwyższe dopuszczalne stężenie/natężenie występujące w czasie 8-
godzinnego, dobowego oraz tygodniowego czasu pracy; wytyczna dla projektantów-
technologów oraz w profilaktyce w zakładach pracy)
NDSP (w miejscu pracy)
NDSCh (najwyższe dopuszczalne stężenie chwilowe – nie dłużej niż 15 min i 2x na zmianę)
Środki o nieustalonych wartościach dopuszczalnych klasyfikuje się w oparciu o 3 zmienne :
1)
Podstawowe zagrożenie daną substancją chemiczną
2)
Skłonności do przedostawania się substancji do środowiska
3)
Ilośd substancji użyta w danej operacji
Zapewnienie bezpiecznych warunków pracy
Ograniczanie ryzyka zawodowego
Przeprowadzenie oceny ryzyka zawodowego
Likwidowanie zagrożeo u źródeł
Dostosowanie warunków i procesów pracy do możliwości pracownika
Stosowanie nowych rozwiązao technicznych
Wymiana niebezpiecznych elementów i procesów na bezpieczniejsze
Priorytet środków ochrony zbiorowej nad indywidualną
Instruowanie pracowników o BHP
Dokumentacja oceny ryzyka zawodowego:
Opis ocenianego stanowiska pracy, w tym wyszczególnienie stosowanych maszyn, narzędzi i
materiałów, wykonywanych zadao, czynników szkodliwych na stanowisku a także osób na tym
stanowisku. Kolejnymi elementami są wyniki, data oraz osoby zatwierdzające.
Wartości najwyższych dopuszczalnych stężeo
C
Działanie żrące
I
Działania drażniące
A
Działanie uczulające
Kat. 1 lub kat. 2
Działanie rakotwórcze
Ft
Działanie toksyczne na płód
Sk
Wchłaniające się przez skórę
Istnieje również Ps czyli współczynnik narażenia umożliwiający ocenę stężenia średniego ważonego dla
całej zmiany roboczej. Ps < 0,5 NDS ma zastosowanie gdy substancja nie ma określonych NDSCh i
NDSP (odpowiednio do nich istnieją Pch – wskaźnika narażenia dla stężeo chwilowych i Pp – wskaźnik
dla stężeo pułapowych). Poziom ryzyka zawodowego w granicach 10^3 – 10^4 oznacza możliwośd
przyrostu dodatkowych zachorowao w liczbie 1 przypadek na 1000-10 000 osób narażonych.
Norma PN-N-18001:2004 – Zagrożenia
Definicje :
Zagrożenie – stan środowiska pracy mogący spowodowad wypadek/zagrożenie dla
zdrowia
Zagrożenie znaczące – mogące spowodowad poważne uszkodzenie zdrowia/śmierd
występujące w szczególności podczas wykonywania prac mocno niebezpiecznych lub
poważnej awarii
Zagrożenie potencjalnie wypadkowe - niebezpieczne zdarzenie związane z wykonywaną
pracą podczas którego nie dochodzi do urazów lub pogorszenia stanu zdrowia
System zarządzania higieną u bezpieczeostwem pracy
Częśd ogólnego systemu zarządzania organizacją obejmująca strukturę organizacyjną, planowanie,
odpowiedzialnośd, zasady postępowania, procesy i zasoby potrzebne do opracowania, wdrażania,
realizacji, przeglądu i utrzymywania polityki BHP. Systemowe pojmowanie BHP pozwala
uporządkowad wszystkie działania związane z BHP w oparciu o ideę pełnego zaangażowania ze strony
kierownictwa i pracowników.
Działania w obszarze BHP
1.
Opracowanie i ogłoszenie polityki i celów w zakresie BHP (wyraz zaangażowania
kierownictwa);
2.
Określenie odpowiedzialności i uprawnieo poszczególnych pracowników na rzecz BHP
3.
Zapewnienie właściwych szkoleo oraz motywowanie zespołu do BHP
4.
Organizacja sprawnego systemu komunikacji w zakresie BHP
5.
Ocena ryzyka zawodowego
6.
Opracowanie zasad reagowania na wypadki przy pracy
7.
Wdrażanie działao korygujących i zapobiegawczych związanych z BHP
8.
Monitoring i audit systemu zarządzania BHP
Polityka BHP
Ogólnie jest to deklaracja organizacji dotycząca jej intencji i zasad odnoszących się do ogólnych
efektów działalności w zakresie BHP określająca ramy do działania i ustalania celów dotyczących
zarządzania BHP.
Kierownictwo w trosce o zdrowie pracowników wdrożyło, utrzymuje i doskonali SZ BHP zgodny z
wymaganiami normy ISO 18001:2004, obowiązującymi przepisami prawnymi i wymaganiami BHP a
także własnymi planami i programami doskonalenia BHP. Tym samym kierownictwo deklaruje że
będzie dokonywad przeglądu tej polityki, celów i zadao aby weryfikowad je w stosunku do
zmieniających się warunków działalności, a także do analizy auditów, działao zapobiegawczych i
korygujących oraz nadzorowania ustanowionych zapisów i procedur.
Polityka ma kilka zadao, między innymi dbanie o podnoszenie poziomu świadomości i kwalifikacji w
BHP poprzez m.in. szkolenia, poprzez rozmowy kierownictwa z robotnikami zaangażowanie ich na
rzecz BHP oraz prowadzenie ciągłego doskonalenia w tym zakresie. Pomaga również zapewnid
odpowiednie środki finansowe, technologiczne, techniczna i organizacyjne dla jej realizacji, oraz
identyfikuje zagrożenia mające wpływ na bezpieczeostwo i zdrowie pracowników i zapobiega
wypadkom. W przypadku wystąpienia zdarzenia dotyczącego BHP posiada odpowiednie procedury.
Wartościowanie ryzyka
Stopieo szkód – S
Prawdopodobieostwo szkód - P
Poziom
Charakterystyka
Poziom
Charakterystyka
Znikome urazy
Lekkie szkody
Nieprawdopodobne
Lekkie obrażenia
Wymierne szkody
Mało prawdopodobne
1 raz na 10 lat
Ciężkie obrażenia
Znaczne szkody
Doraźne wydarzenie
1 raz na rok
Pojedyncze wypadki
śmiertelne
Ciężkie szkody
Dosyd częste wydarzenie
1 raz w miesiącu
Zbiorowe wypadki
śmiertelne
Szkody na dużą skalę na
terenie zakładu
Częste, regularne
wydarzenia
1 raz w tygodniu
Masowe wypadki
śmiertelne
Szkody na dużą skalę poza
terenem zakładu
Duże
prawdopodobieostwo
Wskaźnik ryzyka W = S x P
Rrisk score określa się z iloczynu R = E x S x P gdzie E jest ekspozycją na zagrożenie.
Ryzyko zaniedbywane
Brak jakichkolwiek działao
Ryzyko akceptowalne
Brak działao profilaktycznych
Ryzyko średnie
Działania profilaktyczne po uwzględnieniu ich kosztów (3-6 miesięcy)
Ryzyko poważne
Wstrzymanie pracy, redukcja w ciągu 1-3 msc.
Ryzyko nieakceptowalne
Wstrzymanie pracy do odpowiedniej redukcji zagrożenia
Korzyści
Jest to przede wszystkim spełnienie wymogów prawa pracy, oraz świadomośd tego jakie są zagrożenia
i ryzyko zawodowe a także wiedza o prawidłowości rozwiązao profilaktycznych. Wymiernymi
korzyściami są ulgi po wprowadzeniu zróżnicowane j składki finansowej oraz przy ubezpieczeniach
majątkowych. Działania profilaktyczne stają się systematyczne a nie intuicyjne co polepsza pozycję w
pertraktacjach i ewentualnych procesach o odszkodowania z tytułu np. wypadku w pracy

CZĘŚD III – BRANŻOWE NORMY ZARZĄDZANIA
Są to ogólnie normy które powstały w związku z dużą elastycznością normy ISO 9001, jednak to ona
nadal stanowi filar tych dokumentów stosowanych w różnych branżach.
ISO/ICE 27000 – System Zarządzania Jakością w Informatyce
Zwraca uwagę na strategiczne znaczenie informacji w organizacji i zależności trafności i szybkości
decyzji od jej dostępności i jakości. Bezpieczeostwo informacji oznacza zachowanie poufności (dostęp
tylko dla osób upoważnionych), integralności (wiarygodnośd źródła i brak niepożądanych zmian) oraz
dostępności (zapewnienie swobodnego dostępu określonym osobom). W wyniku podatności zasobów
na działania zagrożeo bezpieczeostwo informacji może zostad osłabione, a zagrożenia te mogą
pochodzid tak od człowieka (haker, niewiedza i niefrasobliwośd), środowiska (zalanie, pożar) oraz
samego sprzętu(niewłaściwa konfiguracja, brak antywirusa).
System Zarządzania Bezpieczeostwem Informacji ISO/IEC 27001:2004
System opiera się na podejściu procesowym, jest zgodny z modelem PDCA i polega na przede
wszystkim zrozumieniu biznesowych wymagao bezpieczeostwa informacji oraz potrzeby ustanowienia
polityki i celów BI, wdrażaniu i eksploatacji zabezpieczeo, monitorowaniu i przeglądzie wydajności i
skuteczności system oraz ciągłym doskonaleni na podstawie obiektywnego pomiaru. Główne
wymagania tej normy są ujęte w 4 punktach normy :
IV. System Zarządzania Bezpieczeostwem Informacji
V. Odpowiedzialnośd kierownictwa
VI. Audyt wewnętrzny SZBI
VII. Przegląd SZBI realizowany przez kierownictwo
VIII. Doskonalenie SZBI
Polityka SZBI powinna określad poszczególne wymagania, od biznesowych po wymagania klientów.
Udziela wskazówek odnośnie szacowania skutków poprzez określenie zasobów i ich właścicieli,
podatności które mogą wykorzystad zagrożenia, skutków w stosunku do aktywów w przypadku utraty
integralności, dostępności i poufności danych. Ryzyko szacuje się poprzez określenie odpowiedniej skali
szacowani oraz stwierdzenia poziomu akceptowalności ryzyka. Dokumentem wieoczącym szacowanie
jest Deklaracja Stosowana (SoA).
Systemy Zarządzania w Branży Medycznej
Normy te są podstawą do oceny dostawcy wyrobów medycznych. Obowiązujące normy to :
ISO 13 485 – Systemy Jakości – Wyroby medyczne - wymagania dla celów przepisów prawnych
ISO/TR 14 949 – SZJ – Wyroby medyczne – wytyczne do stosowania ISO 13485
ISO 15 189 – Laboratoria medyczne – Szczególne wymagania dotyczące jakości i kompetencji
ISO 15195 – Medycyna laboratoryjna, podstawy referencyjnych laboratoriów pomiarowych
IWA 1 (International Workshop Agrement) – wytyczne doskonalenia w organizacjach służby zdrowia
Systemy Zarządzania w Branży Motoryzacyjnej
Bardziej restrykcyjne niż ISO 9001, np. system QS 9000, VDA 6.1 oraz ISO/TS -16949.
QS 9000
Tzw. System Wielkiej Trójki (Daimler Chrysler, GM, Ford Motor)i ma zastosowanie do dostawców tak
wewnętrznych jak i zewnętrznych. Dotyczy w szczególności dostawców materiałów produkcyjnych,
części i podzespołów, prac wykooczeniowych oraz dostawców urządzeo precyzyjnych. Na system QS
składają się 3 sekcje :
1.
Obejmująca 20 podstawowych wymagao i formułująca podstawy tego systemu
2.
Obejmuje tzw. specyficzne wymagania sektorowe
3.
Obejmuje tzw. specyficzne wymagania klienta, i każdy z Wielkiej Trójki formułuje je
osobno.
Druga częśd systemu składa się następujących elementów : proces aprobowani części produkcyjnych i
zmian w dokumentacji, ciągłych ulepszeo (wyższa jakośd i efektywnośd) oraz zdolnośd procesów
wytwórczych. W zbiorze podręczników zapisane są wymagania :
APQP – zaawansowane planowanie jakości
FMEA – analiza potencjalnych wad i skutków
MSA – analiza systemów pomiarowych
PPAP – proces zatwierdzania części do produkcji
SPC – systematyczne sterowanie jakością
QSA – ocena systemu jakości
VDA 6. 1
Norma niemieckiego sektora motoryzacyjnego, zorganizowana na obszarach kierownictwo oraz wyrób
i proces, i obowiązuje dostawców koncernów VW Group, Porsche, Adam Opel, Ford –Were.
Dodatkowe 7 wymagao postawił przed dostawcami Mercedes i są to między innymi prace nad
materiałami oraz systemami produkcyjnymi, współpraca z zakładami Mercedesa a także ponowne
wykorzystanie materiałów i aspekty ochrony środowiska.
ISO 16949
Opracowano ją w celu ujednolicenia wymagao dla rynku motoryzacyjnego, stanowiących podstawę
certyfikacji pozwalającej na akceptację na rynku europejskim i amerykaoskim. Zbudowano ją w taki
sposób, aby w każdym punkcie najpierw przywołana była norma ISO 9001, później dodatkowe
wymagania, zharmonizowanie dla wcześniejszych standardów przemysłu motoryzacyjnego. Jej
szczególne wymagania dotyczą dokumentacji technicznej, planowanej jakości, zakupów, analizy
systemów pomiarowych, przeprowadzania audytów i badania wyrobów wadliwych. Standard ten
odróżnia od normy ISO 9001 to, że podkreśla znaczenie klienta, zapobieganie a nie usuwanie
niezgodności, jest nastawiony na ciągłe doskonalenie i minimalizację kosztów, podkreśla znaczenie
planów jakości a także odpowiedzialnośd producenta za wyrób i współpracę z klientem na etapie
tworzenia wyrobu.

Standardy jakościowe w przemyśle lotniczym
AS 9000
Korzyścii z tego systemu to wykazanie zgodności z wymaganiami norm serii ISO 9000 oraz
branżowymi, wprowadzenia atmosfery porozumienia wśród producentów poprzez unifikację
wymagao a także zarządzanie dążące do bezpieczeostwa i niezawodności.
D1-9000
Zespół wymagao opracowanych przez Boeing’a która narzuca dostawcom dodatkowe, względem AS
9000 , wymagania ponieważ Boein’g uznał je za lepsze pod względem zapewnienia bezpieczeostwa
pasażerom.
JAR – 145
Opracowane przez Wspólne Władze Lotnictwa Cywilnego normy mające na celu ułatwienie certyfikacji
w przypadku joint venture, ułatwienie eksportu i importu wyrobów lotniczych, zapewnienie
uniwersalności obsługi
Wymagania w przemyśle zbrojeniowym AQAP
Polityka jakości w krajach NATO, zakładająca pełną odpowiedzialnośd wszystkich zaangażowanych
stron za jakośd wyrobu w ramach GQA (Government Quality Assurance) oraz szacowanie ryzyka
związanego z realizacją kontraktu na podstawie którego podejmuje się decyzję o przeprowadzeniu
GQA. Podstawą jest norma ISO 9001, a dokumenty na niej oparte dotyczą między innymi zapewnienia
jakości w projektowaniu, pracach rozwojowych i produkcji, zapewnienia jakości oprogramowania.
Rozszerzenia względem ISO 9001umożliwienie zamawiającemu dostępu do wszystkich dokumentów
związanych z umową, konieczności opracowania do każdej umowy planu jakości, uzyskanie w zakresie
nadzorowania wyposażenia do monitorowania i pomiarów zgodności z normą ISO 10012 i tym
podobne dotyczące tak produktu jak i systemów jakości.
CZĘŚD IV – PCA (Polskie Centrum Akredytacyjne)
Podstawy
Akredytacja PCA są uznawane na całym świecie. PCA jest członkiem organizacji skupiających jednostki
akredytujące laboratoria, certyfikujące i kontrolujące a także wzorcujące w Europie (EA – European co-
operation for Acreditation) i na świecie (ILAC – International Laboratory Acreditation Cooperation).
PCA zachęca laboratoria do stosowania metod badawczych wynikających z najnowszych zdobyczy
wiedzy oraz zgodnych z normami europejskimi i międzynarodowymi, a akredytacji udziela tylko na
takie badania na które dane laboratorium ma kompetencje. Nie udziela natomiast akredytacji na
badania zlecane podwykonawcom oraz takich których laboratorium ma zawartą umowę na dorywcze
wykorzystanie sprzętu i pomieszczeo. Wnioski można składad dla pojedynczego laboratorium lub
grupy.
Dokumenty opisujęce realizację metod badawczych wymienionych przy akredytacji są głównie normy
(polskie, międzynarodowe, paostw członkowskich ISO), przepisy prawne (PL i UE) oraz kodeksy
postępowania a także ogólnie dostępne publikacje metodyczne oraz własne procedury.
Akredytowane laboratoria same wykonują badania w ramach posiadanego zakresu akredytacji,
jednak wyjątkowo może podzielid badania własne, i spoza tego zakresu akredytacji, innemu
laboratorium akredytowanemu którego zakres akredytacji obejmuje podzlecane badania.
Jeśli laboratorium zleca badania podwykonawcy, to powinno poinformowad klienta o tych działaniach
i uzyskad jego zgodę na to zlecenia oraz uzyskad od podwykonawcy sprawozdanie z tych badao. Może
również załączyd zamieścid w swoim sprawozdaniu wyniki podwykonawcy po odpowiednim ich
oznaczeniu i otrzymaniu zgody od podwykonawcy. Ważny jest monitoring zakresu akredytacji
podwykonawcy.
Dokumenty
DA – 05 polityka wykorzystywania badao/porównao przy akredytacji i nadzorze lab.
Badanie biegłości (PT) - określenie za pomocą porównao międzylaboratoryjnych zdolności
laboratorium do przeprowadzania wzorcowao, badao lub zdolności jednostki inspekcyjnej do
przeprowadzania badao.
Porównanie międzylaboratoryjne (ILC) – zorganizowanie, wykonanie i ocena wzorcowao/badao tego
samego lub podobnych obiektów wzorcowao przez co najmniej dwa laboratoria zgodnie z ustalonymi
warunkami.
PT/ILC są podstawowymi elementami wykazania kompetencji technicznych akredytowanych
laboratoriów, jednak nie wymaga objęcia uczestnictwem w tym programie wszystkich
badao/pomiarów objętych zakresem akredytacji jeśli laboratorium przedstawiło rzetelny dowód
biegłości, udokumentowanych i określonych w Księdze Jakości. Warunkiem akceptacji rezultatów jest
to,, aby żadne wynik nie znalazł się w grupie wyników niezadowalających . Organizatorami takich
programów mogą byd np. krajowe jednostki akredytujące, organizatorzy komercyjni ,organizacje
zrzeszające jednostki akredytacyjne organy stanowiące oraz przemysł lub organizacje i zrzeszenia
producentów, a każdy z nich musi mied wdrożony SZJ.
DA-07 polityka dotycząca akredytacji podmiotów zagranicznych
Każdy przyrząd powinien byd wzorcowany przez krajową instytucję metrologicznę (Główny Urząd
Miar) lub akredytowane laboratoria wzorcujące w odpowiedniej najlepszej możliwości pomiarowej, a
istotna jest tu również niepewnośd pomiarów.
W związku z tym dokumentem, zakres laboratorium badawczego można rozszerzyd o nowe obiekty,
cechy, zakresy już akredytowanych metod badawczych oraz nowe metody a także nowe działy
techniczne i lokalizacje.
Normy – EN 45000 oraz ISO/IEC 17025
Pierwsza norma powstała w 1989r przez CEN i określa zasady działania jednostek certyfikujących i
laboratoriów badawczych.
Druga norma posiada pewne określone wymagania w sferze zarządzania (uregulowanie
funkcjonowania, zarządzanie i komunikacja wewnątrz laboratorium, doskonalenie, dokumentacja,
podwykonawstwo, obsługa klienta, nadzór nad niezgodnymi działaniami, działania korygujące oraz
audyt i przegląd zarządzania) a także techniczne (personel, warunki lokalowe i środowiskowe, metody
badao wraz z walidacją i szacunkiem niepewności, nadzór wyposażenia, spójnośd pomiarowa,
pobieranie i postępowanie z próbkami, zapewnienie jakości badao oraz prezentacja wyników)
Audyty
Audyt pierwszej strony
Przeprowadzany z inicjatywy kierownictwa dla potrzeb własnych przez własnych pracowników. W jego
trakcie następuje weryfikacja poszczególnych elementów systemu jakości (przestrzeganie zasad).
Najważniejszym dokumentem w trakcie jego przeprowadzania (jak i każdego audytu) jest Księga
Jakości, opisująca system zapewnienia jakości w przedsiębiorstwie.
Audyt drugiej strony
Przedsiębiorstwo występuje w roli zamawiającego i przeprowadza audyt jakości u
aktualnych/potencjalnych podwykonawców przy wykorzystaniu własnego zespołu audytorów lub
odpowiedniej firmy. Dzięki temu możliwe jest wybranie najlepszego podwykonawcy oraz poprawienie
systemu jakości aktualnego.
Audyt trzeciej strony
Przeprowadzane na przedsiębiorstwie przez odpowiednią instytucję, na własne lub kontrahenta
życzenie, celem podbudowania renomy lub ugruntowania pozycji. Pozytywny wynik pozwala nadad
certyfikat SJZ.
CZĘŚD V – ZARZĄDZANIE JAKOŚCIĄ W LABORATORIUM – ISO 17025
Ogólne wymagania i zakres
Wszystkie wymagania normy ISO 9001, jednak posiadanie tego certyfikatu nie jest równoznaczne z
uzyskaniem akredytacji. W jej spisie znajdziemy informację o normach powołanych, terminach i
definicjach a także wymagao dotyczących zarządzania.
Laboratorium i personel – co powinno byd
1.
Zatrudniany personel kierowniczy i techniczny ma odpowiednie uprawnienia i środki
2.
Istnieją ustalenia zapewniające niezależnośd, strukturę organizacyjną i zarządzanie
3.
Istnieje polityka i procedury zapewniające ufnośd
4.
Zapewnienie kompetentnego nadzoru nad personelem
5.
Zatrudnienie kierownictwa technicznego odpowiadającego za laboratorium
6.
Wyznaczenie kierownika ds. jakości oraz zastępców ważnego personelu
System jakości
Laboratorium powinno ustanowid, wdrożyd i utrzymywad SJ właściwy dla zakresu obowiązków, czyli
udokumentowad politykę, systemy, programy, procedury oraz instrukcje i zakres odpowiedzialności w
Księdze Jakości w odpowiednim stopniu i podad do wiadomości całego personelu aby ten to zrozumiał i
wdrożył.
Nadzór nad dokumentami
Powinny byd opracowane i utrzymywane procedury nadzorowania wszystkich dokumentów
(przepisów, norm, metod badawczych, wzorcowao itp. ) a te z kolei powinny byd jednoznaczne
zidentyfikowane, przeglądane i zatwierdzane przez upoważnione osoby. Procedury nadzoru powinny
uniemożliwiad stosowanie nieważnych dokumentów, a dokumenty archiwalne muszą byd jasno
oznaczone. Istotne są również procedury wprowadzania zmian w dokumentach.
Określone przez normę w skrócie – czyli co ma byd, jak ma byd, po co ma byd i co z tym zrobid
Cz. I - robota papierkowa
I. Przegląd zamówieo,
ofert i umów
Istnieją na to procedury; różnice wyjaśniane i naprawione przed
badaniami; należy utrzymywad zapiski w tym rozmów z klientem;
informacja o odstępstwach od umowy
II. Podwykonawstwo
badao i wzrocowao
Istnieje rejestr podwykonawców; informowanie klienta o zatrudnieniu
podwykonawcy; odpowiedzialnośd za podwykonawcę (nie kiedy dany)
III. Zakupy usług i dostaw
Istnieje polityka ds. wyboru i zakupu wykorzystywanych zasobów; lista
kwalifikowanych dostawców; procedury nabywania i magazynowania
odczynników i materiałów pomocniczych
IV. Obsługa klienta
Możliwa jest współpraca z klientem w celu usatysfakcjonowania
klienta; skargi i procedury ich rozpatrywania (trzymanie zapisów)
V. Nadzór niezgodnych
badao
Istnieje polityka i procedury postępowania z pracą niezgodną z
procedurami lub klientem; ustalenie odpowiedzialności i info do klienta
VI. Działania korygujące
Procedury i polityka dla niezgodności; analiza, wybór, wdrożenie i
monit działao korygujących oraz dodatkowe audyty; procedury działao
zapobiegawczych; plany poprawy i nadzór ich realizacji
VII. Nadzór nad zapisami
Procedury nadzoru; zapisy dot. jakości (raporty); procedura kopiowania
i ochrony zapisów elektronicznych; czas trzymania zapisów z badao
VIII. Audyty wewnętrzne
Okresowe przeprowadzanie; prowadzenie przez odpowiedni personel;
nie audytowad własnej pracy; zapis i sprawdzanie skuteczności
Cz. II – wchodzimy do laboratorium
I . Wymagania
techniczne
Na poprawnośd badao wpływają – ludzie, lokal i środowisko, metody badao i
walidacji, wyposażenie i próbki, spójnośd pomiarów oraz postępowanie z
obiektami
II. Personel
Odpowiednia wiedza i kompetencje; osobiste certyfikaty; upoważnienie do
poboru próbek; procedury szkoleo; zakres obowiązków;
III. Lokal i
środowisko
Monitoring środowiska jeśli wpływają; przeciwdziałanie zanieczyszczeniu
próbek; środki utrzymania czystości
IV. Wyposażenie
Niezbędne do przeprowadzenia badao; spełnia specyfikacje; odpowiedni ludzie;
instrukcje obsługi; jednoznacznie zidentyfikowane (producent, lokalizacja, typ,
SN, informacje o naprawach, wadach i serwisie); wadliwe separujemy; ochrona
przed adjustacjami wpływającymi na wynik pomiaru
Cz. III – bawimy się próbką
I . Spójnośd pomiarowa
Program i procedury dot. wzorcowania wzorców odniesienia; wzorce
tylko do wzorcowania; w jednostkach SI lub innych certyfikowanych;
sprawdzanie
II. Pobieranie próbek
Plan i procedury pobierania i zapisu danych oraz czynności z próbką;
oparcie na metodach statystycznych
III. Obiekty badao
Transport, przejmowanie, magazynowanie; system identyfikacji
IV. Zapewnienie jakości
wyników badao
Procedury do monitu badao; śledzenie kierunków zmian; techniki
statystyczne; przegląd i planowanie monitoringu
V. Przedstawienie
wyników
Podane jasno, jednoznacznie, obiektywnie i zgodnie z instrukcjami badao
i wzorcowao.
CZĘŚD VI – ZARZĄDZANIE JAKOŚCIĄ ŻYWNOŚCI
Ważne ze względu na emocjonalny stosunek klienta do produktów żywnościowych oraz możliwośd
zagrożenia bezpieczeostwa zdrowotnego.
Normy obowiązujące w Polsce :
Obligatoryjne przepisy HACCP (Hazard Analysis and Critical Control Point)- system
opracowany w celu rozpoznania i kontroli zagrożeo możliwych w każdym momencie
produkcji i składowania żywności
PN-EN ISO 22000 – system zarządzania bezpieczeostwem żywności; szczegółowe
wymagania zależą od organizacji
Systemy zapewnienia jakości żywności :
GMP – Good Manufacture Practice
GHP – Good Hygiene Practice
GLP – Good Laboratori Practice
HACCP
ISO 9001
ISO 22000
Kierownictwo określa zakres HACCP uwzględniając poszczególne produkty przetwarzane w zakładzie
oraz etapy postępowania z tymi produktami. Powinno również określid ramy czasowe wdrażania
systemu, szacunkowe koszty, inwestycje oraz zmiany organizacyjne. Przed przystąpieniem do
wdrażania tego systemu powinno przejrzed aktualnie obowiązujące zasady stanu technicznego i
higienicznego oraz możliwości zapewnienia im pełnego bezpieczeostwa żywności.
Programy Warunków Wstępnych z zasadami GHP i GMP
W gruncie rzeczy zasady te odnoszą się do obszaru bezpośrednio produkcyjnego oraz otoczenia
zakładu, dostaw surowców i dystrybucji czyli obszaru przyprodukcyjnego.
Kilka zagadnieo do których zadajemy odpowiednie pytania:
Stan sanitarno-higieniczny zakładu i otoczenia
Kwalifikacje personelu
Wielkośd , funkcjonalnośd i usytuowanie pomieszczeo
Zabezpieczenie przed szkodnikami
Prawidłowośd linii technologicznych i prowadzenia procesów
Jakośd wody
Wyposażenie w maszyny i prowadzenia i ich funkcjonowanie
Wyposażenie w sprzęt kontrolno-pomiarowy
Jakośd sprowadzanych surowców
i materiałów pomocniczych
Organizacja pracy
Procesy mycia i dezynfekcji
Magazynowanie żywności
Higiena i sposób postępowania załogi
Warunki transportu żywności
Co to jest HACCP i jakie ma zasady?
Z definicji jest systemowym postępowaniem mającym na celu zapewnienie bezpieczeostwa
zdrowotnego żywności poprzez identyfikację i oszacowanie skali zagrożeo bezpieczeostwa żywności z
punktu widzenia jej jakości zdrowotnej oraz ryzyka wystąpienia tych zagrożeo podczas przebiegu
wszystkich etapów produkcji i dystrybucji żywności. Ogranicza również te zagrożenia i ustala działania
naprawcze.
Zasady HACCP
1.
Analiza zagrożeo (identyfikacja i ocena a także środki kontroli i zapobiegania)
2.
Ustalanie Krytycznych Punktów Kontroli (eliminacja/minimalizacja zagrożeo)
3.
Ustalenie dla każdego CCP wymagao (parametry i limity krytyczne)
4.
Ustalenie i wprowadzenie systemu monitorowania CCP
5.
Ustalenie działao korygujących, jeśli CCP nie spełnia wymagao
6.
Ustalenie procedur weryfikacji dla potwierdzenia skuteczności i zgodności systemu
7.
Opracowanie i prowadzenie dokumentacji HACCP
Zasady wdrażania HACCP (12 sekwencyjnych zaleceo Kodeksu Żywnościowego)
1.
Powołanie zespołu HACCP (dobrze wyszkolony, kontakt z praktyką produkcyjną)
2.
Opisanie produktu (skład, technologia, cechy, pakowanie, transport, magazynowanie)
3.
Określenie przewidywanego sposobu wykorzystania produktu przez konsumenta
4.
Opracowanie schematu blokowego procesu technologicznego
5.
Weryfikacja schematu procesu technologicznego
6.
Sporządzenie listy wszystkich ewentualnych zagrożeo związanych z każdym etapem
produkcji oraz listy wszelkich prewencyjnych środków kontroli danego zagrożenia
7.
Określenie CCP
8.
Określenie celów i granic tolerancji dla CCP
9.
Opracowanie systemu monitorowania każdego CCP
10. Ustalenie działao korygujących
11. Ustalenie procedury weryfikacji
12. Prowadzenie dokumentacji i zapisów (plan i dokumenty potwierdzające skutecznośd)
Plan HACCP – dokument powołujący zespół HACCP i lista jego członków; zakres stosowania systemu;
opis produktu i jego przeznaczenie; schemat produkcyjny; dokument stwierdzający zgodnośd schematu
z praktyką.
KONIEC !!!
Wyszukiwarka
Podobne podstrony:
ZJ W wielkim skrócie cz 1
neurologia w WIELKIM skrocie
Detoks wielkie porządki, cz I
Detoks wielkie porządki, cz III
Detoks wielkie porządki, cz V
Detoks wielkie porządki, cz IV
neurologia w WIELKIM skrocie
Detoks wielkie porządki, cz I
Detoks wielkie porządki, cz III
Detoks wielkie porządki, cz I
Filozofia w wielkim skrócie oraz wiersze filozoficzne 2222222222
22 Późna twórczość wielkich artystów Cz Miłosz, T Różewicz, W Szymborska, Z Herbert(1)
Konflikty na świecie (w wielkim skrócie)
Detoks wielkie porządki, cz V
Wymowa i artyzm Wielkiej Improwizacji z III cz ,,Dziadów” A Mickiewicza
biologia, wykład (cz.1), Powstawanie wszechświata - 14 mld lat temu podczas wielkiego wybuchu
więcej podobnych podstron