
NIEDOKRWISTOŚĆ SIERPOWATOKRWINKOWA
Do szpitala zgłosili się rodzice (emigranci z Afryki) z dzieckiem rasy czarnej, 7-letnim
synem (B.R. - Bob). Bezpośrednią przyczyną przyjęcia chłopca do szpitala, był występujący
uporczywy kaszel oraz płytki, przyspieszony oddech. Badającego lekarza zaniepokoiło także
występowanie bólu w klatce piersiowej przy próbie głębszego oddechu, znaczne
powiększenie śledziony oraz bolesny obrzęk grzbietowych powierzchni dłoni i stóp.
Z wywiadu zebranego od rodziców, uzyskano dodatkowe informacje:
Po raz pierwszy, napady bólu w okolicach bioder oraz ud utrzymujące się 1-2 dni
występowały u dziecka od 2-go roku życia; kilkakrotnie wystąpiły w ciągu 7-letniego okresu
życia dziecka, ale były one znacznie słabsze.
Pobrano krew z żyły odłokciowej chłopca w celu wykonania badań dodatkowych
(morfologia, stężenia elektrolitów, glukozy) oraz aby oznaczyć grupę krwi. Po uzyskaniu
zgody rodziców, pobrano także krew w celu pozyskania i zabezpieczenia DNA (do
identyfikacji ewentualnych mutacji). Ze względu na małe wysycenie, Hb tlenem (90%;
wykonano pomiar przy pomocy pulsoksymetru), zastosowano tlenoterapię.
W badaniach dodatkowych stwierdzono u chłopca (Bob):
Morfologia
Wartości referencyjne
Hb
7,8 g%
(12-16 g%)
Hematokryt 23%
(41-53 %)
Erytrocyty 3,2 mln
(3,5-5,7)
Leukocyty 6000
(4000-10 000)
Bilirubina w surowicy 40 µmol/L
(3-22 µmol/L)
(produkt katabolizmu hemu)
W rozmazie krwi obwodowej, stwierdzono obecność erytrocytów o zniekształconym
kształcie, przypominającym sierpowaty oraz zwiększoną ilość retikulocytów (20%).
Na podstawie obrazu klinicznego oraz wstępnych wyników postawiono rozpoznanie u
dziecka niedokrwistości sierpowatokrwinkowej. Pomimo ujemnego wywiadu rodzinnego
(rozwój dziecka był prawidłowy), podobny profil badań wykonano u 2-letniej siostry (A.R. -
Alice) chorego chłopca (B.R. - Bob). Wyniki podstawowych badań diagnostycznych oraz
parametrów morfologii, nie odbiegały od normy.
W laboratorium wyizolowano z erytrocytów B.R. (Bob) i A.R. (Alice) hemoglobinę i
poddano analizie elektroforetycznej dwoma metodami. Porównano szybkość wędrówki tych
białek w polu elektrycznym z szybkością wędrówki hemoglobiny wyizolowanej z
erytrocytów zdrowego człowieka (o inicjałach H.M.).
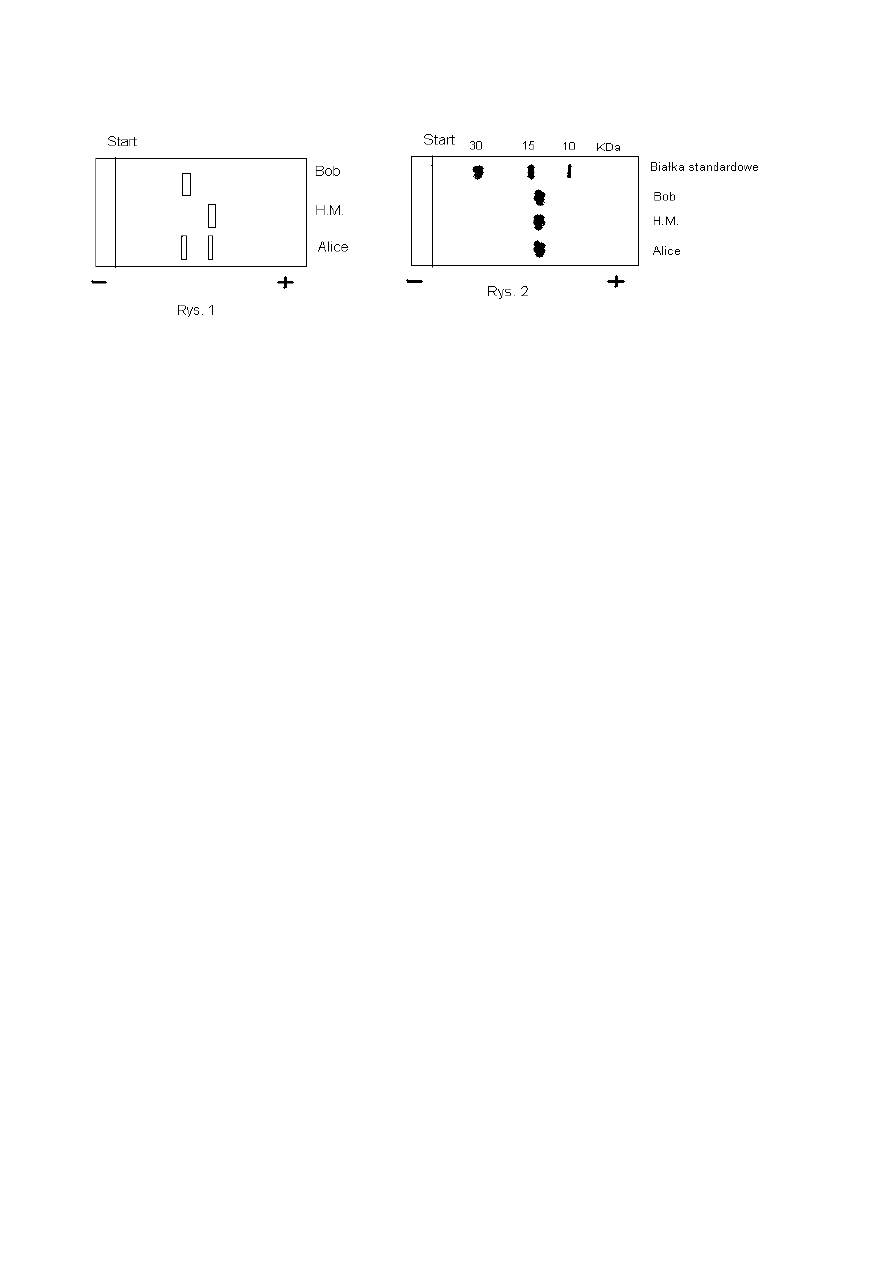
Metoda I. Elektroforeza w warunkach „naturalnych”, bez uprzedniej denaturacji
białka. Rozdział przeprowadzono w buforze o pH 8,6 (Rys. 1).
Metoda II. Elektroforeza w warunkach denaturujących białko. Próbki białek, przed
przeprowadzeniem analizy poddano denaturacji przez ogrzewanie w 100
o
C w 1% roztworze
siarczanu dodecylu sodu (SDS) i redukcji 1% roztworem merkaptoetanolu (redukuje mostki
disiarczkowe). Elektroforezę przeprowadzono w buforze o pH 8,3 (Rys. 2).
Ponieważ w laboratorium pracowali w tym czasie studenci, polecono im przeprowadzić dwa
proste doświadczenia, zanotować ich przebieg i poczynione obserwacje.
Doświadczenie I. Do heparynizowanej probówki pobrano kilka mililitrów krwi Boba
i odstawiono probówkę do statywu. Po 1 min delikatnie pobrano pipetą zawiesinę erytrocytów
z górnej (a), dolnej (b) warstwy zawiesiny komórek, oraz po wstrząśnięciu zawartości
probówki (c). Pod mikroskopem oceniano kształt erytrocytów w wykonanych rozmazach.
Zaobserwowano, że po czasie około 1 min krwinki na dnie próbówki przyjęły kształt
„sierpowaty”, natomiast krwinki w górnej części probówki zachowały normalny wygląd. Po
wstrząśnięciu zawartości probówki prawie wszystkie krwinki powróciły do normalnego
kształtu.
Doświadczenie II. Do czterech kolejnych probówek wlano po 4 ml roztworu: (1) 500
mM sacharozy; (2) 300 mM NaCl; (3) 100 mM NaCl; (4) soli fizjologicznej. Następnie do
każdej z probówek wprowadzono po 1 ml krwi pobranej od Boba. Określono czas, w którym
na dnie każdej z probówek rozpoczynała się „sierpowata” deformacja krwinek:
(1) 500 mM sacharoza
4 min 18 sek
(2) 300 mM NaCl
2 min 11 sek
(3) 100 mM NaCl
21 min 24 sek
(4) sól fizjologiczna
7 min 35 sek
PYTANIA.
1. Czym różni się HbS od HbA ?
2. Co było przyczyną dolegliwości bólowych chłopca?
3. Dlaczego, po przyjęciu do szpitala podano mu tlen? Czy można przewidywać, że to
poprawi jego stan?
4. Wyniki badań biochemicznych krwi Boba znacznie odbiegają od wartości
prawidłowych. Co może być tego przyczyną?
5. Co jest przyczyną zmiany kształtu krwinek zawierających HbS? Jakie czynniki
sprzyjają tej zmianie?
6. Który z zastosowanych systemów elektroforezy może być pomocny w ocenie ryzyka
wystąpienia objawów anemii sierpowatej u siostry chłopca, Alice? Porównaj obrazy
analizy preparatów hemoglobiny w obu systemach i przeprowadź ich interpretację.
7. Czym różni się, w doświadczeniu I, otoczenie krwinek na dnie, od otoczenia krwinek
w górnej części probówki? W jaki sposób wytrząsanie zmieniło to otoczenie? Który z
czynników otoczenia krwinek powoduje ich „sierpowatość”?
8. Oblicz osmolarność każdego z czterech badanych w doświadczeniu II roztworów.
9. Czy na podstawie doświadczenia II można wnioskować o zależności pomiędzy
stężeniem hemoglobiny (HbS) w krwinkach a ich skłonnością do „sierpowatości”?
ZATRUCIE INHIBITOREM ACETYLOCHOLINESTERAZY
Do SOR (Szpitalny Oddział Ratunkowy) Kliniki Toksykologicznej przywieziono 50-
letniego Jana K. Główne dolegliwości zgłaszane przez chorego to: zaburzenia widzenia,
niepokój, kaszel oraz uczucie duszności. Lekarz stwierdził u chorego znaczne łzawienie gałek
ocznych, zwężenie źrenic, znaczną potliwość skóry oraz osłabienie i drżenie mięśni. Nie
stwierdzono u niego zaburzeń świadomości, oraz mowy.
W wywiadzie uzyskano dodatkowe informacje od chorego:
Jan K. był rolnikiem, i w godzinach rannych tego dnia wykonywał w ogrodzie, opylanie
roślin roztworem pestycydu. Nie przestrzegał jednakże czasu ekspozycji na insektycyd, oraz
nie używał maski. Dolegliwości, które zgłaszał pojawiły się kilka godzin później.
Z powodu trudności oddechowych, chorego przyjęto do OIT (Oddział Intensywnej terapii).
Rozpoczęto monitorowanie czynności serca i oddychania oraz wdrożono leczenie atropiną.
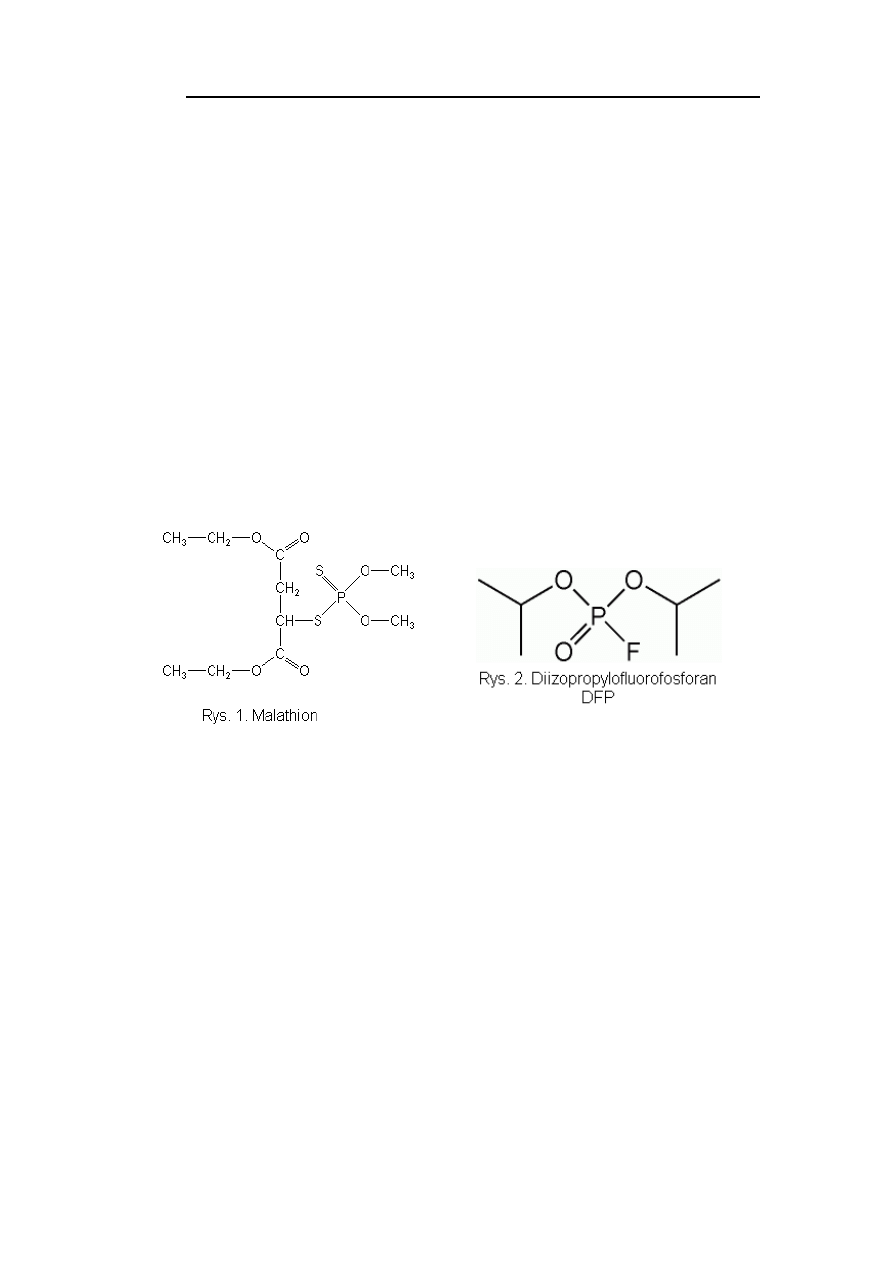
Z opisu środka owadobójczego, który używał Jan K. wynikało, że w jego skład
wchodził malation (Rys. 1), związek fosforoorganiczny, którego mechanizm działania na
centra katalityczne pewnej grupy enzymów jest podobny do mechanizmu działania
diizopropylofluorofosforanu (DFP) (Rys. 2), znanego inhibitora proteinaz serynowych.
Wyniki badań biochemicznych krwi Jana K. nie odbiegały od wartości prawidłowych.
Jedynie aktywność acetylocholinesterazy w krwinkach czerwonych była o 30 % niższa, niż u
ludzi zdrowych. Aktywność acetylocholinesterazy krwinek Jana K. porównywano z
aktywnością handlowego preparatu acetylocholinesterazy, którego parametry K
m
(0,14 M) i
V
max
(10 mol min
-1
g
-1
), wobec acetylocholiny jako substratu, wyznaczyli pracujący w
laboratorium studenci. Studentom polecono ponadto określić wartości tych parametrów w
sytuacji, gdy w mieszaninach reakcyjnych, poza substratem, znajduje się
diizopropylofluorofosforan (DFP) w stężeniu 10 M.
Acetylocholina jest neurotransmiterem, który przenosi sygnał z komórek nerwowych
do np. komórek mięśniowych. Po odebraniu sygnału przez odpowiedni receptor,
neurotransmiter powinien ulec zniszczeniu, co w przypadku acetylocholiny, polega na
hydrolizie cząsteczki sygnalnej. Reakcję hydrolizy acetylocholiny katalizuje enzym,
acetylocholinesteraza:
ACETYLOCHOLINA + H
2
O
OCTAN + CHOLINA
Enzym związany jest z błonami komórek tkanek, które ulegają pobudzeniu (np.
synapsy pomiędzy komórkami nerwowymi a mięśniowymi) i jego aktywność jest ściśle

związana z przekazywaniem impulsu nerwowego. Acetylocholinesteraza znajduje się również
w krwinkach czerwonych.
Centrum katalityczne acetylocholinesterazy ukryte jest w głębokiej kieszeni w
cząsteczce białka, a zasadniczą rolę w reakcji hydrolizy acetylocholiny pełnią znajdujące się
w centrum katalitycznym łańcuchy boczne trzech aminokwasów: seryny, histydyny i
glutaminianu – podobnie jak w przypadku „triady katalitycznej” trypsyny lub chymotrypsyny.
Acetylocholinesteraza jest obiektem ataków trucizn jadu węży i zsyntetyzowanych
przez człowieka toksycznych związków fosfoorganicznych, które były używane jako gazy
bojowe (tabun, sarin, soman). Związki z tej grupy, są także stosowane jako środki
owadobójcze.
Postępowanie terapeutyczne w zatruciach związkami fosforoorganicznymi jest
uwarunkowane od stopnia ekspozycji na związek oraz objawów klinicznych. Podczas
leczenia (które powinno być prowadzone w OIT - monitorowanie czynności serca i
oddychania) podawana jest atropina, która blokuje pozazwojowe receptory cholinergiczne
(znosi działanie acetylocholiny). Reaktywatory acetylocholinesterazy (oksymy - np.
obidoksym) są stosowane, jeżeli zespół cholinergiczny jest wywołany związkami
fosforoorganicznymi, pestycydami lub gazami bojowymi. Mechanizm działania tej grupy
leków polega na reakcji ze zmodyfikowanym przez truciznę centrum katalitycznym
acetylocholinesterazy, co odtwarza funkcjonalny łańcuch boczny odpowiedniego
aminokwasu.
Związki fosfoorganiczne, inhibitory acetylocholinesterazy, stosowane są również jako
leki (np. łagodzące objawy miastenii lub choroby Alzheimera) w celu wzmocnienia sygnału
acetylocholiny.
Odmiennie działają, stosowane jako leki, odwracalne inhibitory acetylocholinesterazy,
np. E2020 czyli Aricept. Te związki blokują bardzo specyficznie i w odwracalny sposób
centrum katalityczne enzymu. Struktury związków tej grupy zostały zaprojektowane na
podstawie znajomości trójwymiarowej struktury centrum katalitycznego enzymu (Rys. 3).
Rys. 3. Kompleks
acetylocholinesterazy z E2020
(Aricept). PDB: 1EVE

PYTANIA.
1. Do jakiej klasy enzymów należy acetylocholinesteraza? Jaką reakcję katalizuje i jaka jest
znaczenie tej reakcji?
2. Acetylocholinesteraza jest enzymem o bardzo wysokiej „liczbie obrotów”. Wyjaśnij to
pojęcie. Jak wyznacza się wartość „liczby obrotów”?
3. Dlaczego cząsteczka sygnałowa powinna, po przekazaniu sygnału, zostać usunięta? Czy
może mieć to związek z wartością K
cat
acetylocholinesterazy?
4. Atropina jest antagonistą receptora muskarynowego acetylocholiny. Co to oznacza? Jaki
jest spodziewany wpływ atropiny na przewodnictwo w synapsach cholinergicznych? Na
czym polega działanie terapeutyczne atropiny w przypadku zatrucia inhibitorami esterazy
acetylocholinowej?
5. Jaką rolę pełnią w centrum aktywnym reszty Ser, His i Glu?
6. Dlaczego związki fosfororganiczne są silnie toksyczne? Do jakiej klasy inhibitorów je
zaliczamy? Jaki jest mechanizm ich działania?
7. Czy obecność DFP w przeprowadzonym doświadczeniu studenckim wpłynie na mierzone
wartości K
m
i V
max
acetylocholinesterazy? Zaproponuj plan eksperymentu pozwalającego
określić wpływ inhibitora na wartości Km i Vmax.
8. Czy obecność atropiny w mieszaninie reakcyjnej doświadczenia studentów może wpłynąć
na mierzone wartości K
m
i V
max
acetylocholinesterazy?
9. DFP i malation hamują esterazę acetylocholinową tworząc wiązanie kowalencyjne z
kluczową dla katalizy resztą seryny. Czy istnieje zatem możliwość reaktywacji enzymu?
10.
Pod adresem Protein Data Bank (
) znajdź stronę Molecule of
the Month: Acetylcholinesterase oraz struktury przedstawione na Rys. 3.
Wyszukiwarka
Podobne podstrony:
Mukowiscydoza, Niedokrwistość sierpowao krwinkowa
Niedokrwisto sierpowatokrwinkowa www
Choroba niedokrwienna serca pol
niedokrwistość sierpowatokrwinkowa, hemofilia A i B
PRZEŁOM W NIEDOKRWISTOŚCI SIERPOWATOKRWINKOWEJ MR
Mukowiscydoza, Niedokrwistość sierpowao krwinkowa
Niedokrwisto sierpowatokrwinkowa www
Niedokrwistość sierpowatokrwinkowa
Ubytki,niepr,poch poł(16 01 2008)
Choroba niedokrwienna serca
(33) Leki stosowane w niedokrwistościach megaloblastycznych oraz aplastycznych
Zajecia 6 7 Test Niedokonczonych Zdan
09 Choroba niedokrwienna sercaid 7754 ppt
więcej podobnych podstron