
BIAŁKA WIĄŻĄCE GTP
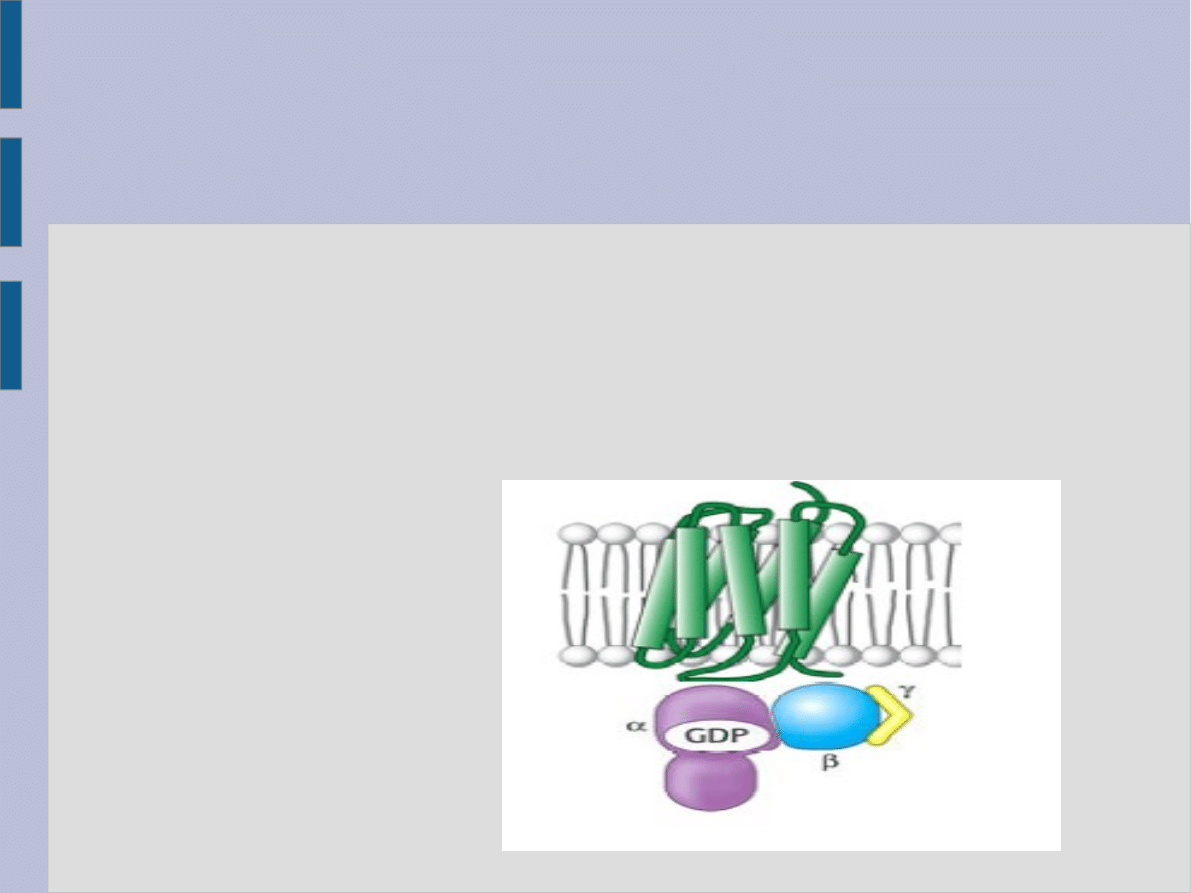
Białko G
Jego nazwa pochodzi od tego, że z białkiem tym wiążą
się nukleotydy guanylowe GDP i GTP. Białko G w stanie
nieaktywnym jest heterotrimerem zbudowanym z
podjednostek α, β i γ.
Podjednostka α jest GTPazą i w stanie nieaktywnym
związany jest z nią nukleotyd GDP. Podjednostki α i γ są
zakotwiczone w błonie komórkowej poprzez
kowalencyjnie związane z nimi kwasy tłuszczowe.

Stwierdzono, że białko G występować może w
wielu izoformach.
Wydaje się, że największe znaczenie dla
specyficzności przekazu sygnału ma rodzaj
podjednostki α. Ma ona wpływ zarówno na
typ receptora z którym wiąże się dane białko
G jak i na rodzaj białka enzymatycznego
odbierającego i przekazującego dalej sygnał.
Dlatego białka G dzieli się na klasy właśnie
ze względu na rodzaj podjednostki α.
.

Główne rodziny białek G
•G αs- typ receptora β-adrenergiczny ligand
adrenalina i noradrenalina, hormony
tarczycy, glukagon, substancje zapachowe
efekt komórkowy stymulacja cyklazy
adenylanowej, wzrost poziomu cAMP
•G αi- typ receptora α2-adrenergiczny ligand
acetylocholina, aminy α-adrenergiczne,
neuroprzekaźniki efekt komórkowy inhibicja
cyklazy adenylanowej

• G αt- typ receptora rodopsyna ligand foton efekt
komórkowy stymulacja fosfodiestrazy cGMP
• G αq- typ receptora α1 adrenergiczny ligand
acetylocholina, aminy α-adrenergiczne,
neuroprzekaźniki efekt komórkowy aktywacja
fosfolipazy C, wzrost poziomu IP3 i wewnątrz
komórkowego stężenia jonów Ca2+
• G α12- ligand trombina, peptydy chamoaktyczne,
interleukiny efekt komórkowy regulacja wzrostu
komórki, rozwój embrionalny, aktywacja wymiany
Na+/H+, aktywacja fosfolipazy D, apoptoza
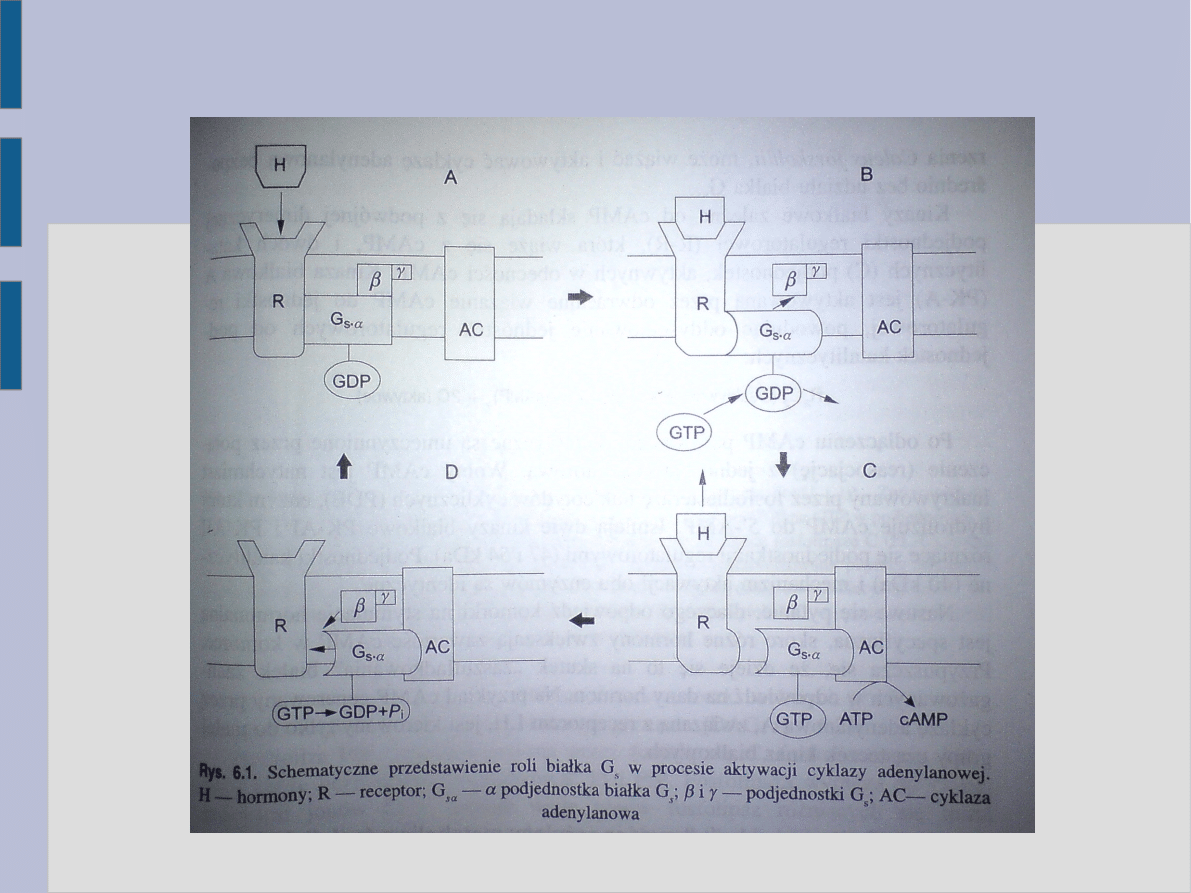
Rola białka Gs w procesie aktywacji
cyklazy adenylanowej- schemat
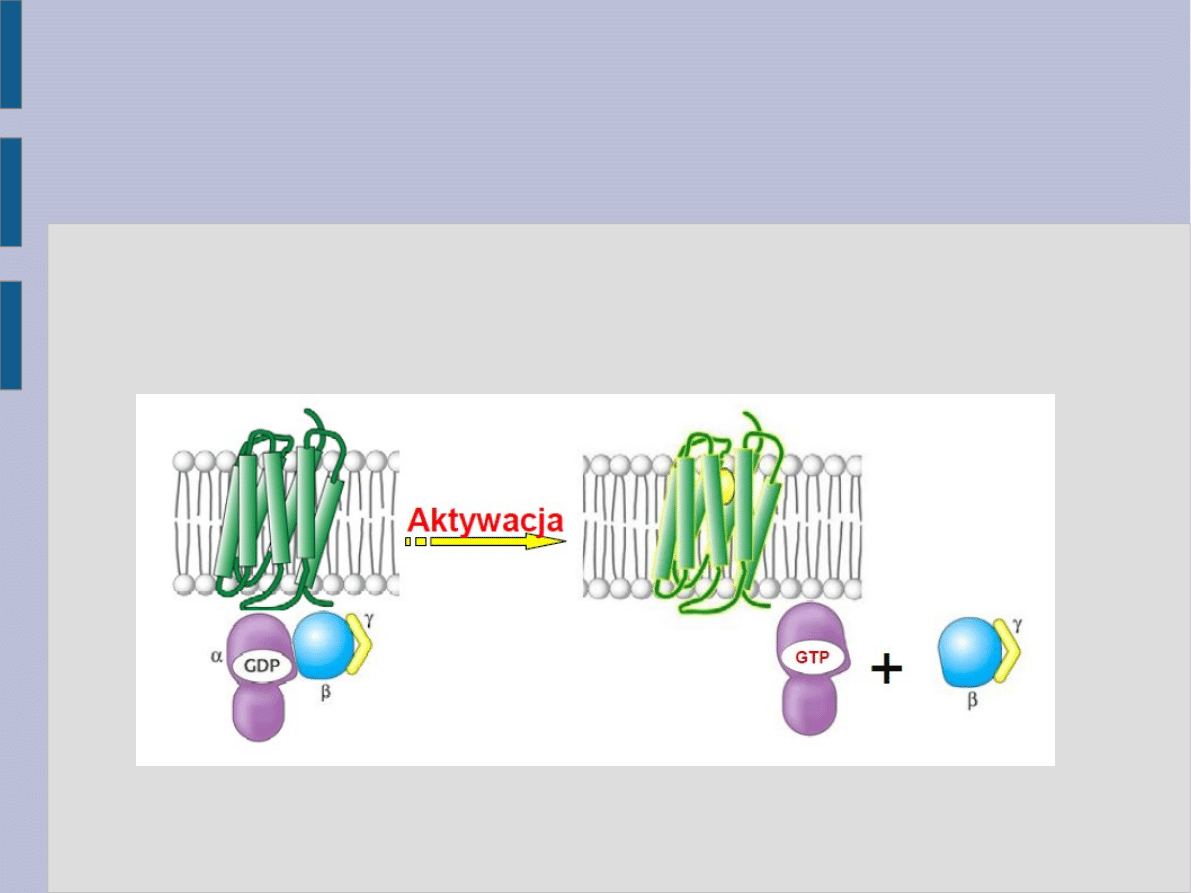
Zmiany konformacyjne w cytoplazmatycznej
domenie receptora 7TM powodują aktywację
białka G. Kompleks ligand-receptor oddziałuje z
podjednostką α katalizując wymianę GDP na
pochodzący z roztworu GTP. Podjednostka α
związana z GTP odłącza się od dimeru βγ
tworząc odpowiedniego typu białko G
α
.

Małe białka G
Inną ważną rodziną białek sygnałowych są
tzw. małe białka G. Są to monomeryczne,
małe białka o aktywności GTPazowej. W
odróżnieniu od omawianych poprzednio
heterotrimerycznych białek G zawierają one
tylko jedną podjednostkę. Podobnie jak
klasyczne białka G małe białka G również
cyklicznie
zmieniają
formę
aktywną
związaną z GTP, na nieaktywną związaną z
GDP i z powrotem
.

Małe białka G stanowią ogromną rodzinę białek
podzieloną
na
podrodziny.
Każda
z
nich
odpowiedzialna jest za regulację odmiennych
procesów zapewniających rozwój i homeostazę
komórki.
Do małych białek G zaliczamy
Ras
Rho
Arf
Rab
Ran

Funkcje małych białek G
• Regulacja wzrostu komórki za pośrednictwem
serynowo-treoninowych kinaz białkowych – białko Ras
• Reorganizacja szkieletu za pomocą serynowo-
treoninowych kinaz białkowych- białko Rho
• Regulacja szlaków wydzielania pęcherzyków,
aktywacja fosfolipazy D- białko Arf
• Pełnienie głównej roli w szlakach wydzielniczych i
endoctozie- białko Rab
• Udział w transporcie białek i RNA z i do jądra
komórkowego- białko Ran
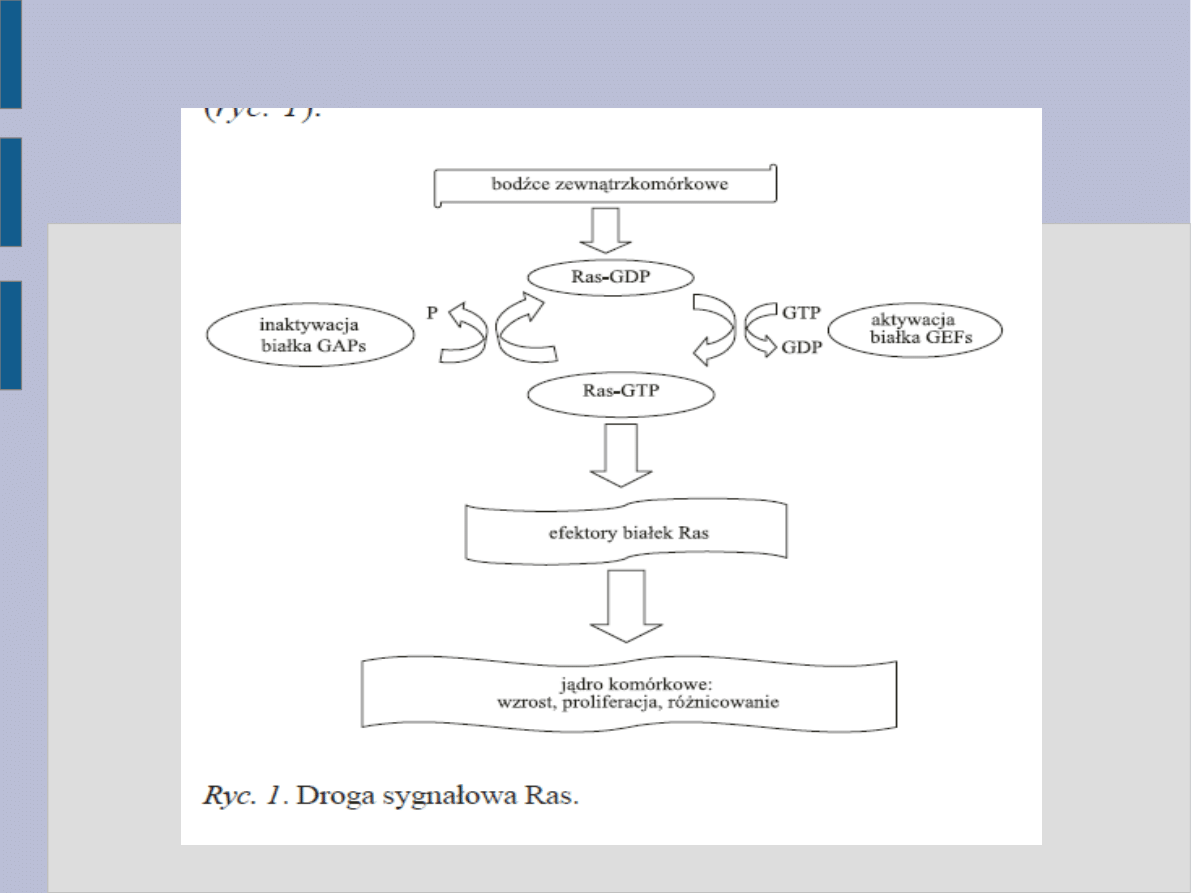
Białko Ras
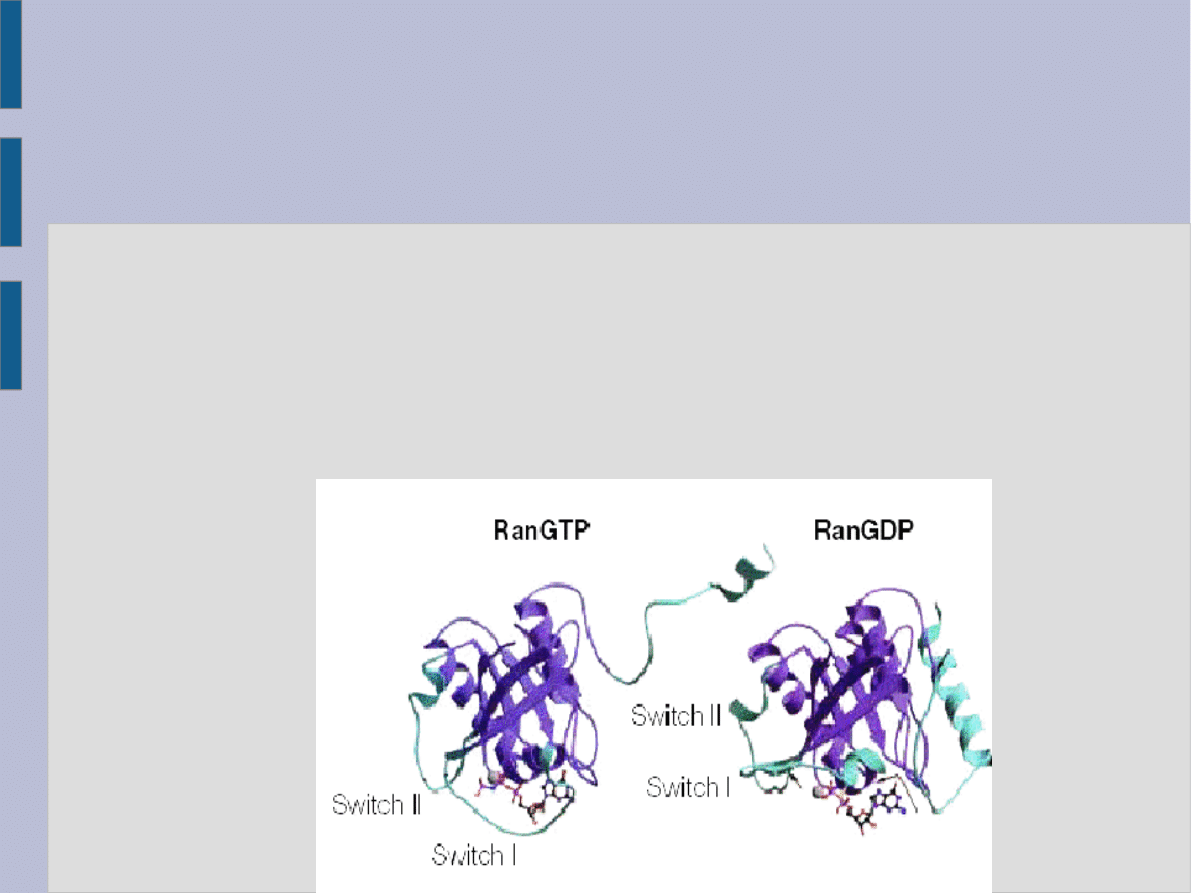
Białko Ran
• Składa się z 6 harmonijek β otoczonych 5 heliksami α
połączonymi pętlami
• Charakterystyczny jest długi C-końcowy koniec, który
oddziaływuje z receptorami transportu
• W zależności od tego czy z białkiem jest GTP czy GDP
zmienia się konformacja przestrzenna pętli I, II i C-końca
co wpływa na siłę interakcji białka Ran z kompleksami
ligand-receptor transportu
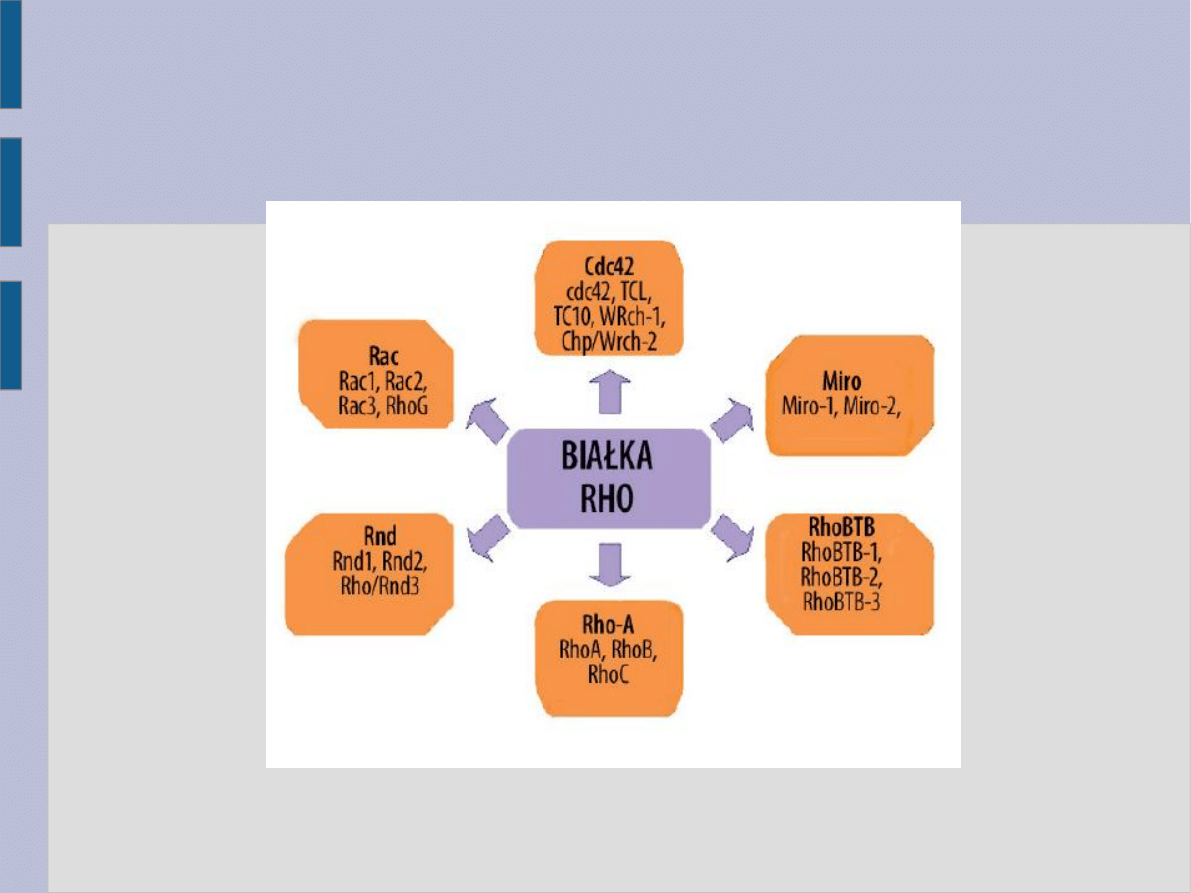
Białko Rho
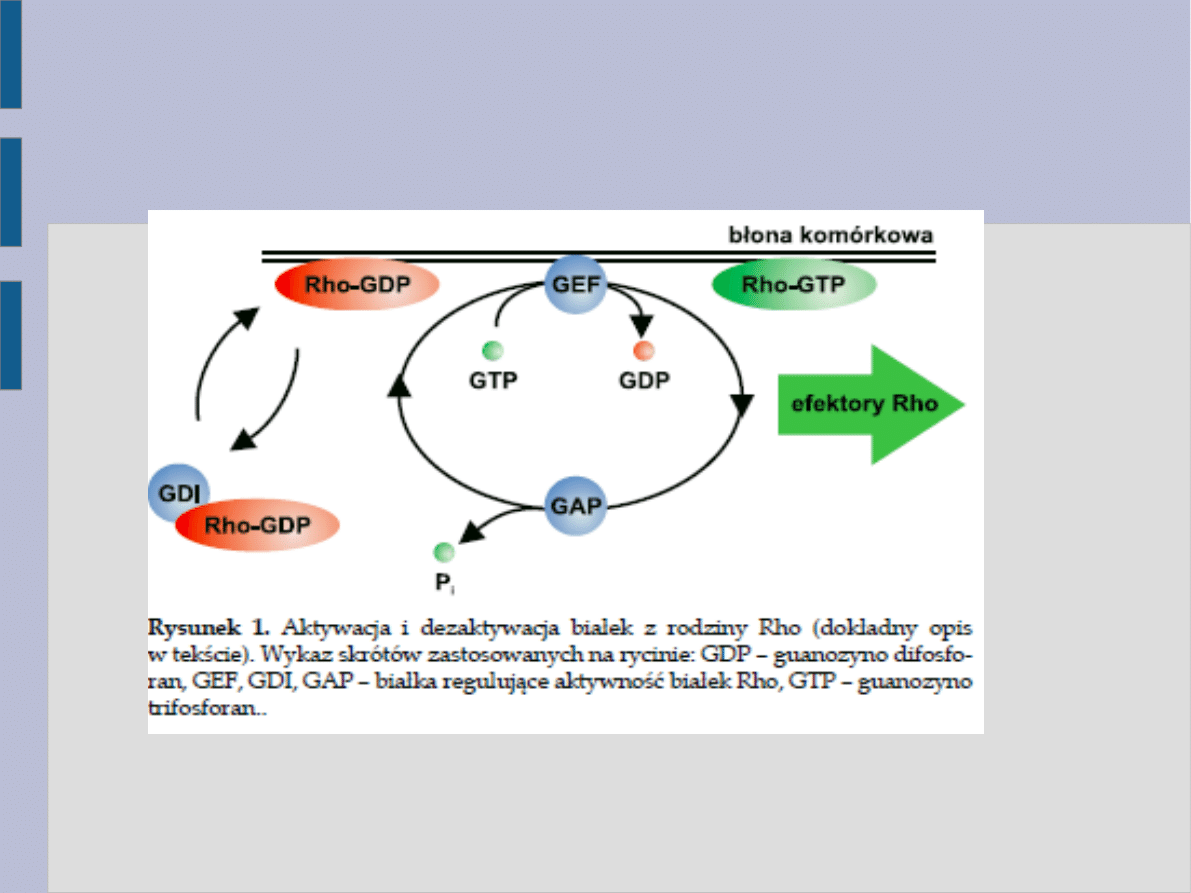
Schemat działania białka Rho

Białko Arf
Białko ARF po aktywacji (zamianie GDP na GTP przy
współpracy innych białek) przyłącza się do błony, co
pociąga za sobą aktywację fosfokinazy D, która
powoduje zmiany w lipidach - rozkład
fosfatydylocholiny do kw. cholinowego i kw.
fosfatylowego, zmieniając tym samym ładunek w
lipidach, co w efekcie prowadzi do uwypuklanie się
błon.

DZIĘKUJEMY
ZA UWAGĘ!
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
Wyszukiwarka
Podobne podstrony:
UNESCO, SGGW TiR zaoczne, GTP
ATP, GTP
OSOBLIWOŚCI PRZYRODY, szkoła, gtp nowe
GTP ściąga, SGGW TiR zaoczne, GTP
ATP, GTP
Wykaz walorów turystycznych Polski wg województw, szkoła, druk gtp
GTP guanozyno
GTP, Studia, Przedmioty, Meteorologia, Klimatologia, Meteorologia - różne
gtp
GTP DO NAUKI
GTP 18H
GTP 22 24 26S2
GTP 24R
GTP 24B
GTP 14B
GTP 28H
gtp taśmy trudnopalne
więcej podobnych podstron