
Organiczne związki
fluorowców
.
Nazwy chlorowcopochodnych omówiliśmy już przy okazji
alkanów
1. Halogenowanie
Cl
CH4 + Cl2 → CH3Cl + HCl
Metan chlorometan chlorowodór
(chlorek metylu)
CH3Cl +Cl2 → CH2Cl2 + HCl
dichlorometan
(chlorek metylenu)
CHCl3 – trichlorometan czyli chloroform,
oraz CCl4 tetrachlorometanu, czyli czterochlorku węgla
Inne halogenoalkany to:
CH3CH2CH2Cl
1-
chloropropan
Cl (chlorek propylenu)
CH3CH2CH2 2-chloropropan (chlorek izopropylenu)
CH3CH-CHCH3
2-bromo-3-chlorobutan
Br Cl
CH2 =CHCl chloroeten (chlorek winylu)
H2C=CH-CH2Br
3-bromo-1-propen (bromek allilu)
.
CH3
Cl
CH2Cl
2-chlorotoluen
chlorek benzylu
CF3Cl
chlorotrifluorometan (freon)
CF2Cl2
dichlorodifluorometan
(freon)
Ze związkami fluorowców zetknęliśmy się już przy reakcjach
halogenowania. Obecnie zajmiemy się tym - jakim
reakcjom te związki ulegają.
W większości będziemy rozpisywali związki chloru, ale
pamiętajmy zastąpienie go bromem lub jodem nie
powoduje większych zmian.

.
Właściwości fizyczne halogenków alkilów
• Z powodu większej masy cząsteczkowej halogenoalkany
mają wyższe temperatury wrzenia niż alkany o tej samej
liczbie atomów węgla w cząsteczce.
• Przy określonej grupie alkilowej temperatura wrzenia
wzrasta wraz ze wzrostem masy atomowej halogenu.
( temperatura wrzenia fluorku jest najniższa, a jodku
najwyższa).
• Halogenki alkilów mimo iż są polarne nie rozpuszczają się
w wodzie (prawdopodobnie dlatego, że nie mogą tworzyć
wiązań wodorowych).
• Rozpuszczają się natomiast w typowych rozpuszczalnikach
organicznych.
• Jodo-, bromo- i polichloropochodne alkanów mają większą
gęstość niż woda.

.
Wyróżnimy trzy podstawowe reakcje halogenków.
1. Wymiana fluorowca na inny podstawnik - podstawienie
nukleofilowe (substytucja)
Np. CH3CH2Cl + OH-
CH3CH2OH + Cl-
Chloroetan
etanol
(chlorek etylenu)
(alkohol etylowy)
Wymiana fluorowca na inne podstawniki przebiega
łatwo i ma duże znaczenie praktyczne w
zależności od tego z jakim atomem węgla jest
połączony fluorowiec. Gdy atom fluorowca jest
połączony z pierścieniem aromatycznym, albo z
atomem węgla tworzącym wiązanie podwójne jak
np.
w
chlorku
winylu
(chloroeten),
to
podstawienie nukleofilowe zachodzi bardzo
trudno i nie ma większego znaczenia.
.
2. Dehydrohalogenacja - eliminacja (odłączenie) atomów wodoru
i fluorowca znajdujących się przy sąsiednich atomach węgla.
Np.
CH3CH2Cl
CH2 = CH2 + HCl
Jest to metoda syntezy związków nienasyconych . Synteza taka
wymaga reakcji eliminacji, czyli odłączenia podstawników od
sąsiednich atomów węgla. Często stosowanymi substratami
eliminacji są związki halogenoorgniczne
. CH3CH2Cl + OH-
CH2 =CH2 + H2O + Cl-
(gdy eliminacja
zachodzi pod działaniem wodorotlenku sodu, to produktem nie są kwasy HX a
ich sole i woda)
Z 1-chlorobutanu powstaje tylko jeden alken
CH3CH2CH2CH2Cl
eliminacja HCl
CH3CH2CH=CH2
Z 2-chlorobutanu powstaje mieszanina 1-butenu i 2-butenu
CH3CH2CHCH3
eliminacja HCl
CH3CH=CHCH3 +
CH3CH2CH=CH2
Cl

.
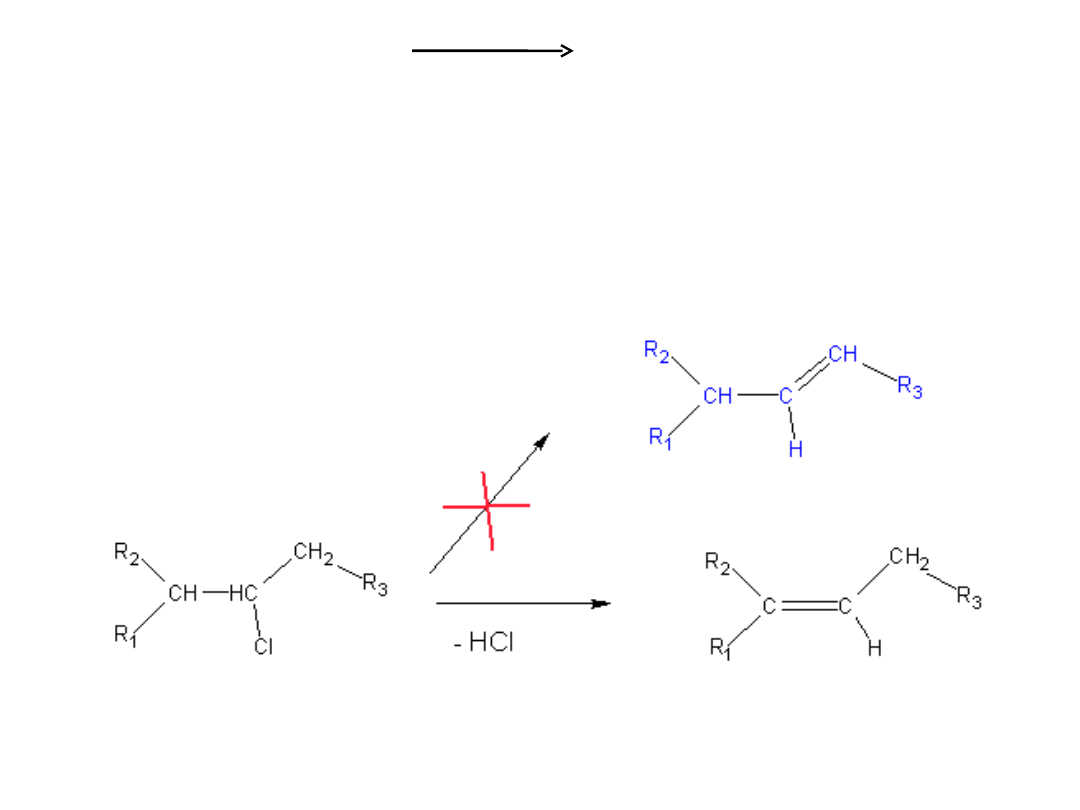
Powstanie mieszanin jest możliwe wtedy, gdy odłączane
atomy wodoru znajdują się przy atomach węgla leżących
po obu stronach atomu z wiązaniem C – Cl
Eliminacja HCl ze związków halogenoorganicznych podlega
tym samym ograniczeniom , co podstawienie nukleofilowe.
Reakcje zachodzą bardzo trudno gdy fluorowiec połączony
jest z pierścieniem aromatycznym lub z atomem węgla
tworzącym wiązanie podwójne
Grupa alkilowa to
grupa węglowodorowa, uzyskana
z
cząsteczki węglowodoru, po oderwaniu od niej jednego
atomu wodoru
Grupa arylowa
- jednowartościowa grupa utworzona przez
oderwanie atomu wodoru od pierścienia aromatycznego.

.
3. Tworzenie związków metaloorganicznych w reakcji z
metalami.
Np. CH3CH2Cl + Mg CH3CH2MgCl
chlorek etylomagnezu
Związek metaloorganiczny to związek zawierający
zawierający wiązania
atomów węgla z atomami metalu.Największe znaczenie w
syntezie organicznej mają związki magnezu nazywane
związkami Gringarda
RMgX (wzór ogólny)
R – grupa alifatyczna lub aromatyczna
X – Cl, Br, I
Związki magnezoorganiczne tworzą się bardzo łatwo z
metalicznego magnezu i związków halogenoorganicznych
C6H5Br + Mg
C6H5MgBr

.
4. Redukcja metalem w środowisku kwasowym
RX + M + H+ → RH + M
+
+ X-
Np.
CH
3
CH
2
CHCH
3
Zn, H+
CH
3
CH
2
CHCH
3
Br
H
Otrzymywanie halogenków alkilów
1. Wymiana grupy –OH
R-OH
HX lub PX3
RX
Np. CH3CH2CH2OH
stęż.HBr lub NaBr, H2SO4
CH3CH2CH2Br
alkohol n-propylowy ogrzewanie bromek n-propylu
2. Halogenowanie niektórych węglowodorów
R-X
X2
RX + HX
Np. CH3
CH3
CH3 – C - CH3
Cl2 ogrzew. lub światło
CH3 - C - CH2Cl
CH3
CH3
neopentan
chlorek neopentylu
3. Addycja halogenowodorów do alkenów
- C = C -
HX
- C – C -

.
Np.
CH3CH2CH=CH2 + HI
CH3CH2CHICH3
1-buten
2-jodobutan
CH3
CH3
CH3 – C = CH-CH3 + HI CH3 –C – CH2-CH3
I
2-metylo-2-buten 2-jodo-2-metylobutan (
jodek tetr-pentylu)
Skąd wiemy, że powstaje taki właśnie produkt?
Na podstawie badań reakcji addycji rosyjsko uczony Włodzimierz
Markownikow wyciągnął wniosek, że w przypadkach w których mogą
powstać dwa izomeryczne produkty, tworzy się zazwyczaj jeden z nich w
nadmiarze.
W 1869 roku
Markownikow
wykazał, że
: podczas jonowej addycji
kwasu do wiązania podwójnego węgiel-węgiel alkenu, atom
wodoru cząsteczki kwasu przyłącza się do tego atomu
węgla , z którym połączona jest już większa liczba atomów
wodoru
.
Czyli ogólnie mówiąc „każdemu, kto posiada będzie dane”, lub „ci, co
posiadają otrzymają”
.
CH3CH2CH=CHCH3 + HI
CH3-CH2-CHI-
CH2-CH3 +
2-penten
CH3-CH2-CH2-CHI-CH3
W przypadku pentenu każdy z atomów węgla połączonych
wiązaniem podwójnym ma jeden atom wodoru i dlatego
powinniśmy się spodziewać powstania obu produktów
mniej więcej w równych ilościach.
Reguła Zajcewa - w reakcji eliminacji wodór zostanie
odłączony od tego atomu węgla, który posiada mniej
atomów wodoru.
.
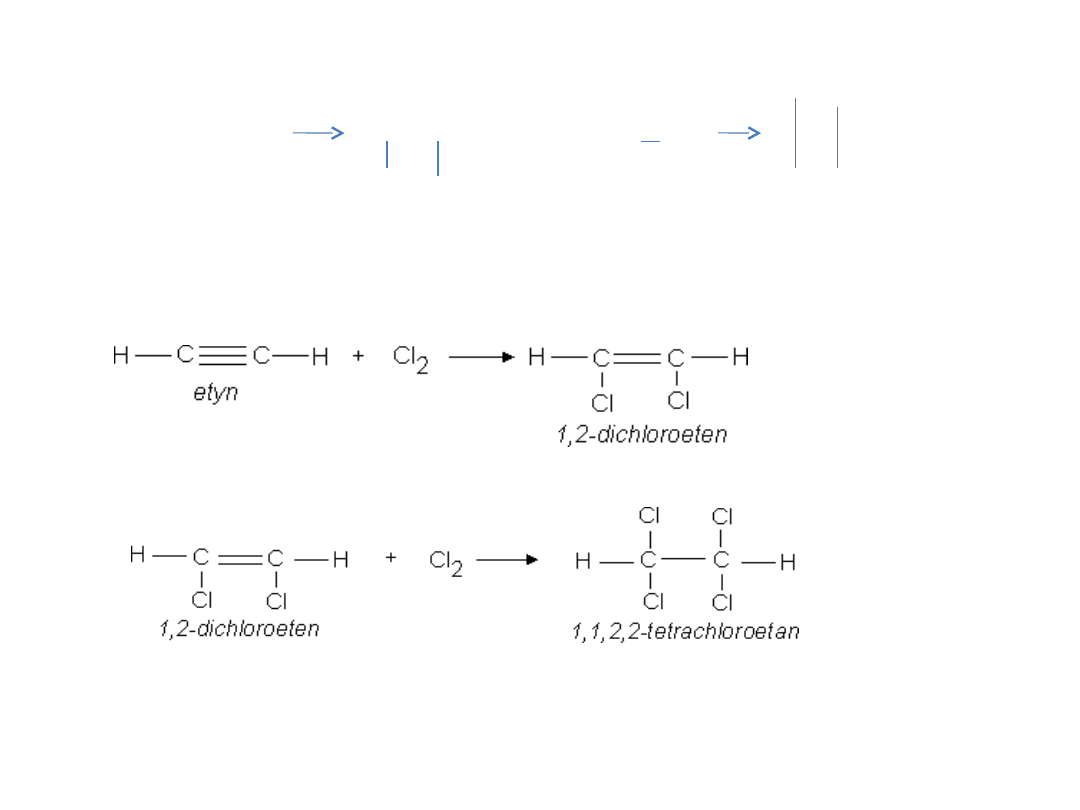
4. Addycja halogenków do alkenów i alkinów
X X
- C = C -
X2
- C – C –;
-C = C -
2X2
- C – C -
X X
X X
Np.
CH2=CH2 + Cl2 → CH2Cl-CH2Cl
CH3CH=CH2 + Cl2 → CH3CHCl-CH2Cl

.
5. Wymiana halogenu
RX + I-
aceton
R- I + X-
Halogenki alkilów otrzymuje się niemal zawsze z alkoholi,
ponieważ w wielu przypadkach są one dostępne jako
produkt handlowy lub stosunkowo łatwo można je
zsyntetyzować .
Niektóre halogenki można najdogodniej otrzymać w wyniku
bezpośredniego halogenowania
.
Otrzymywanie związków halogenoorganicznych
Chlorek winylu jest wytwarzany obecnie z etylenu w procesie
dwuetapowym, polegającym na przyłączaniu chloru i eliminacji
chlorowodoru.
CH2=CH2
Cl2
ClCH2CH2Cl
-HCl
CH2=CHCl
chlorek winylu (chlorekwinylu)
Jest on wykorzystywany do produkcji polichlorku winylu. Jest to
jeden z najtańszych i najbardziej pożytecznych polimerów
n CH3=CHCl
polimeryzacja
(-CH2-CH-)n
Cl
polichlorek winylu
„TRI” – dawniej używany w pralniach chemicznych, stosowany
jako rozpuszczalnik tłuszczów, obecnie znany jako „Narkotyk dla
ubogich” .
Otrzymujemy go z etylenu (wysoka temperatura)
CH2=CH2
Cl2
CH2Cl-CCl3
-HCl
CHCl=CCl2
1,1,1,2-tetrachloroetan 1,1,2-trichloroeten („tri”)

.
Teflon to potoczna nazwa politetrafluoroetylenu tworzywa
sztucznego o wielu zastosowaniach . Podstawową zaletą
teflonu jest jego odporność na wysokie temperatury i
odporności na działanie wielu substancji chemicznych.
Produkcja teflonu polega na polimeryzacji tetrafluoroetylenu
nCF2=CF2
polimeryzacja
(-CF2-CF2-)n
teflon
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
Wyszukiwarka
Podobne podstrony:
powiadamianie organizacji zwiazkowej, Prawo, Prawo Pracy
chem-związki organiczne, Związki organiczne
Związki fluorowców z tlenem, charakterystyka poszczególnych grup układu okresowego
Mikrobiologiczne przemiany?zazotowej materii organicznej i związków organicznych
2 14 Organiczne związki z azotem(aminy, amidy, aminokwasy, biaka)
Identyfikacja zwiazkow organicznych, związki nienasycone
ROLA ZAKŁADOWEJ ORGANIZACJI ZWIĄZKOWEJ W SPORZE ZBIOROWYM Z PRACODAWCĄ
2 14 Organiczne związki z azotem(aminy, amidy, aminokwasy, biaka)
izomeria zwiazkow organicznych
Witaminy są związkami organicznymi, uniwersytet warmińsko-mazurski, inżynieria chemiczna i procesowa
Analiza klasyczna związku organicznego I 2012
Identyfikacja zwiazkow organicznych
Izomeria związków organicznych
analiza zwiazkow organiczna id Nieznany (2)
analiza związku, chemia, organiczna
chemia sprawdzian ze zwiazkow organicznych
więcej podobnych podstron