Imińô i nazwisko:
|
ńÜWICZENIE ,,C2” POMIAR CIEPŇĀA WŇĀAŇöCIWEGO POWIETRZA METODńĄ ROZŇĀADOWANIA KONDESATORA. |
||
Kierunek i rok:
|
Ocena z kolokwium:
....................................... data ....................... podpis........................... |
Ocena ze sprawozdania:
....................................... data ....................... podpis........................... |
Ocena koŇĄcowa:
....................................... data ....................... podpis........................... |
Nazwisko prowadzńÖcego zajńôcia:
|
|
|
|
I.WSTńėP TEORETYCZNY
R√≥wnanie stanu gazu doskonaŇāego:
Przemianńô izotermicznńÖ (T = const) opisuje prawo Boyle'a i Mariotte'a:
Dla ustalonej porcji gazu iloczyn ciŇõnienia i objńôtoŇõci jest w ustalonej temperaturze wielkoŇõcińÖ staŇāńÖ
p1V1 = p2V2 = const
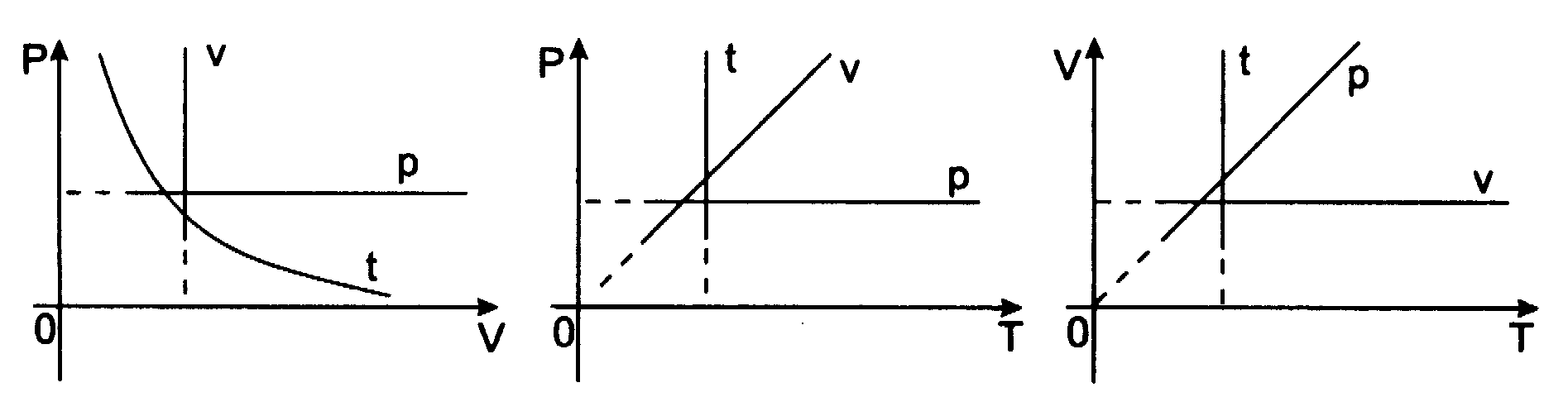
Przemianńô izobarycznńÖ opisuje prawo Gay - Lussaca:
Dla ustalonej porcji gazu pod staŇāym ciŇõnieniem wzrost temperatury o 1oC powoduje wzrost objńôtoŇõci gazu o
objńôtoŇõci, jakńÖ zajmowaŇā gaz w temperaturze 0oC
V - objńôtoŇõńá gazu w temperaturze t (oC) V0 - objńôtoŇõńá gazu w temperaturze 0oC
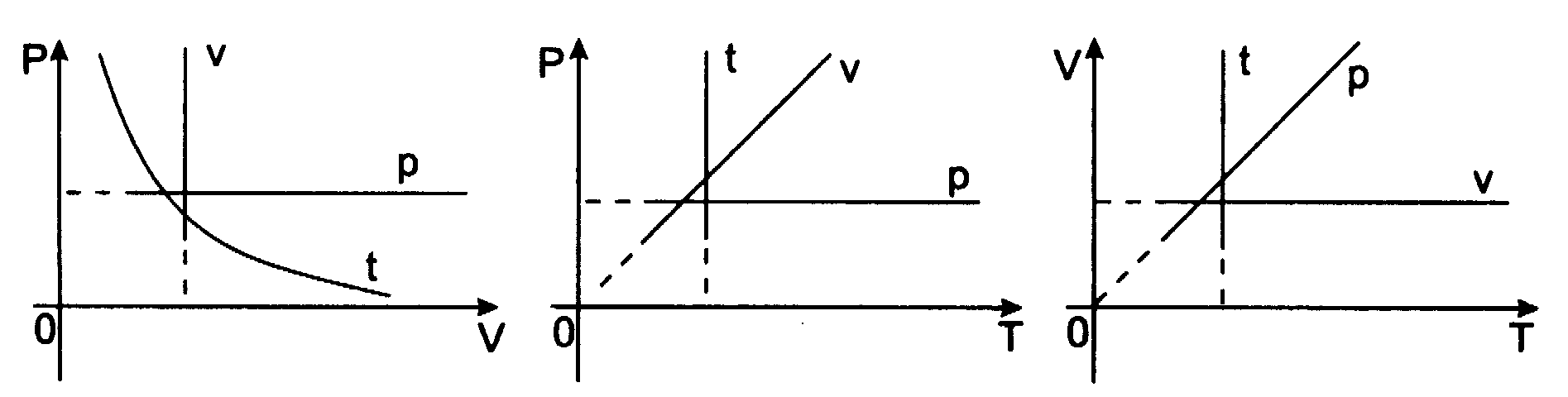
Przemianńô izochorycznńÖ (V = const) opisuje prawo Charlesa:
Dla ustalonej porcji gazu w staŇāej objńôtoŇõci wzrost temperatury o 1oC powoduje wzrost ciŇõnienia gazu o
ciŇõnienia, jakie miaŇā gaz w temperaturze 0oC
p - ciŇõnienie w temperaturze t
p0 - ciŇõnienie w temperaturze 0oC
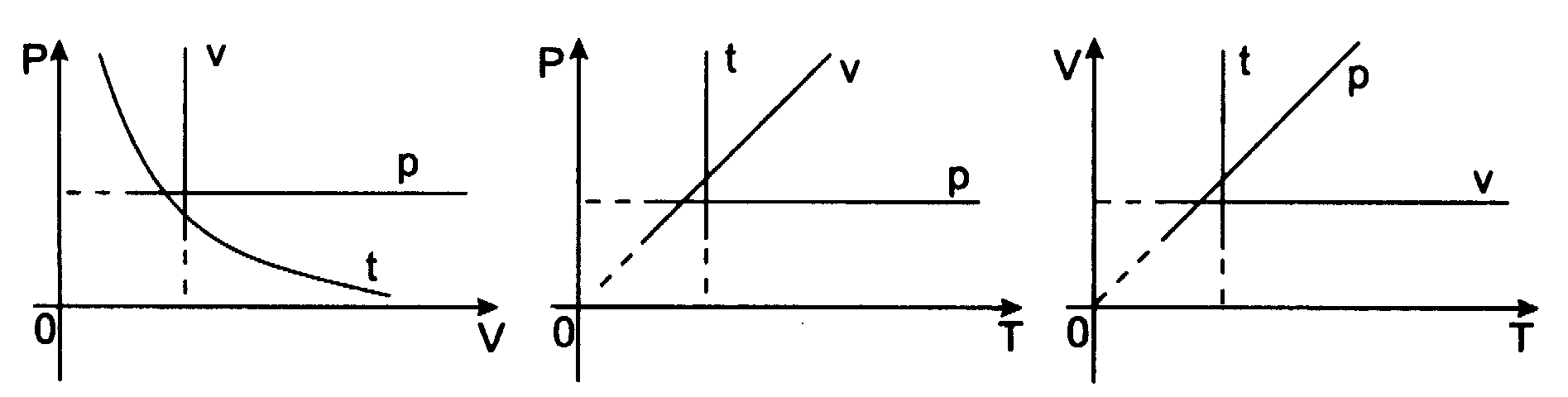
Prawo Gay - Lussaca i Charlesa uzyskujńÖ postańá, gdy temperaturńô podajemy w skali Kelwina:
T - odpowiada temperaturze t
T0 - odpowiada temperaturze 0oC
Pierwsza zasada termodynamiki - zmiana energii wewnńôtrznej ciaŇāa r√≥wna jest algebraicznej sumie pracy wykonanej nad ciaŇāem przez siŇāy zewnńôtrzne i ciepŇāa wymienionego z otoczeniem
őĒEk = W + Q
őĒEk - zmiana energii wewnńôtrznej
W - wykonana praca
Q - ciepŇāo wymienione z otoczeniem
Zasada ta stwierdza, Ňľe dostarczone ciepŇāo dQ moŇľe byńá wykorzystane na wzrost energii wewnńôtrznej dE i wykonanie przez gaz pracy dW.
dQ = dE + dW = dE + pdW
Podczas ogrzewania ciaŇāa z zachowaniem staŇāej objńôtoŇõci, ciepŇāo musi byńá dostarczone jedynie na wywoŇāanie przyrostu energii wewnńôtrznej, zwińÖzanego ze wzrostem temperatury, natomiast podczas ogrzewania pod staŇāym ciŇõnieniem gaz sińô rozszerza i wykonuje prace (dV‚Ȇ0), co wymaga dostarczenia wińôkszej iloŇõci energii potrzebnej zar√≥wno na wzrost energii wewnńôtrznej, jak i wykonanie pracy.
CiepŇāo molowe - to iloŇõńá ciepŇāa potrzebna do ogrzania 1 mola substancji o 1 Kelwin. CiepŇāo molowe przy staŇāej objńôtoŇõci wnosi:
n - liczba moli
i - liczba stopni swobody
Ňörednia energia czńÖsteczki gazu jest proporcjonalna do temperatury:
i - liczba stopni swobody
k - staŇāa Boltzmana
Dla gazu jednoatomowego i = 3 (do opisu tego gazu wystarczy znajomoŇõńá trzech skŇāadowych prńôdkoŇõci). Dla gazu dwuatomowego, i = 5, gdyŇľ ruch takiej czńÖsteczki opisujńÖ trzy skŇāadowe prńôdkoŇõci ruchu Ňõrodka masy i dwie skŇāadowe zwińÖzane z ruchem obrotowym.
Dla gazu dwuatomowego energia wewnńôtrzna wyniesie:
N - liczba Avogadro
Nk = R - staŇāa gazowa
Dlatego teŇľ ciepŇāo molowe przy staŇāej objńôtoŇõci wyniesie:
Zasada ekwipartycji energii - gdy liczba punkt√≥w jest bardzo duŇľa i obowińÖzuje mechanika Newtonowska, w√≥wczas wszystkie wyrazy tj.
, majńÖ takńÖ samńÖ wartoŇõńá i ta wartoŇõńá zaleŇľy wyŇāńÖcznie od temperatury.
Innymi sŇāowy dostńôpna energia zaleŇľy wyŇāńÖcznie 0od temperatury i rozkŇāada sińô w r√≥wnych porcjach na wszystkie sposoby, w jakie moŇľe jńÖ absorbowańá czńÖsteczka. KaŇľdy z takich sposob√≥w absorbcji energii nazywany stopniami swobody.
Kondensatorem - nazywamy taki ukŇāad przewodnik√≥w, w kt√≥rym obecnoŇõńá jednego wpŇāywa na obecnoŇõńá drugiego przewodnika. TworzńÖce go przewodniki nazywamy okŇāadkami kondensatora.
PojemnoŇõcińÖ kondensatora - nazywamy stosunek zgromadzonego na nim Ňāadunku Q do r√≥Ňľnicy potencjaŇā√≥w mińôdzy jego okŇāadkami. WielkoŇõńá ta jest staŇāa dla danego kondensatora, jeŇõli znajdujńÖce sińô w pobliŇľu naŇāadowane lub uziemione przewodniki nie zmieniajńÖ poŇāoŇľenia. WielkoŇõńá ta informuje nas, jaki Ňāadunek wprowadzińá na okŇāadki, by napińôcie mińôdzy nimi wynosiŇāo 1V. JednostkńÖ pojemnoŇõci w ukŇāadzie ,,SI” jest
(jeden Farad)
W ukŇāadzie pomiarowym nastńôpuje rozŇāadowanie kondensatora przez opornik (kt√≥ry, w tym przypadku stanowi spirala), znajdujńÖcy sińô w naczyniu z gazem (naczynie Dewara). Wzrost temperatury spirali powoduje wzrost temperatury gazu w wyniku czego, gaz zwińôksza swojńÖ objńôtoŇõńá i ciŇõnienie. Wzrost ciŇõnienia mierzymy za pomocńÖ manometru rtńôciowego. Przy duŇľej objńôtoŇõci naczynia w stosunku do objńôtoŇõci manometru przemianńô moŇľemy uznańá za przemianńô izochorycznńÖ, zgodnie z zaleŇľnoŇõcińÖ:
U - napińôcie
C - pojemnoŇõńá kondensatora
Przyrosty ciŇõnienia zaleŇľńÖ liniowo do U2, zaŇõ wsp√≥Ňāczynnik kierunkowy (nachylenia) tej prostej:
pozwala obliczyńá CV:
II.CZńėŇöńÜ PRAKTYCZNA
WartoŇõci ustalone:
V = 0,5 · 10-3 m3
C = 5000
1000őľF = 0,005F
T = 296 K
p = 735 · 10-3 m · 9,81
· 13609
= 98060,76
Wyniki otrzymane podczas przeprowadzania doŇõwiadczenia zestawiŇāem w tabeli nr. 1:
Tab. 1
L.p |
U [V] |
U2 - xi [V] |
p [mm H2O] |
‚ąÜp - yi [Pa] |
xiyi |
xi2 |
yi2 |
1 |
12 |
144 |
0,0065 |
66,217 |
953,248 |
20736 |
4384,70 |
|
|
|
0,007 |
|
|
|
|
2 |
14 |
196 |
0,0115 |
110,3625 |
21631,05 |
38416 |
12179,90 |
|
|
|
0,011 |
|
|
|
|
3 |
16 |
256 |
0,0017 |
167,751 |
42944,256 |
65536 |
28140,40 |
|
|
|
0,0172 |
|
|
|
|
4 |
18 |
324 |
0,024 |
240,345 |
77871,78 |
104976 |
577657,72 |
|
|
|
0,025 |
|
|
|
|
5 |
20 |
400 |
0,029 |
289,395 |
115758 |
160000 |
83749,45 |
|
|
|
0,030 |
|
|
|
|
6 |
22 |
484 |
0,037 |
367,875 |
178051,5 |
234256 |
135332,02 |
|
|
|
0,038 |
|
|
|
|
7 |
24 |
576 |
0,044 |
441,45 |
254275,2 |
331776 |
194878,1 |
|
|
|
0,046 |
|
|
|
|
8 |
26 |
676 |
0,055 |
549,36 |
371367,36 |
456976 |
301796,41 |
|
|
|
0,057 |
|
|
|
|
9 |
28 |
784 |
0,067 |
664,6275 |
521067,96 |
614656 |
441729,71 |
|
|
|
0,0685 |
|
|
|
|
‚ąĎ |
|
3840 |
|
2897,383 |
1583920,354 |
2027328 |
1779848,40 |
Obliczam wsp√≥Ňāczynnik a i b:
Wyznaczam odchylenie standardowe od wartoŇõci a:
Wyznaczam odchylenie standardowe od wartoŇõci b:
Wyznaczam prostńÖ teoretycznńÖ:
y = ax + b ‚Üí y = 0,89x - 60
x = 0 ; y = - 60
x = 790 ; y = 643,1
Wyznaczam proste y1, y2:
y1 = (a + Sa)x + (b + Sb) y2 = (a - Sa)x + (b - Sb)
x = 0 ; y1 = 12151,85 x = 0 ; y2 = -12271,185
x = 790 ; y1 = 13036,65 x = 790 ; y2 = 12270,525
Obliczam ciepŇāo wŇāaŇõciwe ze wzoru:
Wyznaczam niepewnoŇõńá ciepŇāa wŇāaŇõciwego metodńÖ r√≥Ňľniczki zupeŇānej:
Wyznaczam niepewnoŇõńá procentowńÖ pomiaru ciepŇāa wŇāaŇõciwego:
Wnioski:
Celem doŇõwiadczenia byŇāo wyznaczenie ciepŇāa wŇāaŇõciwego powietrza metodńÖ rozŇāadowania kondensatora. BŇāńôdy obliczeniowe powstaŇāy na skutek niedokŇāadnoŇõci przyrzńÖd√≥w pomiarowych. Pomimo to wyniki sńÖ obarczone doŇõńá maŇāńÖ niepewnoŇõcińÖ ok. 3,31%.
1
Wyszukiwarka
Podobne podstrony:
2 definicje i sprawozdawczoŇõńáid 19489 ppt
PROCES PLANOWANIA BADANIA SPRAWOZDAN FINANSOWYC H
W 11 Sprawozdania
Wymogi, cechy i zadania sprawozdawczoŇõńái finansowej
Analiza sprawozdan finansowych w BGZ SA
W3 Sprawozdawczosc
1 Sprawozdanie techniczne
Karta sprawozdania cw 10
eksploracja lab03, Lista sprawozdaniowych bazy danych
2 sprawozdanie szczawianyid 208 Nieznany (2)
Fragmenty przykŇāadowych sprawozdaŇĄ
Lab 6 PMI Hartownosc Sprawozdan Nieznany
Mikrokontrolery Grodzki Sprawoz Nieznany
biochemia sprawozdanie O (1)
Chemia fizyczna sprawozdanie (6 1) id 112219
201 sprawozdanie finansoweid 26953
Czarne orly sprawozdanie2
lrm sprawozdanie kck lab2
wińôcej podobnych podstron