POBUDLIWOŚĆ I MIĘŚNIE
Osoby odpowiedzialne za pytania:
1-5 Przemysław Cnota
6-14 Adam Cugowski
15-23 Anna Gwizdek
24-28 Rafał Młotek
1. Jakie są rodziaje transportu błonowego?
Rodzaje transportu błonowego:
Dyfuzja
Dyfuzja jest zjawiskiem fizycznym któremu ulegają wszystkie cząsteczki. Jednym zdaniem jest to samorzutny ruch cząsteczek. Cząsteczki mają to do siebie że jak jest ich za dużo to przepływają tam gdzie jest ich mniej i tak prostymi słowy wygląda dyfuzja. Jest ona wszechobecna we wszelkich układach biologicznych i nie tylko. Podlega ona prawu Ficka które wyrażone jest za pomocą prawidłowości:
Gdzie:
F- dyfuzja
K- stała
C1, C2 - stężenia substancji w dwóch przedziałach
Prawo to mówi iż szybkość dyfuzji jest wprost proporcjonalna do różnicy stężeń pomiędzy dwoma przestrzeniami, natomiast odwrotnie proporcjonalna do masy cząsteczek.
Dyfuzja ułatwia ruch cząsteczek na małych odległościach, np. wymiana składników pomiędzy osoczem a komórkami, czy też wymiana tlenu i dwutlenku węgla pomiędzy pneumocytami a powietrzem. Dyfuzja cząsteczek przez błony komórkowe nie jest jednak prostym procesem, albowiem zależy od strunktury owej błony, a mianowicie jest to twór lipidowy który jest nieprzepuszczalny dla cząsteczek hydrofilnych takich jak jony, woda, czy też białka, za to swobodnie jest przepuszczalna dla małych cząsteczek obojętnych elektrycznie (tlen, dwutlenek węgla, amoniak, alkohol) i lipidów. Jony natomiast transportowane są za pomocą odpowiednich kanałów dla tych jonów, czy też przenośników. Kanały te mogą być bramkowane odpowienimi zjawiskami fizycznymi lub chemicznymi (bramkowanie napięciem, chemiczne, fizyczne).
Przy dyfuzji warto wspomnieć o zjawisku osmozy. Wobraźmy sobie dwie przestrzenie przedzielone błoną półprzepuszczalną. Jak w każdym środowisku oba przedziały dążą do wyrównania stężeń pomiędzy sobą, lecz nie zapominajmy iż błona nie przepuszcza żadnych jonów, więc wyrównanie stężeń opiera się na ruchach wody. Jeśli do jednej przestrzeni dodamy soli i wzrośnie osmotyczność w tym miejscu druga przestrzeń będzie dążyła do wyrównania stężenia i nastąpi ruch wody z przestrzeni o mniejszej zawartosći (stężeniu) soli do tej drugiej, co spowoduje wzrost objętości. Nie można tego też tak interpretować, że jeśli w pierwszej przestrzeni nie będzie wcale soli to cała woda przejdzie do drugiej, bo trzeba mieć jeszcze na uwadze takie zjawiska jak wzrost ciśnienia hydrostatycznego w drugiej przestrzeni, które w pewnym momencie wzrośnie na tyle i będzie hamować ruch wody.
Transporty na nośnikach
Jest to specyficzny rodzaj transportu przeznaczony dla cząstek takich jak glukoza, czy aminokwasy. Cząstki te są wysoce spolaryzowane, natomiast ich średnica znacznie przekracza wielkość porów. Transport ten polega na reakcji tej cząstki z białkiem błonowym, czyli najpierw nasza cząstka A łączy się z białkiem przenośnikowym B, tworząc kompleks A-B. Kompleks ten następnie albo zmienia swoją konformacje, lub też może dyfundować, albo ulec zwykłej rotacji, umieszczając naszą cząstkę A po drugiej stronie błony, gdy do tego dojdzie na drodze dysocjacji cząsteczki rozdzielają się.
Wg Konturka transport nośnikowy ma kilka istotnych cech:
Stereospecyficzność - swoistość, czyli transporter glukozy nie przeniesie aminokwasu
Nasycenie - w przeciwieństwie do dyfuzji, transport na nośnikach może ulec wysyceniu, ponieważ po prostu zabraknie nośników i utrzymuje się na stałym maksymalnym poziomie.
Współzawodnictwo - cząsteczki podobne walczą o nośniki
Transport ten można podzielić na dwie klasy:
Transport ułatwiony
Istotnym jest iż transport ten ma wszystkie te cechy transportu na nośnikach, lecz jest bierny energetycznie, gdyż zachodzi zgodnie z gradientem stężeń, a więc wykorzystuje zjawisko wszechobecnej dyfuzji. Przyładem takiego transportu jest transport glukozy, który może odbywać się na nośnikach GLUT 1-5, lub może być sprzężony z wchłanianiem sodu np. w jelitach, czy kanalikach nerkowych.
Transport aktywny
Jest to transport wymagający nakładów energetycznych, najczęściej w postaci ATP, który umożliwia przechodzenie przez błony substancjom nawet wbrew gradientom ich stężeń. Znamiennym przykładem takiego transportera są ATPazy jonowe, które napędzane energią z hydrolizy ATP przerzucają jony warunkując odpowiednie środowisko dla więkoszości przemian w organizmie, zaczynając od pobudliwości, a kończąc na wydzielaniu soku żołądkowego i wchłanianiu kanalikowym w nerkach. Możemy uwzględnić tutaj dwa rodzaje transportu aktywnego, pierwotny oraz wtórny. Transport aktywny pierwotny jest to typowa ATPaza i możemy wyróżnić 4 takie transportery czynne pierwotne: ATPazy (1. sodowo-potasowa; 2. wapniowa; 3. wodorowa; 4. wodorowo- potasowa). Wtórny transport aktywny polega na tym iż źródłem energii do transportu substancji jest różnica stężeń jonów. Np. Glukoza wiąże się z białkiem przenośnikowym które przenosi ją wraz z jonami sodowymi zgodnie z ich gradientem stężeń, natomiast ten gradient wytworzony jest przez działającą ATPazę sodowo-potasową, która stale wypompowywuje jony sodowe stważając gradient.
Pinocytoza i fagocytoza
Procesy tzw. picia i jedzenia komórkowego. Pinocytoza polega na tym, że wchłaniane są przez komórki cząsteczki znajdujące się w roztworze wodnym, wytwarzając charakterystyczne pęcherzyki pinocytozowe w miejscu receptorowym dla tej substancji. Ten pęcherzyk z kolej wnika w głąb komórki i tam jest dalej wykorzystany w odpowiedni sposób. Jeżeli pinocytoza nie zachodzi z użyciem receptora, wtedy jest to pinocytoza podstawowa, dla odróżnienia od pinocytozy za pośrednictwem receptorów. Przykłady pinocytozy: Wchłanianie LDL, insuliny, EGF, toksyn i wirusów.
Fagocytoza z kolei jest nazwana pożeraniem komórkowym. Powszechnie wykorzystywana przez makrofagi, które oczyszczają nasz organizm z bakterii, obumarłych lub uszkodzonych komórek. Cząstka wchłaniająca w tym mechaniźmie ściśle przylega do cząstki wchłanianej, która następnie wpukla się w obręb cz. wchłaniającej wytwarzając tzw. pęcherzyk fagocytowy który przemieszcza się w głąb komórki gdzie lizosomy przyłączają się i wpuszcają do niego enzymy trawienne. Fagocytoza wymaga receptorów błonowychi wiązania cząstek z powierzchnią błony.Czasami jest wspomagana opsoninami które opłaszczają potencjalną cząstkę przeznaczoną do wchłonięcia i umożliwiając jej wchłonięcie są tzw. „usmaczniaczami”. Resztki niestrawione tworzą tzw. ciałko resztkowe, które albo ulega rozpuszczeniu w cytoplaźmie, albo jest usuwane z komórki.
2. Jak powstaje potencjał spoczynkowy w neuronie?
Jony które biorą udział w powstawaniu potencjału spoczynkowego:
jony sodowe
jony potasowe
jony chlorkowe
jony wodorowe, wodorowęglanowe, wapniowe i magnezowe (stosunkowo niewielki udział w potencjale spoczynkowym w porównaniu do pozostałych)
Błona komórkowa ma kanały jonowe stale otwarte i jest przepuszczalna dla wszystkich trzech rodzajów jonów, jednakże w różnym stopniu. Najbardziej przepuszczalna jest dla jonów potasowych (ok. 10 razy bardziej niż dla jonów sodowych), nieco mniej dla jonów chlorkowych, a tylko nieliczne dla jonów sodowych. Potencjał spoczynkowy w głównej mierze zależy od przepuszczalności dla jonów sodowych i potasowych. Istotne jest iż te jony przepływają jednocześnie, jednakże w przeciwnych kierunkach. Potencjał błonowy zależy od przepuszczalności i gradientów chemicznych dla tych jonów. W związku iż błona jest 10-krotnie bardziej przepuszczalna dla jonów potasowych, potencjał błonowy jest zbliżony do ich potecjału równowagi (-70mV dla jonów potasowych) i wynosi ok. -90mV.
Istotnym jest iż gdyby nie istniały żadne mechanizmy zapewniające stały rozkład jonów w komórce i przestrzeni okołokomórkowej, po czasie doszłoby do wyrównania stężeń jonów pomiędzy tymi przestrzeniami i zaniku funkcji komórki nerwowej. Z tego powodu w błonie komórki nerwowej znajduje się specyficzne białko zwane „pompą sodowo-potasową”, które za ten rozkład jonów jest odpowiedzialne. (dalszy opis tej pompy pytanie II.3)
3. Na czym polega rola pompy sodowo-potasowej?
Pompa sodowo-potasowa jest specyficznym białkiem zlokalizowanym w błonie komórkowej. Jest ona białkiem przenośnikowym i transportuje jony sodowe i potasowe, jak sama jej nazwa na to wskazuje. Jej działanie jest asymetryczne, albowiem na każde 3 jony sodowe wypompowane z komórki, 2 jony potasowe wnikają do komórki, jej działanie można więc nazwać działaniem pompy elektrogennej. Jest to aktywny transport tych jonów, gdyż do tego procesu jest zużywana energia w postaci rozkładu ATP. Rozkład ATP jest procesem kilkuetapowym:
przyłączenie 3 jonów sodu i rozpad ATP do ADP i fosforanu
fosforylacja ATP-azy → zmiany konformacyjne białka
wyrzucenie jonów sodowych na zewnątrz komórki
przyłączenie dwóch jonów potasowych
defosforylacja ATP-azy → powrót do pierwotnej konformacji
wyrzucenie jonów potasowych do wewnątrz komórki
Pozbawiona jonów potasowych pomopa może wykonać ten cykl od nowa. Warto nadmienić również iż pompę sodowo-potasową możemy zablokować niektórymi związkami:
glikozydami naparstnicy (ouabaina, strofantozyna)
nitrofenolem (bloker fosforylacji)
Przeciętnie jedna komórka ma ok miliona pomp, a każda wykazuje 30 cykli na sekundę.
Podsumowując do funkcji tej pompy należą:
Transport jonów przeciwko gradientowi stężeń
Utrzymanie różnicy stężeń jonów po obu stronach błony
Utrzymanie potencjału błonowego
Utrzymanie stałej osmolarności wnętrza komórki i jej objętości
Napęd do wtórnego transportu czynnego innych związków (wchłanianie jelitowe)
Utrzymanie prawidłowej funkcji tej pompy wymaga spełnienia kilku istotnych warunków:
Stały dopływ tlenu i odpływ dwutlenku węgla
Niezaburzone mechanizmy resyntezy ATP
Odpowiedniego stosunku stężeń jonów wewnątrz i na zewnątrz komórki
Odpowiedniej temperatury
4. Jaką funkcję pełnią jony wapnia w pobudliwości?
Zmiana stężenia jonów wapnia w plynie zewnątrzkomórkowym wiążę się z pewnymi skutkami dotyczącymi pobudliwości i tak:
Wzrost stężenia jonów wapniowych prowadzi do:
Stabilizacji błony komórkowej → zmniejszenia pobudliwości;
Spadek stężenia jonów wapniowych prowadzi do:
podniesienia pobudliwości komórek nerwowych i mięśniowych;
zmniejszenie stopnia depolaryzacji wymaganej do osiągnięcia potencjału progowego
znaczny spadek powoduje całkowitą utratę pobudliwości i prowadzi do tężyczki (spadek stężenia jonów magnezu też)
przyczyna wzrostu pobudliwosci przy obnizaniu stezenia jonów wapniowych jest nieznana, przypuszca się że jony wapniowe są zlokalizowane w błonie komórkowej regulując przepuszczalność tej błony dla jonów sodowych i potasowych wpływając na pobuliwość
Warto też wspomnieć o tym iż od jonów wapnia zależy potencjał rozrusznikowy komórek które go generują, oraz cały mechanizm skurczu mięśnia i warto pamiętać iż jony wapnia są tzw. drugim przekaźnikiem dla niektórych hormonów.
5. Jak generowany jest potencjał czynnościowy w neuronie? (schemat)
Potencjał czynnościowy to szybka zmiana potencjału błonowego , trwajaca w neuronie ok. 1ms,
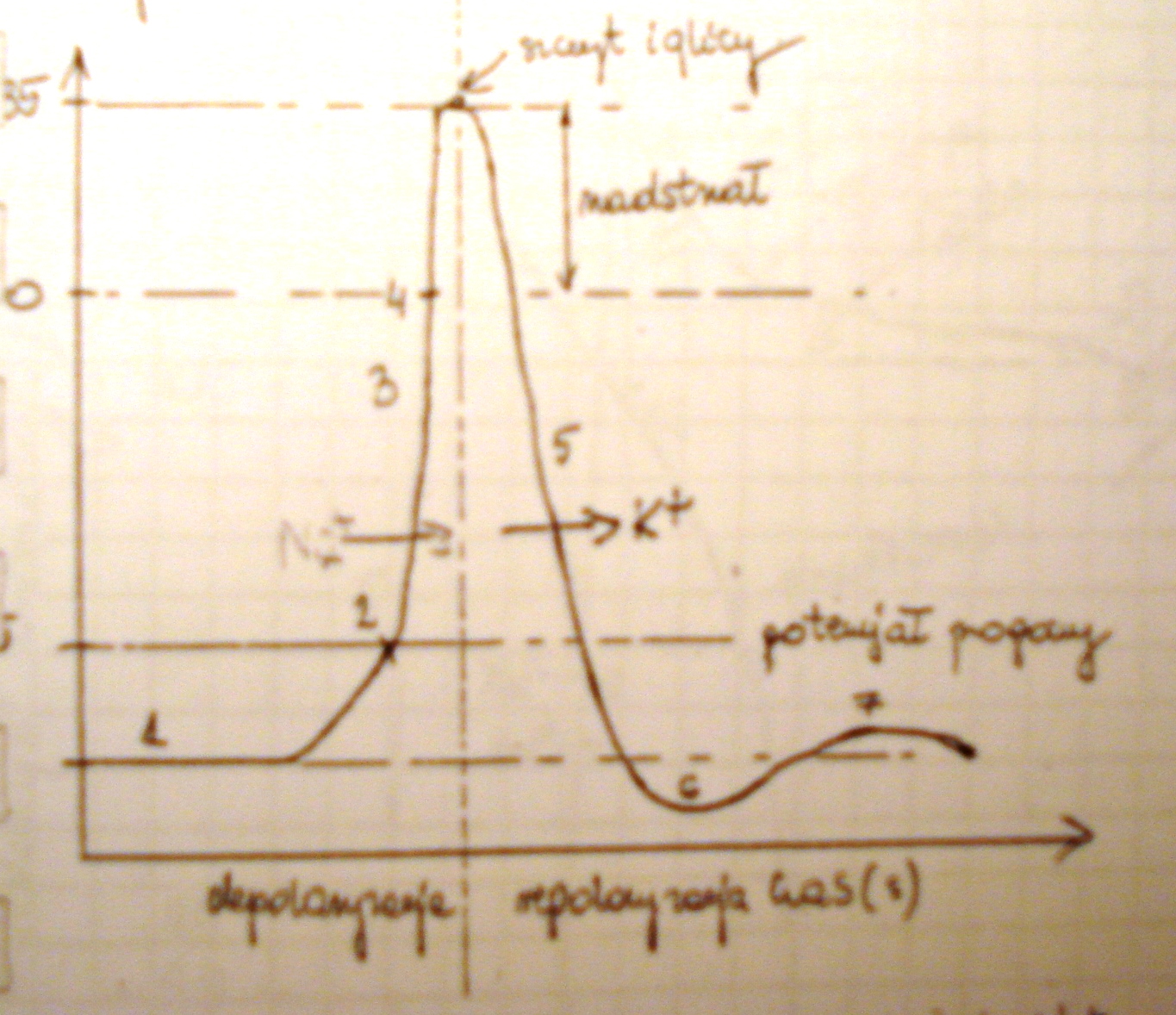
1-potencjał spoczynkowy - równowaga Na i K
2- potencjał progowy - min. Wartość bodźca wywołująca potencjał czynnościowy
3- faza wznosząca lub depolaryzująca - kom b szybko traci swój ujemny potencjał spoczynkowy na skutek aktywacji sodowej- wzrost ok. 600x dokomórkowego prądu Na+, przewodność dla K bez mian. Aktywacja sodowa jest skutkiem otwierania bramkowanych potencjałem kanałów dla Na , potencjał błonowy spada do 0- (pkt 4) a nast. Ulega odwróceniu (nadstrzał') osiągając war dodatnie, tuż przed „szczytem iglicy następuje Inaktywacja sodowa, czyli zamykaja się kanały Na+.
Repolaryzacja- Na+ zamknięte → inaktywacja sodowa → nast. Aktywacja potasowa → powolne otwieranie się bramkowanych potencjałem kanałów K. jony K wypływaja zgodnie z gradientem co prowadzi do powrotu eletkroujemności wewnętrznej strony błony komórkowej.
4 Hiperpolaryzacyjny potencjał następczy- wnętrze kom bardziej elektruj. I w spoczynku
5 Podpolaryzacyjny potencjał następczy -wnętrze kom bardziej dodatnie niż w spoczynku
6 i 7 - powstają na skutek bezwładności aktywacji potasowej i przepływu K i cykl się powtarza
6. Jak generowany jest potencjał czynnościowy w miocytach serca (schemat)?
ZAJEBIŚCIE=D
Szybko narastająca depolaryzacja z nadstrzałem do +25mV, wywołana wzrostem dokomórkowego prądu jonów Na+ (z otwarciem szybkich kanałów dla Na+ bramkowanych potencjałem czynnościowym) i inaktywacja kanałów potasowych
„wstępna repolaryzacja” - początkowa, szybka repolaryzacja przechodząca w fazę 2, spowodowana inaktywacją sodową i przejściowym wzrostem przewodności dla jonów Cl- i aktywacja kanałów wapniowych
„plateau”- trwający ok. 200-300ms okres, charakteryzujący się dokomórkowym napływem jonów Ca2+, z jednoczesnym powoli narastającym wypływem jonów K+
Końcowa repolaryzacja, będąca wynikiem zamykania kanałów Ca2+( zmniejszenie prądu dokomórkowego) i silniejszą aktywacją kanałów potasowych (wzrost odpływu jonów K+ z komórki)
Powrót do wartości błonowego potencjału spoczynkowego; Aktywacja pompy Na+/K+ -ATP ( wyrzucanie Na+ na zewnątrz, a K+ do środka). Jest to okres pomiędzy skurczami.
Przez okres faz 0-2 i połowy 3 mięsień sercowy jest w stanie refrakcji bezwzględnej, a do fazy 4 refrakcji względnej.
7. Jaki jest mechanizm powstawania różnych rodzajów refrakcji?
Refrakcja limituje liczbę możliwych potencjałów czynnościowych w komórce. Wyróżniamy 2 rodzaje refrakcji (niepobudliwości):
-Bezwzględna
-Względna
Bezwzględna - w okresie potencjału iglicowego, żaden z bodźców, niezależnie od swej siły, nie jest zdolny do wywołania pobudzenia. Mechanizm powstawania opiera się na okresie potencjału iglicowego, odpowiadającemu otwieraniu kanałów dla jonów Na+ i wzmożonej przewodności dla tych jonów.
Względna - występuje bezpośrednio po refrakcji bezwzględnej. Podczas niej pobudliwość komórki stopniowo powraca, ale przez ok. 10-15ms jest jeszcze obniżona. Pobudzenie może być jedynie wywołana przez bodźce nadprogowe. Okres refrakcji względnej wiąże się z okresem wzrostu przepuszczalności błony dla jonów K+.
8. Jak dzielą się włókna nerwowe pod względem szybkości przewodzenia i od czego to zależy.
Grupa |
Podgrupa |
Czynność |
Średnica |
V(m/s) |
Osłona mielinowa |
A |
Alfa |
Czucie priopioceptywne i somatyczne,ruchowe |
12-20 |
70-120 |
Obecna
|
|
Beta |
Czucie dotyku i ucisku |
5-12 |
30-70 |
Obecna
|
|
Gamma |
Ruchowe do wrzecionek nerowo-miesniowych |
3-6 |
15-30 |
Obecna
|
|
Delta |
Czucie zimna,bólu i dotyku |
2-5 |
12-30 |
Obecna
|
B |
|
Ukł autonomiczny |
<3 |
3-15 |
Obecna
|
C |
D.R. (korzenie grzbietowe rdzenia kręgowego) |
Czucie bólu,temp, czesc czucia mechanoceptywnego, łuki odruchowe |
0,4-1,2 |
0,5-2,0 |
Brak |
|
Współczulna |
Zawzgórzowa układu autonomicznego |
0,3-1,5 |
0,7-2,3 |
Brak |
Szybkość przewodzenia w nerwach zależy od grubości poszczególnych włókien i od stopnia ich izolacji przez osłonki mielinowe. Szybkość wzrasta proporcjonalnie do średnicy wł osiowych. Przewodzenie we włóknach z osłonką ma charakter skokowy, a w bezosłonkowych ciągły.
9. Jaki jest wpływ hipo- i hiperkalemii na potencjał spoczynkowy i czynnościowy w neuronie?
Przepuszczalność błony komórkowej w spoczynku jest ok. 10 razy większa dla jonów K+ niż dla Na+. Z tego względu rozdział ładunków poprzez błonę jest uzależniony od dyfuzji jonów K+.
Dla komórki nerwowej potencjał spoczynkowy (-70mV) jest nieznacznie mniejszy od potencjału równowagi dla samego K+ (-90mV).
Hiperkalemia - obniża gradient stężeń dla jonów K+ poprzez błonę pobudliwą, powodując obniżenie potencjału błonowego w kierunku potencjału progowego. Błona staje się bardziej pobudliwa i bodźce o mniejszej sile mogą wywołać potencjał progowy.
Hipokalemia - prowadzi do hyperpolaryzacji błony i zmniejsza pobudliwość.
10. Jaki jest wpływ hipo- i hiperkalcemii na potencjał spoczynkowy i czynnościowy w neuronie.
Zmiana stężenia jonów Ca2+ modyfikuje pobudliwość komórek.
Hipokalcemia - podnosi pobudliwość, na skutek zmniejszenia stopnia depolaryzacji wymaganej do osiągnięcia potencjału progowego. Może to być wynik wzmożonego napływu jonów Na+ do komórki, który łatwiej następuje przez kanały Na+ przy obniżeniu poziomu Ca2+.
Niekiedy wyładowania potencjałów, mogą występować samorzutnie i bez bodźców. Dalsze obniżanie stężenia jonów Ca2+ powoduje jednak całkowitą utratę pobudliwości. Wzmożoną pobudliwość układu nerwowo-mięśniowego obserwuje się w tężyczce.
Hiperkalcemia - przeciwnie powoduje obniżenie pobudliwości, a tym samym stabilizuje błonę komórkową.
11. Jak schematycznie przedstawienia się krzywa pobudliwości włókien nerwowych?
Krzywa pobudliwości - krzywa Hoorwega-Weissa, określa pobudliwość włókien nerwowych.
Czas użyteczny - najkrótszy czas potrzebny do pobudzenia tkanki pobudliwej, przy użyciu bodźca o wysokim napięciu. Mierzony w ms.
Reobaza - bodziec o możliwie najniższym napięciu, przy którym występuje pobudzenie niezależnie od czasu jego trwania.
Chronaksja - czas użyteczny bodźca o sile dwukrotnie większej od reobazy. Im chronaksja mniejsza, tym większa pobudliwość.
12. Jak funkcjonuje synapsa chemiczna.
Synapsa jest wyspecjalizowanym złączem do przewodzenia stanu czynnościowego pomiędzy dwoma neuronami lub pomiędzy neuronem a komórką nieneuronową. Wyróżniamy synapsy chemiczne i elektryczne. Większość synaps ośrodkowego i obwodowego układu nerwowego ma charakter chemiczny.
Synapsa chemiczna cechuje się tym, że:
- element presynaptyczny w kształcie kolby, zawiera liczne mitochondria, neurofilamenty, siateczkę śródplazmatyczną i skupiska pęcherzyk synaptycznych w których wytwarza się i gromadzi neurotransmiter
- element pre- od postsynaptycznego oddziela szczelina synaptyczna wynosząca około 20-30nm
- w elemencie postsynaptycznym znajdują się odpowiednie receptory działania neurotransmitera
Przewodzenie impulsu elektrycznego w synapsie chemicznej rozpoczyna się depolaryzacją elementu presynaptycznego pod wpływem potencjału czynnościowego. Proces depolaryzacji zakończenia i uwalnianie z niego neuromediatora nazywa się sprzężeniem elektryczno-wydzielniczym. Wymaga obecności jonów Ca2+ w płynie zewnątrzkomórkowym, które po depolaryzacji wnikają do elementu presynaptycznego i łączą się z kalmoduliną, aktywując odpowiednia kinazę białkową. Kalmodulina fosforyluje synapsynę - białko „unieruchamiające” pęcherzyki synaptyczne. Po fosforylacji synapsyna oddziela się od pęcherzyków, które uruchomione mają możliwość zetknięcia i fuzji z błoną komórkową presynaptyczną. Pewne znaczenie ma też aktywacja fosfolipazy, dzięki której „przerzedzeniu” ulega warstwa lipidowa błony presynaptycznej w miejscu zetknięcia z pęcherzykami. W wyniku tego do szczeliny synaptycznej uwolniona zostaje zawartość pęcherzyka (neuromediator, niektóre enzymy związane z jego syntezą, ATP i białko).
W synapsach chemicznych dochodzi czasami, poza okresami depolaryzacji, do spontanicznego uwolnienia niewielkich porcji neuromediatora. Jest to proces o niewielkim nasileniu w porównaniu z uwalnianiem przekaźnika podczas depolaryzacji błony presynaptycznej.
Nerotransmitter dyfunduje przez szczelinę w czasie bardzo krótkim (0,6 ms), łączy się z receptorami i prowadzi do zmian konformacyjnych białek tej błony, co z kolei warunkuje zmiany przepuszczalności jonowej błony. Neurotransmitter może wywoływać postsynaptyczny potencjał pobudzający (EPSP) poprzez inaktywacje kanałów sodowych, prowadzącą do wzrostu przepuszalności i przewodności tylko dla jonów Na+ i depolaryzacji błony postsynaptycznej. Również może być wywołany działaniem neuroprzekaźnika postsynaptyczny potencjał hamujący (IPSP) poprzez otwieranie kanałów jonowych dla K+ i Cl-, warunkując zwiększenie przepuszalności i przewodności dla tych jonów i odpowiednio hyperpolaryzację błony.
Neuromediator może także reagować z receptorami i aktywować poprzez białka G odpowiednie enzymy, uwalniając w elemencie postsynaptycznym drugi przekaźnik w postaci cAMP, Comp, tri fosforanu inozytolu lub jonów Ca2+, co również prowadzi do aktywacji odpowiednich kinaz białkowych i ostatecznie prowadzi do zmian przepuszalności i przewodności jonowej.
Synapsy EPSP zwane są pobudzającymi (neurotransmiter np. acetylocholina, dopamina, noradrenalina, serotonina, histamina, kw. Glutaminowy), a IPSP hamującymi( GABA, glicyna). Proces łączenia neuromediatora z receptorami i wzbudzenie aktywności elektrycznej nosi nazwę sprzężenia chemiczno-elektrycznego.
Synaptyczne przewodnictwo chemiczne ma charakterystyczne właściwiości:
Jednokierunkowość - tylko zakończenie presynaptyczne zdolne jest do wytwarzania i uwalniania pakietów neurotransmitera, a błona postsynaptyczna posiada receptory, na które działa uwolniony przekaźnik. Czasami błona presynaptyczna posiada też receptory dla neurotransmitera, co po związaniu go powoduję działanie hamujące na uwalnianie mediatora przez element presynaptyczny.
Opóźnienie synaptyczne - na nie składa się czas potrzebny na uwolnienie neurotransmitera, pokonanie szczeliny synaptycznej i reakcji z receptorem postsynaptycznym. Przekazanie stanu czynnego z jednego neuronu na drugi wymaga zwykle ok. 0,1-0,5 ms u ssaków i 1-2 ms u bezkręgowców.
Wrażliwość na hipoksję, leki i zmęczenie - hipoksja, zmęczenie wywołane długim okresem przewodzenia wpływają hamująco na przewodnictwo. Również zaburzenie stosunku stężeń Ca2+ do Mg2+ w płynie zewnątrzkomórkowym zwalnia przewodnictwo. Wzrost stężenie jonów Ca2+ ułatwia, a jonów Mg2+ utrudnia przewodzenie. Zadziałanie TTX (tetrodotoksyna) lub TEA (jony tetraetyloamonowe) uniemożliwia powstawanie i przewodzenie potencjałów w nerwach.
Sumowanie czasowe i przestrzenne - elementy postsynaptyczne są miejscem integracji EPSP i IPSP, potencjały postsynaptyczne zajmują określone obszary błony neuronu pozastylowego i trwają określony czas, co jest wynikiem sumowania albo czasowego albo przestrzennego. (wiecej o tym patrz. Pytanie 5 z działu VII. Układ nerwowy)
Torowanie - amplituda pobudzającego potencjału pozastykowego rośnie wraz z częstością działania bodźca, ułatwiając wyładowanie potencjału czynnościowego.
Hamowanie pre- i postsynaptyczne - hamowanie może powstać na zasadzie sumowania IPSP powodując hyperpolaryzację takie hamowanie zwane jest bezpośrednim. Hamowanie pośrednie będące następstwem refrakcji bezwzględnej po poprzednim wyładowaniu, może być realizowane za pomocą neuronów wstawkowych i miech charakter hamowania zwrotnego, reciprokalnego i „podawanego naprzód”. Hamowanie presynaptyczne związane jest z istnieniem synaps aksono-aksonalnych, polega ono na redukcji amplitudy impulsów nerwowych dopływających do zakończeń synaptycznych i stanowi to swoisty „filtr” regulujący uwalnianie neurotransmitera i przepływ tych impulsów z jednego na następny neuron.
13. Czym jest neuroprzekaźnik?
Neuroprzekaźnik jest to substancja w ośrodkowym i obwodowym układzie nerwowym, pośrednicząca w przewodnictwie synaptycznym. Cechy jakie musi spełniać neurotransmiter:
- musi być zawarta w zakończeniu neuronu presynaptycznego (chemiczne jej wykazanie oraz identyfikacja układu enzymatycznego zdolnego do jej syntezy i rozkładu)
- powinna być uwalniana z zakończeń neuronu presynaptycznego w obecności jonów Ca2+
- działanie powinno polegać na zmianie potencjału błonowego elementu postsynaptycznego, a sam mediator powinien być szybko inaktywowany albo przez swoisty enzym albo przez wychwyt neuronalny
- działanie na element postsynaptyczny powinno być podobne do efektu stymulacji neuronu presynaptycznego
- działanie powinno podlegać wpływom środków blokujących w podobny sposób, jak ich wpływom podlega zwykłe przenoszenie synaptyczne
- obecność w błonie postsynaptycznej receptorów zdolnych do swoistej reakcji z neuromediatorem
14. Na czym polega zjawisko torowania (rysunek).
Torowanie polega na depolaryzacji błony w kierunku potencjału progowego, tak że neuron postsynaptyczny staje się bardziej pobudliwy.
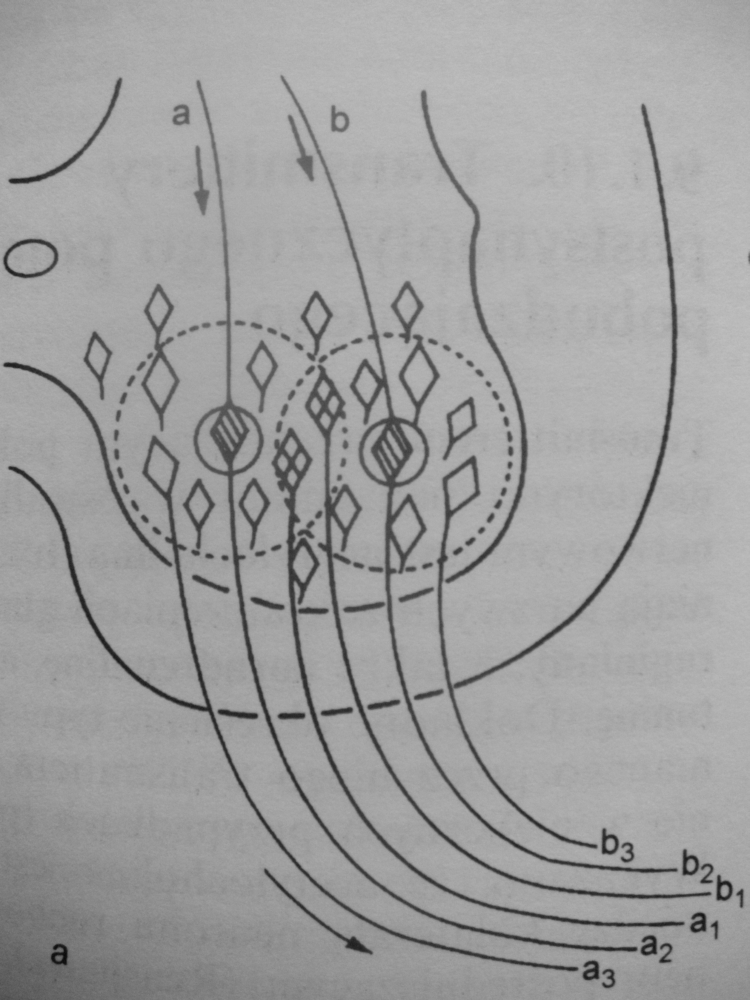
Czynnikiem, który określa wielkość reakcji odruchowej jest zbieżność dróg dośrodkowych na neuronach ruchowych.
Po podrażnieniu nerwu dośrodkowego (a), tylko 1 neuron (a2) znajduje się w strefie wyładowania (ograniczona linią ciągła). Ten neuron wysyła impulsy przez korzenie brzuszne. Trzy neurony zawarte są w strefie zwiększonej podprogowo pobudliwości ( ograniczona linią przerywana) - te neurony ulegają torowaniu.
Droga dośrodkowa (b) podobnie jak droga (a) ma jeden neuron w strefie wyładowania i trzy w strefie zwiększonej pobudliwości. Strefy zwiększonej pobudliwości częściowo na siebie zachodzą.
Jeśli pobudzone zostaną jednocześnie obie drogi, to pobudzenie neuronów, które znajdują się w strefie podprogowej będzie większe i osiągnie potencjał krytyczny wyładowania. Wielkość reakcji odruchowej będzie opowiadała pobudzeniu 4 neuronów. Tak więc reakcja będzie znacznie większa od sumy reakcji wywołanych osobnym drażnieniem każdej drogi.
Różnica między reakcją na jednoczesne pobudzenie obu dróg, a sumą reakcji wywołanych osobnym ich drażnieniem oznacza torowanie reakcji odruchowej i jest miarą wielkości strefy zwiększonej podprogowo pobudliwości.
15. Jakie jest znaczenie konwergencji i dywergencji w przewodnictwie nerwowym? (Przykłady)
Konwergencja - jest to występowanie na błonie pojedynczej komórki postsynaptycznej tysięcy synaps pochodzących z kolbek różnych neuronów presynaptycznych.
Przykład: przekazywanie impulsów czuciowych z neuronów II rzędu na neurony III rzędu w obrębie jądra brzusznego tylno-przyśrodkowego wzgórza.
Dywergencja - rozbieżne łączenie neuronu z sąsiednimi neuronami, aksonv rozgałęziając się, przesyła impulsy do wielu innych neuronów, wpływając na ich pobudliwość.
Przykład: Sieć neuronalna układu tylno-powrózkowego, gdzie wyładowanie pojedynczego receptora trafiają jednocześnie do kilku sąsiednich neuronów korowych
Na każdym z 100 miliardów neuronów ludzkiego mózgu znajduje się ok. 1000 synaps konwergujących i każdy wysyła ok 1000 synaps dywergujących.
Aktywacja pojedynczej synapsy zwykle nie wywołuje potencjału czynnościowego w neuronie postsynaptycznym.
Neurony tworzą sieci z wykorzystaniem zjawiska konwergencji i dywergencji
Przewaga synaps pobudzających toruje wyładowania neuronów postsynaptycznych
Rekrutacja dodatkowych neuronów presynaptycznych zwiększa zjawisko sumowania czasowo-przestrzennego i wyładowań neuronów postsynaptycznych
W wieloneuronowym łańcuchu impulsacja wysyłana przez jeden neuron przekazywana jest jednocześnie do kilku neuronów, a z nich do jeszcze większej liczby neuronów. Tworzą się w ten sposób zwielokrotnione sieci neuronów: zamknięte (zamknięte obwody) lub otwarte (przekazujące pobudzenia na inne sieci neuronalne).
16. Czym jest i jaką rolę pełni złącze nerwowo- mięśniowe?
zakończenia aksonu neuronu ruchowego, który w pobliżu unerwionego miocytu traci osłonkę mielinową i rozdziela się na wiele kolbek końcowych lub stopek końcowych. W obrębie zakończenia wypustka tworzy element presynaptyczny, który zawiera liczne mitochondria oraz pęcherzyki z acetylocholiną.
Strzelina synaptyczna o szerokości 20nm
Błona postsynaptyczna w bezpośrednim sąsiedztwie zakończenia ruchowego jest pogrubiona i tworzy palisadowate zagłębienia z licznymi fałdami, pomiędzy którymi wciśnięte są stopki końcowe. Ta zgrubiała i pofałdowana cześć błony nosi nazwę końcowej płytki motorycznej. Znajdują się tutaj receptory cholinergiczne typu nikotynowego (N). Są one hamowane przez kurarę.
Pod wpływem impulsu nerwowego przesuwającego się wzdłuż włókna nerwowego błona presynaptyczna ulega depolaryzacji uwalniając Ach zgromadzoną w pęcherzykach synaptycznych. Zjawisko to nosi nazwę sprzężenia elektrowydzielniczego.
Jest ono zwiększane przez jony Ca, a zmniejszane przez jony Mg.
Związanie Ach z receptorami w błonie postsynaptycznej powoduje zwiększenie przepuszczalności błony dla Na i K, czego skutkiem są wahania potencjału elektrycznego w tej okolicy noszące nazwę Potencjału Płytki Końcowej (End Plate Potencial = EPP). EPP rozchodzi się spontanicznie wzdłuż błony komórki mięśniowej prowadząc do skurczu (płytka końcowa znajduje się w połowie włókna mięśniowego). EPP charakteryzuje się dużą amplitudą, dlatego prawie zawsze wywołuje potencjał czynnościowy we włóknie mięśniowym.
Pojedyncze włókno mięśniowe reaguje pojedynczym skurczem na pojedynczy potencjał czynnościowy, zgodnie z zasadą „wszystko, albo nic”. Impuls nerwowy uruchamia mechaniczne efektory skurczu pozostając bez wpływu na siłę skurczu. Jego intensywność zwiększa się zostanie pobudzona większa ilość jednostek motorycznych w danym mięśniu.
17. Na czym polega skurcz izotoniczny, izometryczny i auksotoniczny?
Skurcz jest to aktywny proces podczas którego w mięśniu wytwarza się siła.
Skurcz izometryczny - występuje gdy siła zewnętrzna przewyższa siłę skurczu mięśniowego i długość mięśnia pozostaje niezmieniona, mimo jego aktywnego skurczu. Wzrasta jedynie napięcie mięśniowe. Utrzymują ciężar w określonej pozycji.
Skurcz izotoniczny - włókna mięśniowe i cały skurcz ulegają skróceniu, napięcie zaś się nie zmienia. Przyczepy mięśnia w układzie szkieletowym zbliżają się do siebie.
Czas trwania skurczu izotonicznego jest nieco krótszy od izometrycznego, dłuższy jest także okres latencji. W miarę wzrostu obciążenia wydłuża się okres latencji, zmniejsza się szybkość, czas trwania i wielkość skurczu.
Skurcz auksotoniczny - skurcz z jednoczesnym skróceniem długości i wzrostem napięcia mięśnia. Jest to najczęściej występujący typ skurczów mięśni kończyn i tułowia.
Niezależnie od rodzaju skurczu zjawiska fizykochemiczne we włóknach mięśniowych są identyczne, a różnią się one jedynie w/w efektami mechanicznymi.
18. Jakie zmiany zachodzą w sarkomerze w czasie skurczu i rozkurczu mięśnia? (rysunek)
[Sarkomer jest podstawową jednostką kurczliwą mięśnia. Przyjmuje się, że sarkomer leży pomiędzy liniami Z, które regularnie powtarzają się w mięśniu. W obrębie sarkomeru można wyróżnić odcinki anizotropowe (prążek A) i izotropowe (prążek I). Długość sarkomeru 2,0-2,8 mikrometra. Sakromer jest w istocie złożonym kompleksem kilkunastu białek, które tworzą dwa podstawowe filamenty:
filamenty grube, składające się z miozyny i titiny
filamenty cienkie, składające się z aktyny, troponiny i tropomiozyny
Strefa H znajdująca się w środku prążka A, odpowiada przestrzeni pomiędzy dośrodkowymi końcami cienkich filamentów i składa się wyłącznie z grubych filamentów . Jest ona przedzielona błoną środkową M.
W części prążka A, gdzie cienkie i grube filamenty zachodzą na siebie, stwierdza się regularny układ heksagonalny w którym każdy filament gruby otoczony jest przez 6 filamentów cienkich, a wokół każdego cienkiego filamentu znajdują się 3 filamenty grube. Występują tu także promieniście sterczące wyrostki nitek miozyny, zwane mostkami poprzecznymi, ułożonymi spiralnie wokół grubych filamentów.
W czasie skurczu w wyniku depolaryzacji uwolnione zostają jony wapnia, które łącza się z troponiną C następuje osłabienie połączenia aktyny z troponiną I pozwalając na przemieszenie do boku cząsteczki troponiny i odsłonięcia miejsca aktywnego monomerów G-aktyny gotowych do interakcji z głowami miozyny. Nitki aktyny przesuwają się pomiędzy nitkami miozyny, czyli zachodzi ślizganie się nitek cienkich wzdłuż nitek grubych.
Długość miofilamentów i szerokość prążków A jest stała, ale prążki I znikają. Strefa H ulega skróceniu, może nawet całkowicie zniknąć.
Ślizganie zachodzi, gdy głowa miozyny ściśle złączy się pod kątem 900 z cząsteczkami aktyny, powodując ruch obrotowy miozyny po cząsteczkach aktyny, odłączenie i ponowne przyłączenie do najbliższego miejsca wiążącego na aktynie.]
W rozkurczu głowa miozyny połączona z ATP może tylko minimalnie hydrolizować ATP, co uniemożliwia uwalnianie produktów hydrolizy:
M*ATP → M*ADP*Pi
Po związaniu głowy miozyny z miejscem aktywnym aktyny wybitnie wzrasta aktywność ATP-azowa głowy miozyny i zachodzi uwolnienie produktów hydrolizy ATP. Część energii zostaje zużyta jako siła napędowa ruchów mostków poprzecznych a reszta zamieniana jest na ciepło:
A + M*ADP*Pi → A*M + ADP + Pi
Następuje wtedy zmiana konformacji mostka i jego ruch o 450 pociągający nitkę aktyny do środka sarkomeru.
Jeśli dostępne są dalsze cząsteczki ATP to przyłączają się one do kompleksu aktynomiozyny (A*M) a ponieważ M*ATP ma słabe powinowactwo do aktyny oddziela się mostek poprzeczny miozyny od aktyny. Rozpoczyna się rozkurcz:
A*M + ATP → A + M*ATP.
Cykliczne ruchy mostków utrzymują się przez cały okres wysokiego stężenia jonów wapnia. Powrót jonów wapnia do zbiorniczków siateczki sarkoplazmatycznej i spadek jego stężenia w sarkoplazmie powoduje jego odłączanie się od troponiny, przywrócone zostaje działanie hamujące układu troponina-tropomiozyna i rozpada się aktynomiozyna. Po kolejnym potencjale czynnościowym uwalniającym jony wapnia cały cykl powtarza się.
(ryc 7.8 Konturek t.I)
Jakie są rodzaje troponin oraz ich funkcje we współpracy z tropomiozyną?
Troponina jest kompleksem złożonym z trzech białek:
-troponina C - kwaśne białko wiążące jony wapnia
-troponina I - hamowanie interakcji aktyny z miozyną, zasłaniając miejsce aktywne aktyny
-troponina T - łączenie kompleksu troponiny z tropomiozyną
-tropomiozyna - zbudowana z dwóch łańcuchów polipeptydowych skręconych w superhelisę, co nadaje jej kształt pałeczki. Blokuje miejsce wiązania miozyny z aktyną.
Jony wapnia uwolnione przez potencjał czynnościowy wiążą się z troponiną C, co osłabia połączenie aktyny z troponiną I pozwalając na przemieszczenie do boku cząsteczek tropomiozyny i odsłonięcie miejsc aktywnych monomerów G-aktyny gotowych do interakcji z głowami miozyny. Umożliwia to rozpad ATP i skurcz.
Kompleks troponino-tropomiozynowy uważany jest za „białko rozkurczające”, hamujące wtórne oddziaływanie między aktyną i miozyną.
Jakie są molekularne podstawy skurczu mięśnia szkieletowego?
Miozyna jest głównym składnikiem włókienek grubych. Ma ona kształt walca zakończonego mostkiem poprzecznym z głową sterczącą w stronę aktyny. Może się ona odchylać o 45o od osi miofilamentu, posiada dwa miejsca aktywne:
wiążące aktynę
miejsce enzymatycznej hydrolizy ATP
Miozyna składa się z dwóch łańcuchów ciężkich i czterech lekkich.
Pod wpływem papainy miozyna rozpada się na meromiozynę lekką i meromiozynę ciężką.
Cząsteczki miozyny w dwu sąsiadujących połówkach grubego filamentu są zorientowane w przeciwnych kierunkach.
Aktyna jest głównym składnikiem włókienek cienkich. G-aktyna w obecności ATP silnie polimeryzuje tworząc F-aktynę.
W skład filamentów wchodzą też białka regulatorowe tropomiozyna i troponina (patrz pyt. 19).
-Przemieszczająca się fala depolaryzacji po włóknie mięśniowym powoduje uwalnianie się dużych ilości wapnia z cystern siateczki sarkoplazma tycznej. Zachodzi to z udziałem receptorów dihydropirydynowych (DHP), stanowiących kanały dla Ca bramkowane potencjałem w błonie cewek poprzecznych T
-Jony wapnia reagują z białkiem C tropiny, co w efekcie powoduje zmianę konformacji białka, następuje odsłonięcie przez tropomiozynę miejsc aktywnych w łańcuchu aktynowym.
-Do odsłoniętych miejsc aktywowanych przyłącza się mostek miozynowy i znaczny wzrost aktywności ATP-azy w główce miozyny
-Aby zerwać to połączenie, potrzebne znowu jest, ATP, które zmniejsza powinowactwo miozyny do aktyny powodując zerwanie połączenia miedzy aktyną i miozyną w wyniku, czego następuje rozkurcz
- Pompa wypompowująca jony Ca z powrotem do siateczki sarkoplazmatycznej jest Ca-Mg-ATP-azą. W siateczce sarkoplazmatycznej wapń wiąże się z kalsekwestryną, co kończy pojedynczy skurcz.
21. Jakie są rodzaje skurczu tężcowego i na czym one polegają?
Skurcz tężcowy- powstaje, gdy stosujemy bodźce w czasie krótszym niż czas trwania skurczu pojedynczego. Każde następne pobudzenie podtrzyma aktywację układów kurczliwych wywołanych pobudzeniem poprzedzającym.
W rezultacie skurcz rozwinięty w odp. na pierwsze pobudzenie zostanie podtrzymany tak długo jak długo mięśnie będzie drażniony.
Niezupełny - pobudzenie mięśnia następuje w odstępach czasu dłuższych niż czas trwania fazy skurczowej, a więc kiedy następne pobudzenie zaczyna się w momencie, gdy mięsień zaczął już się rozkurczać. Wykres tego skurczu wykazuje drobne załamki i wahania.
Zupełny- bodźce pobudzą mięsień w odstępach krótszych niż faza skurczowa, więc mięsień nie może się przed następnym pobudzeniem rozkurczyć. Wykres tego skurczu ulega zupełnemu wygładzaniu.
(ryc 7.20 konturek t.1)
22. Na czym polega zależność miedzy szybkością skracania, a obciążeniem mięśnia? (rysunek)
Mięśnie kurczą się tym szybciej, im mniej są obciążone, najszybciej kurczą się mięśnie w ogóle nie obciążone.
Początkowa szybkości skracanie mięśnia nieobciążonego to maksymalne szybkość kurczenie(V max). Niesień kurczący się z szybkością Vmax rozwija zerowa sile skurczu taki skurcz nosi nazwę izotonicznego bez obciazenia. W miarę obciążenia mięśnia prędkość skurcz stopniowo maleje. Gdy obciążenie mięśnia osiągnie wartość maksymalną i zrównoważy siłę jego skurczu, czyli gdy skurcz przyjmie charakter izometryczny, wtedy szybkość skurczu spada do zera, a mięsień mimo pobudzenia nie skraca się.
Spadek szybkości skurczu mięśnia przy jego obciążeniu jest wywołany mniejszą liczbą mostków poprzecznych pomiędzy nitkami aktynowymi i miozynowymi. Im szybciej kurczy się mięsień, tym szybciej nitki aktynowe wsuwają się pomiędzy filamenty miozynowe.
23. Na czym polega dług tlenowy w mięśniach i jakie jest jego znaczenie?
Głównym źródłem energii dla pracujących mięśni jest glukoza, która rozpada się do pirogronianu. W obecności wystarczającej ilości tlenu zostaje on utleniony do CO2 i H2O. Jest to glikoliza tlenowa. Gdy zaopatrzenie mięśni w tlen jest niewystarczające pirogronian przechodzi w mleczan. Mówimy wtedy o glikolizie beztlenowej. Dostarcza ona znacznie mniej związków wysokoenergetycznych (głównie ATP), a więc także mniej energii (5% energii z glikolizy tlenowej). Przy braku tlenu pirogronian nie ulega przemianie acetylo-CoA i ulec włączeniu do cyklu Krebsa. Po zakończeniu wysiłku następuje dodatkowe pobieranie tlenu w celu usunięcia nadmiaru mleczanu, odnowy fosfokreatyny, ATP i utlenowania mioglobiny.
Obecność kwasu mlekowego w mięśniach jest przyczyną zmęczenia i utrudnia dalsze skurcze.
Całkowity dług tlenowy może osiągnąć nawet 20L tlenu. Zostaje on spłacony dopiero podczas odpoczynku, wzmożonej wentylacji płuc. 20% mleczanu jest zużywana przez mięśnie, mózg i serce w celu dostarczenia energii, zaś 80% zużywa wątroba w procesie glukoneogenezy.
Wydajność tego procesu jest bardzo dużo umożliwia skurcz mięśni w czasie intensywnego wysilku nawet pomimo braku tlenu. Niestety powoduje on także przyspieszoną glikogenolizę w mięśniach, co prowadzi do zmęczenia.
24. Jak generowany jest tonus mięśni szkieletowych?
Opór jaki stawia mięsień rozciągającej go sile, jest często określany jako napięcie lub tonus. Jest to stan napięcia występujący nawet w czasie zupełnego spoczynku.
Generowany jest odruchowo. Receptorem tego odruchu jest wrzecionko nerwowo-mięśniowe. Wrzecionko jest zbudowane ze zmodyfikowanych mięśni intrafuzalnych otoczonych torebką łącznotkankową. Końcami wrzecionko połączone jest z włóknami ekstrafuzalnymi. Włókna intrafuzalne są unerwione ruchowo przez gamma-motoneurony. W połowie długości tych włókien, gdzie brak poprzecznego prążkowania, są nawinięte zakończenia pierścieniewospiralne, które są mechanoreceptorami.
Ulegają one pobudzeniu przy biernym rozciąganiu bądź pod wpływem skurczu włókien intrafuzalnych. W związku z połączeniem wrzecionka z resztą mięśnia, ulega też ono pobudzeniu przy jego rozciągnięciu. Przy pobudzeniu wrzecionko wysyła salwę impulsów do korzeni grzbietowych skąd pobudzenie może być przekazane do wyższych pięter OUN lub przekazane bezpośrednio na alfa-motoneurony,które powodują skurcz włókien ekstrafuzalnych. Część impulsów jest przekazane na neurony wstawkowe hamujące alfa-motoneurony mięśni antagonistycznych.
25. Czym są mięśnie gładkie typu trzewnego?
Trzewne mięśnie gładkie zwane jednostkowymi występują w ścianach przewodu pokarmowego w moczowodach i w macicy. Stanowią warstwy równolegle ułożonych komórek ściśle przylegających do siebie. W miejscach kontaktowych wykazują obecność mostków i niski opór elektryczny z dużą przewodnością dla bioprądów. Dzięki temu stany pobudzenia przechodzą między komórkami i komórki jednej warstwy działają jak czynnościowe syncytium. Występują wśród nich komórki rozrusznikowe co daje duży automatyzm. Cechy charakterystyczne to mała precyzja, odpowiedz skurczowa na mechaniczne rozciąganie, mała kontrola ze strony układu nerwowego, rozlana odpowiedź na pobudzenie nerwowe utrzymująca się długo oraz wrażliwość na katecholaminy pochodzące z krwi.
26. Czym są mięśnie gładkie typu wielojednostkowego?
Wielojednostkowe mięśnie gładkie występują w tęczówce, ciałku rzęskowym, mięśniach wyprostnych włosów i ścianach naczyń krwionośnych. Składają się z małych pęczków lub pojedynczych miocytów kurczących się niezależne niemal wyłącznie pod wpływem impulsów z zaopatrujących je obficie nerwów autonomicznych. Odpowiedź na pobudzenie jest precyzyjna i szybka. Mięśnie te są mało wrażliwe na katecholaminy pochodzące z krwi.
27.Czym różnią się, pod względem morfologicznym i czynnościowym mięśnie szkieletowe od gładkich?


28. Na czym polega mechanizm sprzężenia elektromechanicznego mięśnia?
Sprzężenie elektromechaniczne to suma procesów łączących pobudzenie błony komórkowej z aktywacja układów kurczliwych mięśnia.
Pierwszym procesem jest depolaryzacja błony płytki ruchowej pobudzonej przez acetylocholinę uwolnioną z pobudzonego alfa-motoneuronu. Depolaryzacja ta przenosi się na całą sarkolemmę i przez ciągłość w głąb cewek poprzecznych (kanalików T). Depolaryzacja powoduje otwarcie kanałów dla Ca2+ w sarkolemmie i zbiorników końcowych siateczki sarkoplazmatycznej. Zbiorniki końcowe to zgrubienia siateczki sarkoplazmatyczne w miejscach styku z kanalikami T. Dwa zbiorniki końcowe i jeden kanalik T tworzy triadę mięśniową.
Po otwarciu zbiorników następuje wypływ jonów Ca2+ i nagły wzrost ich stężenia w sarkoplaźmie z 10-7mmol(wartość spoczynkowa) do przynajmniej 10-6mmol(wartość progowa do wywołania aktywacji układów kurczliwych). Jony wiążą się z troponiną C zmieniając konformacje przestrzenna układu troponina-tropomiozyna co odsłania aktywne miejsca wiązania na niciach aktyny. Aktyna łączy się mostkami poprzecznymi z miozyną i następuje skurcz.
Następnie jony są usuwane z sarkoplazmy do płynu zewnątrzkomórkowego i zbiorników końcowych.
Sprzężenie w mięśniach gładkich ma podobnym mechanizm. Pobudzenie jednak pochodzi często z komórek rozrusznikowych lub jest przekazane z innych miocytów, a jony Ca2+ pochodzą z płynu zewnątrzkomórkowego. Wnikają one podczas depolaryzacji błony przez kanały jonowe bramkowane potencjałem. Tam łączą się z kalmoduliną aktywującą kinazę lekkich łańcuchów miozynowych. Miozyna ulega fosforylacji i tworzy mostki z aktyną. Następuje skurcz. Fosfatazy następnie defosforylują miozynę. Następuje rozkurcz i aktywne usunięcie jonów Ca2+ z komórki. Skurcz może się jednak utrzymać dłużej przez mechanizm „ryglowania” mostków poprzecznych.
Wyszukiwarka
Podobne podstrony:
Pobudliwość mięśni, STOMATOLOGIA, II ROK, fizjologia
pobudliwość mięśni
Pobudliwość i mięśnie - 2008, fizjoterapia, fizjologia
FIZJOLOGIA Pobudliwość komórki Mieśnie przykładowe pytania i odpowiedzi Gumed
S stomat miesnie pobudliwosc i krew, II ROK STOMATOLOGIA SUM ZABRZE, FIZJOLOGIA, SEMINARIUM I
V Mięśnie i pobudliwość
V Mięśnie i pobudliwość
Układ mięśniowy
Mięśnie brzucha ppt
Środki zwiotczające mięśnie poprzecznie prążkowane
Leki rozkurczajace miesnie gladkie oskrzeli
miesnie szkieletowe glowy, szyji, brzucha i grzbietu bez ilustr
więcej podobnych podstron