Nr ćwicz. |
Politechnika Radomska im. Kazimierza Pułaskiego |
Wydział MiTO |
|
Data ćwicz. |
|
|
|
Nazwisko: |
Temat ćwiczenia |
|
|
Zasada Sobiesław |
|
|
|
Numer grupy ćwiczeniowej |
Sprawozdanie oddano dnia |
OCENA |
Prowadzący |
|
|
|
|
I Cel ćwiczenia
Celem ćwiczenia jest doświadczalne wyznaczenie współczynnika podziału kwasu octowego pomiędzy wodę a organiczny rozpuszczalnik (toluen).
II Część teoretyczna
Jeżeli do roztworu dwóch nie mieszających się cieczy wprowadzić substancję, która rozpuszcza się w obydwu warstwach to już po ustaleniu się stanu równowagi stosunek stężeń tej substancji w obydwu ciekłych fazach jest w danej temperaturze wielkością stałą. Własność tę, odkrytą przez Nernsta, nazywamy prawem podziału i opisujemy wzorem:
![]()
Prawo to jest nieźle spełnione gdy nie ulega zmianie wielkość cząsteczek rozdzielanego składnika. W przypadku elektrolitów mocnych, które w roztworze wodnym są całkowicie zdysocjowane, a w rozpuszczalnikach organicznych o niskiej stałej dielektrycznej wykazują przewodnictwo znacznie mniejsze, ,
możemy mieć do czynienia ze zjawiskiem asocjacji. Asocjacji na tzw. pary lub dwójki, czyli łączeniu w pary jonowe, sprzyjają także niewielkie rozmiary jonów i duża ich wartościowość. W przypadku dużej asocjacji substancji prawo podziału Nernsta przyjmuje postać:
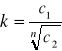
gdzie: n- liczba cząsteczek substancji asocjujących w rozpuszczalniku 2.
Wzór ten ma zastosowanie w przypadku substancji, która w rozpuszczalniku 1 ulega bardzo nieznacznej dysocjacji. W przypadku dużego stopnia dysocjacji wzór na współczynnik podziału przyjmuje postać:
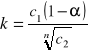
gdzie: α - stopień dysocjacji substancji w rozpuszczalniku 1
n - liczba cząsteczek --> [Author:MŁ] substancji asocjujących w rozpuszczalniku 2
Podział trzeciego składnika między dwie fazy ciekłe znajduje ważne zastosowanie praktyczne w procesie ekstrakcji. Bardzo często stosuje się ją do usuwania rozpuszczonych w wodzie substancji organicznych, źle mieszających się z wodą. Jeżeli przez n oznaczymy liczbę moli substancji zawartej w objętości v rozpuszczalnika 1, którą ekstrahuje się kolejno porcjami o objętości z rozpuszczalnika 2, rozpuszczającego substancję x znacznie lepiej od rozpuszczalnika 1, to po pierwszej ekstrakcji w rozpuszczalniku 1 pozostanie n1 moli substancji x. Stosując prawo podziału można zapisać:
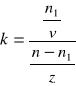
![]()
Natomiast po i-tej ekstrakcji będziemy mieć:
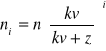
moli substancji x w rozpuszczalniku 1.
III Wykonanie ćwiczenia
Etap 1)
Z każdego z roztworów kwasu octowego 0,5 molowego i 0,25 molowego pobieram próbki po 2 cm3 i przelewam do dwóch kolbek stożkowych. Rozcieńczam je następnie wodą destylowaną do ok. 20 cm3. do każdej z próbek dodaję kilka kropel fenoloftaleiny i miareczkuję 0,1 molowym roztworem wodorotlenku sodu dla oznaczenia całkowitej początkowej ilości kwasu (c0, wyrażonej w cm3 0,1 M NaOH).
Etap 2)
Do dwóch rozdzielaczy wlewam po 20 cm3roztworu: do I - 0,5 M CH3COOH, do II - 0,25 M CH3COOH. Następnie do każdego rozdzielacza dolewam po 20 cm3 toluenu. Po zamkięciu rozdzielaczy korkami wstrząsam nimi przez kilka minut, a następnie pozostawiam je na ok. 20 min do rozdzielenia i wyklarowania się faz.
Etap 3)
Po tym czasie pobieram próbki po 2 cm3 z dolnych (wodnych) faz z rozdzielaczy i postępuję podobnie jak w etapie pierwszym tzn. umieszczam te próbki w dwóch kolbach stożkowych, rozcieńczam wodą destylowaną do ok. 20 cm3 i miareczkuję 0,1 M NaOH wobec fenoloftaleiny oznaczając stężenie kwasu octowego w fazie wodnej (c1, wyrażone w cm3 0,1 M NaOH ).
IV Wyniki
Reakcja zobojętniania kwasu octowego wodorotlenkiem sodu przebiega następująco:
CH3COOH + NaOH CH3COONa + H2O
Etap 1)
Do zobojętnienia 20 cm3 rozcieńczonego roztworu 0,5 M kwasu octowego zużyłem 12,5 cm3 NaOH (0,1 M).
Do zobojętnienia 20 cm3 rozcieńczonego roztworu 0,25 M kwasu octowego zużyłem 6,25 cm3 0,1 M roztworu NaOH
Etap 3)
Po ekstrakcji kwasu octowego toluenem stężenia CH3COOH wyrażone w cm3 NaOH wynoszą odpowiednio:
Do zobojętnienia 20 cm3 roztworu kwasu octowego z dolnej fazy 0,5 M CH3COOH zużyłem 11,5 cm3 NaOH.
Do zobojętnienia 20 cm3 roztworu kwasu octowego z dolnej fazy 0,25 M CH3COOH zużyłem 6 cm3 NaOH.
Obliczam stężenia kwasu octowego w fazie toluenowej z różnicy całkowitej początkowej ilości kwasu oraz ilości tego kwasu zawartej w fazie wodnej:
C2=C0-C1
Dla roztworu 0,5 M kwasu wynosi ono:
C2=(12,5-11,5)cm3=1cm3 0,1M NaOH
Dla roztworu 0,25 M kwasu wynosi ono:
C2=(6,25-6)cm3=0,25cm3 0,1M NaOH
Aby sprawdzić czy prawo podziału ma zastosowanie w podanym doświadczeniu rysuję tabelę i wpisuję otrzymane wyniki
Nr. Kolbki |
Ilość cm3 0,1M NaOH |
|
log c 1 |
log c 2 |
||
|
c 0 |
c 1 |
c 2 |
|
|
|
1 |
12,5 |
11,5 |
1 |
11,5 |
1,06 |
0 |
2 |
6,25 |
6 |
0,25 |
24 |
0,78 |
-0,6 |
Jak wynika z tabeli współczynniki podziału różnią się znacznie od siebie, a więc prawo podziału nie ma tu zastosowania. Należy zatem wartość k wyznaczyć graficznie z równania dla cząsteczek asocjujących (niewielką dysocjację kwasu octowego w wodzie pomijamy).
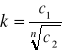
![]()
![]()
Jak wynika z rysunku zależności logc1=f(logc2) wartość k jest równa rzędnej punktu przecięcia prostej z osią rzędnych, a tangens nachylenia prostej do osi odciętych = 1/n.
Szukasz gotowej pracy ?
To pewna droga do poważnych kłopotów.
Plagiat jest przestępstwem !
Nie ryzykuj ! Nie warto !
Powierz swoje sprawy profesjonalistom.
Wyszukiwarka
Podobne podstrony:
Oceania z Australią podział polityczny, Dokumenty Edukacyjne, Podział polityczny kontynentów
chazarowie - korzenie wspolczesnego zydostwa, ► Ojczyzna, Dokumenty
WSPOŁCZESNY POLSKI FILM DOKUMENTALNY, Filologia polska, polonistyka, rok III, specjalizacja filmozna
Sprawozdania Karol, Współczynnik podziału, Gr
lab 7 - współczynnik podziału słabego kwasu pomiędzy fazą wodną a organiczną, kiciaqq
Wspolczynnik podzialu, Farmacja, II rok farmacji, I semstr, fizyczna, Fizyczna, Sprawozdania z fizyc
Współczynnik podziału Sprawozdanie
Europa podział polityczny, Dokumenty Edukacyjne, Podział polityczny kontynentów
Sprawozdania z fizycznej 1 ~$rawozdanie Współczynnik podziału
7. Współczynnik podziału Nernsta - zbiorcze, Zespół 1
Współczynnik podziału Nernsta
10 Współczynnik podziałuid 11179
Łuszków 30, DOKUMENTY 1, SKANY
29. Wyznaczanie współczynnika podziału Nernsta metodą potencjometryczną, chemia fizyczna
Azja podział polityczny, Dokumenty Edukacyjne, Podział polityczny kontynentów
współczynnik podziału, Chemia fizyczna, laboratorium, Chemia fizyczna
Wyznaczanie współczynnika lepkosci cieczy, dokumenty, Fizyka
pyt.+odp. z współczesnego społeczeństwa, moje dokumenty, współczesne społeczeństwo polskie
Współczesny kryzys ojcostwa, Dokumenty praca mgr
więcej podobnych podstron