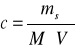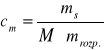SPORZĄDZANIE WODNYCH ROZTWORÓW ELEKTROLITÓW O OKREŚLONYM STĘŻENIU MOLOWYM |
ĆW.9. |
Cel ćwiczenia
Stosowanie w reakcjach chemicznych roztworów wymaga znajomości ich stężenia, to znaczy ilości substancji rozpuszczonej w danej ilości roztworu. Chemicy wyrażają stężenia roztworów w różny sposób, każdy z nich ma swoje zalety i ograniczenia. Obecnie poznamy cztery najbardziej popularne sposoby określania stężenia: molowość, molalność, stężenie procentowe i ułamek molowy. Celem ćwiczenia jest przygotowanie wodnego roztworu elektrolitu o stężeniu podanym przez asystenta, a następnie przeliczenie tego stężenia na inne jednostki.
Odczynniki:
► substancje rozpuszczane (sole nieorganiczne, wodorotlenki, kwasy itp.)
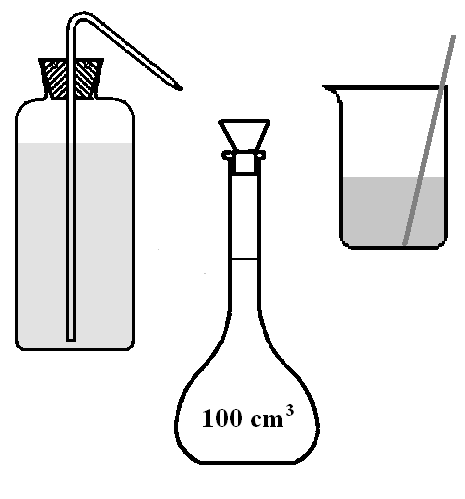
Sprzęt laboratoryjny:
► zlewka o pojemności 50 lub100 cm3
► kolba miarowa o pojemności 50 cm3
► bagietka
► łyżeczka porcelanowa
► waga analityczna
► cylinder miarowy o pojemności 50 cm3
► areometr
Wykonanie ćwiczenia:
Skład i stężenie wykonywanego roztworu określa prowadzący ćwiczenia.
Oblicz masę substancji potrzebnej do przygotowania 50 cm3 roztworu.
Odważ w zlewce na wadze technicznej odpowiednią ilość substancji.
Do zlewki z substancją dodaj około 25 cm3 wody destylowanej, mieszaj bagietką, aż do całkowitego rozpuszczenia substancji, a następnie przelej roztwór do kolby miarowej.
Zlewkę przemyj wodą destylowaną z tryskawki i roztwór ten również wlej do tej samej kolby miarowej.
Roztwór w kolbie miarowej uzupełnij wodą destylowaną do kreski, zamknij kolbę korkiem i tak otrzymany roztwór dokładnie wymieszaj.
W celu zmierzenia gęstości otrzymanego roztworu należy przelać go do cylindra miarowego, zanurzyć w nim areometr i odczytać gęstość otrzymanego roztworu.
Obliczenia:
W obliczeniach skorzystaj z poniższej tabeli. Pamiętaj, że w przypadku hydratów przez masę substancji (ms) rozumiemy masę substancji bezwodnej zawartej w odważce hydratu.
Wielkość |
Symbol i wyrażenie matematyczne |
Definicja |
Jednostka |
Stężenie procentowe (procent masowy) |
|
Liczba gramów substancji w 100 g roztworu |
% (m/m) lub % (w/w) |
Stężenie molowe |
|
Liczba moli substancji w 1 dm³ roztworu |
mol/dm³ |
Stężenie molalne |
|
Liczba moli substancji przypadająca na 1 kg rozpuszczalnika
|
mol/kg rozp. |
Ułamek molowy |
|
Udział liczby moli substancji A w liczbie moli wszystkich składników mieszaniny
|
- |
ms - masa substancji (bezwodnej) rozpuszczonej [g]; mr - masa roztworu [g]; mrozp. - masa rozpuszczalnika [kg]; V - objętość roztworu [dm³]; M - masa molowa substancji rozpuszczonej [g];
nA, nB, n... - liczba moli substancji A, B, ...
Wyniki:
Wyniki umieść w tabeli. W opisie ćwiczenia zamieść również wszystkie wykonane obliczenia.
Molowość [mol/dm³] |
Molalność [mol/kg] |
Stężenie procentowe [%] |
Ułamek molowy
|
|
|
|
|
Wyszukiwarka
Podobne podstrony:
stezenie molowe roztworow wodnych 2
Stężenie molowe roztworów wodnych
stezenie molowe roztworow wodnych
stezenie molowe roztworow wodnych 2
10 5 Stężenie molowe roztworów zadania do lekcji nr 2
Stezenie molowe-rozwiazania, Dla licealistów
4 Roztwory i stężenia
Odpowiedzi 5 1 Stęzenia molowe
Chemia mieszaniny, roztwory, stężenia
Stezenie molowe-rozwiazania, Licencjat, Semestr IV, biologia molekularna
Stężenie % molowe oraz ph zadania, dokumenty, chemia, Zadania
Wykład 2. Roztwory i stężenia, chemia, CHEMIA OGÓLNA -Walkowiak- (WPC 1002w) DOC
0 roztwory procentowe i molowe, Biologia molekularna, laborki
Stężenie molowe, Farmacja(0)
Roztwory i stężenia
więcej podobnych podstron