Zad. 1. Oznaczanie barwników chlorofilowych w olejach roślinnych metodą absorpcjometryczną
Cel ćwiczenia
Celem ćwiczenia jest oznaczenie całkowitej zawartości barwników chlorofilowych w olejach roślinnych, wyrażonej w mg feofityny w 1kg oleju. Oznaczenia dokonuje się na podstawie pomiarów absorbancji przy długości fali 670 nm, uwzględniając korekcję tła. W obliczeniach wykorzystywana jest wartość absorpcyjności feofityny a, która jest głównym barwnikiem chlorofilowym występującym w olejach roślinnych.
Aparatura
Spektrofotometr do pomiarów w zakresie widzialnym.
Kuwety szklane absorpcjometryczne o długości drogi optycznej 0.5 mm lub 10 mm.
Wykonanie ćwiczenia
Próbki oleju (olej rzepakowy tłoczny na zimno i oliwa z oliwek extra virgine) umieścić w kuwetach.
Wykonać pomiary absorbancji przy długościach fali 630 nm, 670 nm i 710 nm, względem powietrza.
Opracowanie wyników
1. Zawartość barwników chlorofilowych, wyrażoną w mg feofityny w 1kg oleju, obliczyć według wzoru:
![]()
gdzie:
c - zawartość barwników chlorofilowych, wyrażoną w mg feofityny w 1kg oleju
A - wartość absorbancji przy odpowiedniej długości fali
l - długość drogi optycznej (wyrażona w mm).
Instrukcja obsługi Spektrofotometru UV-VIS SP 8001 (Metertech Inc.)
Włączyć przyrząd - następuje inicjalizacja systemu.
Pojawia się ekran z głównym menu systemu System Main Menu.
Wybrać opcję 1. Photometric - wpisując wartość 1 z klawiatury numerycznej, potwierdzić przyciskiem Enter.
Otwiera się okno Photometric Parameter Setup:
Wybrać odpowiednie parametry (używając przycisków strzałka góra/dół, przesunąć kursor do odpowiedniego parametru i wpisać odpowiednią wartość, potwierdzić przyciskiem Enter ):
1. Input the Number of λ : 3
λ1 :630 λ2 :670 λ3 :710
2. Measure mode : ABS
3. Cycle number : 1
4. Cycle interval (sec) : 0
5. Print every cycle : No
Klawiszem funkcyjnym F4 wybrać opcję Sample Control i ustawić odpowiednie parametry:
Multicell parameter setup
1. Drive cell number : 3
2. Reagent blank correction : 1
6. Powrócić do poprzedniej strony klawiszem funkcyjnym F5 (Previous Screen).
7. Przejść do strony pomiarowej (tablica Photometric) klawiszem funkcyjnym F5 (Next Screen).
8. Umieścić kuwety z badanymi próbami w pozycjach 2 i 3.
9. Nacisnąć przycisk Read w celu wykonania pomiarów.
10. Zapisać zmierzone wartości absorbancji.
Instrukcja obsługi Spektrofotometru GenesysTM 6 ( Milton Roy)
Włączyć przyrząd - następuje inicjalizacja systemu.
Przyciskiem Test wybrać stronę z rodzajami programów, a następnie wybrać klawiszem funkcyjnym funkcję Main Screen.
Przyrząd będzie gotowy do pomiaru absorbancji, gdy w lewym górnym rogu ekranu pojawi się parametr, który ma zostać zmierzony; jeżeli nie jest to absorbancja - Absorbance, przyciskiem Change Mode, działającym w pętli, zmienić parametr pomiarowy.
Ustawić analityczną długość fali:
a) nacisnąć przycisk funkcyjny Set nm;
b) wpisać odpowiednią długość fali (630 nm lub 670 nm lub 710 nm) i zatwierdzić ją przyciskiem enter.
Wstawić do przyrządu kuwety z badanymi próbami w pozycjach 1 i 2.
5. Ustawić 100% T (0 ABS) przez naciśnięcie klawisza funkcyjnego Measure Blank.
6. Dokonać pomiaru absorbancji badanego roztworu przy określonej długości fali. Przyciskami na pulpicie, oznaczającymi pozycje ustawienia kuwet w stosunku do wiązki promieniowania, ustawić próbę w wiązce światła (pozycja 1), odczytać wynik pomiaru na ekranie.
7. Aby dokonać pomiaru absorbancji dla drugiej długości fali, należy powtórzyć czynności z punktów 3−6.
8. Po zakończeniu pomiarów nacisnąć przycisk test, aby wyjść z ekranu pomiarowego i spowodować wyłączenie lampy.
Zad. 2. Oznaczanie siarczanu (VI) chininy metodą fluorymetryczną
Cel ćwiczenia
Celem ćwiczenia jest zapoznanie się z metodyką pomiarów fluorymetrycznych na przykładzie oznaczania siarczanu chininy metodą krzywej wzorcowej w próbce napoju.
Aparatura
Absorpcjometr Spekol 11 z przystawką do pomiaru fluorescencji FK, firmy C. Zeiss, Jena.
Wykonanie ćwiczenia
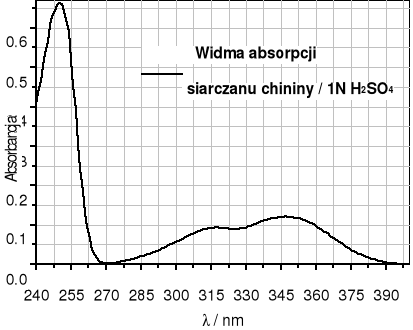
Na podstawie widma absorpcji siarczanu chininy oraz wykazu linii lampy rtęciowej zaproponować analityczną długość fali monochromatora pierwotnego.
Ustawić długość fali na monochromatorze pierwotnym.
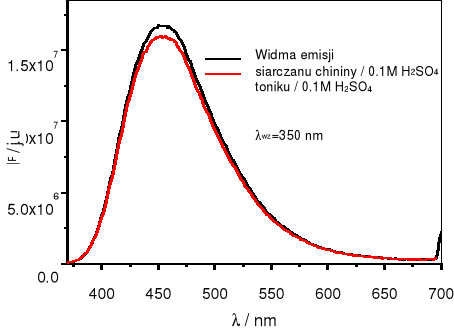
Ustawić wartość 100% intensywności fluorescencji (IF):
a) do przystawki wprowadzić roztwór wzorcowy o największym stężeniu (10.0 μg/ml);
b) nacisnąć klawisz T (migoce lampka sygnalizacyjna R);
c) nacisnąć klawisz R - na wyświetlaczu pojawia się wartość 100.
4. Zmierzyć intensywność fluorescencji dla roztworów wzorcowych i próby:
a) wprowadzić do przystawki kuwety z roztworami wzorcowymi o stężeniach siarczanu chininy 0 μg/ml, 1.25 μg/ml, 2.5 μg/ml, 5.0 μg/ml, 7.5 μg/ml, 10.0 μg/ml, na wyświetlaczu odczytywać intensywność fluorescencji,
b) przygotować próbę: do kuwety dodać 100 μl toniku i 1500 μl 0.1M H2SO4 , wprowadzić do przystawki kuwetę z próbą, na wyświetlaczu odczytać intensywność fluorescencji.
Opracowanie wyników
1. Wykreślić krzywą wzorcową: IF = f (c)
gdzie: IF − intensywność fluorescencji,
c − stężenie.
Wyznaczyć stężenie siarczanu chininy w próbce na podstawie krzywej wzorcowej, obliczyć stężenie siarczanu chininy w toniku.
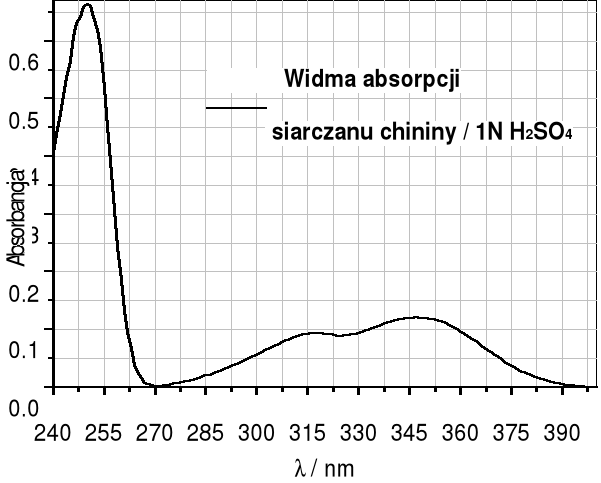
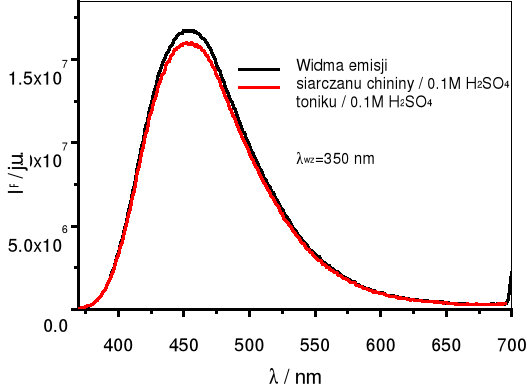
Wykaz długości fal dla poszczególnych linii widma lampy rtęciowej:
225,9 |
x 264,0 |
x 312,6 |
491,6 |
228,4 |
265,2 |
x 313,2 |
x 546,1 |
x 230,2 |
x 269,9 |
x 334,1 |
x 577,0 |
232,3 |
x 275,3 |
(339,0) |
x 579,1 |
x 234,6 |
(276,0) |
354,3 |
(623,4) |
x 235,3 |
x 280,4 |
356,1 |
(671,6) |
x 237,8 |
282,0 |
x 365,0 |
(690,7) |
x 239,9 |
285,7 |
(365,5) |
708,2 |
244,6 |
x 289,4 |
390,6 |
772,9 |
x 246,4 |
x 292,5 |
x 404,7 |
(819,7) |
x 284,3 |
x 296,7 |
x 407,8 |
(878,4) |
257,6 |
x 302,2 |
x 435,8 |
944,3 x 1014,0 |
Uwaga! „x” - zaznaczono linie silne, w nawiasach - linie bardzo słabe.
Wyszukiwarka
Podobne podstrony:
Zagadnienia zal.c NMI-st niest2009-10, Nowoczesne medoty instrumentalne
Zadania M6 09.10.2012, mechanika i budowa maszyn, politechnika, polibuda, matma, matma
Liga zadaniowa 5 (09-10), Liga zadaniowa, Archiwalne + rozwiązania, 2009 - 2010
MP 09-10 Z inz dz s3 cw zad 1
FiR ćw 1, Ćwiczenia 1 (11.10.09)
I W kamień Kaflińska ćw 09-10
I D W Egipt i Bliski Wschód Czarnowicz ćw 09 10
MP 09-10 Z inz dz s3 cw zad 2, Zarządzanie i Inżynieria Produkcji - studia, Marketing
MP 09-10 Z inz dz s3 cw zad 3, Zarządzanie i Inżynieria Produkcji - studia, Marketing
MP 09-10 Z inz dz s3 cw zad 1, Zarządzanie i Inżynieria Produkcji - studia, Marketing
MP 09-10 Z inz dz s3 cw zad 0, Zarządzanie i Inżynieria Produkcji - studia, Marketing
ćw 28 09, 05 10, 12 10
Liga zadaniowa 2 (09-10), Liga zadaniowa, Archiwalne + rozwiązania, 2009 - 2010
II D W Grecja Dobosz ćw 09-10
Liga zadaniowa 1(09-10), Liga zadaniowa, Archiwalne + rozwiązania, 2009 - 2010
MP 09-10 Z inz dz s3 cw Z3 Wyt do raportu , Case 1
Liga zadaniowa 4 (09-10), Liga zadaniowa, Archiwalne + rozwiązania, 2009 - 2010
więcej podobnych podstron