Mariusz Musiatowicz
Ćwiczenie 42
Grupa środa 1400
SZYBKOŚĆ INWERSJI SACHAROZY
Celem ćwiczenia jest zbadanie szybkości inwersji sacharozy w zależności od stężenia jonów wodorowych w roztworze wodnym.
Substancje optycznie czynne to substancje skręcające płaszczyznę polaryzacji światła.
Substancje takie mogą skręcać płaszczyznę bądź w prawo bądź w lewo.
Jeżeli przepuścimy światło przez polaryzator którym może być np. pryzmat Nicola
To zauważymy że wektory drgań tego światła po przejściu są ułożone do jednej płaszczyzny drgań. Takie ułożenie wektorów drgań światła do jednej płaszczyzny nazywamy
- POLARYZACJĄ ŚWIATŁA.
Gdybyśmy zbudowali zestaw doświadczalny, w skład którego wchodziłby polaryzator, analizator i jakaś lunetka i włożylibyśmy pomiędzy polaryzator a analizator (ustawione względem siebie o 90 0) jakąś substancję optycznie czynną to spoglądając przez lunetkę zauważylibyśmy, że zamiast zaciemnionej plamki otrzymaliśmy rozjaśnienie.
Wniosek byłby prosty - substancja optycznie czynna skręciła płaszczyznę polaryzacji światła o pewien kąt, stąd to rozjaśnienie.
RZĘDOWOŚCIĄ - badanej reakcji nazywamy sumę wykładników potęg w równaniu na szybkość reakcji dla najwolniejszego procesu.
CZĄSTECZKOWOŚĆ - reakcji wskazuje ile, ile cząsteczek: jedna dwie czy trzy bierze udział w najwolniejszym etapie reakcji.
Cząsteczkowości i zwykle równej jej rzędowości reakcji nie można przewidzieć ani obliczyć teoretycznie, można tylko wyznaczyć doświadczalnie.
-2-
Wyniki przeprowadzonych pomiarów
Tabela I.
t [min] |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
t [s] |
600 |
1200 |
1800 |
2400 |
3000 |
3600 |
4200 |
|
|
α1 |
13,35 |
12,65 |
12,10 |
11,20 |
10,40 |
9,90 |
9,20 |
α |
α2 |
12,95 |
11,80 |
10,60 |
9,60 |
8,45 |
7,50 |
6,70 |
|
α3 |
11,90 |
10,45 |
9,45 |
8,0 |
6,20 |
5,0 |
3,60 |
αśr |
38,20 |
34,9 |
32,15 |
28,8 |
25,05 |
22,40 |
19,5 |
|
Temperatura pomiaru 24oC ![]()
α0 =14,70 ![]()
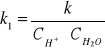
Stężenia jonów wodorowych :
CH+=
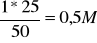
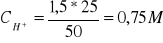
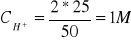
Ogólne stężenie wody:
1) ![]()
2) ![]()
3) ![]()
Tabela II dla roztworu o stężeniu 1M:
t [s] |
αt |
|
|
|
k |
k1 |
600 |
13,35 |
19,404 |
18,4878 |
0,021006 |
8,063·10-5 |
3,29·10-6 |
1200 |
12,65 |
19,404 |
17,354 |
0,048492 |
9,306·10-5 |
3,798·10-6 |
1800 |
12,10 |
19,404 |
16,804 |
0,062479 |
7,99·10-5 |
3,26·10-6 |
2400 |
11,20 |
19,404 |
15,904 |
0,086385 |
8,289·10-5 |
3,38·10-6 |
3000 |
10,40 |
19,404 |
15,104 |
0,108799 |
8,352·10-5 |
3,41·10-6 |
3600 |
9,90 |
19,404 |
14,604 |
0,123419 |
7,895·10-5 |
3,22·10-6 |
4200 |
9,20 |
19,404 |
13,904 |
0,144782 |
7,939·10-5 |
3,24·10-6 |
|
|
|
|
|
|
|
-3-
Za pomocą metody najmniejszych kwadratów wyznaczam parametry prostych.
xiyi |
xi2 |
12,6036 |
360000 |
58,1904 |
1440000 |
112,4622 |
3240000 |
207,324 |
5760000 |
326,397 |
9000000 |
444,3084 |
12960000 |
608,0844 |
17640000 |
|
|
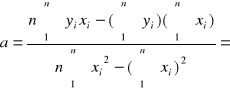
![]()
3,378·10-5![]()
k = a ·2,303 = 7,78·10-5
τ =![]()
8909,35s
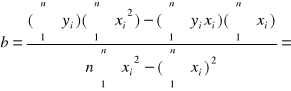
0,00398
Tabela III dla roztworu o stężeniu 1.5M:
t[s] |
αt |
C0 |
Ct |
|
k |
k1 |
600 |
12,95 |
19,404 |
17,654 |
0,041048 |
1,576·10-4 |
4,26·10-6 |
1200 |
11,80 |
19,404 |
16,504 |
0,070302 |
1,349·10-4 |
3,651·10-6 |
1800 |
10,60 |
19,404 |
15,304 |
0,103086 |
1,32·10-4 |
3,57·10-6 |
2400 |
9,60 |
19,404 |
14,304 |
0,132434 |
1,27·10-4 |
3,44·10-6 |
3000 |
8,45 |
19,404 |
13,154 |
0,168833 |
1,296·10-4 |
3,51·10-6 |
3600 |
7,50 |
19,404 |
12,204 |
0,201389 |
1,288·10-4 |
3,49·10-6 |
4200 |
6,70 |
19,404 |
11,404 |
0,230834 |
1,266·10-4 |
3,43·10-6 |
|
|
|
|
|
|
|
-4-
xiyi |
xi2 |
24,6288 |
360000 |
84,3624 |
1440000 |
185,5548 |
3240000 |
317,8416 |
5760000 |
506,499 |
9000000 |
725,0004 |
12960000 |
969,5028 |
17640000 |
|
|
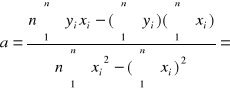
5,341·10-5
k = a ·2,303 = 1,23·10-4 ,
τ =![]()
5635,34s
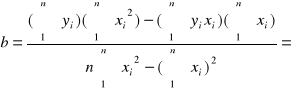
0,007235
Tabela IV dla roztworu o stężeniu 2M:
t[s] |
αt |
C0 |
Ct |
|
k |
k1 |
600 |
11,90 |
19,404 |
16,604 |
0,067679 |
2,598·10-4 |
5,329·10-6 |
1200 |
10,45 |
19,404 |
15,154 |
0,104364 |
2·10-4 |
4,103·10-6 |
1800 |
9,45 |
19,404 |
14,154 |
0,137012 |
1,753·10-4 |
3,596·10-6 |
2400 |
8,0 |
19,404 |
12,704 |
0,183951 |
1,765·10-4 |
3,621·10-6 |
3000 |
6,20 |
19,404 |
10,904 |
0,250305 |
1,92·10-4 |
3,938·10-6 |
3600 |
5,0 |
19,404 |
9,704 |
0,30094 |
1,925·10-4 |
3,949·10-6 |
4200 |
3,60 |
19,404 |
8,304 |
0,368604 |
2,021·10-4 |
4,146·10-6 |
|
|
|
|
|
|
|
-5-
xiyi |
xi2 |
40,6074 |
360000 |
125,2368 |
1440000 |
246,6216 |
3240000 |
441,4824 |
5760000 |
750,915 |
9000000 |
1083,384 |
12960000 |
1548,1368 |
17640000 |
|
|
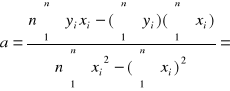
8,388·10-5
k = a ·2,303 = 1,932·10-4
τ =![]()
3587,72s
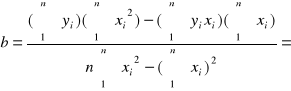
0,0005193
Wyznaczam parametry prostej :
k = kn + k' · (CHCl)
k' - stała szybkości reakcji katalitycznej
kn - stała szybkości reakcji inwersji cukru bez katalizatora . Jeśli reakcja bez katalizatora przebiega bardzo powoli jej stała szybkości jest bliska zeru lub nawet ujemna.
Tabelka V :
CHCl = xi [M] |
K = yi |
xiyi |
xi2 |
0,5 |
7,78·10-5 |
3,89 ·10-5 |
0,25 |
0,75 |
1,23·10-4 |
9,225·10-5 |
0,5625 |
1 |
1,932·10-4 |
1,932·10-4 |
1 |
|
|
|
|
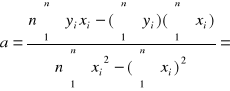
2,308·10-4 -stała szybkości inwersji cukru bez katalizatora
-6-
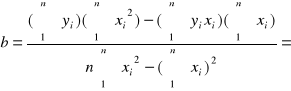
- 4,17667·10-5
Wnioski:
Wraz ze wzrostem stężenia HCl w roztworach stałe szybkości reakcji rosną , natomiast czas połowicznej przemiany maleje. Szybkość reakcji inwersji w poszczególnych reakcjach rośnie wraz ze wzrostem stężenia jonów wodorowych.
Wyszukiwarka
Podobne podstrony:
ćwiczeniee 43, materiały naukowe do szkół i na studia, chemia fizyczna moja, Chemia fizyczna, Opraco
ćwiczenie 43, materiały naukowe do szkół i na studia, chemia fizyczna moja, Chemia fizyczna, Opracow
ćwiczenie 42Piotr Osuch, materiały naukowe do szkół i na studia, chemia fizyczna moja, Chemia fizycz
ćwiczeniee 43Aneta Łoboda, materiały naukowe do szkół i na studia, chemia fizyczna moja, Chemia fizy
wykaz cwiczen, materiały naukowe do szkół i na studia, technologia chemiczna sprawozdania
wypalanie kamienia wapiennego oraz ocena jakości produktu – wapna palonego. (3), materiały naukowe
Otrzymywanie wapna palonego, materiały naukowe do szkół i na studia, technologia chemiczna sprawozda
20. Oznaczanie zawartosci wody w cialach stalych i cieczach, materiały naukowe do szkół i na studia,
wypalanie kamienia wapiennego oraz ocena jakości produktu – wapna palonego, materiały naukowe do sz
16. Oznaczanie zawartosci tluszczu w nasionach oleistych, materiały naukowe do szkół i na studia, te
otrzymanie żywicy fenolowo-formaldehydowej, materiały naukowe do szkół i na studia, technologia chem
kolokwium, materiały naukowe do szkół i na studia, polimery chomikuj, polimery chomikuj
15. Otrzymywanie polistyrenu metoda perelkowa, materiały naukowe do szkół i na studia, technologia c
Wnioski wapno palone, materiały naukowe do szkół i na studia, technologia chemiczna sprawozdania, wa
Polimery we fryzjerstwie, materiały naukowe do szkół i na studia, praca licencjacka - ZASTOSOWANIE P
erozja gleby, materiały naukowe do szkół i na studia, Geografia
wypalanie kamienia wapiennego oraz ocena jakości produktu – wapna palonego. (3), materiały naukowe
System Nagradzania, Różne materiały do szkoły,na studia
więcej podobnych podstron