Wydział Fizyki Technicznej
Edukacja Techniczno - Informatyczna |
Paweł Kwiatecki (Imię i Nazwisko studenta) |
15.10.2010r. (Data wykonywania ćwiczenia) |
Nr grupy: 6
Nr zespołu: 3 |
Nr ćwiczenia: 8 |
dr Elżbieta Górnicka-Koczorowska (Nazwisko Prowadzącego) |
Temat ćwiczenia: Entalpia zobojętniania.
Cel ćwiczenia: Wyznaczenie entalpii zobojętniania kwasu zasadą.
Pomiary: Wykonano dwukrotnie pomiary dla :
37,5 ml wody destylowanej dodano 0,25 ml 3 mol dm-3 H2SO4
36 ml wody destylowanej i 1,5 ml 0,2 mol dm-3 NaOH (roztwór ustabilizowany) dodano 0,05 ml 3 mol dm-3 H2SO4
37,5 ml wody destylowanej dodano 0,25 ml gliceryny
Wykresy:
Wykresy pomiaru efektu cieplnego dla 37,5 ml wody destylowanej do której dodano 0,25 ml 3 mol dm-3 H2SO4
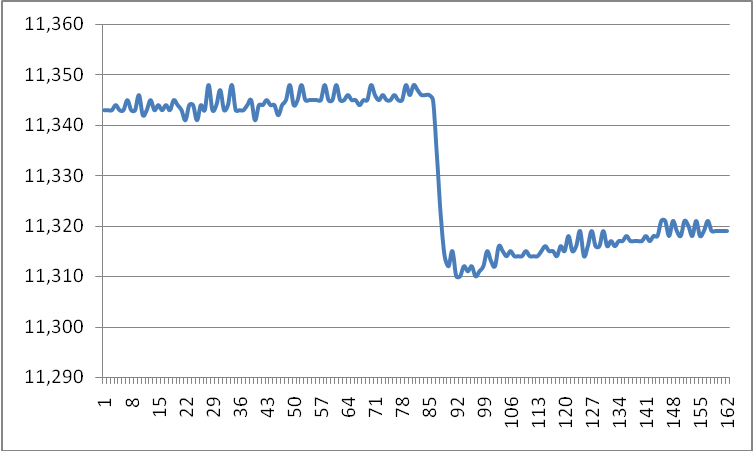
T1= 11,343 , T2= 11,314
![]()
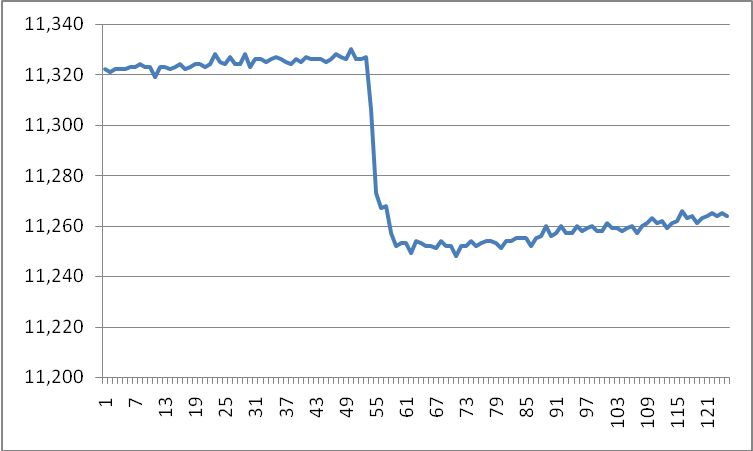
T1= 11,322 , T2= 11,252
![]()

Wykresy pomiaru efektu cieplnego dla 36 ml wody destylowanej i 1,5 ml 0,2 mol
dm-3 NaOH (roztwór ustabilizowany) do którego dodano 0,05 ml 3 mol dm-3 H2SO4
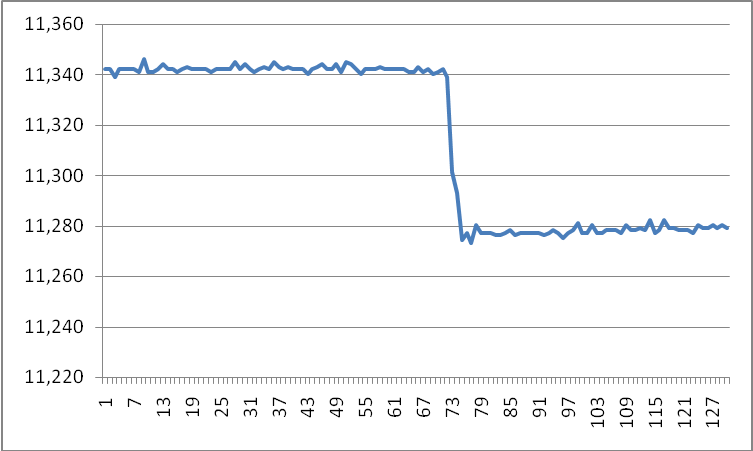
T1=11,342 , T2= 11,274
![]()
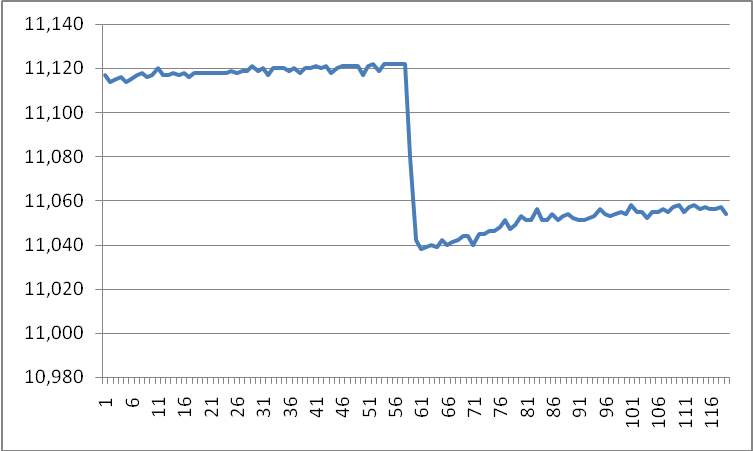
T1= 11,117 , T2= 11,040
![]()
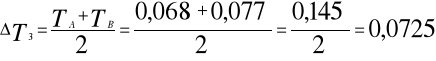
Wykresy pomiaru efektu cieplnego dla 37,5 ml wody destylowanej do której dodano 0,25 ml gliceryny
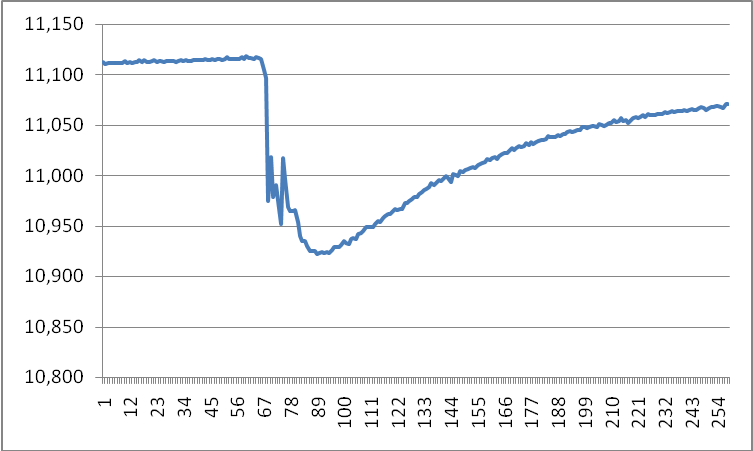
T1= 11,112 , T2= 10,978
![]()
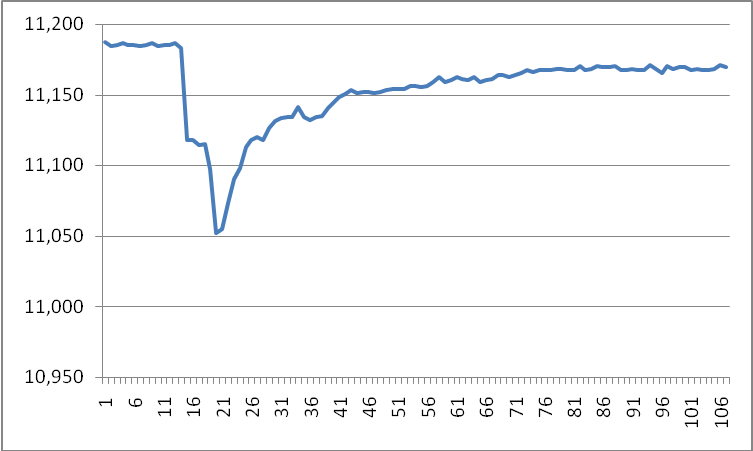
T1= 11,187 , T2= 11,052
![]()
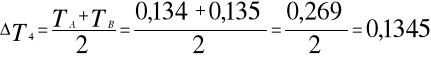
Obliczenia:
Korzystając ze wzoru na wartość molową entalpii zobojętniania ![]()
![]()
gdzie:
![]()
- molowe ciepło rozpuszczania gliceryny w wodzie(![]()
)
![]()
- molowe ciepło zobojętniania
![]()
- ilość moli H2SO4 użytego w reakcji rozcieńczania kwasu siarkowego
![]()
- ilość moli gliceryny użytej w reakcji rozpuszczania gliceryny w wodzie
![]()
, ![]()
, i ![]()
- temperatury układu spowodowane przebiegiem odpowiednio reakcji: rozcieńczania kwasu siarkowego, zobojętniania zasady sodowej kwasem siarkowym, i rozpuszczania gliceryny w wodzie
Obliczam wartość molową entalpii zobojętniania ![]()
:
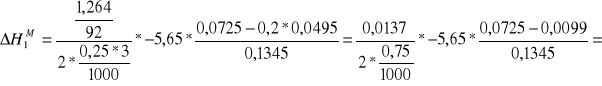
![]()
Wnioski:
Na podstawie powyższych danych można stwierdzić, że:
- przy dodaniu 0,25 ml gliceryny do 37,5 ml wody destylowanej temperatura gwałtownie maleje, później stopniowo wzrasta
- efekt cieplny reakcji zobojętniania zasady sodowej(NaOH 0,2 mol dm-3) kwasem siarkowym (H2SO4 3 mol dm-3) jest bardzo podobny do reakcji wody destylowanej z kwasem siarkowym
- dla reakcji wywołanej dodaniem 0,05 ml H2SO4 3 mol dm-3 do roztworu 36 ml wody destylowanej z 1,5 ml NaOH 0,2 mol dm-3 wartość molowa entalpii zobojętniania ![]()
wynosi około -23,98 kJ/mol
- Ujemny wynik (![]()
) świadczy o tym, że reakcja ta była reakcją egzotermiczną (-> polega ona na emitowaniu ciepła do otoczenia podczas przebiegu reakcji chemicznej).
1)
2)
2)
2)
1)
![]()
![]()
![]()
1)
Wyszukiwarka
Podobne podstrony:
fizyka laborki, STUDIA POLIBUDA, INŻYNIERIA MATERIAŁOWA, SEMESTR I, Fizyka, Laboratoria, 304
Korozja metali II oksydowanie, STUDIA POLIBUDA, INŻYNIERIA MATERIAŁOWA, SEMESTR I, Chemia, Laborator
Sprawozdanie 5 GIG B, II Rok WIMiC inżynieria materiałowa AGH, Chemia, Chemia -, Chemia - Laborki, S
SPRAWOZDANIE NR 3, II Rok WIMiC inżynieria materiałowa AGH, Chemia, Chemia -, Chemia - Laborki, redo
Roztwory Elektrolitow, Inzynieria Materiałowa, I semestr, Chemia
Sprawozdanie 5 GIG B, II Rok WIMiC inżynieria materiałowa AGH, Chemia, Chemia -, Chemia - Laborki, S
chemia fizyczna cw 13, Politechnika Wrocławska inżynieria materiałowa 2012, chemia fizyczna lab
sprawozdanie cw 1!(1), Inzynieria Materiałowa, I semestr, Elektrotechnika
moje sprawozdanie-Seweryn, Inzynieria Materiałowa, I semestr, Elektrotechnika, elektrotechnika, 3.0
Sprawozdanie nr 3 - zaprawa, Studia Budownictwo polsl, II semestr, Materiały budowlane, Sprawko 7
Sprawozdanie nr3 - zaprawa, Studia Budownictwo polsl, II semestr, Materiały budowlane, Sprawko 7
sprawko 13, inżynieria materiałowa - semestr 4, Inżynieria Materiałowa pwr - semestr 4, Chemia Fizyc
więcej podobnych podstron