Pobrano ze strony www.sqlmedia.pl
Pobrano ze strony www.sqlmedia.pl
Wpisuje zdaj!cy przed rozpocz"ciem pracy
P E S E L Z D A J ! C E G O
Miejsce na nalepk"
z kodem szko#y
PRÓBNY EGZAMIN MATURALNY
Z CHEMII
Arkusz II
(dla poziomu rozszerzonego)
Czas pracy 120 minut
Instrukcja dla zdaj"cego
1. Prosz" sprawdzi$, czy arkusz egzaminacyjny zawiera 12
stron. Ewentualny brak nale%y zg#osi$
przewodnicz!cemu zespo#u nadzoruj!cego egzamin.
2. Do arkusza do#!czone s! tablice chemiczne (3 strony).
3. Prosz" uwa%nie czyta$ wszystkie polecenia i informacje do zada&.
4. Rozwi!zania i odpowiedzi nale%y zapisa$ czytelnie w miejscu na to przeznaczonym przy ka%dym
zadaniu.
5. W rozwi!zaniach zada& rachunkowych trzeba przedstawi$ tok rozumowania prowadz!cy do
ostatecznego wyniku oraz pami"ta$ o jednostkach.
6. W trakcie oblicze& mo%na korzysta$ z kalkulatora.
7. Prosz" pisa$ tylko w kolorze niebieskim lub czarnym; nie pisa$ o#ówkiem.
8. Nie wolno u%ywa$ korektora.
9. B#"dne zapisy trzeba wyra'nie przekre(li$.
10. Brudnopis nie b"dzie oceniany.
11. Obok ka%dego zadania podana jest maksymalna liczba punktów, któr! mo%na uzyska$ za jego
poprawne rozwi!zanie.
!yczymy powodzenia!
Wpisuje egzaminator / nauczyciel sprawdzaj!cy prac"
Nr. zadania
31. 32. 33. 34. 35. 36. 37.
38.
39.
40.
41.
42.
Maksymalna
liczba punktów
3
1
2
4
2
3
3
2
4
3
3
3
Uzyskana
liczba punktów
Nr. zadania
43. 44. 45. 46. 47. 48. 49.
50.
51.
52.
SUMA
Maksymalna
liczba punktów
2
2
3
3
3
3
4
4
2
1
60
Uzyskana
liczba punktów
Pobrano ze strony www.sqlmedia.pl

Strona 2 z 12
Zadanie 31. (3 pkt)
Próbka pewnego materia#u promieniotwórczego zawiera obecnie 40 g izotopu
60
Co o okresie
pó#trwania równym 5 lat.
Oblicz, ile gramów tego izotopu rozpadnie si# w ci"gu najbli$szych 15 lat.
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Informacja do zadania 32. i 33.
Poni%ej przedstawiono konfiguracje elektronowe atomów kilku pierwiastków.
Pierwiastek W: 1s
2
2s
1
Pierwiastek X: 1s
2
2s
2
2p
6
3s
2
3p
5
Pierwiastek Y: 1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
10
4p
6
5s
1
Pierwiastek Z: 1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
10
4p
6
5s
2
4s
10
5p
5
Zadanie 32. (1 pkt)
Który z powy$szych pierwiastków charakteryzuje si# najwi#ksz" elektroujemno%ci"?
................................................................................................................................................................
................................................................................................................................................................
Zadanie 33. (2 pkt)
Spo%ród pierwiastków W, X, Y i Z wybierz par# takich, których atomy &"cz"c si# tworz"
wi"zanie o najbardziej jonowym charakterze.
................................................................................................................................................................
................................................................................................................................................................
Pobrano ze strony www.sqlmedia.pl

Strona 3 z 12
Informacja do zadania 34. i 35.
W temperaturze 1900 K w stanie równowagi reakcji
wyznaczono
nast"puj!ce
st"%enia reagentów: [N
2
] = 0,64
mol)dm
–3
, [O
2
] = 0,16 mol)dm
–3
,
[NO] = 0,02 mol)dm
–3
.
Zadanie 34. (4 pkt)
Oblicz:
1) sta&" równowagi reakcji syntezy tlenku azotu(II) w temperaturze 1900 K,
2) pocz"tkowe st#$enie azotu przy za&o$eniu, $e pocz"tkowa mieszanina reakcyjna
nie zawiera&a tlenku azotu(II).
1) obliczenie sta#ej równowagi: ............................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
2) obliczenie pocz!tkowego st"%enia azotu: .........................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Zadanie 35. (2 pkt)
Okre%l, jak wzrost temperatury wp&ywa na:
1) równowag# tej reakcji,
2) warto%' sta&ej równowagi reakcji.
1) wp#yw na równowag" reakcji: ..........................................................................................................
2) wp#yw na warto($ sta#ej równowagi reakcji: ....................................................................................
+
N
2
O
2
2NO
!
H>0
Pobrano ze strony www.sqlmedia.pl

Strona 4 z 12
Pobrano ze strony www.sqlmedia.pl

Strona 5 z 12
Zadanie 36. (3 pkt)
Reakcja chemiczna
A + 3B " AB
3
przebiega wed#ug równania kinetycznego v = k[A][B]
3
.
Okre%l ca&kowity rz"d tej reakcji oraz oblicz, jak zmieni si# szybko%' tej reakcji, je$eli
st#$enie substratu A zmniejszymy czterokrotnie i równocze%nie st#$enie substratu B
zwi#kszymy dwukrotnie.
Rz!d reakcji: .........................................................................................................................................
Obliczenie zmiany szybko(ci reakcji: ...................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Zadanie 37. (3 pkt)
Zaproponuj przyk&ad soli potasowej, której roztwór nale$y podda' elektrolizie
z u$yciem elektrod w#glowych, by otrzyma' z roztworu oboj#tnego roztwór silnie zasadowy.
Odpowied( uzasadnij, zapisuj"c odpowiednie równania reakcji elektrodowych.
Wzór soli: ..............................................................................................................................................
Równania reakcji elektrodowych: .........................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Zadanie 38. (2 pkt)
Korzystaj"c z szeregu napi#ciowego metali wska$, którego metalu – cynku czy cyny – nale$y
u$y' jako protektora do ochrony stalowego ($elaznego) ruroci"gu przed korozj". Wybór
krótko uzasadnij.
Wybrany metal: .....................................................................................................................................
Uzasadnienie: ........................................................................................................................................
................................................................................................................................................................
Pobrano ze strony www.sqlmedia.pl

Strona 6 z 12
Zadanie 39. (4 pkt)
Oblicz, ile gramów roztworu KOH o st#$eniu 10% i ile gramów roztworu tej zasady o st#$eniu
10 mol)dm
–3
i g#sto%ci d = 1,4 g)cm
–3
nale$y u$y', aby przygotowa' 200 g roztworu KOH
o st#$eniu 20%.
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Zadanie 40. (3 pkt)
W poni$szych przyk&adach doko*cz zapis równa* reakcji lub zaznacz, $e reakcja nie
zachodzi.
1) Na
2
HPO
4
+ NaOH * .......................................................................................................................
2) K + H
2
O * .......................................................................................................................................
3) BaSO
4
+ HCl * ...............................................................................................................................
Pobrano ze strony www.sqlmedia.pl
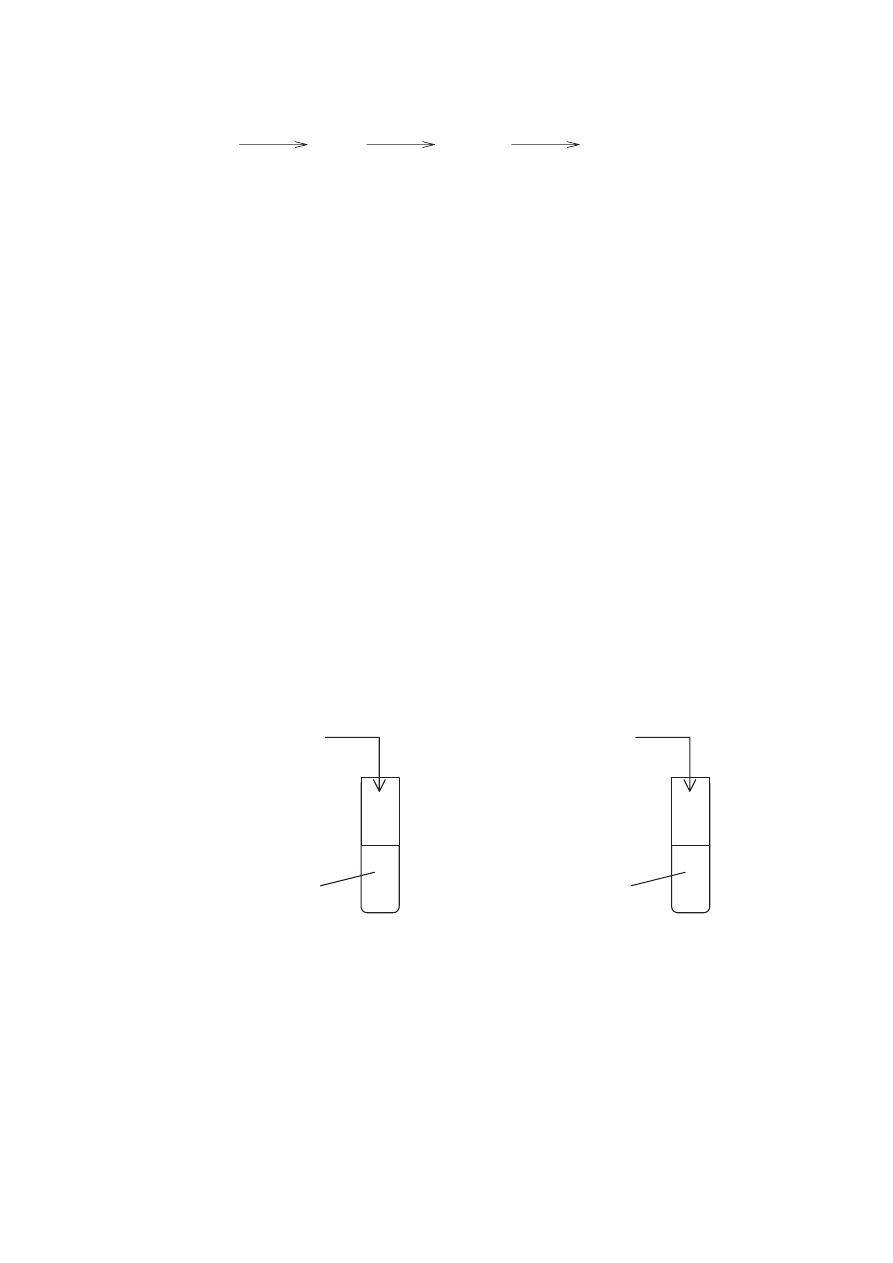
Strona 7 z 12
Zadanie 41. (3 pkt)
Dany jest ci!g reakcji:
Cu
CuCl
2
Cu(OH)
2
Na
2
[Cu(OH)
4
]
+ A
+ B
+ C
Zapisz wzory sumaryczne brakuj"cych w ci"gu przemian substratów.
Substrat A: ............................................................................................................................................
Substrat B: .............................................................................................................................................
Substrat C: .............................................................................................................................................
Zadanie 42. (3 pkt)
Który z wymienionych ni$ej zwi"zków ma charakter amfoteryczny?
Zapisz w formie cz"steczkowej dwa równania reakcji, które charakteryzuj" jego
amfoteryczno%'.
Al(NO
3
)
3
, CaO, H
3
PO
4
, ZnO
Odpowied': ...........................................................................................................................................
Równanie 1.: .........................................................................................................................................
Równanie 2.: .........................................................................................................................................
Informacja do zada* 43. i 44.
W celu zidentyfikowania jodku amonu przeprowadzono nast"puj!ce do(wiadczenia:
roztwór NaOH
roztwór NH
4
I
I.
roztwór Pb(NO
3
)
2
roztwór NH
4
I
II.
Zadanie 43. (2 pkt)
Zapisz obserwacje do powy$szych do%wiadcze*.
Do(wiadczenie I: ...................................................................................................................................
................................................................................................................................................................
Do(wiadczenie II: .................................................................................................................................
................................................................................................................................................................
Pobrano ze strony www.sqlmedia.pl

Strona 8 z 12
Zadanie 44. (2 pkt)
Zapisz w skróconej formie jonowej równania reakcji zachodz"cych w powy$szych
do%wiadczeniach.
Równanie I: ...........................................................................................................................................
Równanie II: ..........................................................................................................................................
Informacja do zadania 45. i 46.
Sta#a dysocjacji wodorotlenku sodu jest bardzo du%a, za( sta#a dysocjacji kwasu azotowego(III)
wynosi 2)10
–4
.
Zadanie 45. (3 pkt)
Na podstawie powy$szej informacji okre%l odczyn wodnego roztworu NaNO
2
.
Zapisz w skróconej formie jonowej równanie hydrolizy tej soli.
Jak" rol# wed&ug teorii Brönsteda pe&ni w tej reakcji woda?
Odczyn roztworu: ..................................................................................................................................
Równanie hydrolizy: .............................................................................................................................
Rola wody: ............................................................................................................................................
Zadanie 46. (3 pkt)
Oblicz stopie* dysocjacji oraz pH roztworu kwasu azotowego(III) o st#$eniu
0,5 mol·dm
–3
.
Obliczenie stopnia dysocjacji: ..............................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Obliczenie pH roztworu: .......................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Pobrano ze strony www.sqlmedia.pl

Strona 9 z 12
Zadanie 47. (3 pkt)
Okre%l typ ka$dej z nast#puj"cych reakcji:
1) etynu z bromem: ...............................................................................................................................
2) chloroetanu z NaOH w (rodowisku etanolu: ....................................................................................
3) powstawania polietylenu z etenu.: ....................................................................................................
Zadanie 48. (3 pkt)
Aldehydy o odpowiedniej budowie ulegaj! w (rodowisku zasadowym reakcji dysproporcjonowania,
która przebiega wed#ug schematu:
aldehyd + zasada " sól kwasu karboksylowego + alkohol
U$ywaj"c wzorów pó&strukturalnych zapisz równanie takiej reakcji dla aldehydu
benzoesowego (benzenokarboaldehydu) z NaOH. Podaj nazw# w#glowodoru, którego
pochodnymi s" reagenty tej reakcji.
Równanie reakcji: .................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Nazwa w"glowodoru: ...........................................................................................................................
Zadanie 49. (4 pkt)
Pewien ester o wzorze sumarycznym C
4
H
8
O
2
poddano hydrolizie. Jeden z produktów hydrolizy
daje pozytywny wynik próby Tollensa, a drugi poddany utlenieniu daje jako produkt propanon.
Zapisz wzór strukturalny estru i podaj jego nazw#. Przedstaw krótko swój tok rozumowania.
Wzór strukturalny estru: ........................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Nazwa estru: ..........................................................................................................................................
Uzasadnienie: ........................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Pobrano ze strony www.sqlmedia.pl

Strona 10 z 12
Zadanie 50. (3 pkt)
C
H
3
CH
C
N
CH
2
C
N
NH
2
O
O
CH
COOH
CH
3
H
H
Zapisz równanie reakcji pe&nej hydrolizy powy$szego peptydu i wska$, który z produktów
hydrolizy jest zwi"zkiem optycznie czynnym. Napisz wzory stereochemiczne obu
enancjomerów tego aminokwasu.
Równanie hydrolizy: .............................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Wzór zwi!zku optycznie czynnego: .....................................................................................................
................................................................................................................................................................
Wzory stereochemiczne: .......................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Pobrano ze strony www.sqlmedia.pl

Strona 11 z 12
Zadanie 51. (2 pkt)
Poni%ej przedstawiono nazwy otrzymywanych pi"ciu tworzyw, otrzymywanych w procesach
polimeryzacji lub polikondensacji:
poliamid, polichlorek winylu, poliformaldehyd, polistyren, teflon.
Uzupe&nij nast#puj"c" tabel#, wpisuj"c obok wzoru zwi"zku nazw# tworzywa, które
otrzymuje si# na drodze polimeryzacji lub polikondensacji tego zwi"zku.
Wzór zwi#zku
Nazwa tworzywa
1. H
2
N–(CH
2
)
5
–COOH
2.
HCHO
3.
CF
2
=CF
2
4.
CH
2
=CHCl
Zadanie 52. (1 pkt)
Etylen (eten) jest monomerem, z którego w reakcji polimeryzacji otrzymuje si" polietylen.
Wska$ cech# cz"steczek etylenu, dzi#ki której mog" one ulega' reakcji polimeryzacji.
................................................................................................................................................................
................................................................................................................................................................
Pobrano ze strony www.sqlmedia.pl

Strona 12 z 12
BRUDNOPIS (nie podlega ocenie)
Pobrano ze strony www.sqlmedia.pl

Strona 13 z 12
Pobrano ze strony www.sqlmedia.pl
Wyszukiwarka
Podobne podstrony:
2004 MCH A1 pro2004 id 603780 Nieznany (2)
2004 MCH A1 pro2004 id 603780 Nieznany (2)
2004, MCH A2 model pro2004
pr A2 2012 id 381782 Nieznany
A2 plytazelbetowa id 49693 Nieznany (2)
A2 kolor id 49688 Nieznany (2)
pp A2 2012 id 381124 Nieznany
antropomotoryka 26 2004 id 6611 Nieznany (2)
3 p1 a2 id 33942 Nieznany
2004 2005 szkolny id 245044 Nieznany (2)
2004 2005 wojewodzki id 245045 Nieznany (2)
pale A2 id 345813 Nieznany
podnosnik A2 by Arti id 365542 Nieznany
asm state of the art 2004 id 70 Nieznany (2)
Lista A2 id 269943 Nieznany
matura 2009 roz a2 styczen id 6 Nieznany
fosfolipaza A2 id 179963 Nieznany
więcej podobnych podstron