
108 Â
WIAT
N
AUKI
Listopad 1996
TERAPIE JUTRA
W
ciàgu ostatniego stulecia na
przemian ros∏o i mala∏o za-
interesowanie mo˝liwoÊcià
wykorzystania uk∏adu odpornoÊciowe-
go – niezwykle skutecznego w przypad-
ku wielu chorób – do walki rakiem.
Dzisiaj wàtpliwoÊci znikn´∏y i liczna rze-
sza badaczy zajmuje si´ przek∏adaniem
tej idei na nowe biologiczne metody
leczenia.
Obserwacje kliniczne wspierajàce hi-
potez´, ˝e uk∏ad odpornoÊciowy mo˝e
hamowaç rozwój nowotworów, pocho-
dzà z XIX wieku. Wówczas lekarze za-
uwa˝yli, ˝e guzy nowotworowe u pa-
cjentów, którzy przebyli zaka˝enie ba-
kteryjne, czasem si´ zmniejszajà. Wil-
liam B. Coley, chirurg pracujàcy w Me-
morial Hospital w Nowym Jorku
w latach 1892–1936, ca∏e swoje ˝ycie po-
Êwi´ci∏ opracowaniu sposobów lecze-
nia opartych na tym zjawisku. Poczàt-
kowo zaka˝a∏ on umyÊlnie chorych na
raka ˝ywymi bakteriami; z czasem opra-
cowa∏ szczepionk´ zawierajàcà zabite
bakterie, która mia∏a pobudzaç uk∏ad
odpornoÊciowy do niszczenia nowotwo-
ru. Te metody leczenia – obecnie okre-
Êlane mianem immunoterapii, ponie-
wa˝ wykorzystujà mechanizmy obron-
ne organizmu do walki z chorobà –
przynios∏y znacznà popraw´ stanu
zdrowia niektórych chorych. Nie zosta-
∏y jednak wprowadzone powszechnie
do leczenia ze wzgl´du na trudne do
przewidzenia rezultaty.
W poczàtkach naszego wieku tak˝e
inni badacze próbowali opracowaç te-
rapie wykorzystujàce procesy odporno-
Êciowe, jednak ˝adna z nich nie da∏a
przekonujàcych wyników. Mimo to idea
zwiàzku pomi´dzy odpornoÊcià a ra-
kiem nie opuszcza∏a umys∏ów wielu
osób. Na przyk∏ad w latach szeÊçdziesià-
tych i siedemdziesiàtych powszechnie
uznano hipotez´ „nadzoru immunolo-
gicznego”, której autorami byli Lewis
Thomas z New York University i Mac-
Farlane Burnett z Hall Institute w Mel-
bourne w Australii. Zak∏ada∏a ona, ˝e
uk∏ad odpornoÊciowy stale wyszukuje
i niszczy pojawiajàce si´ komórki no-
wotworowe. Zgodnie z tà hipotezà guz
powstaje wówczas, gdy system nadzo-
ru zawodzi. Jednak przez kolejne lata
nagromadzono dane Êwiadczàce, ˝e
uk∏ad odpornoÊciowy atakuje jedynie
nowotwory wywo∏ane przez wirusy.
Poniewa˝ stanowià one mniejszoÊç po-
Êród wszystkich typów nowotworów,
powy˝sza teoria wydawa∏a si´ b∏´dna.
Uzyskane niedawno informacje spo-
wodowa∏y jednak nawrót zainteresowa-
nia immunoterapià nowotworów, przede
wszystkim wskutek rewolucyjnych prze-
mian w immunologii. Odkryto i wyizo-
lowano komórki i substancje, dzi´ki któ-
rym uk∏ad odpornoÊciowy broni orga-
nizm przed infekcjà oraz usuwa zaka˝o-
ne i uszkodzone tkanki. Badajàc te sk∏ad-
niki, immunolodzy dok∏adnie poznali
dzia∏anie tego uk∏adu, a zajmujàcy si´
immunologià nowotworów zdobyli wie-
dz´ o mechanizmach i czàsteczkach, za
pomocà których b´dà mogli w przysz∏o-
Êci kontrolowaç raka.
Pobudzanie uk∏adu odpornoÊciowego
Dzisiaj okreÊlilibyÊmy próby Coleya
jako terapi´ nieswoistà: wzmaga∏a ona
aktywnoÊç ca∏ego uk∏adu odpornoÊcio-
wego zamiast wybiórczo pobudzaç ele-
menty szczególnie skuteczne w walce
z nowotworami. Podczas ostatniego
dziesi´ciolecia uczeni opracowali wie-
le innych nieswoistych immunoterapii.
Ich strategia przypomina naprawianie
telewizora kopniakami: porzàdne po-
trzàÊni´cie uk∏adem odpornoÊciowym
mo˝e zwi´kszyç jego zdolnoÊç do usu-
wania komórek nowotworowych. Na-
dal nie wiadomo jednak, który ze sk∏ad-
ników lub jakie ich kombinacje przy-
czyniajà si´ do zniszczenia nowotworu.
Pomimo to strategia ta przynosi pewne
rzeczywiste sukcesy.
Przyk∏adowo brodawczak wyst´pu-
jàcy na wewn´trznej Êcianie p´cherza
moczowego, dobrze reaguje na szcze-
pionk´ u˝ywanà w walce z gruêlicà, za-
wierajàcà pràtki bydl´cego szczepu Cal-
mette-Guérin, czyli BCG. Pràtki tego
szczepu chronià przed gruêlicà, ponie-
wa˝ wywo∏ujà silnà odpowiedê immu-
nologicznà. Brodawczak zwykle nawra-
ca po chirurgicznym usuni´ciu i w
kolejnych stadiach nacieka Êcian´ p´-
cherza i jego otoczenie. Jednak wpro-
wadzenie szczepionki BCG do p´che-
rza moczowego przez cewnik wywo∏uje
przewlek∏à reakcj´ zapalnà – d∏ugotrwa-
∏e pobudzenie komórek uk∏adu odpor-
noÊciowego zwalczajàcych napastni-
ków. Sposób dzia∏ania komórek od-
czynu zapalnego nie jest dok∏adnie zna-
ny, lecz wiemy, ˝e wraz z wydzielany-
mi przez siebie substancjami zabijajà ist-
niejàce lub powstajàce w Êcianie p´che-
rza komórki nowotworowe. Dzi´ki
temu pacjenci, którzy po operacji otrzy-
mujà BCG, sà nara˝eni na znacznie
mniejsze ryzyko wznowy nowotworu.
Chocia˝ powy˝sza szczepionka jest
przyk∏adem skutecznoÊci nieswoistej im-
munoterapii, to jednak, wywo∏ujàc za-
palenie p´cherza moczowego, dzia∏a wy-
∏àcznie miejscowo. Wi´kszoÊç nowo-
tworów zaÊ zagra˝a ˝yciu chorego, po-
niewa˝ rozprzestrzenia si´ i powoduje
powstanie guzów w odleg∏ych miejscach.
˚eby je wyeliminowaç, immunoterapia
Immunoterapia
nowotworów
Post´py wiedzy o uk∏adzie odpornoÊciowym
pozwolà opracowaç metody wprz´gajàce
w∏asne si∏y organizmu do walki z rakiem
Lloyd J. Old
Â
WIAT
N
AUKI
Listopad 1996 109
powinna oddzia∏ywaç na nie we wszyst-
kich cz´Êciach cia∏a. Dlatego w latach sie-
demdziesiàtych i osiemdziesiàtych wie-
lu badaczy onkologów zaj´∏o si´ czà-
steczkami zwanymi dziÊ cytokinami, któ-
re powstajà w organizmie w odpowie-
dzi na zaka˝enia bakteryjne czy wiruso-
we i pomagajà koordynowaç odpowiedê
immunologicznà. Nale˝à do nich takie
bia∏ka, jak interferony, interleukiny
i czynnik martwicy nowotworu (TNF –
tumor necrosis factor). Poczàtkowo ba-
dacze mieli nadziej´, ˝e leczenie cytoki-
nami b´dzie mia∏o niezwyk∏à wartoÊç.
Jednak wyniki licznych prób klinicznych
z zastosowaniem nieswoistej immuno-
terapii ostudzi∏y ich entuzjazm. Lecze-
nie wy∏àcznie cytokinami prowadzi do
poprawy jedynie u nielicznych chorych.
Antygeny nowotworowe
Byç mo˝e cytokiny oka˝à si´ skutecz-
niejsze, jeÊli b´dà stosowane w ró˝nych
po∏àczeniach lub razem z innymi meto-
dami leczenia. Wielu badaczy poszuku-
je jednak bardziej swoistych sposobów
walki z rakiem. ˚eby nakierowaç immu-
noterapi´ wybiórczo na komórki nowo-
tworowe, nale˝y najpierw odró˝niç je od
normalnych. Uk∏ad odpornoÊciowy po-
trafi wykryç ró˝nice pomi´dzy komór-
kami dzi´ki temu, ˝e na ich powierzch-
ni pojawiajà si´ czàsteczki zwane an-
tygenami. Ju˝ dawno uczeni przypusz-
czali, ˝e komórki nowotworowe mogà
byç wyposa˝one w czàsteczki Êwiadczà-
ce o ich nieprawid∏owoÊci. Gdyby da∏o
si´ znaleêç antygeny swoiste dla komó-
rek nowotworowych, mo˝na by opraco-
waç sposoby uczynienia ich lepiej rozpo-
znawalnymi przez uk∏ad odpornoÊcio-
wy. Tym samym komórki te sta∏yby si´
celem ataku uk∏adu odpornoÊciowego –
podobnie antygeny bakteryjne i wiruso-
we pobudzajà organizm do walki z drob-
noustrojami chorobotwórczymi.
Odkrycie przeciwcia∏ pod koniec XIX
wieku dostarczy∏o Êrodków do poszuki-
wania takich swoistych dla nowotwo-
rów antygenów, a póêniej umo˝liwi∏o
liczne badania nad zastosowaniem prze-
ciwcia∏ w immunoterapii nowotworów.
Przeciwcia∏a – czàsteczki bia∏kowe, pod-
stawowe sk∏adniki uk∏adu odpornoÊcio-
wego, krà˝à we krwi i wià˝à si´ z obcy-
mi antygenami. Dzi´ki temu napastnicy
op∏aszczeni przeciwcia∏ami stajà si´ ce-
lem ataku komórek ˝ernych zwanych
makrofagami, innych komórek i uk∏adu
specjalnych bia∏ek krwi zwanych bia∏ka-
mi dope∏niacza.
ZdolnoÊç przeciwcia∏ do wykrywa-
nia nieznacznych ró˝nic mi´dzy czà-
steczkami to cecha niezwykle przydat-
na w badaniach nad poszukiwaniem
antygenów nowotworowych. W ciàgu
ostatniego stulecia naukowcy wstrzy-
kiwali ludzkie komórki rakowe niezli-
czonej liczbie koni, owiec, królików, my-
szy i szczurów, analizujàc nast´pnie
powstajàce w odpowiedzi przeciwcia-
∏a. Gdyby uk∏ad odpornoÊciowy tych
zwierzàt odpowiada∏ na obce komórki
nowotworowe wytwarzaniem przeciw-
cia∏, nie reagujàcych z komórkami pra-
wid∏owymi, mog∏oby to sygnalizowaç
istnienie antygenów, które po identyfi-
kacji da∏oby si´ wykorzystaç jako cel
ataku w terapii z zastosowaniem prze-
ciwcia∏. Wielu badaczy próbowa∏o tego
podejÊcia i donosi∏o o znalezieniu anty-
genów swoistych dla nowotworów.
Niestety, ˝adne z tych odkryç nie zosta-
∏o potwierdzone w dalszych badaniach.
Era przeciwcia∏ monoklonalnych
Poszukiwanie antygenów nowotwo-
rowych u∏atwi∏o odkrycie, jakiego do-
konali w 1975 roku César Milstein i
Georges J. F. Köhler z University of
Cambridge. Wykazali oni, ˝e komórka
produkujàca przeciwcia∏a mo˝e ˝yç nie-
skoƒczenie d∏ugo, jeÊli po∏àczy si´ jà
z komórkà nowotworowà. Technika, za
którà otrzymali Nagrod´ Nobla, pozwa-
la uzyskiwaç nieograniczone iloÊci iden-
tycznych, czyli monoklonalnych prze-
ciwcia∏, poniewa˝ ka˝da komórka pro-
dukujàca przeciwcia∏a wytwarza wy-
∏àcznie jeden ich rodzaj. Powy˝sza tech-
nika wywar∏a znaczny wp∏yw na im-
munologi´ nowotworów, i to z wielu
powodów. Po pierwsze, dostarczy∏a po-
t´˝nego narz´dzia do poszukiwania an-
tygenów nowotworowych. Po drugie,
badacze mogli w koƒcu otrzymywaç
okreÊlone przeciwcia∏a w iloÊciach wy-
starczajàcych do klinicznego prze-
testowania skutecznoÊci tego rodzaju
immunoterapii.
Z tà spektakularnà metodà wiàzano
wielkie nadzieje; przedwczeÊnie i nie li-
czàc si´ z realiami, zapewniano o mo˝-
liwoÊci zastosowania przeciwcia∏ jako
„magicznych pocisków”. Sàdzono, ˝e
rozpoznawszy swoiste antygeny, prze-
Za zgodà PILAR BARIN-CHESA
Memorial Sloan-Kettering Cancer Center
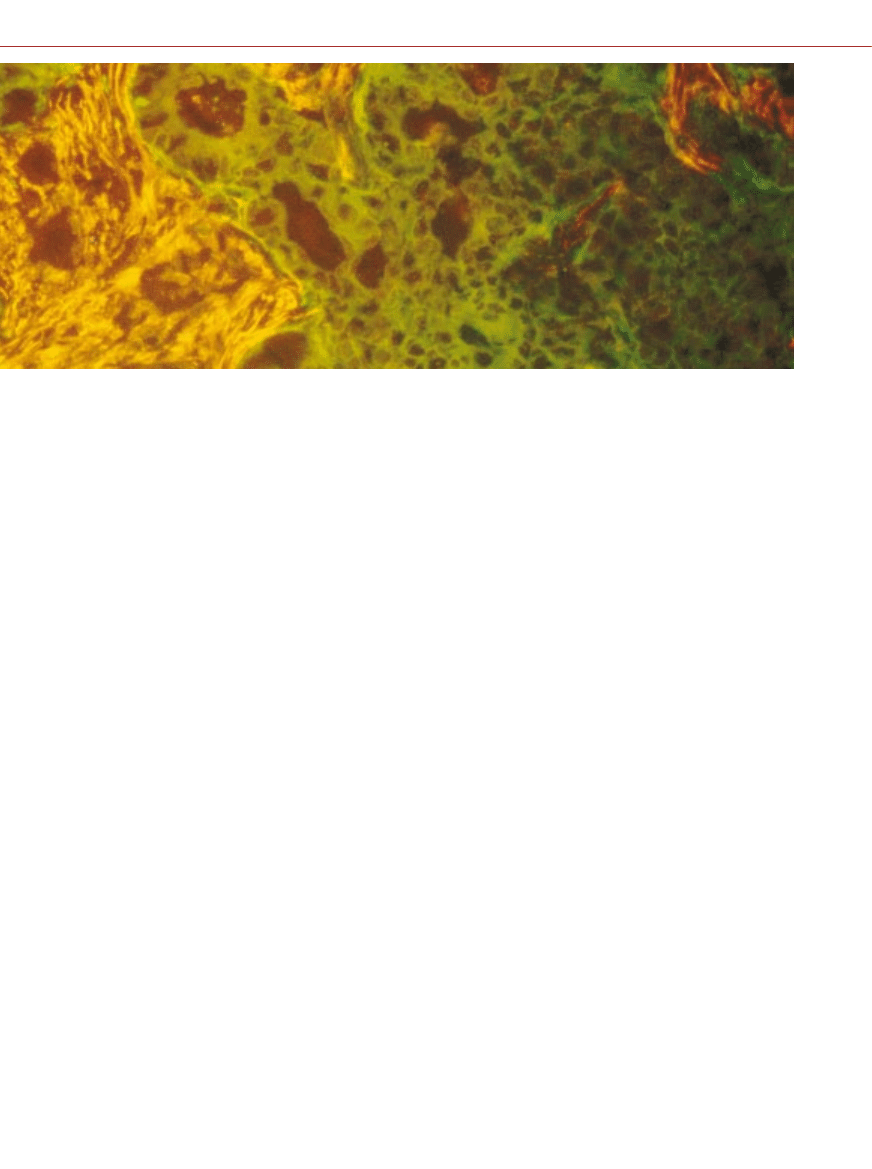
WYCINEK RAKA JELITA GRUBEGO zabarwiony przeciwcia∏ami monoklonalnymi
w dwóch ró˝nych kolorach. Ka˝de przeciwcia∏o wià˝e odmienne bia∏ko na powierzchni
ró˝nych populacji komórek. Kolor zielony oznacza komórki nowotworowe, natomiast po-
maraƒczowy – komórki tkanki ∏àcznej (podÊcieliska). Poniewa˝ przeciwcia∏a rozpoznajà
okreÊlone komórki, mo˝na je wykorzystaç do wyszukiwania i wybiórczego niszczenia
komórek nowotworowych, jak równie˝ tkanek, które podtrzymujà i od˝ywiajà guz.
ciwcia∏a monoklonalne osiàdà na komór-
kach nowotworowych i uruchomià od-
powiedê odpornoÊciowà, która zniszczy
komórki docelowe, lecz oszcz´dzi zdro-
we, pozbawione antygenów nowotwo-
rowych. Wielu badaczy przewidywa∏o,
˝e mo˝na b´dzie zwi´kszyç niszczàcà
si∏´ przeciwcia∏, do∏àczajàc do nich che-
miczne trucizny; „uzbrojone” przeciw-
cia∏o transportowa∏oby takà czàsteczk´
bezpoÊrednio do guza, gdzie powinna
zabiç jego komórki.
Wywo∏ane tym emocje sprawi∏y, ˝e
przemys∏ farmaceutyczny i prywatni in-
westorzy wydali na ten cel olbrzymie
sumy. Lecz kiedy przypuszczeƒ nie uda-
∏o si´ potwierdziç w oczekiwanym ter-
minie, nastroje uleg∏y radykalnej zmia-
nie; wielu ekspertów i inwestorów
oÊwiadczy∏o, ˝e przeciwcia∏a monoklo-
nalne zawiod∏y. RzeczywistoÊç wyglà-
da jednak znacznie bardziej optymi-
stycznie. Koncepcja nadal wydaje si´
uzasadniona i stale dokonywane sà po-
wolne post´py w opracowaniu metod
leczenia z zastosowaniem przeciwcia∏.
Przeciwcia∏a monoklonalne ujawni∏y
olbrzymià liczb´ antygenów na ludzkich
komórkach nowotworowych. Niestety,
prawie wszystkie wyst´pujà tak˝e na
zdrowych komórkach, a wi´c i one mo-
g∏yby zostaç uszkodzone w czasie lecze-
nia przeciwcia∏ami. Nawet ten fakt nie
musi jednak wykluczaç zastosowania
przeciwcia∏ w terapii: antygeny znajdu-
jàce si´ w zdrowych tkankach mogà byç
niedost´pne dla przeciwcia∏ krà˝àcych
we krwi; komórki nowotoworowe mo-
gà mieç wi´cej czàsteczek antygenu ani-
˝eli zdrowe; uszkodzenia zdrowych ko-
mórek spowodowane przez przeciwcia∏a
mogà byç odwracalne.
Przeciwcia∏a mog∏yby nie tylko wy-
szukiwaç komórki nowotworowe; mo-
g∏yby one tak˝e oddzia∏ywaç na inne,
niezb´dne do wzrostu nowotworu,
rodzaje komórek i czàsteczek lub te˝
neutralizowaç czynniki wzrostowe –
substancje potrzebne do rozwoju guza
i jego unaczynienia, w ten sposób ha-
mujàc rozrost nowotworu. Przeciwcia-
∏a mo˝na równie˝ skierowaç na jego
podÊcielisko – tkank´ ∏àcznà znajdujà-
cà si´ pomi´dzy komórkami nowotwo-
rowymi, która czasami stanowi nawet
ponad 60% masy guza, a gdy jej brak,
nowotwory nie przekraczajà mikrosko-
pijnych, niegroênych rozmiarów. W Me-
morial Sloan-Kettering Cancer Center
w Nowym Jorku Wolfgang J. Rettig i Pi-
lar Garin-Chesa wraz ze mnà wykryli
antygen nazwany FAP-alfa, który ule-
ga silnej ekspresji powierzchniowej na
komórkach podÊcieliska wielu typów
nowotworów. Ten i inne antygeny,
charakterystyczne dla podÊcieliska lub
naczyƒ krwionoÊnych guza, uwa˝a si´
za obiecujàce cele ataku w immunote-
rapii przeciwcia∏ami.
Przeciwcia∏a monoklonalne uzysku-
je si´ obecnie najcz´Êciej od myszy im-
munizowanych komórkami nowotwo-
rowymi cz∏owieka. Próby kliniczne
dowiod∏y, ˝e wi´kszoÊç ludzi rozwija
odpowiedê immunologicznà neutrali-
zujàcà te pochodzàce od myszy bia∏ka.
Wobec tego uczeni zacz´li konstruowaç
ludzkie lecznicze przeciwcia∏a, które po-
winny uniknàç ataku uk∏adu odporno-
Êciowego. JednoczeÊnie przerabia si´
mysie przeciwcia∏a tak, aby bardziej
przypomina∏y ludzkie. Wszystkie zb´d-
ne (tj. nie wià˝àce swoistego antygenu –
przyp. t∏um.) fragmenty mysiego prze-
ciwcia∏a zostajà wtedy zastàpione ludz-
kimi odpowiednikami. Ta sztuczka
zwana ucz∏owieczeniem, czyli humani-
zowaniem, pozwoli∏a uzyskaç przeciw-
cia∏a, które – jak wykazujà wyniki
pierwszych testów klinicznych – wy-
mykajà si´ uk∏adowi odpornoÊciowe-
mu. In˝ynierowie przeciwcia∏ doskona-
là równie˝ inne w∏aÊciwoÊci humani-
zowanych czàsteczek, zwi´kszajàc ich
zdolnoÊç do wiàzania antygenu i wni-
kania do wn´trza guza.
Testy kliniczne przeciwcia∏
Po zidentyfikowaniu docelowego an-
tygenu, wybraniu i skonstruowaniu od-
powiedniego przeciwcia∏a, naukowcy
muszà teraz zdecydowaç, jakiego ro-
dzaju niszczàcy sygna∏ chcieliby prze-
kazaç komórkom guza. Sà na to dwa
sposoby. Jeden wykorzystuje w∏aÊciwà
przeciwcia∏om zdolnoÊç do niszczenia
komórek nowotworowych. Drugi trak-
tuje przeciwcia∏a jak wehiku∏y prze-
noszàce Êrodki toksyczne, na przyk∏ad
leki przeciwnowotworowe, zwiàzki ra-
dioaktywne czy trucizny roÊlinne lub
zwierz´ce. Pojawi∏o si´ tak wiele poten-
cjalnych docelowych antygenów i skon-
struowano tyle przeciwcia∏, ˝e niemo˝-
liwe jest obecnie przetestowanie ich
wszystkich w próbach klinicznych.
Jednym z kryteriów decydujàcych
o wyborze przeciwcia∏a jako potencjal-
nego leku jest prawdopodobieƒstwo, ˝e
w wi´kszym stopniu nagromadzi si´
ono w tkankach guza ani˝eli zdrowych.
Aby sprawdziç, czy badane przeciwcia-
∏o spe∏nia ten warunek, znakuje si´ je
izotopem jodu (
131
I), wstrzykuje ochotni-
kowi i Êledzi losy tego przeciwcia∏a w
organizmie, pos∏ugujàc si´ odpowied-
nimi technikami obrazowania. W celu
dok∏adniejszego pomiaru jego st´˝enia
w guzie pobiera si´ fragment chorej
tkanki. Poniewa˝ ˝aden ze znanych an-
tygenów docelowych nie wyst´puje wy-
∏àcznie na komórkach nowotworowych,
wyniki badaƒ obrazowych sà tak˝e nie-
zwykle istotne w ocenie iloÊci przeciw-
cia∏a gromadzàcego si´ w zdrowych
tkankach. Przeciwcia∏a wykazujàce naj-
lepsze w∏aÊciwoÊci sà pierwszymi kan-
dydatami do testów leczniczych.
Opracowanie tylko jednego protoko-
∏u do prób klinicznych terapii przeciw-
cia∏ami wymaga olbrzymiego wysi∏ku
i czasu, co t∏umaczy, dlaczego przejÊcie
od najlepszych pomys∏ów do przydat-
nych sposobów leczenia trwa znacznie
d∏u˝ej ni˝ byÊmy chcieli. Jako przyk∏ad
niech pos∏u˝à badania nad mysim prze-
ciwcia∏em monoklonalnym zwanym
110 Â
WIAT
N
AUKI
Listopad 1996
TERAPIE JUTRA
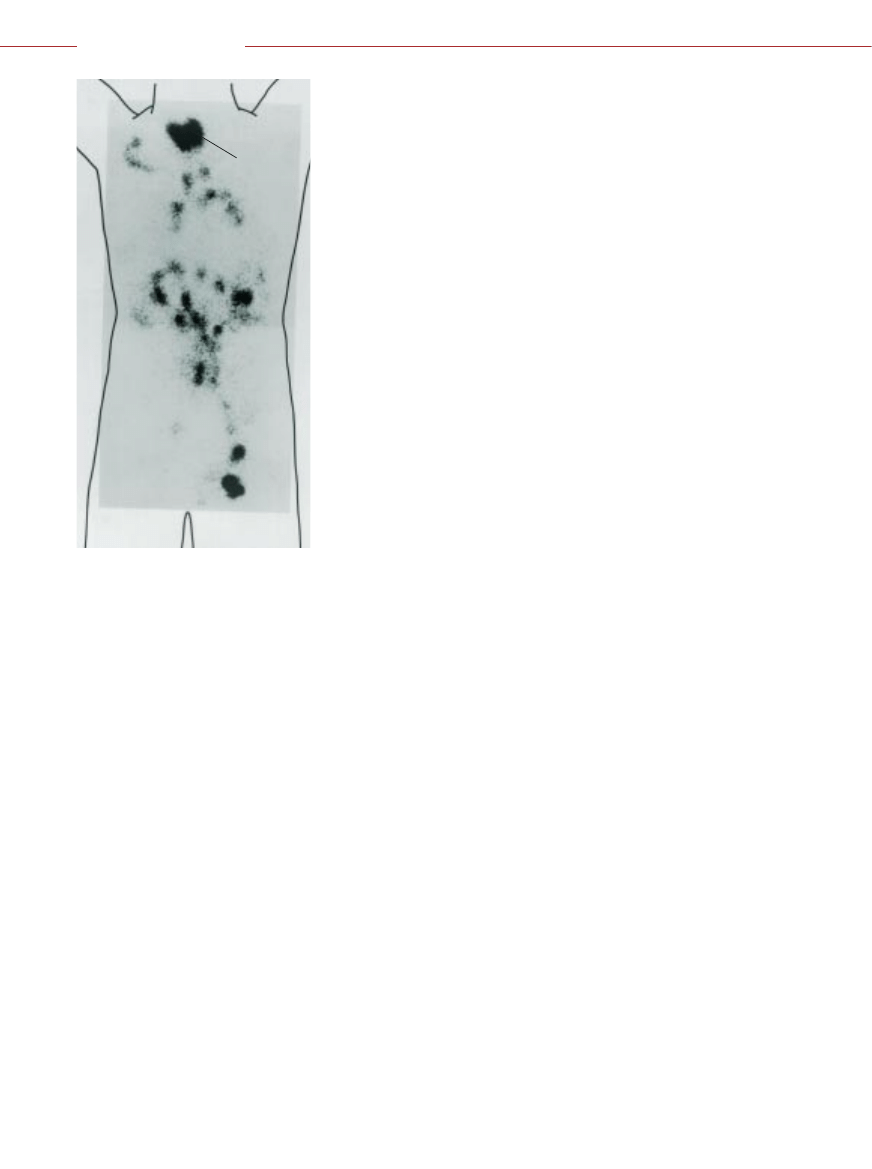
PRZERZUTY RAKA JELITA GRUBEGO
zlokalizowane w jamie brzusznej i poza nià
dajà zacienienia na scyntygramie, poniewa˝
wychwyci∏y i zag´Êci∏y przeciwcia∏o mono-
klonalne A33 znakowane radioizotopem.
Prawid∏owe komórki jelita równie˝ wy-
chwytujà A33, lecz go nie zatrzymujà. (Ra-
dioaktywnoÊç w obszarze tarczycy jest spo-
wodowana wychwytem wolnego radioizo-
topu jodu.) To zjawisko selektywnej aku-
mulacji przeciwcia∏ rodzi nadziej´ na roz-
wój ukierunkowanych terapii, dajàcych
mniej objawów niepo˝àdanych ni˝ chemio-
terapie konwencjonalne.
Za zgodà SYDNEYA WELTA
Memorial Sloan-Kettering Cancer Center
TARCZYCA
A33 prowadzone obecnie przez Syd-
neya Welta i naszà grup´ w Memorial
Sloan-Kettering. Wykrywa ono antygen
obecny na zdrowych komórkach jelita
i praktycznie na wszystkich rodzajach
raka jelita grubego. Badania kliniczne
z A33 nisko wyznakowanym radioak-
tywnym izotopem wskazujà na znaczà-
cy jego wychwyt przez komórki raka je-
lita grubego. Prawie 0.01% podanej
ca∏kowitej dawki przeciwcia∏a groma-
dzi si´ w obr´bie nowotworu; co wi´cej
– przechodzi ono do wn´trza guza.
Te korzystne wyniki uzasadni∏y ko-
lejny krok: u˝ycie go w drugiej fazie
prób klinicznych w celu ustalenia sku-
tecznoÊci leczniczej. „Na∏adowaliÊmy”
przeciwcia∏o A33 znacznie wi´kszà
dawkà izotopu zdolnà napromieniç
i zniszczyç komórki nowotworowe i po-
stawiliÊmy dwa pytania: czy do guza
dotrze wystarczajàca iloÊç przeciwcia-
∏a oraz jaki wp∏yw wywrze ono na pra-
wid∏owe komórki przewodu pokarmo-
wego? Poniewa˝ osoby badane w tej
próbie rozwija∏y odpowiedê immuno-
logicznà neutralizujàcà mysie A33,
wstrzykiwaliÊmy im pojedynczà daw-
k´ przeciwcia∏a. (Kolejne iniekcje by∏y-
by bezu˝yteczne, uk∏ad odpornoÊciowy
bowiem rozpozna∏by i usunà∏ t´ czà-
steczk´, zanim mia∏aby szans´ dotarcia
w pobli˝e guza.) Nawet przy tak ogra-
niczonym dawkowaniu u niektórych
chorych guzy uleg∏y zmniejszeniu. Ale
co bardziej istotne i zaskakujàce, prze-
ciwcia∏o to nie wywo∏ywa∏o ˝adnych
objawów toksycznych w jelicie, chocia˝
si´ w nim gromadzi∏o.
Naszym zdaniem komórki jelita nie
ulegajà uszkodzeniu, poniewa˝ szybko
pozbywajà si´ przeciwcia∏a, natomiast
komórki guza zatrzymujà je na po-
wierzchni. Powsta∏a równie˝ zhumani-
zowana wersja przeciwcia∏a A33, która
przechodzi obecnie próby kliniczne. ˚e-
by daç wyobra˝enie, ile czasu wymaga-
∏a realizacja tego projektu, przedstaw-
my nast´pujàce dane: antygen wykryto
w 1982 roku, pierwsze badania klinicz-
ne rozpocz´to w 1988 roku, a testy lecz-
Â
WIAT
N
AUKI
Listopad 1996 111
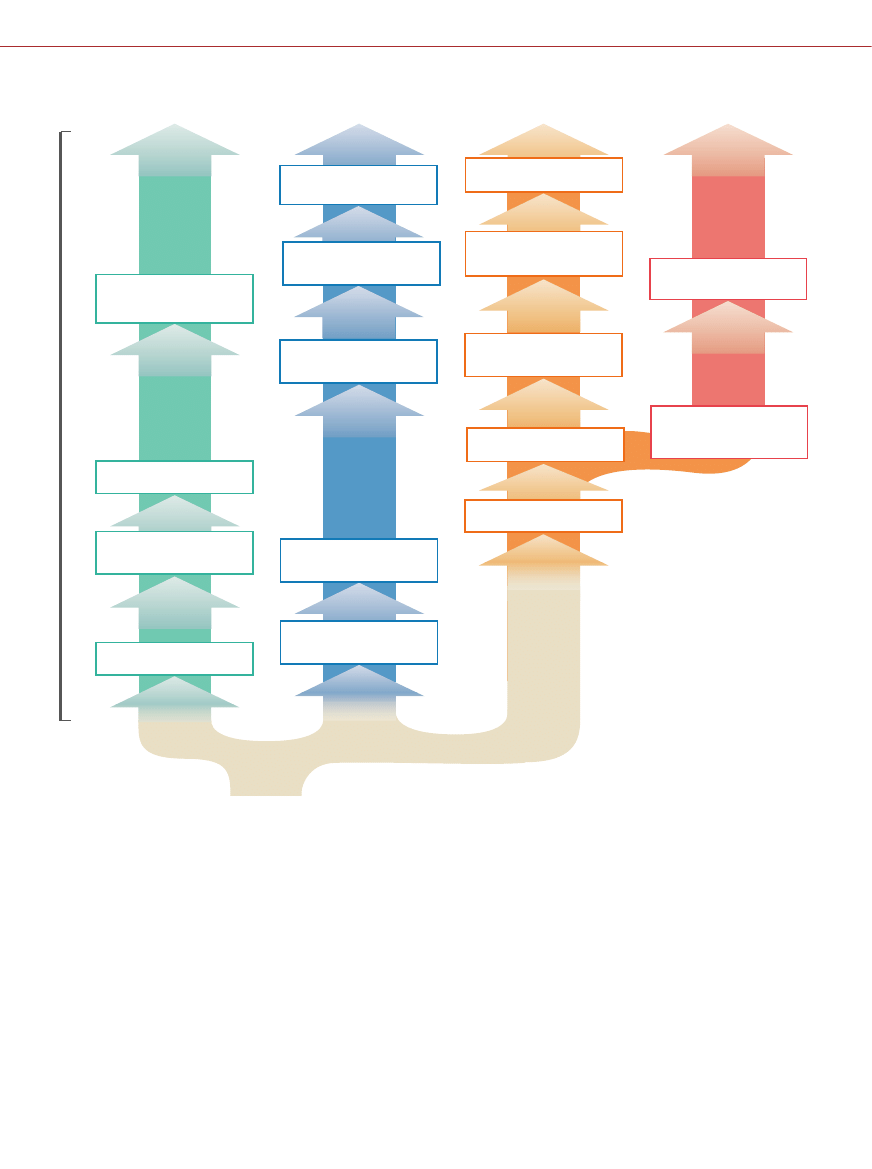
Punkty zwrotne w historii immunoterapii nowotworów
ODKRYCIE I PRÓBY
STOSOWANIA CYTOKIN:
INTERFERONÓW, TNF, IL-2,
IL-12, GM-CSF
BADANIA PRZECIWNOWOTWOROWYCH
W¸AÂCIWOÂCI SK¸ADNIKÓW
BAKTERII U ZWIERZÑT
PIERWSZE PRÓBY COLEYA
Z TOKSYNAMI
PRÓBY ZE SZCZEPIONKÑ BCG
NA ZWIERZ¢TACH I LUDZIACH
PIERWSZE PRÓBY KLINICZNE
Z PRZECIWCIA¸AMI
HUMANIZOWANYMI
OPRACOWANIE METODY
UZYSKIWANIA MYSICH
PRZECIWCIA¸ MONOKLONALNYCH
POCZÑTEK POSZUKIWANIA
PRZECIWCIA¸ PRZECIWKO ANTYGENOM
SWOISTYM DLA NOWOTWORÓW
POCZÑTEK STOSOWANIA PRZECIWCIA¸
W DIAGNOSTYCE I TERAPII
NOWOTWORÓW
POCZÑTEK BADA¡ KLINICZNYCH
MYSICH PRZECIWCIA¸
MONOKLONALNYCH
PIERWSZE PRÓBY KLINICZNE
ZE SZCZEPIONKAMI ZAWIERAJÑCYMI
PEPTYDY NOWOTWOROWE
WYKRYCIE U LUDZI
PRZECIWCIA¸ I LIMFOCYTÓW T
REAGUJÑCYCH Z NOWOTWORAMI
OKREÂLENIE ROLI LIMFOCYTÓW T
W IMMUNOLOGII NOWOTWORÓW
WYKRYCIE SWOISTYCH ANTYGENÓW
NOWOTWOROWYCH U MYSZY
CZASY
OBECNE
1880
SKLONOWANIE LUDZKICH ANTYGENÓW
NOWOTWOROWYCH ROZPOZNAWANYCH
PRZEZ LIMFOCYTY T
PIERWSZE PRÓBY KLINICZNE
Z LIMFOCYTAMI CHORYCH
NA NOWOTWORY
PIERWSZE WZMIANKI
O PRZENOSZENIU
OPORNOÂCI NA NOWOTWORY
PRZEZ LIMFOCYTY T U MYSZY
IMMUNOTERAPIA
NIESWOISTA
BIERNA IMMUNOTERAPIA
(PODAWANIE PRZECIWCIA¸)
CZYNNA IMMUNOTERAPIA
(PODAWANIE SZCZEPIONEK)
ADOPTYWNA
IMMUNOTERAPIA
JANA BRENNING

nicze – w 1991 roku. Pierwsi chorzy
otrzymali humanizowane przeciwcia∏o
w 1995 roku.
Najwi´kszym dotàd osiàgni´ciem w
tego rodzaju terapii okaza∏y si´ wyniki
badaƒ nad przeciwcia∏em, które wià˝e
antygen obecny zarówno na prawid∏o-
wych limfocytach B – komórkach, które
po pobudzeniu wytwarzajà przeciwcia-
∏a – jak i na komórkach ch∏oniaka, no-
wotworu wywodzàcego si´ z limfocy-
tów B. Stuart F. Schlossmann z Da-
na-Farber Cancer Institute w Bostonie
pierwszy wykry∏ ten antygen nazwany
CD20, który sta∏ si´ obiektem zaintereso-
wania wielu badaczy, m.in. zespo∏u z
University of Michigan, prowadzonego
przez Marka S. Kaminskiego, oraz gru-
py Olivera W. Pressa z University of Wa-
shington School of Medicine. Uzyskane
wyniki sà niezwykle emocjonujàce. Sa-
mo to przeciwcia∏o mo˝e spowodowaç
zmniejszenie si´ masy guza, a w po∏à-
czeniu z
131
I efekt ten jest znaczny i d∏u-
gotrwa∏y. Równie wa˝ne jest, ˝e lecze-
nie powoduje niewiele objawów nie-
po˝àdanych. Tym samym przekonali-
Êmy si´, ˝e nawet jeÊli antygen wyst´-
puje na zdrowych komórkach, mo˝e
w pewnych okolicznoÊciach zostaç wy-
korzystany jako obiekt immunoterapii.
Podobnie jak w wi´kszoÊci doÊwiad-
czalnych metod leczenia nowotworów
terapii przeciwcia∏ami w pierwszej kolej-
noÊci poddawani sà chorzy z zaawan-
sowanà postacià choroby. Ale bywa ona
znacznie skuteczniejsza, gdy podejmuje
si´ jà wczeÊniej. Gert Riethmüller z Uni-
wersytetu w Monachium bada∏ efekt
dzia∏ania przeciwcia∏a monoklonalnego
zwanego 17.1A u chorych we wczesnym
(miejscowym) stadium raka jelita gru-
bego. Leczenie przeciwcia∏ami rozpo-
cz´to natychmiast po usuni´ciu wykry-
tego guza. Pomimo zabiegu opera-
cyjnego wielu pacjentom zagra˝a nawrót
spowodowany przez pozostawione ko-
mórki nowotworowe. Jednak˝e w bada-
niach prowadzonych przez Riethmüllera
wÊród chorych otrzymujàcych przeciw-
cia∏o odnotowano znacznie ni˝szy wskaê-
nik nawrotu choroby. Leczenie komórek
nowotworowych, które nie zosta∏y usu-
ni´te w czasie zabiegu lub zacz´∏y roz-
przestrzeniaç si´ w innych narzàdach, jest
wysoce zasadne i b´dzie to jeden z
g∏ównych celów przysz∏ej immunoterapii.
W opisanych powy˝ej metodach le-
czenia przeciwcia∏a pochodzi∏y od zwie-
rzàt; w przysz∏oÊci byç mo˝e b´dà otrzy-
mywane in vitro. Ten sposób okreÊla si´
mianem biernej immunoterapii: chory
otrzymuje czàsteczki uk∏adu odporno-
Êciowego, których sam nie wytwarza.
112 Â
WIAT
N
AUKI
Listopad 1996
TERAPIE JUTRA
Ârodki niszczàce nowotwory
przenoszone przez przeciwcia∏a
P
rzeciwcia∏a wià˝à antygeny na powierzchni komórek nowotworowych. W ten spo-
sób zaznaczajà nieprawid∏owe komórki do zniszczenia przez inne sk∏adowe uk∏a-
du odpornoÊciowego lub wywo∏ujà w nich proces autodestrukcji. Podobnie mogà dzia-
∏aç na naczynia krwionoÊne od˝ywiajàce nowotwór lub tkank´ ∏àcznà podÊcieliska.
Przeciwcia∏a potrafià neutralizowaç czy hamowaç dzia∏anie czynników wzrostowych
– substancji koniecznych do jego wzrostu. Oprócz tego mogà s∏u˝yç jako samona-
prowadzajàce si´ pociski, dostarczajàc wiele toksycznych substancji (niektóre wymie-
niono poni˝ej) bezpoÊrednio do nowotworu.
RADIOAKTYWNE IZOTOPY, takie jak jod 131 czy itr 99, za-
bijajà komórki nowotworowe, uszkadzajàc ich DNA.
TOKSYNY mogà byç dostarczone do nowotworu przez prze-
ciwcia∏a. W badaniach cz´sto stosowana jest rycyna otrzy-
mywana z nasion ràcznika, która hamuje syntez´ bia∏ek i po-
wstrzymuje rozwój nowotworów. Tak˝e pewne sk∏adniki
bakterii i innych drobnoustrojów blokujà wzrost komórek no-
wotworowych w hodowli. Dzi´ki przeciwcia∏om mo˝na b´-
dzie prawdopodobnie doprowadzaç do guza wiele innych
zwiàzków o silnym dzia∏aniu przeciwnowotworowym, na przy-
k∏ad CC-1065, kalichamycyn´, majtanosinoidy (mayta-
nosinoids), zbyt toksycznych, by obecnie stosowaç je w
chemioterapii.
ÂRODKI CHEMIOTERAPEUTYCZNE cz´sto docierajà do
guza w wi´kszych, bardziej toksycznych dawkach, jeÊli sà
dostarczone przez przeciwcia∏a.
ENZYMY zmieniajàce nieszkodliwe pre-
kursory leków w ich zabójcze dla komó-
rek pochodne mogà dostaç si´ do nowo-
tworu, gdy zostanà przy∏àczone do prze-
ciwcia∏. Poniewa˝ zadzia∏ajà wy∏àcznie
w obr´bie guza, zdrowe tkanki organizmu
nie zostanà uszkodzone.
LEKI GENETYCZNE wyst´pujà w wielu
postaciach. Tzw. antysensowne czàsteczki DNA blokujà wy-
twarzanie bia∏ek potrzebnych komórkom nowotworowym. In-
ne sztucznie skonstruowane geny kodujà bia∏ka zabijajàce
komórki guza; mo˝na je bezpoÊrednio po∏àczyç z przeciw-
cia∏ami lub upakowaç w czàstkach wirusów wyposa˝onych
w naprowadzajàce przeciwcia∏o na swojej powierzchni.
CZÑSTECZKI ODCZYNU ZAPALNEGO (czynnik martwicy
nowotworu – TNF) i inne bia∏kowe przekaêniki uk∏adu od-
pornoÊciowego, jak równie˝ pewne sk∏adniki drobnoustrojów
mogà wywo∏aç odczyn zapalny, który zniszczy tkanki w obr´-
bie guza nowotworowego.
KOMÓRKI UK¸ADU ODPORNOÂCIOWEGO
kierowane przez przeciwcia∏a, na przyk∏ad lim-
focyty T przetworzone metodami in˝ynierii
genetycznej, mogà spowodowaç rozpad ko-
mórek nowotworowych.
JENNIFER C. CHRISTIANSEN

Natomiast szczepionki uwa˝a si´ za
czynnà immunoterapi´, poniewa˝ u
osoby, która ulega chorobie, wywo∏ujà
obronnà odpowiedê odpornoÊciowà.
Obiecujàce szczepionki
Próby leczenia nowotworów za po-
mocà szczepionek si´gajà poczàtków
immunologii. Przez lata lekarze szczepi-
li setki chorych napromieniowanymi
komórkami nowotworowymi –
pobranymi od nich samych, ale
tak˝e od innych pacjentów – aby
zapobiec odradzaniu si´ guza.
Chocia˝ czasami przynosi∏o to
efekty, wczesne próby ze szcze-
pionkami mia∏y wiele wad. Do naj-
bardziej znaczàcych nale˝a∏a nie-
mo˝noÊç oceny wp∏ywu szcze-
pionki na uk∏ad odpornoÊciowy.
Po opracowaniu szczepionek prze-
ciwko chorobom zakaênym, na
przyk∏ad chorobie Heinego-Medi-
na (polio), ich dzia∏anie mo˝na by∏o ∏a-
two Êledziç, szukajàc wywo∏anych ni-
mi swoistych przeciwcia∏. Lecz do
niedawna uczeni nie dysponowali od-
powiednià wiedzà o antygenach nowo-
tworowych i wywo∏ywanej przez nie
odpowiedzi immunologicznej. Nie mo-
gli wi´c zrozumieç, dlaczego leczenie
pomaga∏o tylko niektórym chorym. Sta-
∏y post´p badaƒ w ostatnich dziesi´cio-
leciach doprowadzi∏ do tego, ˝e prace
nad nowymi szczepionkami przeciw-
nowotworowymi mo˝na ju˝ oprzeç na
solidnych podstawach naukowych.
Wspó∏czesna historia tych szczepio-
nek rozpocz´∏a si´ w latach czterdzie-
stych i pi´çdziesiàtych wraz z podsta-
wowym odkryciem w dziedzinie im-
munologii nowotworów. Stwierdzono
wówczas, ˝e w guzach wywo∏anych u
myszy zwiàzkami chemicznymi lub wi-
rusami znajdujà si´ antygeny, którymi
mo˝na uodporniç myszy tej samej rasy
na przeszczep komórek guza. W kolej-
nych badaniach wykazano, ˝e komórki
uk∏adu odpornoÊciowego zwane limfo-
cytami T pochodzàce od immunizowa-
nego zwierz´cia potrafià przenieÊç ta-
kà odpornoÊç na zdrowe myszy tej sa-
mej rasy. Opracowano te˝ metod´, któ-
ra wykaza∏a, ˝e limfocyty T immunizo-
wanej myszy potrafi∏y zabijaç równie˝
komórki nowotworowe rosnàce w ho-
dowli. Natomiast przeciwcia∏a wywo-
∏ywane komórkami nowotworowymi
z regu∏y tych zdolnoÊci nie posiada∏y.
ChcieliÊmy sprawdziç, czy podobna
reakcja immunologiczna mog∏aby zajÊç
u ludzi. Wzgl´dy etyczne i praktyczne
uniemo˝liwia∏y nam pos∏u˝enie si´ me-
todami stosowanymi w badaniach na
zwierz´tach. Dlatego prace skoncentro-
wa∏y si´ na tych reakcjach immunolo-
gicznych, które mo˝na dok∏adnie badaç
w hodowlach komórkowych. Nasz ze-
spó∏ wybra∏ komórki czerniaka (raka
skóry), tak˝e z tego powodu, ˝e mo˝na
je ∏atwo hodowaç w laboratorium. Przez
10 lat przebadaliÊmy olbrzymià liczb´
pacjentów z czerniakiem, poszukujàc
przeciwcia∏ czy limfocytów T u tych,
którzy reagowali na w∏asne komórki
czerniaka. StwierdziliÊmy, ˝e niewiel-
ka grupa chorych rzeczywiÊcie rozwija
odpowiedê immunologicznà przeciw-
ko w∏asnym komórkom nowotworo-
wym. OdnieÊliÊmy równie˝ wra˝enie,
˝e wià˝e si´ to z bardziej ∏agodnym
przebiegiem choroby.
Kolejnym zadaniem by∏o wyizolowa-
nie tych antygenów do zastosowania
w szczepionce. Thierry Boon i jego
wspó∏pracownicy z Instytutu Badaƒ nad
Rakiem im. Ludwiga w Brukseli opraco-
wali metod´ [patrz: Thierry Boon, „Im-
munoterapia nowotworów z∏oÊliwych”;
Âwiat Nauki, maj 1993], która wykaza∏a,
˝e u chorych z czerniakiem istniejà dwa
rodzaje antygenów wywo∏ujàcych od-
powiedê limfocytów T i umo˝liwi∏a ich
uzyskiwanie w du˝ych iloÊciach. Do
pierwszego rodzaju nale˝à antygeny
zwane MAGE, BAGE i GAGE, produ-
kowane wy∏àcznie przez ten nowotwór
oraz komórki jàdra. Drugi – to tzw. an-
tygeny ró˝nicowania, takie jak tyrozyna-
za, Melan A, wyst´pujàce zarówno na
komórkach czerniaka, jak i na melano-
cytach, czyli komórkach skóry, z któ-
rych on si´ wywodzi.
Limfocyty T „nie widzà” ca∏ej bia∏ko-
wej struktury antygenu na powierzchni
komórki nowotworowej, lecz tylko jego
fragmenty zwane peptydami. Kiedy ko-
mórki nowotworu przetwarzajà anty-
gen, prezentujà go na powierzchni
komórki w po∏àczeniu z tzw. antygena-
mi zgodnoÊci tkankowej. Naukowcy
dysponujà rosnàcà listà bia∏ek i pepty-
dów antygenów nowotworowych izo-
lowanych za pomocà wprowadzonej
przez Boona i jego zespó∏ metody klono-
wania antygenów nowotworowych.
Wszystkie te czàsteczki sà g∏ównymi
kandydatami do zastosowania w szcze-
pionkach. Jeszcze nowsze metody dajà
nadziej´ poszerzenia tej listy.
Kolejnym êród∏em informacji o po-
tencjalnych antygenach nowotworo-
wych jest lawina nowych odkryç doty-
czàcych zmian genetycznych w ko-
mórkach raka. Ka˝da zmiana w komór-
ce nowotworowej, która mo˝e byç wy-
kryta przez uk∏ad odpornoÊciowy, sta-
nowi wod´ na m∏yn immunologów. Do
najbardziej atrakcyjnych obiektów na-
le˝à nieprawid∏owe bia∏ka wytwarza-
ne wtedy, gdy ich geny na skutek mu-
tacji przejdà w odmiany u∏atwiajàce
rozwój nowotworów. Obecnie powstaje
d∏uga lista genów zwiàzanych z nowo-
tworzeniem, zwanych onkogenami i ge-
nami supresorami hamujàcymi wzrost
nowotworów [patrz: Robert A. Wein-
berg, „Jak powstaje rak?”, strona 32].
G∏ównym obiektem terapii za pomocà
szczepionek stanà si´ ludzkie nowotwo-
ry wywo∏ane przez wirusy, na przyk∏ad
rak szyjki macicy.
Podobnie jak w przypadku przeciw-
cia∏ monoklonalnych obecnie opra-
cowano wi´cej metod immunoterapii
szczepionkami ani˝eli mo˝na prze-
testowaç na chorych. Chocia˝ olbrzy-
mie doÊwiadczenie ze szczepionkami
przeciwko chorobom zakaênym powin-
no ukierunkowaç prace nad szczepion-
kami przeciwnowotworowymi, to jed-
nak znaczne obszary wiedzy pozostajà
nadal nie odkryte. Szczepionki, zawie-
rajàce ca∏e komórki nowotworowe (cza-
sami zmienione metodami in˝ynierii
Â
WIAT
N
AUKI
Listopad 1996 113
TESTY SKÓRNE dajà mo˝liwoÊç stwierdzenia, czy uk∏ad odpornoÊciowy chorego rozpo-
znaje antygeny peptydowe obecne na komórkach nowotworu. JeÊli tak, na skórze pacjen-
ta pojawia si´ podra˝nienie, tzw. odczyn opóênionej nadwra˝liwoÊci. Poczàtkowy odczyn
u chorego z czerniakiem
(z lewej) staje si´ bardziej nasilony po wstrzykni´ciu cytokiny
(GM-CSF) pobudzajàcej uk∏ad odpornoÊciowy
(z prawej). Powy˝szy test przypomina pró-
b´ tuberkulinowà wykonywanà po szczepieniu przeciwko gruêlicy.
Za zgodà ALEXANDRA KNUTHA,
Szpital Pó∏nocny Frankfurt
genetycznej), prawdopodobnie zostanà
zastàpione szczepionkami zawierajà-
cymi okreÊlone antygeny nowotworo-
we. Ponadto poniewa˝ szczepionki pep-
tydowe ∏atwo zsyntetyzowaç, stanà si´
one g∏ównym przedmiotem badaƒ kli-
nicznych. Z pierwszych prób wynika,
˝e mogà powodowaç zmniejszenie
masy guza. Niektórzy immunolodzy
przypuszczajà, ˝e bardziej skuteczne ja-
ko szczepionki b´dà jednak ca∏e czà-
steczki bia∏ek, poniewa˝ stymulujà one
uk∏ad odpornoÊciowy bardzo wieloma
ró˝nymi peptydami. Naukowcy nie-
cierpliwie czekajà na wytworzenie w
du˝ych iloÊciach oczyszczonych anty-
genów nowotworowych, takich jak
MAGE, Melan A, tyrozynaza, aby po-
twierdziç t´ hipotez´.
Obecnie rozwa˝a si´ jeszcze inne po-
dejÊcie lecznicze. Tzw. immunoterapia
adoptywna polega na pobudzeniu lim-
focytów T przez kontakt z antygenami
lub komórkami nowotworowymi w la-
boratorium, a nast´pnie namno˝eniu
ich i podaniu choremu. Inaczej ni˝
w przypadku wsobnych (identycznych
genetycznie) ras myszy, kiedy limfocy-
ty T mogà byç podane ka˝demu osobni-
kowi, limfocyty T pochodzàce od jed-
nego cz∏owieka zwykle sà przez inne-
go odrzucane. Z tego powodu chory
musi byç zarówno dawcà, jak i biorcà
w∏asnych limfocytów T. Pierwsze testy
kliniczne tej metody prowadzi∏ Steven
A. Rosenberg z National Cancer Insti-
tute; nie ustajà wysi∏ki, aby uczyniç jà
bardziej skutecznym, mniej czasoch∏on-
nym i kosztownym sposobem leczenia.
Immunoterapia adoptywna mo˝e oka-
zaç si´ najbardziej pomocna w leczeniu
zaka˝eƒ wirusowych i nowotworów
114 Â
WIAT
N
AUKI
Listopad 1996
TERAPIE JUTRA
Rodzaje szczepionek przeciwnowotworowych
Zadaniem tych szczepionek jest pobudzenie limfocytów T i innych sk∏adowych uk∏adu odpornoÊciowego do rozpoznawania i gwa∏tow-
nego atakowania tkanek nowotworowych.
Ca∏e komórki
Odpowiedê immunologicznà mogà uruchomiç zinaktywowane komórki nowotworowe oraz ich ekstrakty.
nowotworowe
Komórki nowotworowe zmuszone metodà in˝ynierii genetycznej do wydzielania cytokin, na przyk∏ad
IL-2 czy GM-CSF, wzmacniajà si∏´ odpowiedzi przeciwnowotworowej. Te, które w wyniku tych
procedur wykazujà na swej powierzchni czàsteczki dostarczajàce dodatkowy sygna∏ stymulujàcy –
na przyk∏ad bia∏ko B7 – zwi´kszajà zdolnoÊç limfocytów T do rozpoznawania komórek nowotworowych.
Peptydy
Peptydy nowotworowe, czyli fragmenty bia∏ek guza rozpoznawane przez limfocyty T, wstrzykuje si´
osobno lub wraz z pobudzajàcymi odpowiedê immunologicznà adiuwantami.
Bia∏ka
Komórki prezentujàce antygen wychwytujà podane bia∏ka nowotworowe i rozk∏adajà je na ró˝ne
fragmenty peptydowe rozpoznawane przez limfocyty T.
Komórki dendrytyczn
e
Ten rodzaj komórek prezentujàcych antygen po izolacji z krwi pacjenta inkubuje si´ z peptydami
nowotworowymi lub zmusza metodami in˝ynierii genetycznej do wytwarzania bia∏ek nowotworowych,
a nast´pnie ponownie wprowadza do organizmu chorego.
Gangliozydy
Organizm ludzki potrafi wytwarzaç przeciwcia∏a przeciwko czàsteczkom takim jak GM2, które znajdujà
si´ na powierzchni komórek nowotworowych. Badania kliniczne dowiod∏y, ˝e wyst´powanie
u pacjentów z czerniakiem przeciwcia∏ anty-GM2 wià˝e si´ z lepszym rokowaniem.
Bia∏ka szoku termicznego
Te obecne w komórce bia∏ka wià˝à peptydy. Podanie bia∏ek szoku termicznego wyizolowanych
z tkanki guza wywo∏uje odpornoÊç na nowotwór u myszy.
Wektory bakteryjne
Geny kodujàce antygeny nowotworowe wstawia si´ do materia∏u genetycznego wirusów lub bakterii.
i wirusow
e
W organizmie chorego takie drobnoustroje wywo∏ujà odpornoÊç na antygeny w∏asne
i nowotworowe.
Kwasy nukleinowe
DNA lub RNA kodujàce antygeny nowotworowe sk∏aniajà prawid∏owe komórki do ich produkcji.
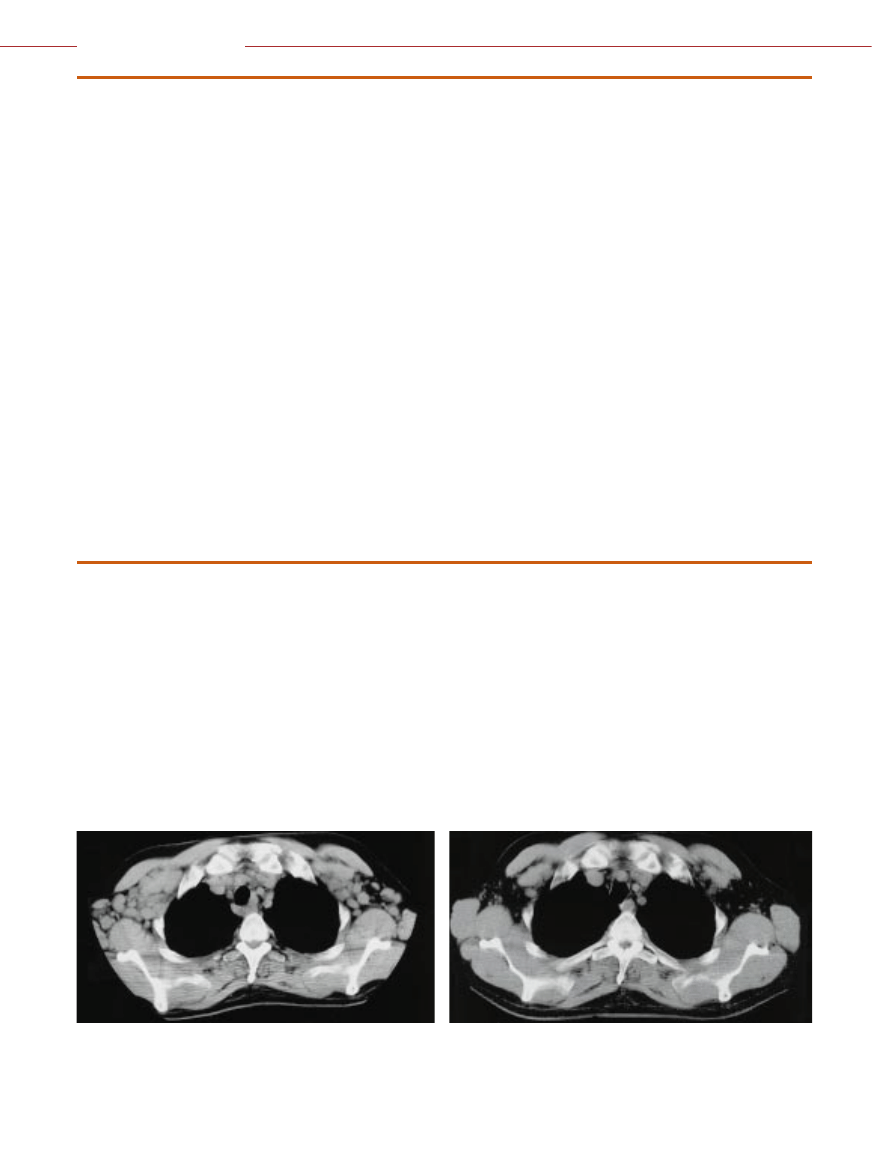
OBRAZ Z TOMOGRAFU KOMPUTEROWEGO pokazuje poprzeczny przekrój górnej cz´Êci tu∏owia 41-letniego m´˝czyzny przed i po
leczeniu ch∏oniaka przeciwcia∏em anty-CD20 sprz´˝onym z radioizotopem (dwa czarne ko∏a to p∏uca). Pomimo wczeÊniejszej chemio-
terapii choroba post´powa∏a, co przejawia∏o si´ du˝à liczbà powi´kszonych w´z∏ów ch∏onnych
(z lewej). Po podaniu pojedynczej daw-
ki przeciwcia∏a anty-CD20 wszystkie objawy ustàpi∏y. Po up∏ywie dwóch lat chory pozostaje nadal w stanie ca∏kowitej remisji
(z prawej).
MARK S. KAMINSKI
University of Michigan

u pacjentów, których uk∏ad odpornoÊcio-
wy zosta∏ os∏abiony przez leki lub wczeÊ-
niejsze choroby. Na przyk∏ad chory na
bia∏aczk´ jest poddawany przed prze-
szczepieniem szpiku chemioterapii i na-
promienianiu, czyli leczeniu immunosu-
presyjnemu w celu zniszczenia wszyst-
kich komórek nowotworowych, co czyni
go niezwykle podatnym na zaka˝enia,
na przyk∏ad wirusem cytomegalii (CMV).
Wykazano jednak, ˝e podanie swoistych
dla CMV limfocytów T zmniejsza ryzyko
zaka˝enia tym wirusem u biorcy prze-
szczepu szpiku. Ponadto wstrzykujàc pa-
cjentowi limfocyty od zdrowego dawcy,
mo˝na uzyskaç remisj´ ch∏oniaków wy-
wo∏anych przez wirusy. Dzi´ki podawa-
niu leków immunosupresyjnych limfo-
cyty nie sà odrzucane i zwalczajà komórki
tego nowotworu.
Zadania na przysz∏oÊç
Pomimo ogromnych nadziei wiàza-
nych z immunoterapià wiele jeszcze
przeszkód dzieli nas od kontrolowania
raka za pomocà uk∏adu odpornoÊcio-
wego. Komórki nowotworowe sà mi-
strzami w oszukiwaniu i udawaniu; jak
magicy b∏yskawicznie zmieniajà swà
postaç, aby uniknàç rozpoznania i ata-
ku [ramka z prawej].
Ze wzgl´du na sta∏à huÊtawk´ mi´-
dzy nadzorem immunologicznym a
ucieczkà spod niego najlepsze strategie
zwalczania raka b´dà polegaç na jedno-
czesnym atakowaniu go ze wszystkich
stron. Rozwa˝a si´ nast´pujàce mo˝li-
woÊci: skonstruowanie szczepionek za-
wierajàcych ró˝norodne antygeny (tzw.
szczepionek wielowa˝nych, poliwalent-
nych); sprawdzenie, czy immunotera-
pie z zastosowaniem szczepionek i prze-
ciwcia∏ wspó∏dzia∏ajà ze sobà, oraz ∏à-
czenie immunoterapii swoistej i nieswo-
istej z innymi metodami leczenia.
Trzeba b´dzie rozwiàzaç wiele innych
problemów. Wydaje si´, ˝e szczepion-
ki przeciwnowotworowe, podobnie jak
wspomniane wczeÊniej przeciwcia∏a,
mogà w pewnym stopniu uszkodziç ko-
mórki prawid∏owe. Jest liczna grupa
chorób, tzw. choroby z autoagresji, po-
wstajàcych wówczas, gdy uk∏ad odpor-
noÊciowy zwraca si´ przeciwko zdro-
wym tkankom organizmu. To na przy-
k∏ad reumatoidalne zapalenie stawów,
stwardnienie rozsiane i niektóre choro-
by nerek. Byç mo˝e pewien stopieƒ
uczulenia na w∏asne tkanki b´dzie ce-
nà, którà zap∏acimy za skutecznà szcze-
pionk´ przeciwnowotworowà.
Patrzàc na d∏ugoletnià histori´ badaƒ
nad immunologià nowotworów – na-
przemiennych okresów wielkich nadziei
i rozczarowaƒ – nale˝y zachowaç ostro˝-
noÊç w stawianiu prognoz. Wiele obie-
cujàcych metod jednak czeka na spraw-
dzenie, co pozwala wierzyç, ˝e skutecz-
na immunoterapia stanie si´ kiedyÊ rze-
czywistoÊcià. Byç mo˝e te nowe metody
umo˝liwià wyleczenie raka, co jest ce-
lem wszystkich badaczy, pracowników
s∏u˝by zdrowia i oczywiÊcie chorych.
Bardziej realne wydaje si´ opracowanie
terapii zmieniajàcych charakter choro-
by nowotworowej – z post´pujàcej i
Êmiertelnej w takà, którà b´dzie mo˝na
kontrolowaç w ciàgu ca∏ego d∏ugiego
˝ycia pacjenta.
Takie rozwiàzanie, choç wydaje si´
doÊç dalekie od idea∏u, mia∏oby olbrzy-
mie znaczenie dla wielu chorych, któ-
rych obecnie trudno wyleczyç.
T∏umaczy∏
Zbigniew Gaciong
Â
WIAT
N
AUKI
Listopad 1996 115
Jak nowotwór unika rozpoznania
przez uk∏ad odpornoÊciowy
Zmiana cech
Na skutek presji uk∏adu odpornoÊciowego komórki nowotworowe wytwarzajà klony
pozbawione cech umo˝liwiajàcych zniszczenie ich przez limfocyty T, inne komórki cy-
totoksyczne i przeciwcia∏a. Proces ten nosi nazw´ immunoselekcji i dzi´ki niemu po-
wstajà komórki nowotworowe pozbawione swoistych antygenów lub czàsteczek zgod-
noÊci tkankowej prezentujàcych antygeny nowotworowe limfocytom. Komórki no-
wotworowe mogà wtedy równie˝ utraciç tzw. czàsteczki kostymulujàce, pobudzajàce
limfocyty T oraz czàsteczki sygna∏owe potrzebne do reagowania na cytokiny (np.
interferon gamma), u∏atwiajàce ich zabijanie.
Supresja odpowiedzi immunologicznej
Komórki nowotworowe potrafià wywo∏ywaç zmiany w organizmie gospodarza, które
os∏abiajà lub znoszà odpowiedê immunologicznà przeciwko nim. Immunosupresja swo-
ista wyst´puje, jeÊli komórki nowotworowe przekazujà wadliwe lub nieskuteczne sy-
gna∏y do limfocytów T, zmniejszajàc ich liczb´ lub zdolnoÊç do odpowiedzi. Natomiast
stan nieswoistego zahamowania odpowiedzi immunologicznej spowodowany jest przez
inne produkty nowotworów (np. TGF-beta), leki przeciwnowotworowe lub radioterapi´.
Ukrywanie si´ przed uk∏adem odpornoÊciowym
Odpowiedê immunologiczna nie wyst´puje wcale lub jest mniej skuteczna w niektórych
narzàdach, na przyk∏ad w mózgu, dlatego guzy tam zlokalizowane unikajà ataku.
Przed rozpoznaniem i zniszczeniem przez uk∏ad odpornoÊciowy os∏ania nowotwór
równie˝ zbita warstwa podÊcieliska guza zbudowana z tkanki ∏àcznej.
Wykorzystanie ignorancji uk∏adu odpornoÊciowego
Wzrost komórek nowotworowych przebiega zwykle bez wywo∏ywania jakiejkolwiek od-
powiedzi immunologicznej. Mo˝na jà jednak spowodowaç, uczulajàc organizm antyge-
nami guza, co Êwiadczy o nie wykorzystanych mo˝liwoÊciach uk∏adu odpornoÊciowego.
Wyprzedzanie uk∏adu odpornoÊciowego
Komórki nowotworowe sà zdolne dzieliç si´ tak szybko, ˝e odpowiedê immunologicz-
na nie zdà˝y si´ rozwinàç i kontrolowaç tempa ich wzrostu.
Informacje o autorze
LLOYD J. OLD otrzyma∏ stopieƒ doktora medy-
cyny w 1958 roku w University of California
w San Francisco. Nast´pnie przeniós∏ si´ do Memo-
rial Sloan-Kettering Institute for Cancer Research,
gdzie w latach 1973–1983 pe∏ni∏ funkcj´ jednego
z kierowników naukowych. Old jest obecnie dyrek-
torem naukowym i administracyjnym Ludwig
Institute for Cancer Research w Nowym Jorku. Po-
wy˝szy artyku∏ to czwarta jego publikacja w Scien-
tific American.
Literatura uzupe∏niajàca
TUMOR ANTIGENS RECOGNIZED BY T LYMPHOCYTES
. T. Boon i in., Annual Reviev of Immuno-
logy. Red. W. E. Paul, C. G. Fathman i H. Metzger, vol. 12, ss. 337-366, 1994.
HUMAN NEOPLASMS ELICIT MULTIPLE SPECIFIC IMMUNE RESPONSES IN THE AUTOLOGOUS HOST
.
U. Sahin i in., Proceedings of the National Academy of Sciences USA, vol. 92, nr 25,
ss. 11 810-11 813, 5 XII 1995.
BIOLOGIC THERAPY OF CANCER
. Red. V. T. DeVita, Jr., i in.; Lippincott-Raven, 1994.
MONOCLONAL ANTIBODIES
. J. P. Mach, Oxford Textbook of Oncology, vol. 1. Red. J. Peckham,
M. Pinedo i U. Veronesi; Oxford University Press, 1995.
CANCER THERAPY WITH RADIOLABELED ANTIBODIES.
Red. David M. Goldenberg;
CRC Press, 1995.
Wyszukiwarka
Podobne podstrony:
Immunologia nowotworów
Immunologia Nowotworów
Immunoterapia nowotworów
immunologia nowotworow
Immunologia nowotworow ok, Immunologia
immunologia nowotworów
Immunoterapia nowotworów (moja)
IMMUNOLOGIA NOWOTWORÓW
Immunohistochemia nowotworów
Immunologia nowotworów
Immunologia Nowotworów
Immunologia nowotworoTŽ w, niedobory odpornosTŽ ci, psychoneuroimmunologia
Immunologia Nowotworów
Immunoterapia nowotworów
immunologia nowotworow
więcej podobnych podstron