
Ć
WICZENIE 7
Małgorzata Płonka
, grupa poniedziałek 8
15
Znaczenie centralnego atomu metalu pierścienia porfirynowego
cząsteczki chlorofilu.
W reakcjach fotochemicznych energia dostarczana jest spoza układu w postaci energii świetlnej.
Zależnie od reakcji, tylko światło o określonej długości fali uczestniczy w zamianie energii
ś
wietlnej na energię swobodną reagujących cząsteczek. Tylko substancje absorbujące światło
o określonej długości fali mogą ulegać przekształceniom fotochemicznym. Układy reakcji
aktywowane przez światło widzialne muszą zawierać barwnik absorbujący to światło. Jeśli światło
jest absorbowane tylko przez jeden składnik układu, to kształt krzywej obrazującej widmo
czynnościowe odpowiada krzywej absorpcji światła wyznaczonej dla tego składnika. Jeśli
w układzie fotochemicznym światło aktywuje kilka składników, to widmo czynnościowe reakcji
jest wynikiem nakładania się na siebie kilku krzywych absorpcji.
Podobnie jak dla prostych reakcji fotochemicznych, również dla reakcji fotobiologicznych można
wyznaczyć widmo czynnościowe i określić receptor promieniowania świetlnego. Podstawowym
receptorem światła aktywnego w procesie fotosyntezy jest barwnik chlorofil, nadający roślinom
zieloną barwę. Absorbuje on światło w zakresie widzialnym, a jego główne pasma pochłaniania
znajdują się w zakresie niebieskiej i czerwonej części widma absorpcji. Istnieje wiele odmian
chlorofilu, oznaczonych kolejnymi literami alfabetu. Różnice strukturalne występujące pomiędzy
poszczególnymi odmianami chlorofilu powodują istnienie pewnych różnic w ich widmach
absorpcyjnych. Wszystkie organizmy fotosyntetyzujące, które produkują tlen, zawierają chlorofil a.
Cząsteczka chlorofilu zbudowana jest z 5-pierścieniowej pochodnej porfiryny, zwanej feoporfiryną,
oraz reszty 20-węglowego alkoholu - fitolu, dołączonej wiązaniem estrowym do reszty kwasu
propionowego, która jest jednym z podstawników IV pierścienia pirolowego feoporfiryny.
Fragmenty czterech połączonych pierścieni pirolowych oraz dodatkowego pierścienia
niepirolowego tworzą układ następujących po sobie kolejno wiązań pojedynczych i podwójnych
(układ wiązań sprzężonych), który charakteryzuje się zdolnością absorpcji promieniowania
ś
wietlnego. Centralne miejsce w pierścieniu porfirynowym zajmuje atom magnezu, połączony
z atomami azotu pierścieni pirolowych. Przyjmuje się, że magnez pełni istotną rolę w agregacji
cząsteczek chlorofilu.
Absorpcja kwantu promieniowania przez cząsteczkę fotoreceptora powoduje, że energia swobodna
tej cząsteczki zwiększa się o porcję energii tego kwantu. To zwiększenie energii swobodnej
1

nazywane jest wzbudzeniem cząsteczki. Związek ten w stanie wzbudzenia jest mniej trwały, łatwiej
wchodzi w reakcje chemiczne, a ponadto zawiera znaczny nadmiar energii swobodnej w stosunku
do związku niewzbudzonego, co zmienia stosunki energetyczne i równowagę reakcji. Jeżeli brak
jest możliwości wykorzystania energii wzbudzenia przez układ, to jest ona uwalniana w postaci
ciepła lub jako wtórne promieniowanie świetlne (fluorescencja - uwalnianie w momencie
naświetlenia lub fosforescencja - uwalnianie przez pewien czas od naświetlenia; w obu tych
przypadkach długość fali światła emitowanego jest większa, niż światła absorbowanego przez
receptor (ponieważ energia kwantu jest mniejsza).
Wykorzystanie energii promieniowania słonecznego w procesie fotosyntezy jest możliwe dzięki
absorpcji światła przez chlorofil. W niektórych sytuacjach fizjologicznych (np. w chloroplastach,
w których łańcuch przenoszenia elektronów jest wysycony) część energii stanu wzbudzenia może
być emitowana w postaci ciepła lub jako czerwone promieniowanie fluorescencyjne. Zgodnie
z regułą Stockesa, maksimum widma emisji przesunięte jest w kierunku fal dłuższych w stosunku
do maksimum absorpcji danego barwnika.
Chlorofile należą do jednych z najmniej stabilnych barwników roślinnych - wysoka temperatura,
ś
wiatło lub działanie rozpuszczalnikami znacząco przyspiesza rozpad cząsteczki; bardzo łatwo
ulegają też rozpadowi pod wpływem kwasów oraz zasad, dając odpowiednio chlorofilidy
(cząsteczki pozbawione fitolu) oraz feofityny (cząsteczki, w których jon magnezu został
wymieniony na dwa jony wodorowe). Jony magnezu w cząsteczce chlorofilu można także łatwo
podstawić jonami innych metali dwuwartościowych, co najczęściej prowadzi do zmiany barwy,
zwiększenia stabilności cząsteczki oraz zmniejszenia jej aktywności biologicznej (zjawisko stresu
ś
rodowiskowego).
Celem ćwiczenia jest określenie swoistej roli magnezu w budowie i funkcjonowaniu chlorofilu.
1. Przygotowanie ekstraktu barwników.
Rozdrobnione liście przenieść do moździerza, dodać 100% acetonu i dobrze rozetrzeć. Przesączyć.
2. Otrzymywanie feofityny.
Do przesączu mieszanego na mieszadle magnetycznym dodać 2N roztworu HCl.
Spektrofotometrycznie określić stężenie otrzymanej feofityny.
C
feo
=22,42⋅A
665
6,81⋅A
653
[
µ
g
ml
] , gdzie:
A
665
, A
653
- wartości absorbancji przy odpowiedniej długości fali
2
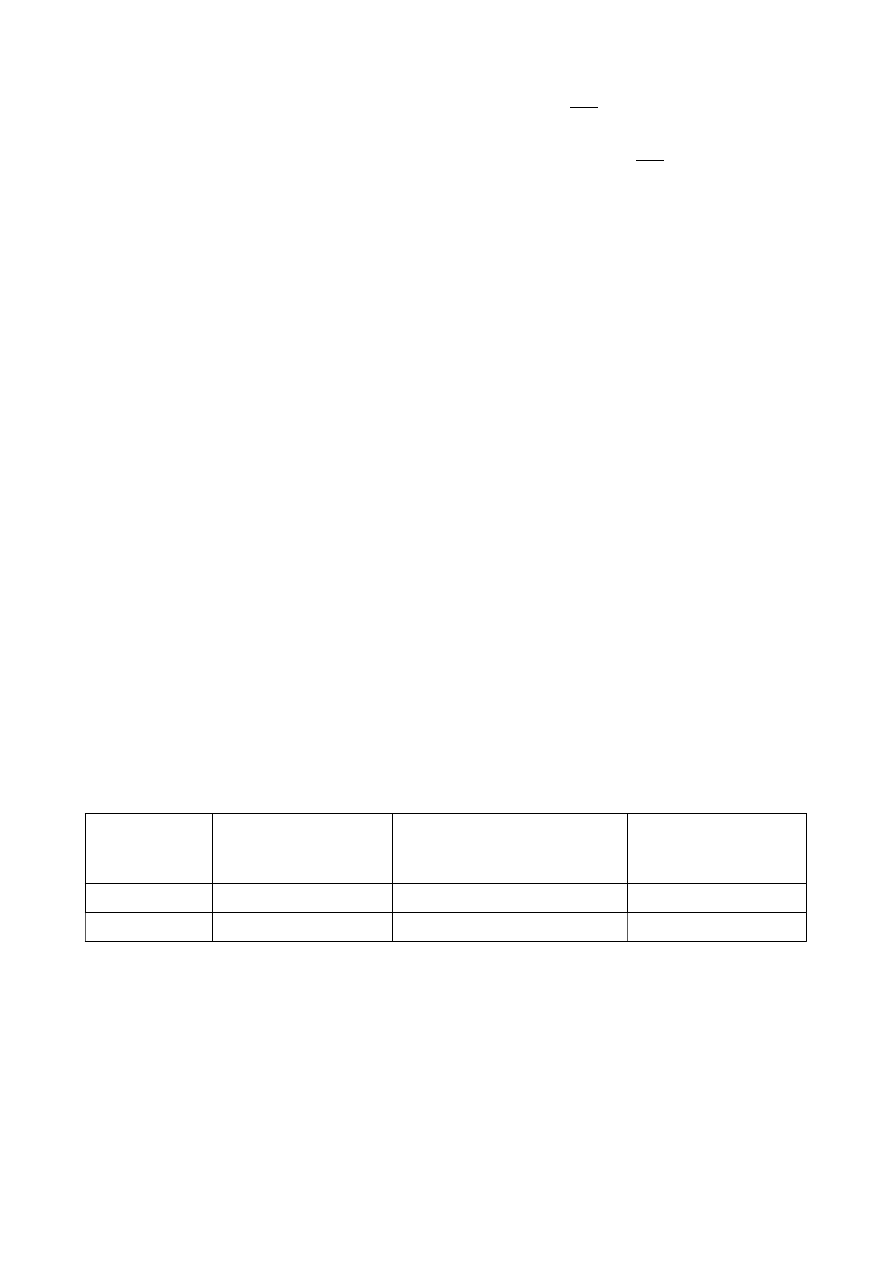
C
feo
=22,42⋅0,21 6,81⋅0,127=3,84[
µ
g
ml
] dla rozcieńczenia 10x
stężenie feofityny w otrzymanej próbce: 38,4 [
µ
g
ml
]
3. Otrzymywanie Cu-porfiryn.
Do zlewki z brunatnym roztworem feofityny dodawać kroplami 0,2 M CuSO
4
do ponownego
uzyskania zielonej barwy (podstawienie atomu miedzi w miejsce centrum pierścienia
porfirynowego feofityny). Przesączyć.
4. Rozdział barwników - chromatografia cienkowarstwowa.
Przesącz Cu-porfiryny rozdzielić w rozdzielaczu z dodatkiem benzyny ekstrakcyjnej i wody
destylowanej - pobrać warstwę benzynową, nanieść na płytkę powleczoną żelem krzemionkowym.
Płytkę umieścić w kamerze zawierającej rozwijacz (100 benzyna : 10 izopropanol : 0,25 woda).
Rozwijacz podsiąkając do góry pociąga za sobą poszczególne barwniki w kolejności zależnej od ich
polarności.
5. Wykreślanie widm absorpcyjnych barwników.
Płytkę z rozdzielonymi barwnikami suszyć przez kilka minut z dala od źródeł światła. Pasma
Cu-chlorofilu a oraz Cu-chlorofilu b zdrapać i wsypać do oddzielnych suchych probówek. Do
każdej z nich dodać 100% acetonu. Przesączyć. Klarownych ekstraktów użyć do
spektrofotometrycznego wykreślania krzywych widm absorpcji barwników.
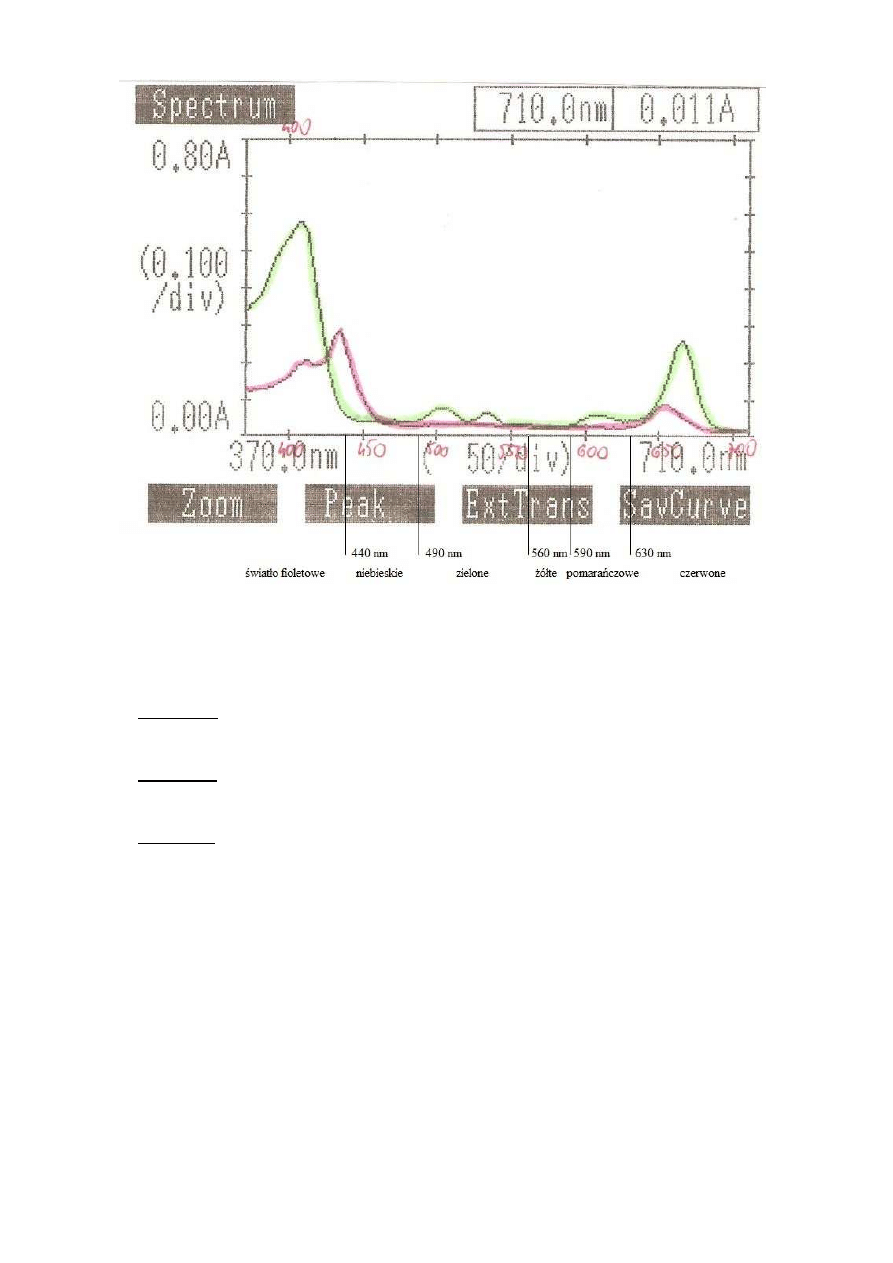
Wnioski:
barwnik
zakres długości
absorbowanej fali [nm]
barwa światła
maksimum dł. fali
absorbowanej przez
chlorofil
*
[nm]
Cu-chlorofil a
370 - 445; 650 - 690
fioletowa; czerwona
405; 665
Cu-chlorofil b
370 - 460; 640 - 680
fioletowoniebieska; czerwona
430; 655
*
odpowiednio: chlorofil a - dla Cu-chlorofilu a oraz chlorofil b - dla Cu-chlorofilu b
3
6. Obserwacja fluorescencji barwników roślinnych.
Trzy ekstrakty otrzymane na różnych etapach eksperymentu:
roztwór A - zielony; przesącz barwników otrzymany pod wpływem ucierania liści
z acetonem (chlorofil) - fluorescencja czerwona
roztwór B - brunatny; otrzymany poprzez działanie 2N roztworem HCl na przesącz
barwników (feofityna) - fluorescencja czerwona
roztwór C - zielony; otrzymany poprzez działanie 0,2 M roztworem CuSO
4
na roztwór
feofityny (Cu-porfiryna) - brak fluorescencji
należy obserwować pod lampą UV. Wyjaśnić obserwowane zjawisko.
Wnioski:
Fluorescencja jest to zjawisko uwalniania energii przez fotoreceptor w przypadku, gdy nie jest
możliwe wykorzystanie jej przez układ. Długość fali światła emitowanego jest większa, niż światła
absorbowanego przez receptor, dlatego - pomimo absorbowania przez chlorofil światła
fioletowoniebieskiego i czerwonego - w przypadku fluorescencji obserwujemy jedynie światło
czerwone. Nie jest możliwe zatem naświetlanie światłem czerwonym i obserwacja światła
4

zielonego. Roztwór Cu-chlorofilu nie wykazuje fluorescencji, ponieważ cząsteczka chlorofilu
z podstawionym atomem miedzi w miejsce atomu magnezu nie jest zdolna do pełnienia funkcji
biologicznej (nie absorbuje energii świetlnej, zatem nie jest w stanie jej emitować).
Literatura
1. Podstawy fizjologii roślin, pod red. Kopcewicz J., Lewak S., Wydawnictwo Naukowe PWN,
Warszawa, 1998
2. Skrypt do ćwiczeń z fizjologii roślin dla studentów III roku biologii
5
Wyszukiwarka
Podobne podstrony:
EŚT 07 Użytkowanie środków transportu
07 Windows
07 MOTYWACJAid 6731 ppt
Planowanie strategiczne i operac Konferencja AWF 18 X 07
Wyklad 2 TM 07 03 09
ankieta 07 08
Szkol Okres Pracodawcy 07 Koszty wypadków
Wyk 07 Osprz t Koparki
zarządzanie projektem pkt 07
więcej podobnych podstron