
2009-03-17
1
Dr n. med. Sławomir Mikosioski
Oddział Kliniczny Medycyny Nuklearnej
Endokrynologii Onkologicznej
UM w Łodzi
Cykl miesiączkowy i jego zaburzenia
Autor prezentacji dr n. med. Ireneusz Salata
Endokrynologia cyklu miesiączkowego
Gonadotropiny i główne steroidy jajnikowe odgrywają
główną rolę w złożonej regulacji prawidłowego cyklu
owulacyjnego.
Ten
dynamiczny
proces
wymaga
najwyższej integracji, aby umożliwid prawidłowy
rozwój pęcherzyków, dojrzewanie oocytu i owulację.
Endokrynologia cyklu miesiączkowego
•
Gonadoliberyna (GnRH) - neurohormon podwzgórza,
podstawowy regulator wytwarzania i uwalniania
gonadotropin (LH i FSH). Uwalniana przez podwzgórze w
sposób pulsacyjny.
•
Gonadotropiny: lutropina (LH) i folitropina (FSH). Są
wydzielane przez przysadkę w sposób:
1.
Toniczny (podstawowy)- regulowany pobudzającym
działaniem podwzgórza i hamującym działaniem steroidów
płciowych.
2.
Pulsacyjny (epizodyczny) – polega na rytmicznym
wydzielaniu z określoną częstością i amplitudą.
3.
Cykliczny – jest skutkiem dodatniego sprzężenia zwrotnego
z estrogenami i jest charakterystyczny dla organizmu
żeoskiego.
Mechanizm działania gonadotropin
• FSH oddziaływuje wybiórczo na komórki ziarniste,
następuje ich zwiększona proliferacja, formowanie płynu
pęcherzykowego, wzrost pęcherzyków oraz uaktywnienie
takich enzymów jak aromataza i hydroksysteroidowe
dehydrogenazy. Ponadto łącznie z estradiolem indukuje
pojawienie się receptorów dla LH.
• LH działa wybiórczo na komórki osłonki pęcherzyka. Pod
jej wpływem następuje synteza androgenów a następnie
progesteronu i 17 - hydroksyprogesteronu.
• Synergistyczne działanie FSH i LH warunkuje wydzielanie
estradiolu.
• Nadmiar prolaktyny hamuje uwalnianie FSH i LH poprzez
działanie na podwzgórze.
Estrogeny (estron E1; estradiol E2; estriol E3)
• Drugo i trzeciorzędowe cechy płciowe kobiece.
• Zmiany wzrostowe w błonie śluzowej macicy.
• Zwiększenie pobudliwości skurczowej macicy.
• Pobudzające dla plemników działanie śluzu.
• Wzrost, dojrzewanie i złuszczanie komórek nabłonka pochwy.
• Wzrost nabłonka kanalików i pęcherzyków gruczołowych w
gruczołach sutkowych.
• Hamowanie osteolitycznego wpływu PTH.
• Zatrzymanie sodu i wody w organizmie.

2009-03-17
2
Gestageny
• Zmiany wydzielnicze, a następnie doczesnowe
w błonie śluzowej macicy.
• Umożliwia implantację zapłodnionego jaja – powoduje wzrost
podścieliska, pobudza wydzielanie gruczołów i blokuje dalszy
wzrost endometrium pod wpływem estrogenów.
• Relaksacja macicy, hamuje działanie PGE.
• Nieprzenikliwy dla plemników śluz.
• Działa diuretycznie.
• Zwiększenie wydalania wapnia i fosforu.
• Podwyższenie temperatury ciała.
• Antyandrogenne działanie w skórze.
Androgeny
• Są wytwarzane u kobiet w jajniku, nadnerczach
i w wyniku obwodowej konwersji proandrogenów.
• W jajniku są wytwarzane pod wpływem LH w komórkach
osłonki, zrębu oraz wnękowych.
• U kobiet wykazują działanie anaboliczne.
• W warunkach prawidłowych wpływ androgenów jest
zdominowany przez aktywnośd estrogenów.
Wzrost oraz dojrzewanie pęcherzyków jajnikowych u
kobiety
Około 7 miesiąca życia płodowego w obu jajnikach znajduje się około 7 milionów pęcherzyków, z
czego około dwa miliony przetrwają do chwili narodzin noworodka.
W okresie pokwitania w jajnikach można znaleźd zaledwie 400 000 pęcherzyków.
Jeżeli zdrowa, niezachodząca w ciążę kobieta jajeczkuje 13-krotnie w ciągu roku, to w okresie od 15
do 50 roku życia mniej niż 500 spośród 400 000 pęcherzyków dojrzewa do owulacji.
Są 2 okresy wzrostu pęcherzyka jajnikowego uzależnione od właściwej
stymulacji gonadotropin przysadkowych:
1. podczas życia prenatalnego, gdy zachodzi formowanie się gonady
2. w życiu dojrzałym, gdy w czasie cykli miesiączkowych dojrzewający
pęcherzyk ulega owulacji
Formowanie się pęcherzyka
Około 24 tygodnia życia płodowego komórki germinalne pojawiają
się w worku żółtkowym.
Około 25 tygodnia migrują do listew gonadalnych i formują
niezróżnicowaną gonadę. Komórki germinalne znajdują się
pierwotnie w skupiskach bez elementów zrębowych i są
nazywane syncytium komórkowym.
Wnikanie tych elementów między oocyty wskazuje na początek
rozwoju pęcherzyków jajnikowych.
Pęcherzyk pierwotny jest to komórka jajowa — oocyt, zatrzymana
w stadium diplotenu profazy pierwszego podziału mejotycznego,
otoczona pojedynczą warstwą komórek ziarnistych
Rozwój niezależny od gonadotropin
Najwcześniejsze etapy rozwoju pęcherzyka pierwszorzędowego
dokonują się niezależnie od wpływu gonadotropin przysadkowych.
Rozwój zależny od gonadotropin
Z chwilą gdy pęcherzyk pierwszorzędowy zaczyna dojrzewać,
wśród komórek ziarnistych zaczynają pojawiać się niewielkie
jamki wypełnione płynem.
Te zmiany morfologiczne rozpoczynają rozwój pęcherzyka
wtórnego, nazywanego również pęcherzykiem antralnym.

2009-03-17
3
Rekrutacja
pęcherzyków
W momencie gdy
pęcherzyk uzyska wrażliwość na gonadotropiny,
dalszy jego
rozwój uzależniony jest od tych hormonów.
Niedostateczna lub
niewłaściwa stymulacja przez gonadotropiny
prowadzi do jego atrezji.
W normalnym cyklu
miesiączkowym, przez większą jego część,
stężenia krążących gonadotropin są zbyt niskie, aby stymulować
rozwój pęcherzyka poza wczesne etapy.
Z
chwilą gdy ustaje funkcja ciałka żółtego, pod koniec cyklu,
w czasie
którego nie doszło do zapłodnienia, stężenia estradiolu
i progesteronu
obniżają się i hamujące działanie tych steroidów
na
układ podwzgórze-przysadka mózgowa ulega zmniejszeniu.
Uwolnienie tej grupy
pęcherzyków oraz stymulacja ich do dalszego
rozwoju zwana jest procesem rekrutacji.
Podczas rekrutacji wszystkie podlegające temu procesowi
pęcherzyki mają zdolność do uzyskania pełnej dojrzałości i owulacji.
Selekcja pęcherzyka
Około 5-7 dnia normalnego 28-dniowego cyklu jeden pęcherzyk
zostaje wyselekcjonowany do owulacji i utworzenia ciałka żółtego.
Proces ten nazywany jest selekcją lub wyborem pęcherzyka
dominującego.
Selekcja jest kulminacją procesu rekrutacji i rozpoczyna okres,
w czasie którego wpływ jednego pęcherzyka wytwarza warunki,
w których tylko on może właściwie dojrzewać i osiągnąć etap
jajeczkowania.
U kobiety w przebiegu cyklu miesiączkowego dojrzewa
do zapłodnienia tylko jeden oocyt.
Dominacja pęcherzyka
Okres rozwoju pęcherzyka następujący po selekcji,
a poprzedzający owulację określany jest dominacją
Przemiany
okołoowulacyjne
W fazie przedowulacyjnej cyklu
następuje ciąg fizjologicznych
procesów stymulujących końcowe dojrzewanie pęcherzyka
i
owulację.
Najważniejszym czynnik → szczyt LH odpowiedzialny za:
• dokończenie podziału mejotycznego,
• pęknięcie pęcherzyka,
• luteinizację.
Stwierdzenie owulacji:
Jedynym pewnym potwierdzeniem dokonania
się owulacji jest:
• ciąża,
• uwidocznienie wolnej komórki jajowej w czasie
laparoskopii.
Pozostałe metody to tylko pośrednie; potwierdzające:
prawidłowy przebieg cyklu jajnikowego, endometrialnego;
potwierdzające: rozwój pęcherzyka, owulację i wytworzenie się
ciałka żółtego.
Są to:
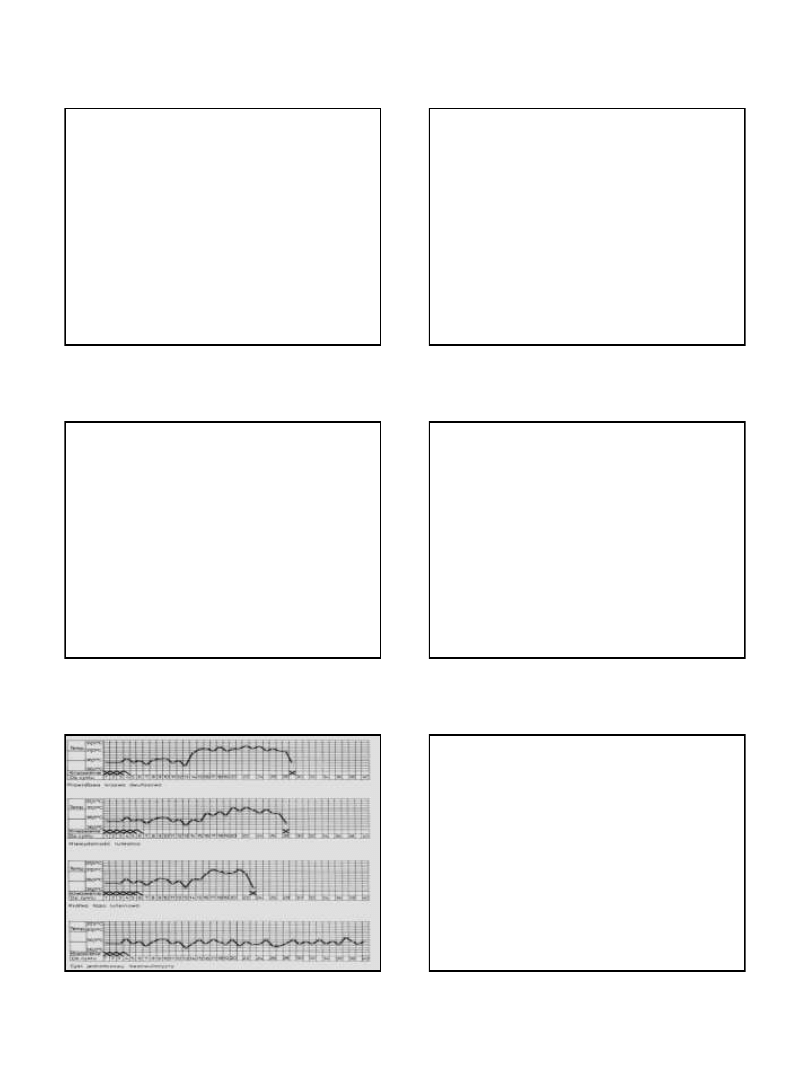
• pomiar podstawowej temperatury ciała,
• ocena śluzu szyjkowego,
• rozmaz cytohormonalny.
1 -
Menstruacja (miesiączka) 2 - Rosnące pęcherzyki 3 - Dojrzały
pęcherzyk z komórką jajową 4 - Owulacja (jajeczkowanie) 5 -
Ciałko żółte 6 - Zanik ciałka żółtego
Okres rekrutacji, selekcji, dominacji i owulacji pęcherzyka.
Etap działania czynników stymulujących właściwe dojrzewanie tylko
jednego pęcherzyka, podczas gdy pozostałe ulegają procesowi atrezji.
Zmiany hormonalne oraz morfologiczne w jajniku i błonie
śluzowej macicy w poszczególnych fazach cyklu
miesiączkowego
Faza krwawienia miesiączkowego (1-5 dzień cyklu)
• obniżenie stężenia FSH,
• LH wartości niskie (utrzymują się na takim poziomie
do momentu jajeczkowania),
• estrogeny — niskie stężenie,
• progesteron — niskie stężenie (niewielka ilość wytwarzana
jest przez
ciałko żółte z poprzedniego cyklu będące w stadium
regresji),
• jajnik — wybór pęcherzyków dla rozpoczynającego się cyklu,
• błona śluzowa macicy — złuszczenie.

2009-03-17
4
Faza folikularna (6-
13 dzień cyklu)
• FSH — utrzymuje się niskie stężenie aż do szczytu
wydzielania LH,
• LH — utrzymuje się niskie stężenie,
• estrogeny — wzrost wartości stężeń,
• progesteron — obniżenie stężenia,
• jajnik — dojrzewanie pęcherzyka i wybór pęcherzyka
dominującego,
• błona śluzowa macicy — na początku występuje proliferacja
nabłonka gruczołowego, później dołączają się wczesne
zmiany
podścieliska.
Faza owulacyjna (14 dzień cyklu)
• FSH — wyraźny wzrost wydzielania, choć mniejszy niż
w przypadku LH,
• LH — po gwałtownym wzroście stężenia estrogenów drogą
sprzężenia zwrotnego dodatniego dochodzi do ostrego
szczytu wydzielania LH,
• estrogeny — po wystąpieniu jajeczkowania dochodzi
do
gwałtownego spadku stężenia estradiolu,
• progesteron — stały wzrost wydzielania w wyniku
stymulacji LH,
• jajnik — uwolnienie komórki jajowej oraz luteinizacja
komórek ziarnistych pękniętego pęcherzyka jajnikowego,
• błona śluzowa macicy — pojawienie się w gruczołach
substancji
odżywczych, głównie glikogenu.
Faza lutealna (15-25
dzień cyklu)
•FSH — stężenie obniża się do wartości obserwowanych
w fazie folikularnej,
•LH — niskie stężenia,
•estrogeny - zwiększają stężenie w związku z produkcją
17
β-estradiolu przez ciałko żółte; przed fazą miesiączkową
stężenie zmniejsza się,
•progesteron — wysokie stężenie utrzymuje się w ciągu całej
fazy; szczyt wydzielania
występuje ok. 8 dnia fazy lutealnej
• jajnik — pełne
unaczynienie
luteinizowanych
komórek
ziarnistych
i
formowanie
ciałka
żółtego;
w
fazie
przedmiesiączkowej regresja ciałka żółtego,
• błona śluzowa macicy — poskręcanie gruczołów błony
śluzowej macicy, przemiana doczesnowa, obrzęk
podścieliska,
powiększanie jego komórek
Cykl endometrialny
Cykl endometrialny
to cykliczne zmiany błony śluzowej macicy powtarzające
się co ok. 28 dni.
Zmiany te
są wywoływane cyklicznymi zmianami stężenia hormonów jajnika
(estrogenów i progesteronu) występującymi w cyklu jajnikowym.
Zmianom
błony śluzowej macicy towarzyszą w cyklu menstruacyjnym zmiany
nabłonka jajowodu i pochwy oraz zmiany w istocie międzykomórkowej tkanki
łącznej całego organizmu kobiety.
Błona śluzowa macicy składa się z warstwy podstawowej i czynnościowej.
Warstwa
czynnościowa dzieli się na warstwę powierzchowną (zbitą)
oraz
pośrednią (gąbczastą).
Warstwa podstawowa nie zmienia swojej struktury i
grubości.
Warstwa
czynnościowa charakteryzuje się dużą wrażliwością na działanie
hormonów.
Podstawowymi elementami struktury
błony śluzowej macicy są: nabłonek
jednowarstwowy,
gruczoły cewkowate, tkanka zrębowa (podścielisko),
czyli tkanka
łączna oraz naczynia krwionośne.
Faza
miesiączkowa
Prostaglandyny
osiągają swe maksymalne stężenie tuż przed
samą miesiączką i wydają się spełniać istotną rolę w inicjacji
krwawienia
miesiączkowego poprzez obkurczenie tętniczek
spiralnych
i
stymulowanie
skurczów
macicy.
Warstwa
czynnościowa składająca się z warstwy gąbczastej i zbitej zostaje
złuszczona. Z fragmentów gruczołów warstwy podstawowej
zaczyna
się odnowa warstwy gąbczastej. Pod koniec tej fazy
właściwa błona śluzowa składa się tylko z warstwy podstawowej o
grubości 0,5 mm. Pierwszy dzień krwawienia jest uznawany za
początek cyklu miesiączkowego. Około 5 dnia cyklu krwawienie
ustaje i rozpoczyna
się faza proliferacyjna — folikularna.
2009-03-17
5
Faza folikularna
Trwa od 5 do 14 dnia cyklu. Faza ta jest
wywoływana
zwiększającym się stężeniem estrogenów we krwi. Pod ich
wpływem błona śluzowa macicy odbudowuje się z pozostałej
części warstwy czynnościowej i podstawowej. Komórki nabłonka
pozostałych fragmentów gruczołów rozmnażają się, co prowadzi
do epitelializacji (pokrycia
nabłonkiem) powierzchni uszkodzonej
błony.
Fibroblasty
dzielą się intensywnie, a także wytwarzają włókna
tkanki
łącznej i składniki istoty podstawowej, co odtwarza zrąb
błony śluzowej właściwej. Zrąb jest zasiedlany innymi komórkami
tkanki
łącznej właściwej i leukocytami
Faza owulacyjna
W fazie tej
błona śluzowa macicy dalej grubieje, jednak
zasadnicza struktura jest taka sama jak w fazie wzrostowej.
W badaniu ultrasonograficznym stwierdza
się przerost grubości
warstwy
czynnościowej oraz zwiększenie echogenności.
Faza lutealna
Około 14 dnia cyklu rozpoczyna się pod wpływem progesteronu
faza lutealna
— sekrecyjna. Trwa do ok. 28 dnia cyklu.
ZZABURZENIA MIESIĄCZKOWANIA
ddotyczą:
• nieprawidłowości rytmu krwawień (zbyt częste, zbyt rzadkie
miesiączki lub ich brak),
• nieprawidłowości związane z obfitością krwawień — skąpe
lub obfite,
• występowanie krwawień dodatkowych w cyklu miesiączkowym
(przed lub po miesiączce, w połowie cyklu).
Symptomatologia miesiączkowania
Dla określenia charakteru cyklu miesiączkowego stosuje się
następujące terminy:
Menarche — pierwsza miesiączka w życiu, prawidłowo
występuje między 9 a 16 rokiem życia, u polskich dziewcząt występuje
średnio ok. 13 roku życia,
Eumenorrhoea — regularne miesiączkowanie, występujące co
28 + /- 4 dni, o prawidłowej obfitości i czasie trwania. Fizjologiczna
utrata krwi w okresie miesiączki (3-5 dni) mieści się w granicach 30-70
ml.
Najczęściej są to cykle w których występuje owulacja i mają one
dwufazowy charakter.
Amenorrhoea primaria
—
Pierwotny brak miesiączki — brak miesiączki do 16 roku życia
Amenorrhoea paraprimaria
—
Pierwsza miesiączka wystąpiła po terapii hormonalnej.
Najczęstsze przyczyny pierwotnego braku miesiączki:
•
Dysgenezja gonad 19%
•
Hipoplazja jajników 15%
Niewydolność podwzgórza 14%
•
Zespół Mayera-Rokitansky'ego-Küstnera-Hausera 9%
•
Interseksualizm 8%
•
Wrodzony przerost nadnerczy 7%
•
Zespół braku wrażliwości na androgeny (zespół feminizujących jąder)
7%
•
Zarośnięcie błony dziewiczej 6%
•
Guzy przysadki 4%
•
Karłowatość przysadkowa 2%

2009-03-17
6
Amenorrhoea secundaria
Wtórny brak miesiączki rozpoznaje się, jeżeli stwierdza się brak
miesiączki przez czas dłuższy niż 3 miesiące.
Najczęstsze przyczyny wtórnego braku miesiączki:
• czynnościowa niewydolność podwzgórza,
• pourodzeniowy przerost nadnerczy,
• zarośnięcie macicy,
• zespół policystycznych jajników.
Oligomenorrhoea
— rzadko występujące miesiączki — odstępy między krwawieniami
nieregularne i trwające więcej niż 35 dni
(wg Pschyrembla 31 dni)
Cykle przedłużone podobnie jak cykle skrócone wiążą się z brakiem
jajeczkowania i są najczęściej jednofazowe.
Ten
typ
zaburzeń miesiączkowania obserwuje się u dziewcząt
w przebiegu pierwszych dwóch lat miesiączkowania. Jeżeli nie są
związane z przedłużonymi lub bardzo obfitymi krwawieniami
i nie towarzyszą im objawy androgenizacji, nie wymagają leczenia
w tym okresie życia.
Po 18 roku życia należy dążyć do ustalenia przyczyn zaburzeń cyklu
miesiączkowego i podjęcia leczenia.
Polimenorrhoea
— zbyt częste miesiączki o cyklu krótszym niż 21 dni (wg Psch.24 dni)
21 dni to najkrótszy czas trwania cyklu dwufazowego.
Występują dość często u dziewcząt 11-12-letnich, które wcześnie
rozpoczęły miesiączkowanie.
Skrócenie cykli miesiączkowych najczęściej występuje w cyklach
bezowulacyjnych, w niewydolności ciałka żółtego lub w efekcie
skrócenia fazy folikularnej dojrzewania pęcherzyka jajnikowego.
Hypomenorrhoea
— skąpe miesiączkowanie o nieprawidłowej, małej utracie krwi poniżej
30 ml, trwające zwykle krócej niż l lub 2 dni (zmniejszenie ilaści krwi
miesiączkowej o ponad 20% w porównaniu z poprzednimi okresami)
Skąpe miesiączki w postaci plamień lub krwistych upławów mogą być
uwarunkowane hormonalnie.
pierwotna niewydolność jajników:
hipoplazja jajników,
zespół wygasania czynności jajników
wtórna niewydolność jajników:
czynnościowa niewydolność podwzgórza,
hiperprolaktynemia.
Zmiany organiczne zesp. Ashermana, zmiany zapalne błony śluzowej
macicy, np. gruźlica.
Hypermenorrhoea
— nadmiernie obfite miesiączkowanie z utratą krwi ponad 80 ml
w regularnych odstępach czasu, długość cykli miesiączkowych
i
czas
trwania
krwawienia
(do
7
dni)
są prawidłowe
(zwiększenie ilości krwi miesiączkowej o ponad 20%)
Menorrhagia
-
krwotok miesiączkowy; przedłużone (powyżej
7 dni) i (wg Becka) nadmierne (powyżej 80 ml)
krwawienie występujące w regularnych odstępach
czasu, długość cykli miesiączkowych prawidłowa
Najczęstszą przyczyną obfitych, krwotocznych miesiączek (90%) są
zmiany organiczne: podśluzówkowe mięśniaki, polipy, przerosty błony
śluzowej macicy, zmiany zapalne, a także zaburzenia krzepnięcia krwi.
Metrorrhagia –
przewlekłe krwawienie z macicy
— acykliczne przedłużające się krwawienie (występuje w nieregularnych
odstępach czasu)
Krwawienia występujące u młodocianych, trwające ponad 10 dni,
niemające charakteru cyklicznego określa się mianem metrorrhagia
iuvenilis.
Mogą one trwać do 3 miesięcy, często są bardzo obfite, ze skłonnością
do nawrotów. Ciężkie przypadki mogą zagrażać życiu.
Metrorrhagia climaterica rozpoznaje się wtedy, gdy krwawienie pojawi
się 12 miesięcy po menopauzie; wymaga ono zawsze postępowania
diagnostycznego z badaniem histopatologicznym włącznie.

2009-03-17
7
Menometrorrhagia
— miesiączka krwotoczna - krwawienie z macicy o dużym nasileniu
pojawiające się w nieregularnych odstępach czasu
Algomenorrhoea (
Dysmenorrhoea)
— bolesne miesiączkowanie
oraz bolesne miesiączkowanie z objawami wegetatywnymi (bóle głowy,
nudności, wymioty, zasłabnięcia, utraty przytomności)
Bolesne miesiączkowanie może mieć charakter pierwotny lub wtórny.
Wtórne bolesne miesiączki częściej pojawiają się na tle organicznym
w przeciwieństwie do pierwotnie bolesnego miesiączkowania.
Podstawą rozpoznania i leczenia w endokrynologii są
starannie zebrany wywiad i dokładne badanie fizykalne.
Krwawienia te mogą wystąpić w wyniku toczącego się procesu
nowotworowego (charakterystyczne mogą być krwawienia kontaktowe
i krwawienia acykliczne).
Przyczyna każdego krwawienia, które występuje poza terminem
prawidłowej miesiączki, musi być wyjaśniona.
Krwawienia czynnościowe i krwawienia uwarunkowane przyczynami
organicznymi mogą nie różnić się przebiegiem ani charakterem
krwawienia.
Należy zawsze brać pod uwagę możliwość istnienia innego źródła
krwawienia niż macica (cewka moczowa, odbyt, pochwa, srom).
Jako czynnościowe krwawienia określa się wszystkie, których przyczyną
są zaburzenia czynności układu
Bolesne miesiączkowanie
Bolesne miesiączkowanie (dysmenorrhoea) objawia się bólami w
obrębie miednicy towarzyszącymi miesiączce.
Częstotliwość: Średnio dolegliwość ta jest powodem 10% ogółu
absencji szkolnej.
Umiejscowienie bólu: Na ogół jest to ból umiejscowiony w podbrzuszu,
promieniujący do krocza, odbytu, a także kończyn dolnych, okolicy
lędźwiowej i brzucha.
Czas występowania
U młodej dziewczyny, bez znaczącej przeszłości ginekologicznej, ból
pojawia się rzadko wraz z pierwszą miesiączką. Występuje on zazwyczaj
po kilku cyklach bezbolesnych. Ten typ bolesnego miesiączkowania
zwany jest pierwotnym i często jest samoistny.
U kobiet w okresie aktywności płciowej bolesne miesiączkowanie
może wystąpić po nieudanym współżyciu płciowym lub bez uchwytnej
przyczyny. Tego typu bolesne miesiączkowanie zwane jest wtórnym
i a priori należy w tym przypadku podejrzewać organiczne podłoże
zaburzenia.
AMENORRHOEA:
Fizjologicznie:
Brak krwawienia występuje u dziewczynek i dziewcząt do chwili
pojawienia się pierwszej miesiączki (menarche).
Akceleracja dojrzewania, zmiana stylu życia, labilność psychoseksualna
są przyczyną pojawienia się pierwszej miesiączki w coraz młodszym
wieku. Na świecie menarche pojawia się obecnie między 9 a 16 rż.,
średnio ok.12,5 rż.
W 1935 roku średni wiek menarche w Belgii wynosił 16 lat, a w USA 14
lat. W tym czasie tzw. masa krytyczna dla wystąpienia krwawienia
u dziewcząt wynosiła 46-47 kg. Obecnie w USA wynosi ona 47,8 kg,
a w Polsce 46,5 kg.

2009-03-17
8
Postępowanie diagnostyczne w przypadku braku
miesiączki:
I. Pierwotny brak miesiączki:
1) badanie kliniczne
2) badania genetyczne
3) testy hormonalne:
·
Gestagenowe
·
Estrogenowe
·
z GnRH celem oceny FSH, LH
·
dodatkowe badania hormonalne: PRL, Estradiol
II. Wtórny brak miesiączki:
1) wykluczyć ciążę!
2) ocena PRL
3) test gestagenowy
4) ocena endokrynologiczna układu podwzgórzowo-przysadkowego,
tarczycy i nadnerczy
Przyczyny zaburzeo miesiączkowania (wg WHO - 1976)
Grupa
Przyczyny zaburzeń miesiączkowania
I
Niewydolność podwzgórzowo - przysadkowa
II
Dysfunkcja podwzgórzowo - przysadkowa
III
Pierwotna niewydolność jajników
IV
Wady lub nabyte uszkodzenia macicy
V
Guzy okolicy podwzgórzowo - przysadkowej
wydzielające prolaktynę
VI
Zaburzenia funkcji podwzgórzowo - przysadkowej
połączone z hiperprolaktynemią
VII
Guzy pourazowe lub pozapalne, uszkodzenie regionu
podwzgórzowo - przysadkowego.
Niewydolność podwzgórzowo-przysadkowa
(grupa I wg WHO)
Określana
dawniej
jako
podwzgórzowy
brak
miesiączki
(amenorrhoea hypothalamica) lub podwzgórzowa niewydolność
jajników (hypothalamic ovariarn failure).
Dwa typy podwzgórzowego braku miesiączki:
I. związany z czynnikami psychicznymi
II. związany z ćwiczeniami fizycznymi
• Psychogenna
postad
zespołu
podwzgórzowo
-
przysadkowego: wstrząs psychiczny np. zgon bliskiej
osoby;
zaburzenia
pulsacyjnego
wydzielania
GnRH
spowodowane
zwiększonym
wydzielaniem
β-endorfin oraz CRF
• Anorexia nervosa – zaburzone wydzielanie pulsacyjne
GnRH,
obniżone
stężenie
LH
przy prawidłowym FSH
• Zespól podwzgórzowy po odchudzaniu – tzw. krytyczna
masa
ciała
wynosząca
48
kg.
niskie stężenia LH, FSH i estradiolu oraz zaburzenia w
pulsacyjnym wydzielaniu LH
• Zespól Sheehana – pokrwotoczna martwica przysadki w
wyniku
wstrząsu
oligowolemicznego
w II okresie porodu
Zzaburzenia
miesiączkowania
związane z ćwiczeniami
fizycznymi: Anorexia athletica
Iintensywne ćwiczenia fizyczne doprowadzają do:
defektu fazy lutealnej i niewydolności ciałka żółtego,
cykli bezowulacyjnych i ewentualnego braku miesiączki,
opóźnienia w pojawieniu się menarche, szczególnie u młodych
dziewcząt trenujących intensywnie jeszcze przed menarche.
W
40-50% występują u:
intensywnie trenujących biegaczek
ttancerek
pływaczek
AAnorexia athletica może się pojawić z lub bez utraty masy
ciała.
Brak miesiączki
wiąże się ubytkiem ustrojowej tkanki
tłuszczowej i stresem, związanym z zawodami, występem
U
pływaczek
(rzadziej
występujący
brak
miesiączki)
zachowane jest 20% tłuszczu ustrojowego, podczas gdy u
biegaczek
i tancerek jest tylko 15%. Część autorów uważa, że jest on
przyczyną zaburzeń miesiączkowania. Uważa się, że 22%
tłuszczu
ustrojowego
jest
niezbędne
do
prawidłowego
funkcjonowania osi podwzgórzowo-przysadkowo-jajnikowej.

2009-03-17
9
ZZaburzenia hormonalne:
defekt pulsacyjnego uwalniania LH,
hipogonadyzm hipogonadotropowy,
hiperprolaktynemia.
LLeczenie:
przerwanie intensywnych ćwiczeń fizycznych,
w sytuacji konieczności kontynuacji ćwiczeń fizycznych
i braku miesiączki wprowadzenie HTZ,
W w przypadku hiperprolaktynemii leczenie typowe dla tego
zaburzenia.
ZZaburzenia czynności podwzgórzowo-przysadkowej
(grupa II wg WHO)
W przypadku pojawienia się zaburzeń w funkcjonowaniu układu
podwzgórzowo-przysadkowego
dochodzi
do
tonicznego
wydzielania gonadotropin z okresowym lub stałym uszkodzeniem
cyklicznego wydzielania lutropiny. Stąd też powstałe zaburzenia
miesiączkowania w okresie dojrzewania i dziewczęcym mogą
przebiegać z:
hipo-
lub
normoestrogenizmem
hipogonadotropowym
(podwzgórzowy brak miesiączki)
normo-
lub
hiperestrogenizmem
współistniejącym
z
zaburzeniami
cyklicznego
wydzielania
gonadotropin
i
hiperandrogenizmem (PCOS)
w hipo- lub normoestrogenizmie hipogonadotropowym dochodzi
do braku jajeczkowania z zaburzeniami miesiączkowania pod
postacią:
o pierwotnego lub wtórnego braku miesiączki,
o rzadkiego miesiączkowania,
o
(rzadko) częstego miesiączkowania lub krwawień około-
miesiączkowych.
Zespół policystycznych jajników (Polycystic Ovary
Syndrome - PCOS)
• to pojęcie obejmujące niejednorodną grupę schorzeo
• dotyczy od 4 do 12% populacji kobiet będących w wieku rozrodczym
• występuje zarówno wśród kobiet z regularnymi cyklami
owulacyjnymi o prawidłowej masie ciała, jak również u kobiet z w
pełni rozwiniętym (opisanym przez Steina i Leventhala) obrazem
klinicznym, na który składają się oligo- bądź amenorrhoea, otyłośd,
hirsutyzm, hiperandrogenizm oraz niepłodnośd i poronienia
nawykowe
• ponadto otyłe pacjentki z PCOS częściej zapadają na inne choroby,
np. nadciśnienie tętnicze, cukrzycę, hiperlipidemię, choroby układu
krążenia i dróg żółciowych. U wielu występuje mniejszego lub
większego
stopnia
opornośd
na
insulinę,
co niekoniecznie wiąże się z otyłością.
Najistotniejszymi kryteriami rozpoznania PCOS są:
• 1. hiperandrogenizm,
2. chroniczny brak owulacji lub rzadkie miesiączkoawnie,
3. obecnośd jajników policystycznych w obrazie USG
przy braku innych, wtórnych przyczyn hiperandrogenizmu,
takich jak: wrodzony przerost nadnerczy lub nowotwór
produkujący androgeny. Muszą byd spełnione 2 kryteria z 3.
• Obecnośd obrazu policystycznych jajników w badaniu USG nie jest
wystarczająca dla postawienia rozpoznania PCOS przy braku objawów
klinicznych lub braku podwyższonego stężenia androgenów w surowicy
krwi.
• Najczęściej
stwierdzaną
nieprawidłowością
biochemiczną
jest
hiperandrogenizm,
który
może
byd
najważniejszą
przyczyną
zahamowania folikulogenezy. Podwyższone stżenie androgenów może
byd pochodzenia jajnikowego lub nadnerczowego.
Otyłość a
zespół policystycznych jajników
• Otyłośd pojawia się u 35 do 60% kobiet, u których występuje
PCOS. Jest ona związana z większym nasileniem objawów
klinicznych, niż u kobiet szczupłych dotkniętych tą chorobą,
przy
występujących
jednocześnie
podobnych
nieprawidłowościach
ujawnianych
w
badaniach
biochemicznych.
• Redukcja wagi ma największe znaczenie przed rozpoczęciem
leczenia, jednak jest ona często bardzo trudna do
przeprowadzenia
.
Patofizjologia PCOS
• Podwyższone stężenie androgenów w surowicy (testosteronu
lub
androstendionu)
hamuje
produkcję
estrogenów
i
progesteronu w pęcherzyku.
• Nieprawidłowa ekspozycja wzrastającego pęcherzyka na zbyt
wysokie
stężenia
androgenów
może
doprowadzić
do zahamowania działania FSH i atrezji pęcherzyka.
• Długotrwałe działanie androgenów powoduje powstanie zmian
policystycznych w obrębie jajników.
• Pierwotnym źródłem zwiększonego stężenia androgenów
może być jajnik lub miejsce wydzielania położone poza
jajnikiem - nadnercza.

2009-03-17
10
Nadnerczowe źródło hiperandrogenemii
• Wydzielanie nadnerczowego siarczanu dehydroepiandrosteronu
zwiększa się o 50% w przypadku występowania PCOS.
• Jest to zwiększenie zarówno wartości podstawowych, jak i wartości
w odpowiedzi na stymulację ACTH.
• U niektórych kobiet hiperandrogenemię można skorygować
za pomocą podawania deksametazonu.
Jajnikowe źródła hiperandrogenemii
• W przypadku PCOS jajniki są głównym źródłem wysokich
stężeń androgenów.
• Głównymi androgenami, których stężenia są podwyższone
w PCOS są testosteron i androstendion.
• Atretyczne pęcherzyki prawie nie są w stanie zmieniać
androstendionu na estradiol, w związku z tym w pęcherzykach
atretycznych dominują androgeny.
• Biosynteza androgenów w jajniku jest regulowana przez
hormon luteinizujący, a także prawdopodobnie przez insulinę.
• Wyodrębnia się dwie grupy kobiet z PCOS:
1) z wysokim stężeniem LH i prawidłowym stężęniem
insuliny w surowicy
2) z prawidłowym stężeniem LH i podwyższonym stężęniem
insuliny w surowicy.
Nieprawidłowości wydzielania LH
• podwyższone stężenie LH w surowicy krwi lub podwyższony
stosunek LH do FSH
• zwiększenie częstości i amplitudy pulsacyjnego wydzielania LH
• zwiększenie reakcji LH na GnRH i zmiana częstości
okołodobowego pulsacyjnego wydzielania LH
• Niemniej jednak stężenia LH w surowicy krwi mogą byd
prawidłowe aż u 40% kobiet z PCOS
Dojrzewanie a PCOS
• nie występuje nocne zwolnienie amplitudy pulsacyjnej LH
we
wczesnej
fazie
folikularnej.
Nieprawidłowości
okołodobowego rytmu wydzielania LH są także opisywane
łącznie z odwróceniem prawidłowego, okołodobowego rytmu
wydzielania LH u nastolatek po menarche, z objawami
klasycznego zespołu PCOS
• dziewczęta cechują się wczesnym, porannym wzrostem LH
w porównaniu z nocnym wzrostem stwierdzanym u zdrowych,
dojrzewających dziewcząt, lecz przed menarche.
• nieprawidłowości pulsacyjnego wydzielania LH sugerują,
że możemy mieć do czynienia z pierwotną nieprawidłowością
wydzielania GnRH, chociaż pozostaje niewyjaśnione, jaka to
centralna dysregulacja jest za to odpowiedzialna.
Wydzielanie FSH a PCOS
• FSH odgrywa kluczową rolę w prawidłowym
procesie owulacyjnym. Stężenie FSH w PCOS jest
albo prawidłowe, albo niskie. Przyczyna tych różnic
w wydzielaniu FSH i LH ciągle nie jest wyjaśniona.
• Stwierdzenie oporności na insulinę i hiperinsulinemia
u kobiet z PCOS przyczyniły się do dalszego
zrozumienia
patogenezy
PCOS,
a
także
udokumentowało, że zespół ten - poza zaburzeniami
reprodukcyjnymi - wiąże się również z poważnymi
zaburzeniami metabolicznymi
.
Rola oporności na insulinę w patogenezie PCOS
• Hiperinsulinemia występująca w PCOS wtórnie w stosunku do
oporności na insulinę przyczynia
się
do
powstania
hiperandrogenemii.
• Supresja insuliny w surowicy krwi osiągana przez doustne
podanie diazoksydu pociągała za sobą obniżenie stężenia
androgenów w surowicy krwi u otyłych kobiet z PCOS.
• Obniżenie wagi ciała kojarzy się ze zmniejszeniem stężenia
insuliny w surowicy krwi, zwiększeniem SHBG, co pociąga
za sobą obniżenie stężenia wolnego testosteronu w krążeniu.
Kojarzy
się to z uregulowaniem cyklu miesięcznego
i powrotem płodności.
2009-03-17
11
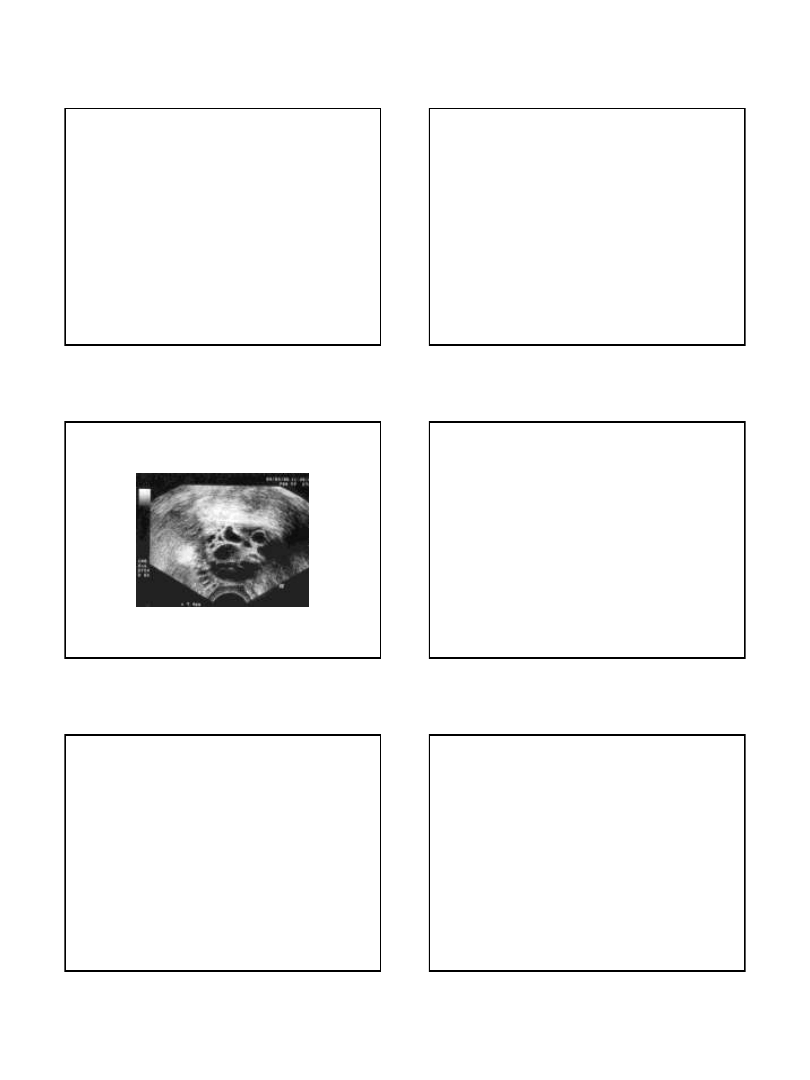
Ultradźwiękowe rozpoznawanie PCOS
• Cechy histologiczne jajników policystycznych wykazują
wzrost liczby małych (5-10mm) pęcherzyków, a także wzrost
objętości zrębu w porównaniu z jajnikiem prawidłowym.
• Oprócz tego u niektórych kobiet stwierdza się cechy rozrostu
osłonki.
• Kryteria
rozpoznawania
jajników
policystycznych
to jajniki zawierające przynajmniej 12 pęcherzyków (o
średnicy 2-9 mm) i/lub powiększona objętość jajnika (>10 ml).
Tylko 1 jajnik spełniający te kryteria jest potrzebny do
rozpoznania PCOS. Definicji tej nie stosuje się do kobiet
stosujących tabletki antykoncepcyjne, gdyż ich stosownie
zmienia wygląd jajników.
Ultradźwiękowe rozpoznawanie PCOS
• Wiadomo, że cechy ultradźwiękowe jajników policystycznych
mogą występować w innych stanach hiperandrogennego braku
owulacji,
takich
jak
guzy
nadnerczowe
wydzielające
androgeny, zespół Cushinga, wrodzona hiperplazja nadnerczy i
hiperprolaktynemia.
• Ultradźwiękowe rozpoznanie PCOS jako jedyne kryterium
diagnostyczne może u 21% pacjentek spowodować błędne
rozpoznanie tego zespołu.
• Zwiększenie objętości zrębu jajnika może być bardziej czułym
znacznikiem tego zaburzenia.
Obraz policystycznych jajników w USG
Profil endokrynologiczny w PCOS
• większy od 2 stosunek LH/FSH i podwyższenie stężenia
całkowitego
testosteronu,
wolnego
testosteronu,
androstendionu lub siarczanu dehydroepiandrostendionu.
• Test obciążenia progesteronem: Foks i HulI wykazali,
że u 92% pacjentek po obciążeniu progesteronem występuje
krwawienie, co przemawia za istnieniem estrogenizacji.
Dokładność diagnostyczna samego dodatniego obciążenia
progesteronem wynosiła 89%
Nieprawidłowości metaboliczne
• Zaburzona tolerancja glukozy
• Nieprawidłowości lipidowe i ryzyko chorób układu
krążenia: Kobiety z zespołem PCOS zdają się być narażone
na szczególnie wysokie ryzyko wystąpienia tych chorób.
Względne ryzyko zawału serca u kobiet z PCOS ustalone
drogą analizy czynnika ryzyka wynosiło 7,4%. Jest to wynik
współistnienia mnogich czynników ryzyka obejmujących
otyłość, nietolerancję glukozy, nadciśnienie, dyslipidemię.
Oporność na insulinę, podwyższone stężenie męskich
sterydów płciowych, otyłość centralna nasilają ryzyko
wystąpienia choroby układu krążenia, chociaż jest możliwe,
że pośredniczy w tym dyslipidemia. W PCOS dyslipidemię
charakteryzuje wzrost stężenia trójgiicerydów i niskie stężenie
HDL w surowicy krwi.
Rozpoznawanie i badanie
• objawy kliniczne takie jak zaburzenia miesiączkowania
i/lub
przewlekły brak owulacji, z pewnymi danymi
wskazującymi na hiperandrogenizm (hirsutyzm, trądzik)
łącznie z wykazaniem jajników policystycznych w badaniu
USG oraz z danymi biochemicznymi przemawiającymi
za hiperandrogenemią.
• Profil hormonalny określony w 7 dniu cyklu powinien
obejmować LH, FSH, testosteron, androstendion i prolaktynę.
• Ważne
jest
wykluczenie
innych
przyczyn
zaburzeń
miesiączkowania,
a
mianowicie
hiperprolaktynemii,
przedwczesnej
niewydolności jajników, podwzgórzowego
braku miesiączki. Stężenie prolaktyny w surowicy krwi
przekraczające 1000 j.m./l, przy więcej niż jednym oznaczeniu
wymagają prowadzenia dalszych badań w celu wykluczenia
prolactinoma.
Należy je przeprowadzić
bez
względu
na istnienie PCOS w obrazie ultradźwiękowym.

2009-03-17
12
Rozpoznawanie i badanie
• U pacjentek z stężeniem testosteronu w surowicy przekraczającymi
5 nmol/l lub androstendionu przekraczającymi 20 nmol/l powinno się
wykonać dalsze badania w celu wykluczenia późno rozpoczynającej się
wrodzonej hiperplazji nadnerczy, zespołu Cushinga i guzów nadnerczy
lub jajnika wydzielających androgeny.
• Test obciążenia progesteronem jest użyteczny klinicznie zwłaszcza u kobiet
z amenorrhoea.
• Ze względu na niedawno uzyskane dane, mówiące o zwiększonej częstości
zaburzeń tolerancji glukozy, zwiększeniu ryzyka zachorowania na choroby
układu krążenia, u otyłych kobiet z PCOS może być celowe wykonanie
doustnego testu tolerancji glukozy i oznaczenie na czczo trójgiicerydów
i cholesterolu zawartego w HDL surowicy krwi, zwłaszcza u kobiet
z BMI>25.
PCOS - Niepłodność - indukcja owulacji
•
PCOS jest najczęstszą (73%) przyczyną niepłodności anowulacyjnej.
•
Przed
rozpoczęciem
indukowania
owulacji
powinno
się
stwierdzić,
że stan nasienia jest zadowalający. Badanie stanu jajowodów można odroczyć o 3-6 cykli,
jeżeli nie ma wskazań klinicznych. Pierwszą linią w indukcji owulacji są antyestrogeny.
W celu chemicznego inicjowania owulacji stosuje się cytrynian klomifenu, będący w
użyciu już ponad 25 lat.
•
Występuje zwiększone ryzyko zajścia w ciążę mnogą (8% wszystkich ciąż), w większości
przypadków będą to bliźnięta.
•
Pacjentka jest oporna na klomifen, jeżeli nie reaguje na dawkę owulacyjną przez ponad 6
miesięcy.
•
Drugą linię leczenia stanowią zwykle gonadotropiny - albo niska dawka gonadotropin,
albo tłumienie analogiem GnRH z następową terapią gonadotropinami. Terapia
gonadotropinami wymaga dokładnego monitorowania za pomocą seryjnych badań USG z
lub bez seryjnych oznaczeń estradiolu - ma to na celu uniknięcie powikłań.
•
Tradycyjna ludzka gonadotropina menopauzalna (HMG) zawiera zarówno FSH jak LH.
Aktywna składowa stanowi tylko 3% całkowitego leku.
PCOS - Niepłodność - indukcja owulacji
• Konwencjonalne sposoby podawania gonadotropin kojarzą się
z
powstawaniem
mnogich
pęcherzyków i zwiększoną
częstością powstawania ciąży mnogiej (opisywano częstości
wynoszące 10-50%), występowaniem zespołu hiperstymulacji
jajnika (OHSS) (od łagodnej do umiarkowanej w zakresie od 8
do 20%) i ciężkiej hiperstymulacji wymagającej hospitalizacji,
występującej do 2% przypadków.
• U pacjentek, u których leczenie gonadotropinami jest
nieskuteczne, może być konieczne zastosowanie technik
wspomaganego rozrodu
.
Hiperandrogenizm - leczenie
• W postępowaniu z hirsutyzmem, trądzikiem i łysieniem należy
podkreślić wagę obniżenia ciężaru ciała u pacjentek otyłych.
Często wystarcza dokładne wyjaśnienie przyczyny schorzenia
i zapewnienie o łagodnym jego charakterze, skojarzone
z
poradą
dotyczącą
takich
środków
kosmetycznych,
jak depilacja.
• W drugiej linii leczenia znajdują się antyandrogeny.
Najczęściej są one stosowane w odwrotnym reżimie
sekwencyjnym, obejmującym octan cyproteronu w dawce 50-
100 mg i etinyloestradiol w dawce 35-50 mcg. Uzyskiwano
poprawę trądzika u 50-100% pacjentek w czasie 3-6 miesięcy,
zaś nasilenie hirsutyzmu obniżało się w ciągu 6-9 miesięcy
o 50%. Można ten efekt podtrzymywać, stosując Diane 35,
to jest preparat zawierający niską dawkę (2 mg) octanu
cyproteronu wraz z 35 mcg etinyloestradiolu.
Hiperandrogenizm - leczenie
.
• Postępowanie takie może być wystarczające u kobiet
z hirsutyzmem o nasileniu słabszym lub umiarkowanym.
Do innych dostępnych antyandrogenów należą spironolakton
i flutamid. U kobiet, u których dominuje hiperandrogenizm
nadnerczowy
stosuje
się
supresję
nadnerczy
glikokortykoidami. Stosuje się również supresję jajnika
za pomocą doustnych pigułek antykoncepcyjnych w terapii
kombinowanej. Możliwe jest także krótkotrwałe stosowanie
agonistów GnRH oraz łączne stosowanie agonistów GnRH
i HTZ (HRT). Współcześnie poddawane są ocenie inhibitory
5α-reduktazy, takie jak finasteride.
Pierwotna niewydolność jajników (grupa III wg WHO)
(hipogonadyzm hipergonadotropowy)
Definicja:
PPojęcie pierwotnej niewydolności jajników obejmuje brak
czynności generatywnej i hormonalnej gonad, pomimo istnienia
prawidłowej endogennej stymulacji gonadotropowej.
Objawy:
ZZespół
objawów
poprzedza
zwykle
kilkuletni
okres
przejściowy z pojawieniem się u 50% dziewcząt plamienia,
będącego efektem odpowiedzi na podanie progesteronu.
o pierwotny lub wtórny brak miesiączki
o eunuchoidalna budowa ciała,
o
niedorozwój płciowy,
o objawy wypadowe, naczyniowe i anatomiczne,
o zanikowe zmiany błony śluzowej macicy i nabłonka pochwy
-efekt niedoboru estrogenów

2009-03-17
13
ZZespół nadnerczowo-płciowy
(adrenogenital syndrom, AGS; WPN)
OObjawy:
-niski wzrost i nadmiernie rozwinięte mięśnie
-Zwiększone stężenie androgenów nadnerczowych,
-niskie stężenie kortykosteroidów
-W ciężkich przypadkach brak jest owulacji i występuje
ooligo- lub amenorrhoea hipogonadotropowa. (ciężkie przypadki)
LLeczenie:
Kortykosterydy
wwystąpienie krwawienia i jajeczkowania stanowi kryterium
normalizacji stężenia androgenów: testosteronu, androstendionu
i siarczanu dehydroepiandro-steronu (DHAS).
Brak miesiączki pochodzenia macicznego (grupa IV wg WHO)
ZZespoły z pierwotnym brakiem miesiączki
W ok. 10-15% spowodowane wrodzonymi wadami wewnętrznych
lub zewnętrznych narządów płciowych.
współistnienie zaburzeń różnicowania płci z cechami obojnactwa:
budowa ciała i rozwój wtórnych cech płciowych są prawidłowe.
Wrodzone
wady
wewnętrznych
i
zewnętrznych
narządów
płciowych powstają ok. 8-10 tyg. życia płodowego.
HIPERPROLAKTYNEMIA, ROZPOZNAWANIE, PRZYCZYNY I
OBJAWY
• Hiperprolaktynemią określa się wzrost stężenia PRL >20 ng/mL (>400 mU/l) u
kobiet i >15 ng/mL (>300 mU/l) u mężczyzn.
• Fizjologicznie naturalny (okresowy) wzrost stężenia PRL w surowicy krwi
obserwuje się w czasie snu, ciąży, laktacji, w okresie noworodkowym, w
odpowiedzi na stres (np. hipoglikemia, wysiłek fizyczny) oraz podczas
orgazmu.
• Stymulacja brodawek sutkowych gruczołów piersiowych także powoduje
zwiększenie syntezy i sekrecji PRL.
• Hiperprolaktynemia jest zjawiskiem stosunkowo często spotykanym w
endokrynologii. Pojawia się ona w trakcie terapii lekami modyfikującymi
bezpośrednio lub pośrednio wydzielanie dopaminy. Z tego też względu
pierwszym
krokiem
w
diagnostyce
hiperprolaktynemii
powinno
być
wykluczenie przyjmowania niektórych leków, jako potencjalnej przyczyny tego
zaburzenia
Patologiczny
przewlekły
(przetrwały)
wzrost
syntezy
i sekrecji PRL jest spowodowany jednak
najczęściej chorobą
ośrodkowego układu nerwowego. Wiele guzów okolicy
podwzgórzowo-przysadkowej zaburzających z powodu masy
guza wydzielanie dopaminy, a
także guzy samej przysadki
wydzielające PRL (prolactinoma) oraz guzy mieszane –
wydzielające oprócz PRL inne hormony przysadkowe są
przyczyną organicznej hiperprolaktynemii. Guzy przysadki
wydzielające PRL dzielimy w zależności od rozmiarów na
mikro-
(o
średnicy
<10
mm)
i
makroprolaktynoma
(średnica >10 mm). Duże stężenia PRL (>200 ng/mL
w warunkach podstawowych)
przemawiają za rozpoznaniem
makroprolaktynoma,
jednak
rozstrzygające jest zawsze
badanie obrazowe: tomografia komputerowa (TK) wysokiej
rozdzielczości lub jądrowy rezonans magnetyczny (NMR)
z kontrastem.
Pojawiające się u kobiet w wieku rozrodczym zaburzenia
miesiączkowania pod postacią oligomenorrhea lub amenorrhea są
przyczyną dużego niepokoju pacjentek i poszukiwania przyczyny
tych
zaburzeń u lekarza specjalisty. Z punktu widzenia klinicznego
u
mężczyzn
najczęściej
obserwuje
się
obniżenie
libido
oraz potencji
płciowej (90% pacjentów z hiperprolaktynemią),
na
które to objawy mężczyźni nie zwracają uwagi lub nie
przyznają się do nich, uważając je za wstydliwe i z tych powodów
nie
zgłaszają się do specjalisty. Objawami budzącymi ich niepokój
(podobnie jak u kobiet)
są mlekotok i ginekomastia, które
to jednak symptomy
pojawiają się stosunkowo rzadko (15–30%
pacjentów). Objawy takie jak bóle głowy czy ubytki pola widzenia,
związane z masą guza uciskającą na skrzyżowanie nerwów
wzrokowych,
pojawiają się w przypadku dużych guzów okolicy
przysadkowo-
podwzgórzowej.
HIPOGONADYZM HIPOGONADOTROPOWY W PRZEBIEGU
HIPERPROLAKTYNEMII
• Prawdopodobna rola endogennych opioidów, które powodują zmniejszenie
częstości wydzielania tzw. pulsów) podwzgórzowego hormonu
uwalniającego gonadotropiny (GnRH). a
• Podanie pacjentkom z wtórnym brakiem miesiączki
i hiperprolaktynemią antagonisty opioidów (naloksonu)
spowodowało przywrócenie menstruacji.
• Hiperprolaktynemia hamuje również wpływ estradiolu na przysadkę
mózgową, przez co zarówno częstośd jak i amplituda pulsów lutropiny (LH)
maleje. Podobnie redukowany jest przedowulacyjny wyrzut LH. Na skutek
obniżenia jajnikowego wytwarzania estradiolu, obniżeniu ulega także
stężenie tego hormonu w surowicy krwi
u kobiet.
• Podobnie, zostaje zmniejszona sekrecja testosteronu u mężczyzn.
• Hipogonadyzm jest także przyczyną szybszej utraty masy kostnej. Przy
hiperprolaktynemii obserwuje się również zaburzenia psychologiczne i
zachowania, podobne do tych jakie występują podczas menopauzy. Do
rzadkich symptomów należy hipotrofia,
a do bardzo rzadkich paradoksalna hipertrofia jąder.
2009-03-17
14
LECZENIE
• farmakologiczne z użyciem agonistów receptorów
dopaminowych (bromokryptyna, lizuryd, pergolid, chinagolid,
kabergolina) oraz chirurgiczne.
• U kobiet leczenie jest więc nakierowane na odzyskanie
płodności i odwrócenie objawów hipogonadyzmu.
U mężczyzn płodnośd jest zaburzona,
ale oligozoospermia nie wyklucza możliwości zapłodnienia,
zatem w tych przypadkach terapia ma
na celu głównie zniesienie pozostałych objawów
hipogonadyzmu.
• W przypadku guzów przysadki, zwłaszcza dużych, celem staje
się dodatkowo zahamowanie wzrostu guza lub zmniejszenie
jego rozmiarów i tym samym redukcja lub całkowite zniesienie
symptomów związanych z masą guza.
Symptomatologia miesiączkowania
Premenopauza:
- okres kilku lat poprzedzający wystąpienie ostatniej
miesiączki, w którym pojawiają się pierwsze hormonalne
objawy niewydolności jajników.
Perimenopauza:
- okres okołomenopauzalny
od wystąpienia pierwszych zaburzeo miesiączkowania do
roku po ostatniej miesiączce
Menopauza
(wg WHO)
:
- utrzymujący się od ponad roku brak miesiączki
Menopauza to termin wystąpienia ostatniej miesiączki, po
którym utrzymuje się co najmniej roczny okres braku
miesiączki.
Spowodowany jest trwałą niedoczynnością jajników
(samoczynnym wygaśnięciem czynności jajników)
Klimakteriuma
• Wcześniejsza menopauza u nałogowych palaczek tytoniu
• W Polsce menopauza około 50 roku życia
• Następstwo fizjologicznej niewydolności jajników
• Zmiana osi podwzgórze – przysadka - jajnik: podwyższone
stężenie FSH do LH
• Zmniejszona synteza estradiolu prze jajnik
• Estrogeny powstają z nadnerczowego androstedionu, ulega
on aromatyzacji do estronu.
Zespól klimakteryczny
• Uderzenia gorąca
• Zlewne poty
• Zawroty głowy
• Podwyższenie temperatury ciała
• Obwodowe poszerzenie żył
• Kołatanie serca
HTZ
• Stosuje się naturalne estrogeny: 17-estradiol, estriol, estron,
skoniugowane estrogeny kooskie
• Stosowanie najmniejszej skutecznej dawki, podawanie
estrogenów łącznie z gestagenami (wyjątek kobiety
po operacji usunięcia macicy)
• Przeciwskazania: ciężkie choroby wątroby, cholestaza,
nowotwory macicy, piersi, czerniak, porfiria, HA, ch. naczyo
mózgu, udar mózgu, ch. naczyo siatkówki, migrena,
niedokrwistośd sierpowatokrwinkowa i ch. zakrzepowa
Ryzyko nowotworów macicy , sutka, wzrostu ciśnienia
tętniczego, ch. zakrzepowej, zaburzeo metabolizmu glukozy
Wyszukiwarka
Podobne podstrony:
III rok harmonogram strona wydział lekarski 2013 2014 II i III Kopia
Pytania i odpowiedzi 2, wydział lekarski - materiały, Toksykologia
termoregulacja, wydział lekarski - materiały, Patofizjologia
II Rok Wydzial Lekarsko-Stomatologiczny, 3 rok stoma, radio
Opracowanie pytan egzaminacyjnych z fizjologii dla wydzialu lekarskiego (2011)
Pyelografia, wydział lekarski - materiały, Radiologia
TEMATY WYKŁADÓW Z FIZJOLOGII DLA STUDENTÓW II ROKU WYDZIAŁU LEKARSKIEGO
III Rok Wydzial Lekarsko-Stomatologiczny-RADIO, 3 rok stoma, radio
Epidemiologia nowotworów narządów płciowych, Materiały z Wydziału Lekarskiego
Cykl miesiączkowy, Pedagogika UŚ, Licencjat 2010-2013, I rok - semestr letni, Biomedyczne podstawy r
odpowiedzi testy na wydział lekarski 2000, pliki zamawiane, edukacja
CYKL MIESIĄCZKOWY
Kolokwium końcowe – wydział lekarski rok V (B), 1
Kolokwium końcowe – wydział lekarski rok V (A), Jednokrotnego wyboru
program nauczania, program seminariów, PROGRAM SEMINARIÓW DLA WYDZIAŁU LEKARSKIEGO
program nauczania, program seminariów, PROGRAM SEMINARIÓW DLA WYDZIAŁU LEKARSKIEGO
Splot ramienny wg. Topola, Anatomia, Anatomia, wydział lekarski, 1 Kończyny
więcej podobnych podstron