
2012-02-21
1
ROZTWORY BUFOROWE
wpływ kwasów i zasad na pH i pojemność buforową
ustroju człowieka
Ćwiczenie 1
P. Niemiec 2011
Wszystkie reakcje biochemiczne zachodz
ące w organizmach żywych
wymaga
ją do swojego przebiegu odpowiedniej wartości pH.
Nawet niewielkie wahania pH mo
gą prowadzić do zaburzeń procesów
biochemicznych
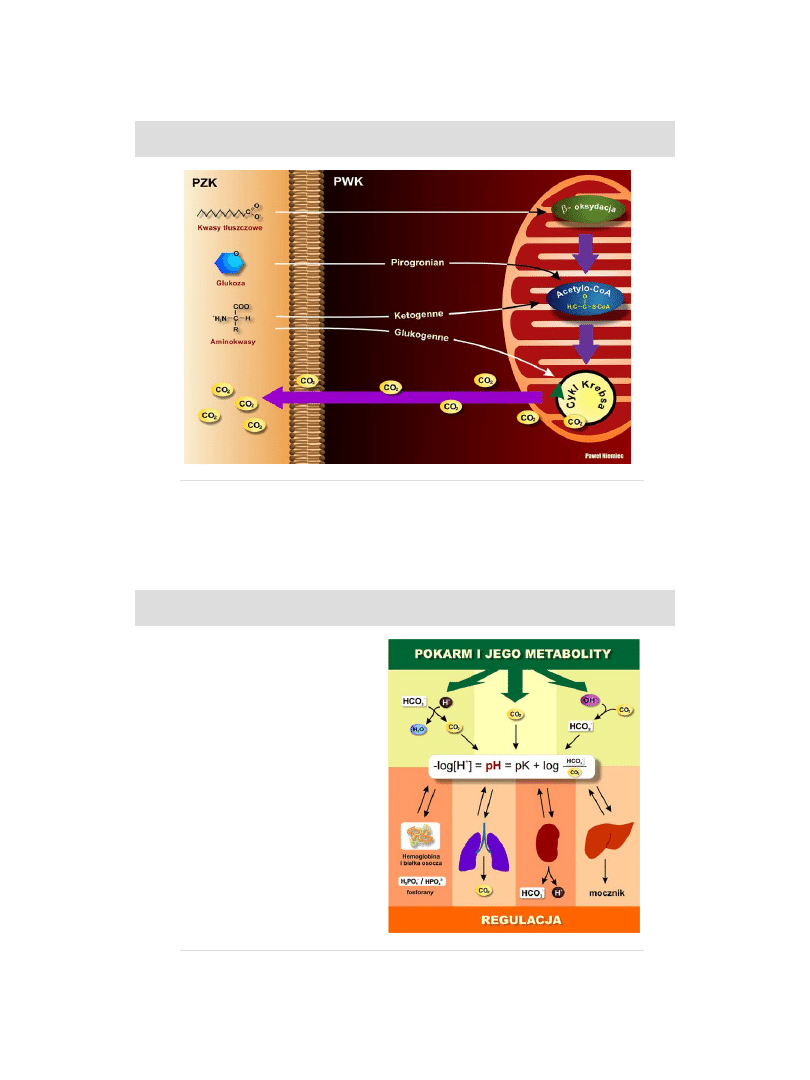
Zachod
zące w komórkach procesy kataboliczne prowadzą do
zakwaszenia
komórek i płynu pozakomórkowego.
Zakwaszenie polega na gromadzeniu s
ię nadmiaru jonów H
+
,
których
głównym źródłem jest CO
2
,
CO
2
powstaje w licznych reakcjach katabolicznych, generowanych
przez
dekarboksylazy
(katalizują reakcję odłączania CO
2
)
ROZTWORY BUFOROWE
CO
2
+ H
2
O
H
2
CO
3
H
+
+ HCO
3
-
2012-02-21
2
P. Niemiec 2011
ROZTWORY BUFOROWE
ROZTWORY BUFOROWE
P. Niemiec 2011
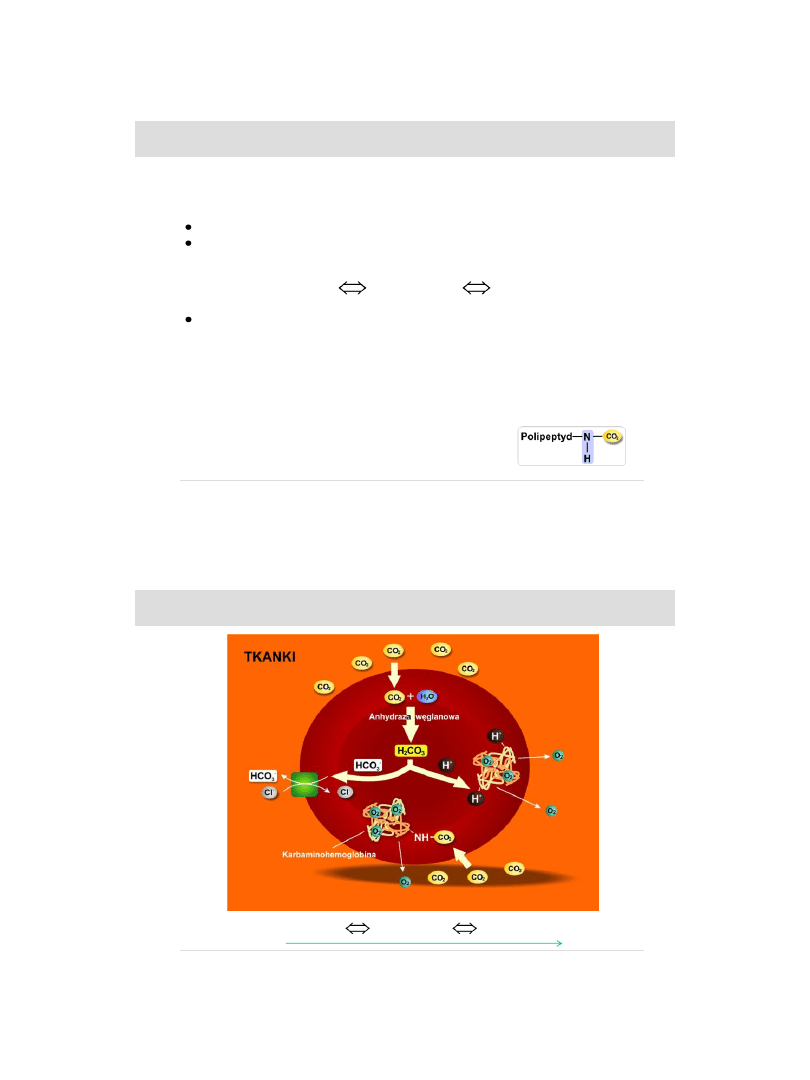
W regulacji gospodarki kwa-
sowo-zasadowej
uczestniczą:
-
płuca
- nerki
-
wątroba
Układy buforowe
są głównym
mechanizmem zabezpiecza
-
jącym przed zakwaszeniem
organizmu

2012-02-21
3
ROZTWORY BUFOROWE
P. Niemiec 2011
Bufory posiada
ją
zdoln
ość buforowania
, czyli przeciwstawiania si
ę
zmianom pH po dodaniu do nich niewielkich il
ości kwasów lub zasad
Są to mieszaniny słabego kwasu i jego soli z mocną zasadą lub
mieszaniny
słabej zasady i jej soli z mocnym kwasem np.;
CH
3
COOH i CH
3
COONa
Wielk
ością charakteryzującą zdolność buforowania danego roztworu
jest
pojemn
ość buforowa
(im
większa tym większe zdolności buforowe)
pH
roztworów buforowych oblicza się wg. następującego wzoru
(równanie Hendersona - Hasselbalcha)
:
pK
k
= - log K
k
,
K
k
– stała dysocjacji kwasu
C
s
– stężenie soli,
C
k
– stężenie kwasu
k
s
k
s
k
k
C
C
lg
pK
C
C
lg
pK
pH
ROZTWORY BUFOROWE
P. Niemiec 2011

2012-02-21
4
ROZTWORY BUFOROWE
P. Niemiec 2011
pH roztworów buforowych zależy od pK kwasu i stosunku stężeń soli
do kwasu
najważniejszym buforem organizmu jest
bufor
wodorowęglanowy
(HCO
3
-
/CO
2
), dlatego pH osocza w warunkach fizjologicznych wynosi:
4
.
7
)
L
/
mmol
2
.
1
(
CO
)
L
/
mmol
24
(
HCO
lg
)
1
.
6
(
pK
pH
2
3
k
ROZTWORY BUFOROWE
P. Niemiec 2011
36
.
7
)
CO
(mmol/L
1.2
)
HCO
(mmol/L
2
24
lg
1
.
6
pH
2
3
94
.
6
)
CO
(mmol/L
2
1.2
)
HCO
(mmol/L
2
24
lg
1
.
6
pH
2
3
2012-02-21
5
ROZTWORY BUFOROWE
P. Niemiec 2011
BUFOR WODORO
WĘGLANOWY
najw
ażniejszy bufor organizmu
jego metabolizm opisuje równanie
losy CO
2
- 75-80 % reaguje z H
2
O (reakcja katalizowana przez
anhydra
zę
węglanową
)
- 15 % tworzy p
ołączenia
karbaminianowe
z resztami aminokwasu
waliny bi
ałek (głównie hemoglobiny)
- 5-10% jest transportowane w postaci gazu rozpuszczonego w wodzie
przestrzeni wew
nątrznaczyniowej
Karbaminian
CO
2
+ H
2
O
H
2
CO
3
H
+
+ HCO
3
-
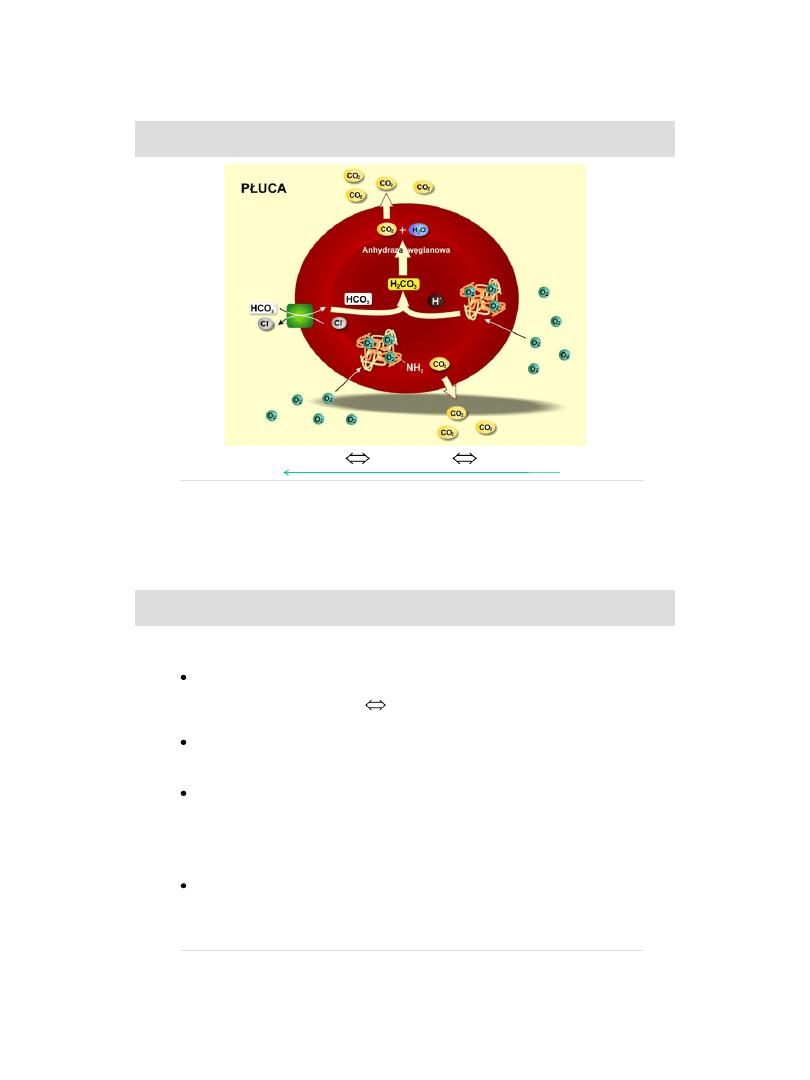
BUFOR HEMOGLOBINIANOWY
– wymiana gazowa
P. Niemiec 2011
CO
2
+ H
2
O
H
2
CO
3
H
+
+ HCO
3
-
2012-02-21
6
P. Niemiec 2011
BUFOR HEMOGLOBINIANOWY
– wymiana gazowa
CO
2
+ H
2
O
H
2
CO
3
H
+
+ HCO
3
-
ROZTWORY BUFOROWE
P. Niemiec 2011
BUFOR FOSFORANOWY
najważniejszy pod względem ilościowym bufor moczu
stosunek H
2
PO
4
-
do HPO
4
2-
we krwi wynosi 1:4, w moczu wynosi 4:1
H
2
PO
4
-
HPO
4
2-
+ H
+
fosforany obecne w moczu pierwotnym warunkują:
- wydalanie H
+
-
powstawanie wodorowęglanów w nerkach
zmiana stosunku
fosforanów w moczu w porównaniu z ich
stosunkiem we krwi wynika ze zmiany fosforanu II-
rzędowego (HPO
4
2-
)
w I-
rzędowy (H
2
PO
4
-
) przez
wiązanie H
+
podczas regeneracji
jonów
HCO
3
-
.

2012-02-21
7
ROZTWORY BUFOROWE
P. Niemiec 2011
ROLA NEREK
w regulacji gospodarki kwasowo-zasadowej
-
eliminacja jonów H
+
z ustroju
-
resorpcja zwrotna HCO
3
-
w kanalikach nerkowych
-
wydalanie nadmiaru jonów HCO
3
-
przy wzroście ich stężenia
..
w płynie pozakomórkowym
-
regeneracja
jonów HCO
3
-
ROZTWORY BUFOROWE
P. Niemiec 2011
PRZYCZYNY:
NAGROMADZENIE
SIĘ KWASÓW
- endogennych (np.
ketokwasów w cukrzycy)
- L-mlekowego (podczas hipoksji lub anoksji)
- D-mlekowego (fermentacja flory bakteryjnej)
UTRATA ZASAD
-
niewydolność nerek (brak wytwarzania HCO
3
-
.....
i
niemożność jego regeneracji)
- utrata HCO
3
-
z przewodem pokarmowym
....
.
(biegunki)
NADMIERNA
PODAŻ K
+
KWASICA METABOLICZNA
ZABURZENIA GOSPODARKI KWASOWO-ZASADOWEJ
2012-02-21
8
ROZTWORY BUFOROWE
P. Niemiec 2011
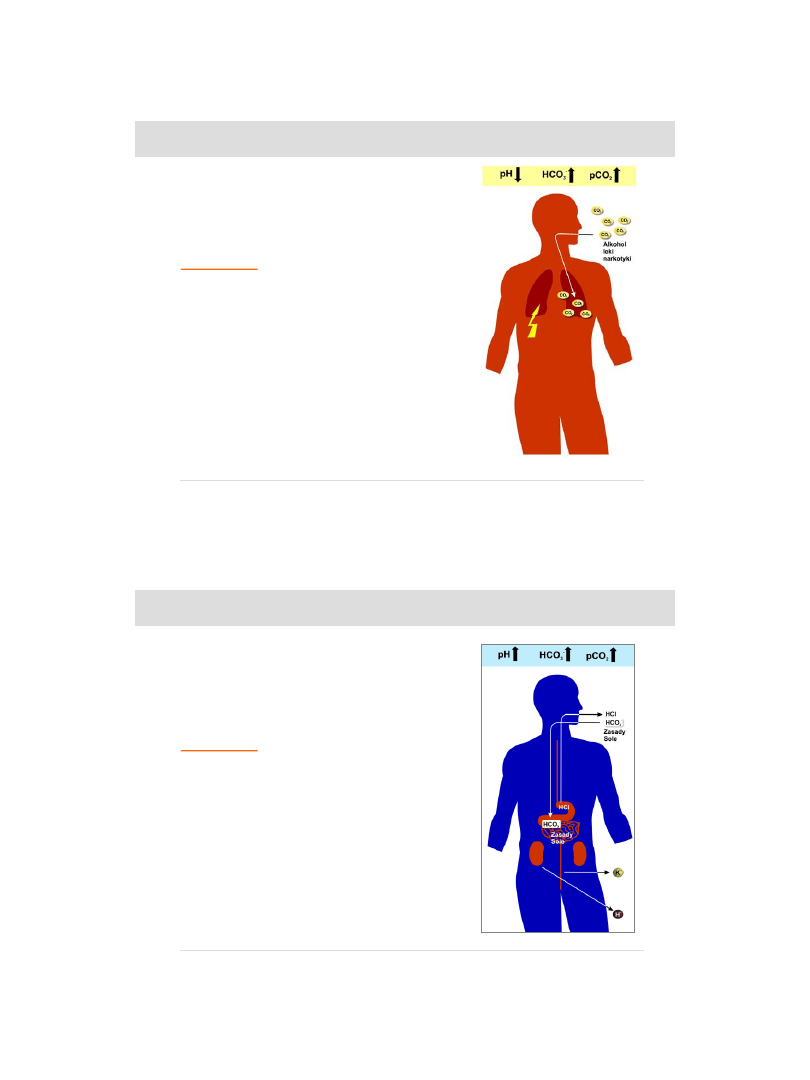
PRZYCZYNY:
ZMNIEJSZONA WENTYLACJA PĘCHERZYKOWA
-
oddychanie powietrzem o dużym stężeniu CO
2
-
zniszczenie miąższu płuc
-
unieruchomienie mięśni oddechowych
-
przedawkowanie leków przeciwbólowych
-
zatrucie alkoholem, morfiną, barbituranami
KWASICA ODDECHOWA
ZABURZENIA GOSPODARKI KWASOWO-ZASADOWEJ
ROZTWORY BUFOROWE
P. Niemiec 2011
ZASADOWICA METABOLICZNA
NIEDOBÓR NaCl, KCl, H
+
PRZYCZYNY:
-
utrata kwaśnej treści żołądka (np. wymioty)
-
nadmierna utrata kwasów z moczem
-
utrata potasu z kałem
-
nadmierna podaż zasad doustnie lub
.....
pozajelitowo
-
nadmierna podaż soli organicznych
ZABURZENIA GOSPODARKI KWASOWO-ZASADOWEJ
2012-02-21
9
ROZTWORY BUFOROWE
P. Niemiec 2011
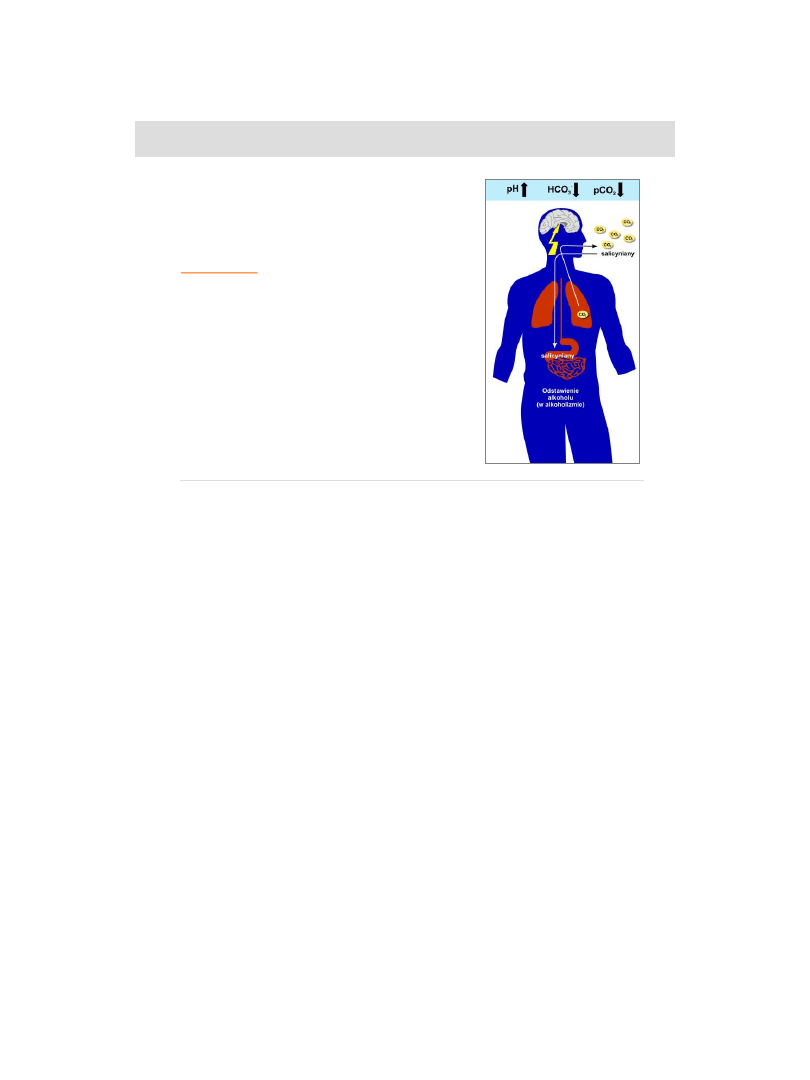
ZASADOWICA ODDECHOWA
PRZYCZYNY:
ZWIĘKSZONA WENTYLACJA PĘCHERZYKOWA
-
zapalenie mózgu i opon mózgowych
-
nowotwory mózgu
-
nagłe odstawienie alkoholu w przewlekłym
.....
alkoholizmie
- zatrucie salicynianami
- stany nerwicowe
ZABURZENIA GOSPODARKI KWASOWO-ZASADOWEJ
Wyszukiwarka
Podobne podstrony:
01 roztwory buforoweid 2924 Nieznany
01 roztwory buforowe 2id 2925 Nieznany (2)
01 roztwory buforoweid 2924 Nieznany
, chemia fizyczna, Równowagi pH w roztworach buforowych
Roztwór buforowy pH 6
Roztwór buforowy pH 1
Roztwór buforowy pH 7
roztwoy buforowe
09 Roztwory buforowe instrukcja
Roztwory buforowe
Roztwór buforowy pH 4
roztwory buforowe
Laboratorium 4 ph, roztwory buforowe
instrukcja - ROZTWORY BUFOROWE, Inżynieria środowiska, inż, Semestr II, Chemia ogólna, laboratorium
więcej podobnych podstron