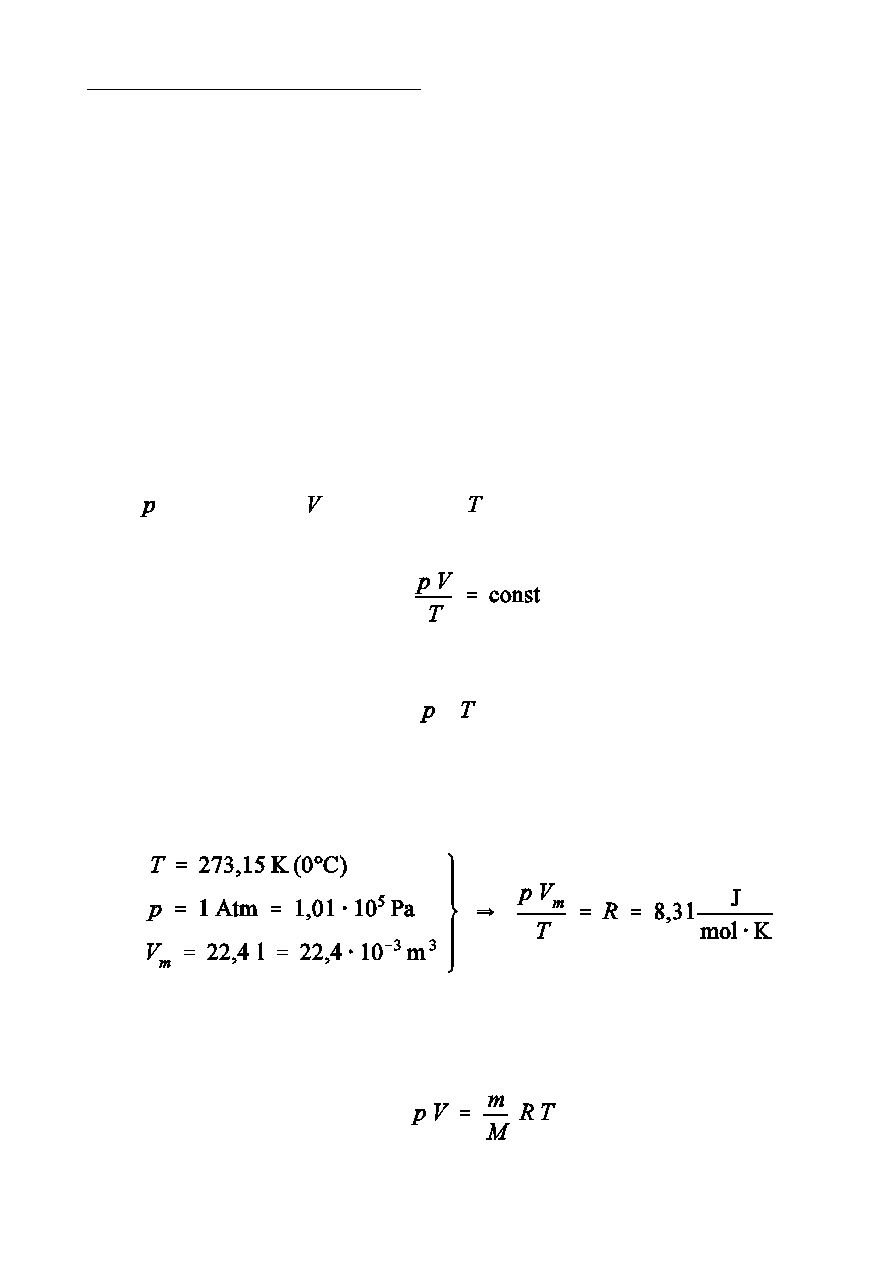
Fizyka cz
steczkowa - wst
p 11
Równanie stanu gazu doskona»ego
Równanie stanu
- równanie wióce parametry stanu
Gaz doskona»y
- gaz, w którym oddzia»ywania midzyczsteczko-
we s pomijalnie ma»e. Kaódy gaz rzeczywisty
pod odpowiednio ma»ym ciÑnieniem ma
w»asnoÑci zblióone do gazu doskona»ego.
Stan gazu doskona»ego jest okreÑlony przez trzy parametry:
-
ciÑnienie,
- objtoÑ,
- temperatura.
Równanie gazu doskona»ego:
Prawo Avogadra
- w warunkach scharakteryzowanych przez te same
parametry i mol kaódego gazu zajmuje t
sam objtoÑ.
Np. w tzw. warunkach normalnych dla jednego mola gazu mamy:
R -
uniwersalna sta»a gazowa
Dla dowolnej masy m gazu:
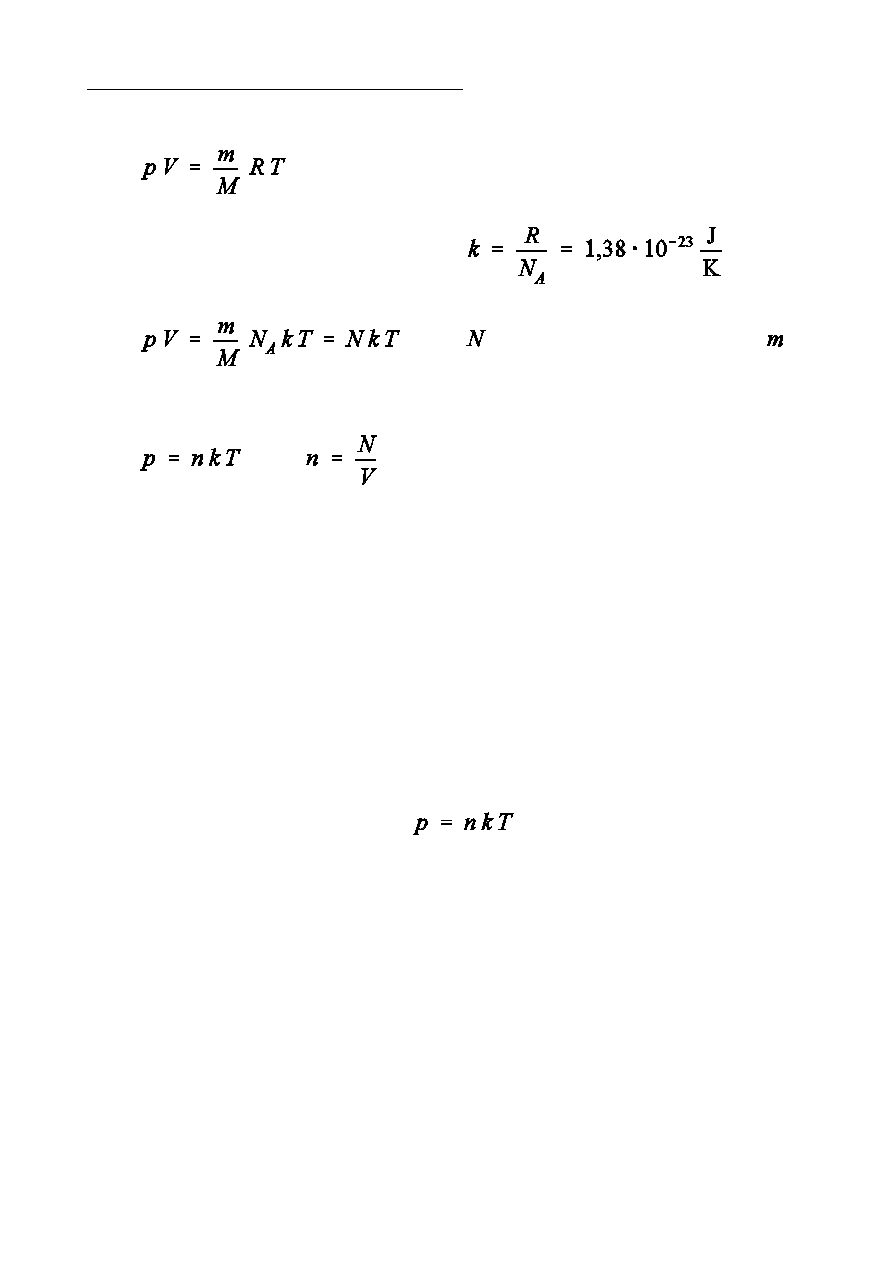
Fizyka cz
steczkowa - wst
p 12
Równanie stanu gazu doskona»ego c.d.
Wprowadïmy sta» Boltzmanna:
,
- liczba czsteczek w masie
,
- liczba czsteczek w jednostce objtoÑci
Przy ustalonej objtoÑci ciÑnienie gazu doskona»ego jest wprost
proporcjonalne do temperatury. Z tego wzgldu gaz doskona»y jest uóywany
jako cia»o termometryczne. Biorc ciÑnienie jako cech termomertyczn,
otrzymuje si termometr o idealnie liniowej skali temperatur, tzw.
doskona»ej gazowej skali temperatur.
Praktyczne znaczenie ma tzw. empiryczna skala temperatur, zbudowana w
oparciu o zastosowanie równania
dla wodoru.
Fizyka cz
steczkowa - wst
p 13
PojemnoÑ cieplna
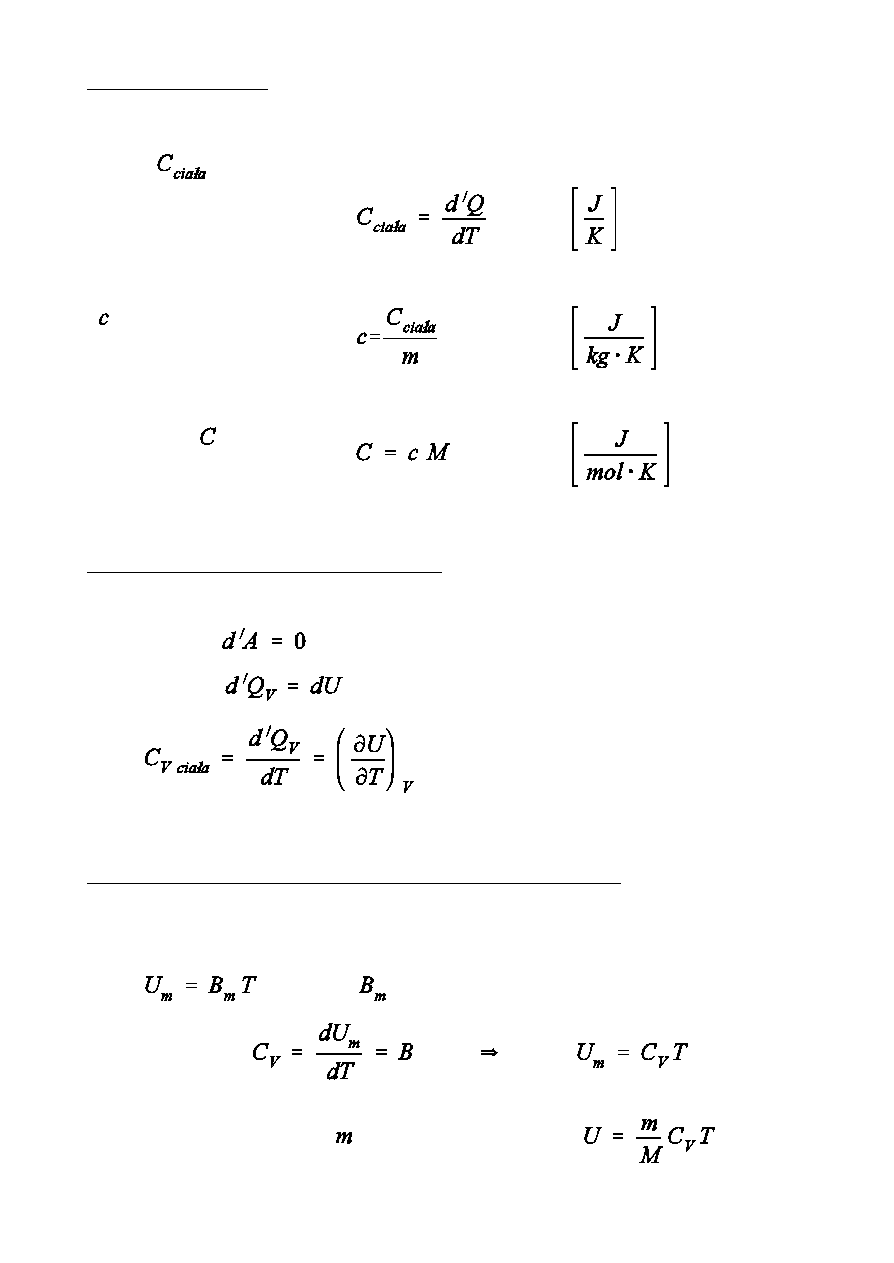
PojemnoÑ cieplna
cia»a,
- iloÑ ciep»a potrzebna do tego, aby podwyószy
temperatur cia»a o jeden kelwin.
Ciep»o w»aÑciwe,
- pojemnoÑ cieplna jednostki masy substancji
Molowe ciep»o
w»aÑciwe,
- pojemnoÑ cieplna mola substancji
PojemnoÑ cieplna w sta»ej objtoÑci
Przy zmianach temperatury cia»a w sta»ej objtoÑci cia»o nie pracy nad
otoczeniem (
) i ca»e ciep»o zamienia si na wzrost energii
wewntrznej (
).
PojemnoÑ cieplna gazu doskona»ego w sta»ej objtoÑci
Z doÑwiadcze½ wynika, óe energia wewntrzna gazu doskona»ego zaleóy
tylko od temperatury. Dla jednego mola gazu moóna napisa
,
- sta»y wspó»czynnik
Std
Dla dowolnej masy
gazu doskona»ego:
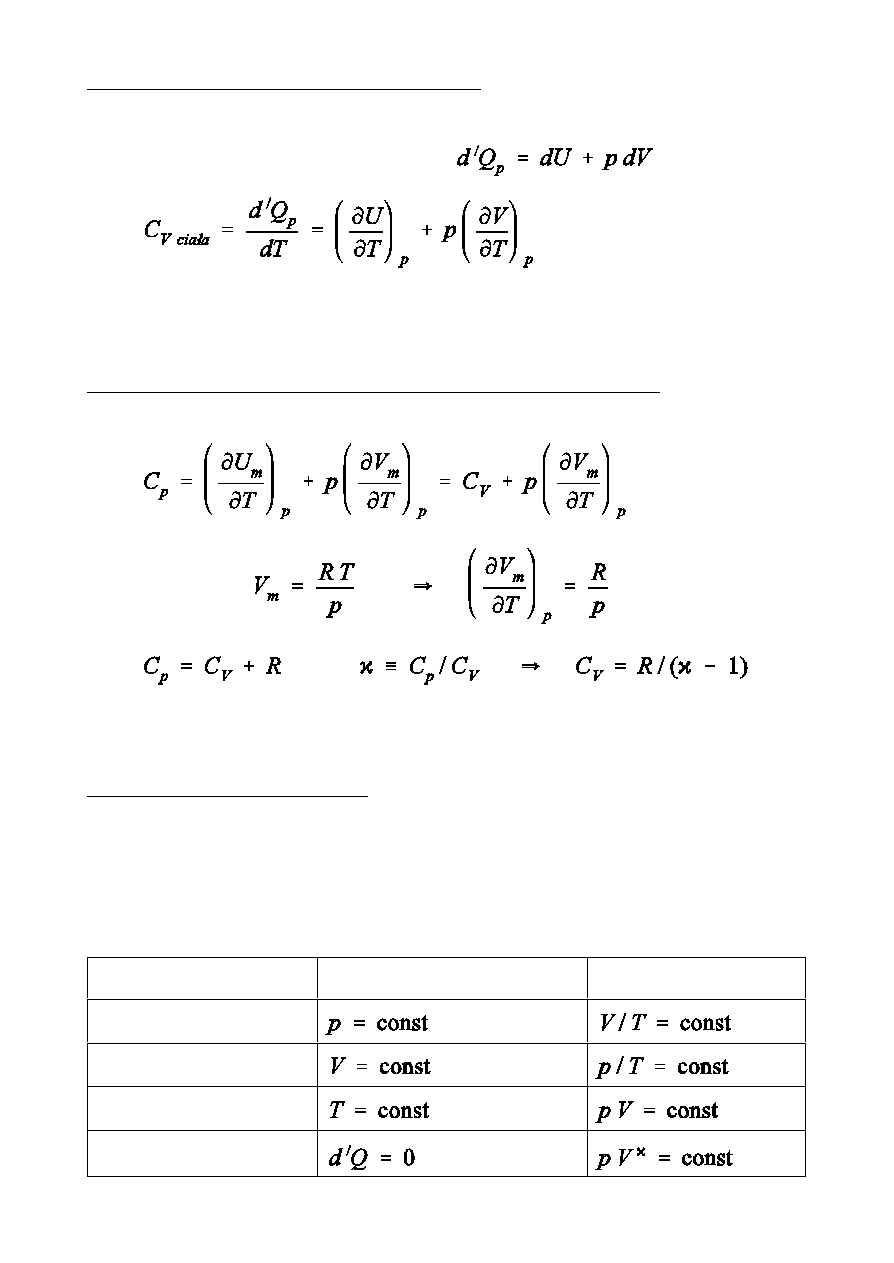
Fizyka cz
steczkowa - wst
p 14
PojemnoÑ cieplna przy sta»ym ciÑnieniu
Przy zmianach temperatury cia»a przy sta»ym ciÑnieniu oprócz zmian energii
wewntrznej wykonywana jest praca (
).
PojemnoÑ cieplna gazu doskona»ego przy sta»ym ciÑnieniu
Dla jednego mola gazu doskona»ego mamy
,
Przemiany gazu doskona»ego
SpoÑród wielu moóliwych przemian gazu doskona»ego na wyróónienie
zas»uguj przemiany, w których - oprócz równania stanu - spe»niony jest
dodatkowy warunek okreÑlajcy rodzaj przemiany
Rodzaj przemiany
Dodatkowy warunek
Równanie stanu
Izobaryczna
Izochoryczna
Izotermiczna
Adiabatyczna
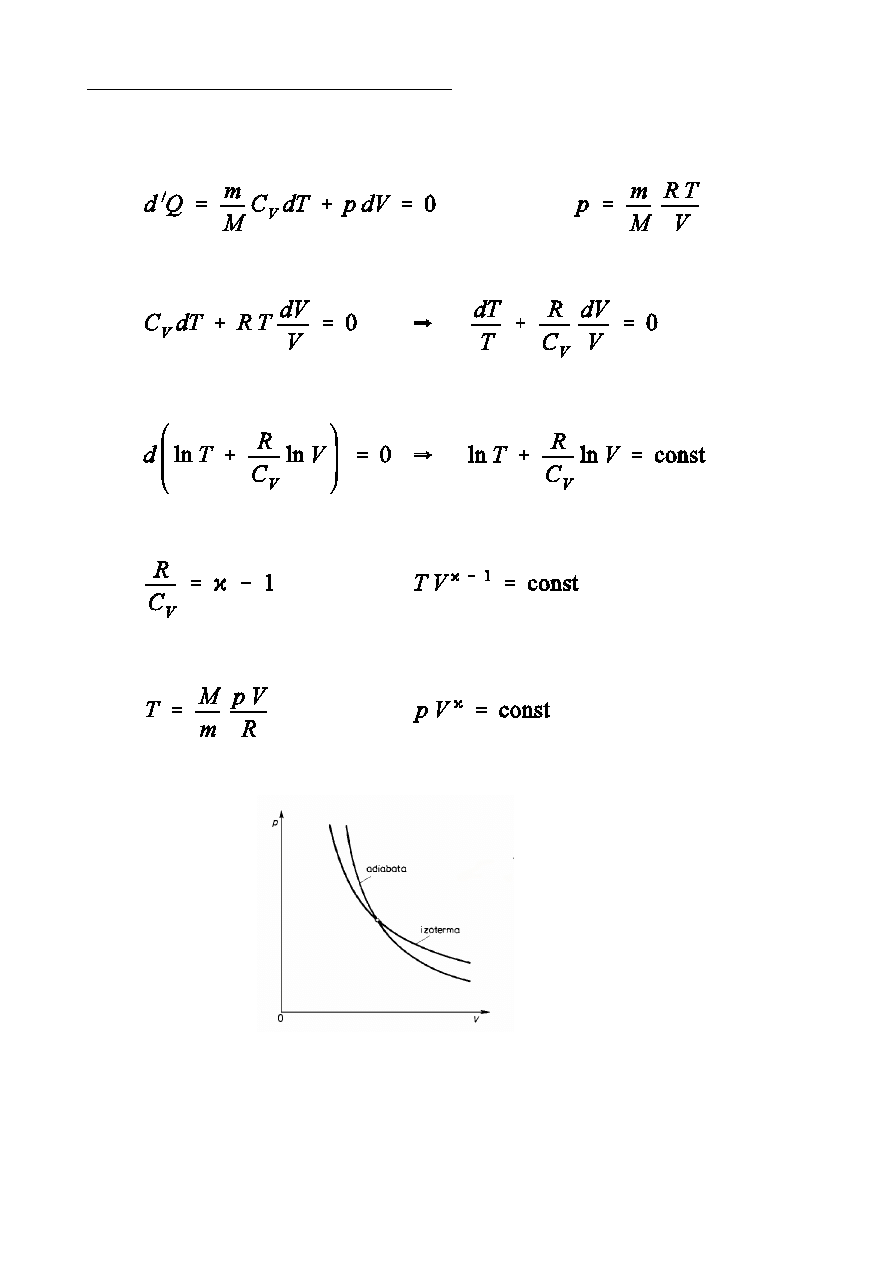
Fizyka cz
steczkowa - wst
p 15
Równanie adiabaty gazu doskona»ego
Przemiana adiabatyczna jest procesem zachodzcym bez wymiany ciep»a z
otoczeniem.
,
(równanie Poissona)
Przyk»adem przemiany adiabatycznej moóe by spróanie i rozpróanie gazu
przy rozchodzeniu si w gazie fali dïwikowej w odniesieniu do ma»ych
objtoÑci.
Fizyka cz
steczkowa - wst
p 16
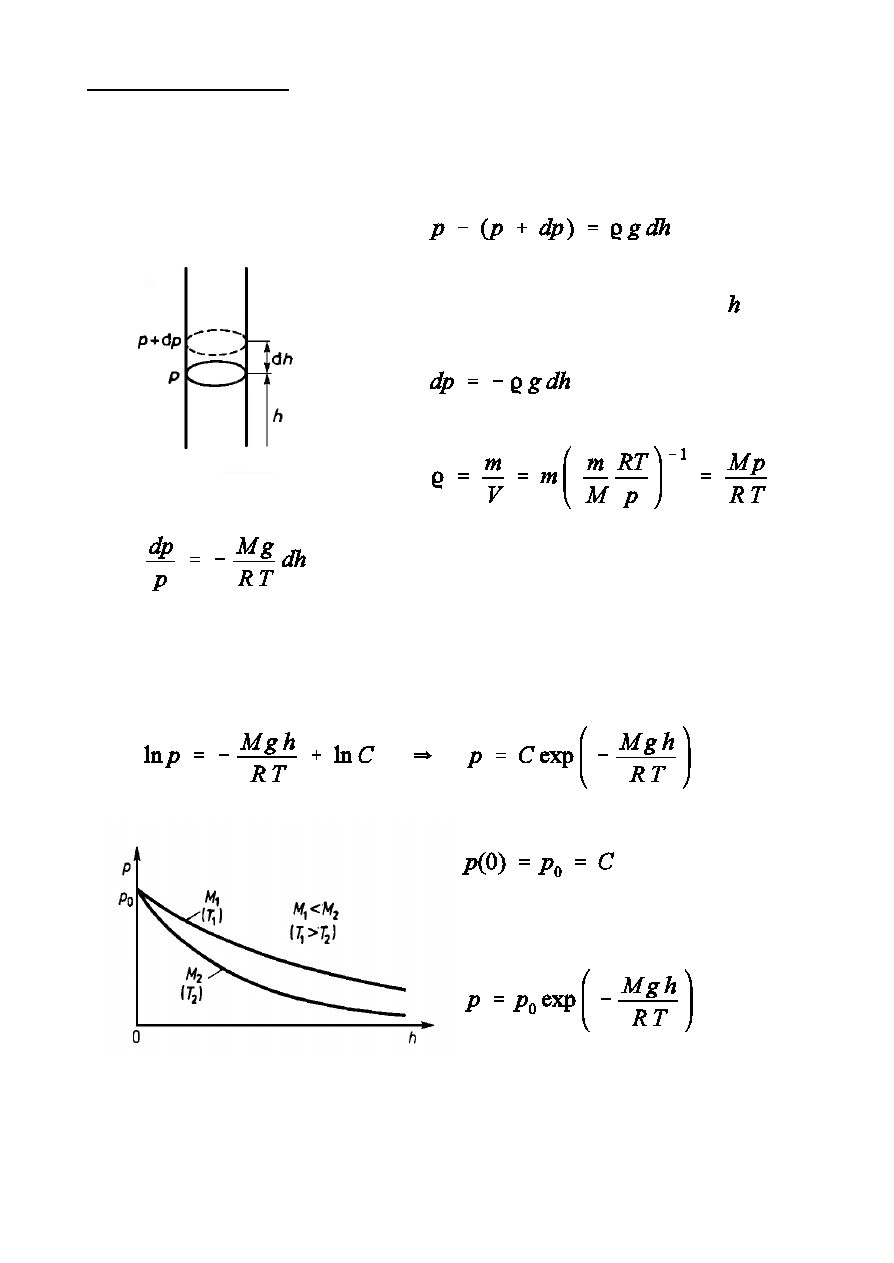
Wzór barometryczny
Wzór barometryczny okreÑla zaleónoÑ ciÑnienia powietrza od wysokoÑci.
Znajdïmy jego posta analizujc w»aÑciwoÑci s»upa gazu zawartego w walcu
o jednostkowej podstawie.
k - gstoÑ gazu na wysokoÑci
W przypadku atmosfery izotermicznej (T = const) w wyniku ca»kowania
otrzymujemy
Wzór barometryczny
Dla powietrza wielkoÑ M oznacza Ñredni mas czsteczkow, obliczon na
podstawie zawartoÑci azotu, tlenu i innych gazów w powietrzu.
Document Outline
Wyszukiwarka
Podobne podstrony:
a06 fizyka czasteczkowa wstep (01 10) IZBOIUERU3RODLRV2 (2)
sprawka fizyka nr [00,11,13,32,51,53] 16 sprawko
CERN FIZYKA CZASTEK ELEMENTARNY Nieznany
2010 08 11 16 29 37
7133 TSCM 52 2 parte (11 16)
2001 11 16
2,6,11,16 Stochniał
Sprawozdanie6, dc, GPF, Fizyka lab, Ćw. 11
rys, Elektrotechnika AGH, Semestr II letni 2012-2013, Fizyka II - Laboratorium, 11 Poziomy energetyc
2003 11 16
więcej podobnych podstron