
ŁAŃCUCH
ODDECHOWY
(=ŁAŃUCH TRANSPORTU
ELEKTRONÓW)
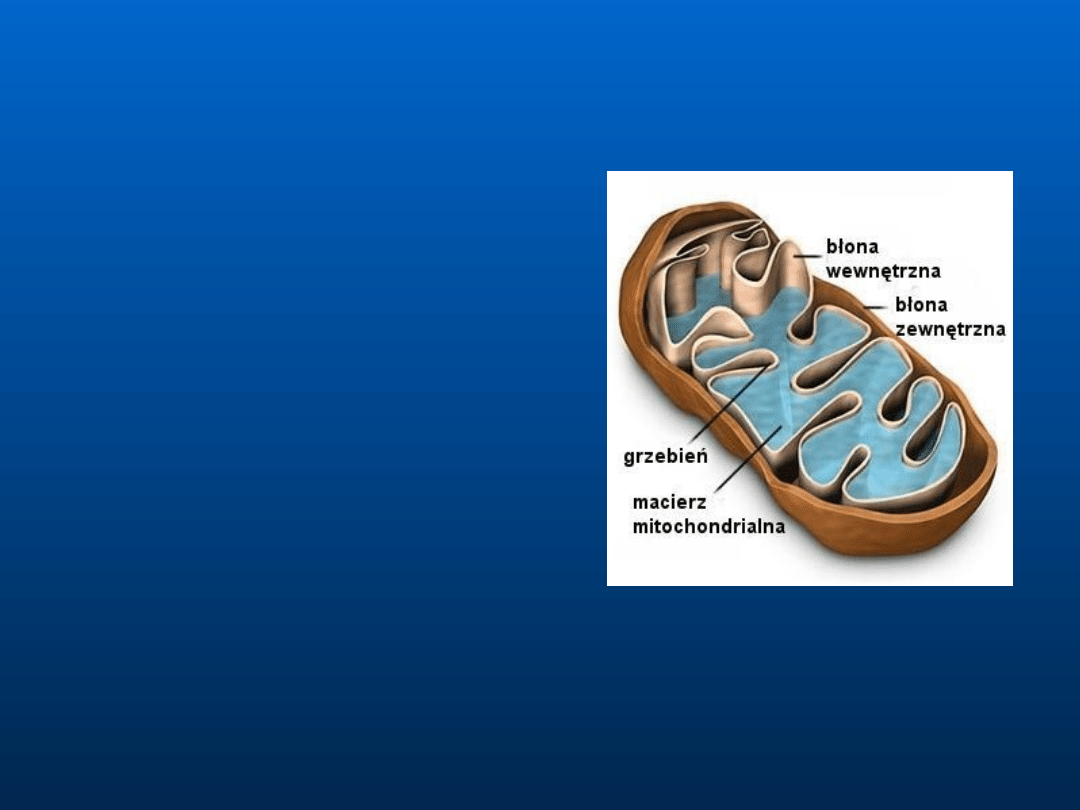
W organizmach
eukariotycznych
transport elektronów
zachodzi w
wewnętrznej błonie
mitochondrialnej.

W łańcuchu
W łańcuchu
oddechowym dokonuje
oddechowym dokonuje
się powtórne utlenianie
się powtórne utlenianie
cząsteczek NADH i
cząsteczek NADH i
FADH
FADH
2
2
pochodzących z
pochodzących z
cyklu kwasu
cyklu kwasu
cytrynowego, glikolizy i
cytrynowego, glikolizy i
utleniania kwasów
utleniania kwasów
tłuszczowych oraz
tłuszczowych oraz
przechwytywanie
przechwytywanie
uwalnianej energii do
uwalnianej energii do
syntezy ATP
syntezy ATP
(fosforylacja
(fosforylacja
oksydacyjna).
oksydacyjna).

CHEMIOSMOZA-podstawowe założenia
Łańcuch akceptorów elektronów w głębi wewnętrznej
błony.
Podczas przekazywania atomów wodoru z jednego
akceptora na drugi protony wodoru (H
+
) oddzielają się
od swych elektronów.
Elektrony przechodząc przez szereg akceptorów tracą
większość energii na rzecz transportu protonów przez
wewnętrzną błonę.
Gradient elektrochemiczny dostarcza energii do syntezy
ATP.
Akceptory elektronów: FMN (mononukleotyd
flawinowy), ubichinon(CoQ) oraz cytochromy.
Ostatni cytochrom a
3
przekazuje dwa elektrony na
cząsteczkę tlenu czyniąc go końcowym akceptorem
wodoru.
Brak tlenu hamuje syntezę ATP.
Z każdej cząsteczki NADH powstają 3 cz. ATP, a z
FADH
2
– 2 cz.
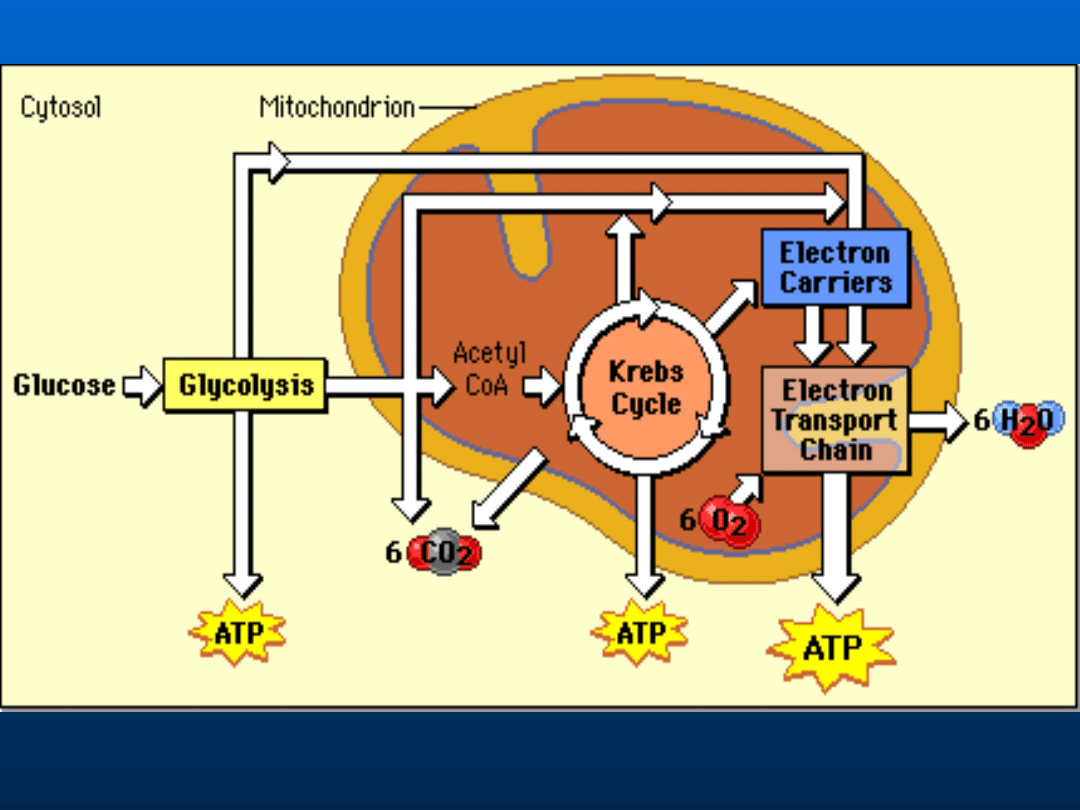
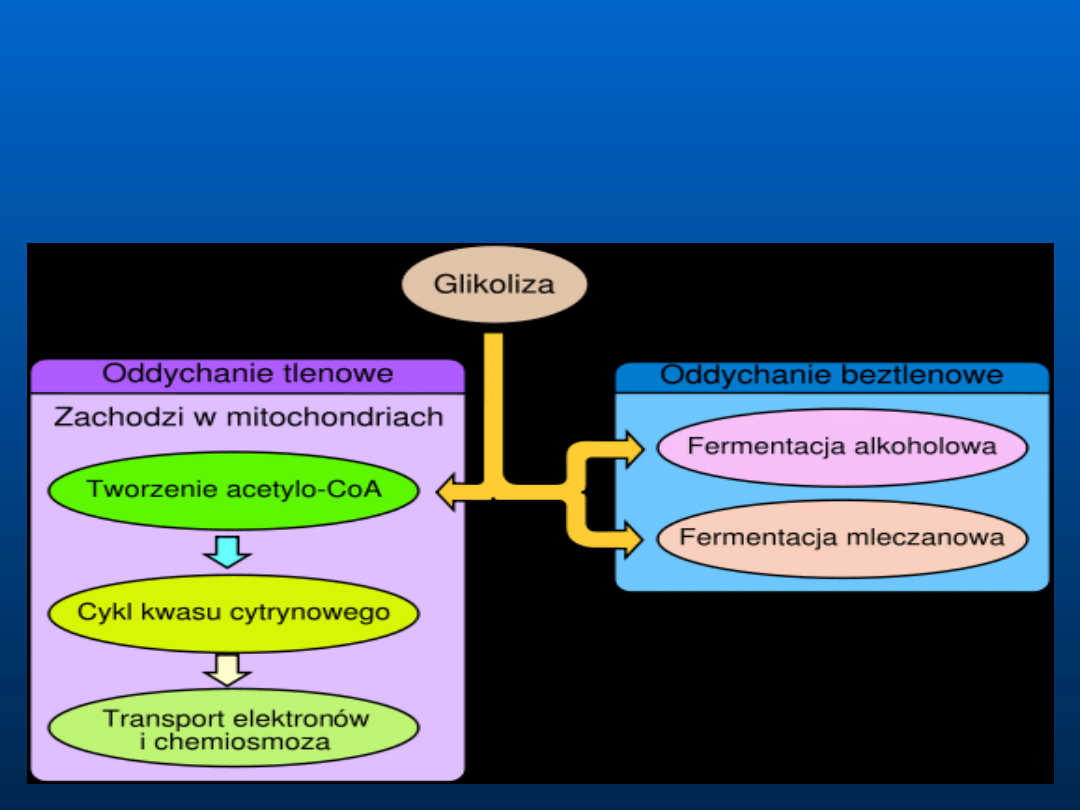
Różne szlaki oddychania
Różne szlaki oddychania
komórkowego
komórkowego
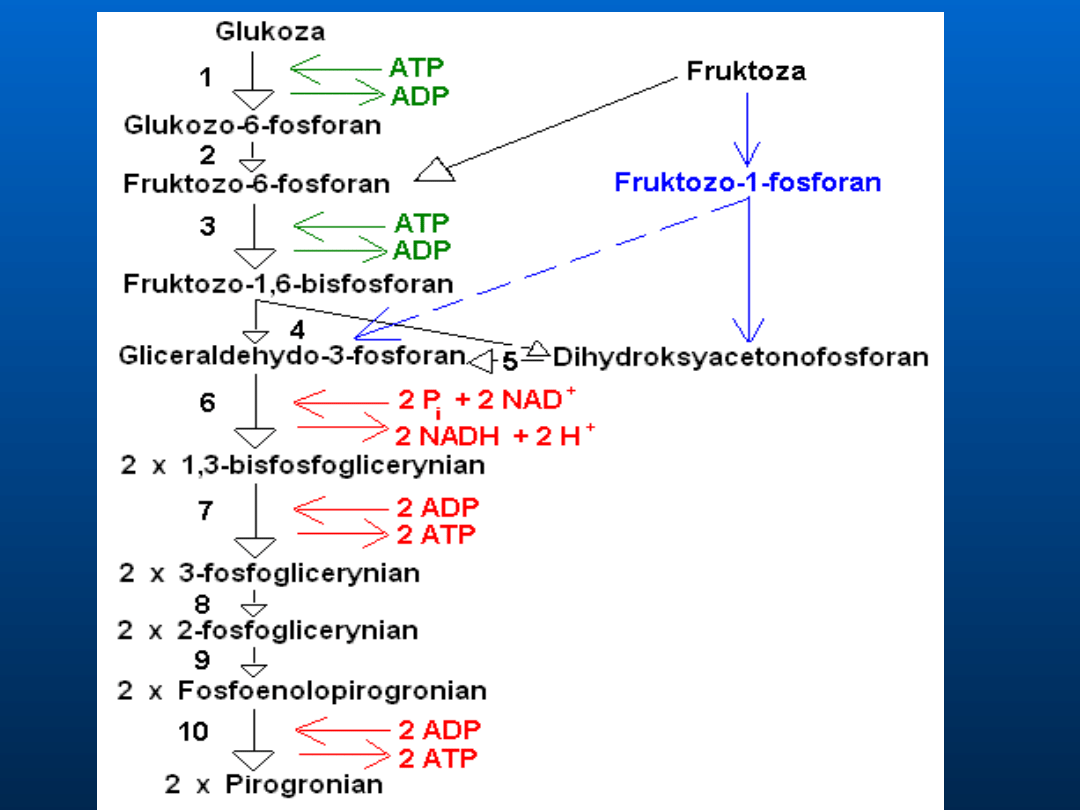
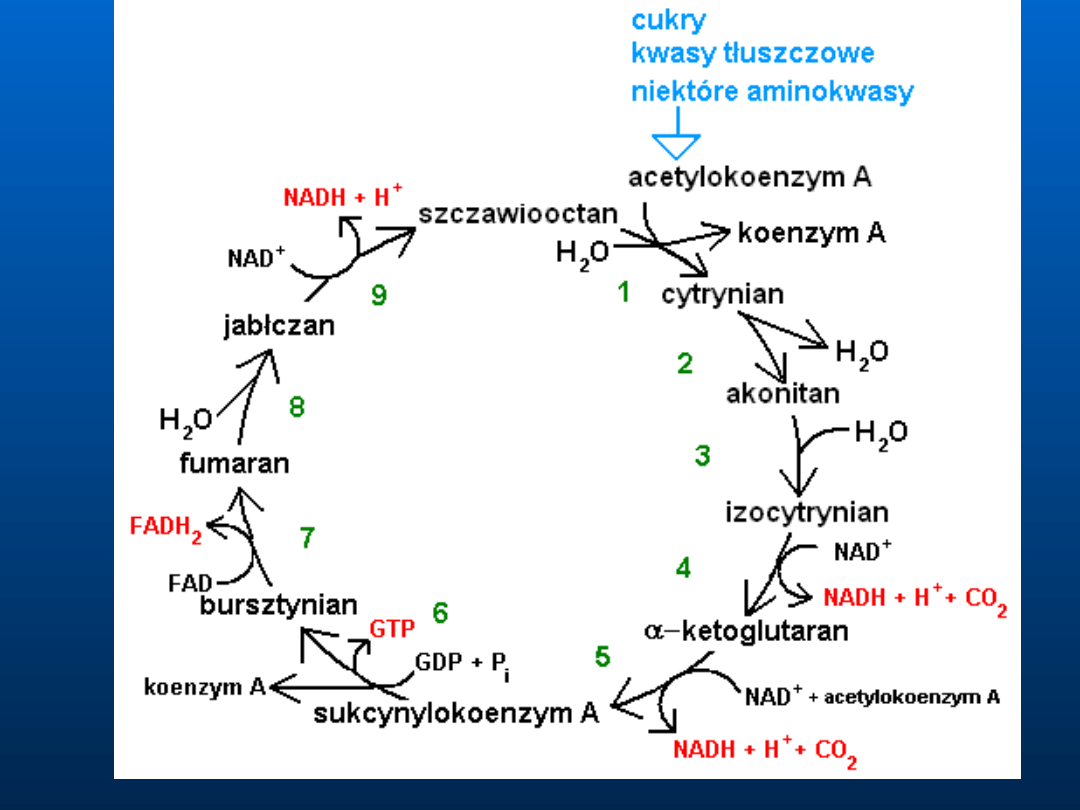

Transport elektronów zaliczany jest
do reakcji oksyredukcyjnych, czyli
takich w których utlenianie (utrata
elektronów) jednej cząsteczki pociąga
za sobą redukcję innej (przyjęcie
elektronów) nie dochodzi do
tworzenia lub niszczenia elektronów.
NADH + H
+
+ ½ O
2
NAD
+
+ H
2
O
Przepływ elektronów przez te
kompleksy powoduje przepływ
protonów w poprzek błony
(od matrix do przestrzeni
międzybłonowej)

Zasady dotyczące funkcjonowania
Zasady dotyczące funkcjonowania
łańcucha oddechowego
łańcucha oddechowego
1.
1.
Składniki łańcucha oddechowego różnią się
Składniki łańcucha oddechowego różnią się
powinowactwem do elektronów – wzrasta ono w
powinowactwem do elektronów – wzrasta ono w
miarę przebiegu łańcucha
miarę przebiegu łańcucha
2.
2.
Powinowactwo do elektronów = potencjał
Powinowactwo do elektronów = potencjał
oksydacyjno–redukcyjny = energia swobodna
oksydacyjno–redukcyjny = energia swobodna
3.
3.
Elektrony (z NADH i FADH
Elektrony (z NADH i FADH
2
2
) wchodzą w łańcuch
) wchodzą w łańcuch
oddechowy z wysoką energią i w trakcie transportu
oddechowy z wysoką energią i w trakcie transportu
energię tę powoli tracą.
energię tę powoli tracą.
4.
4.
W miejscach, w których uwalniana jest wystarczająca
W miejscach, w których uwalniana jest wystarczająca
ilość energii dochodzi do pompowania protonów
ilość energii dochodzi do pompowania protonów
5.
5.
O powinowactwie do elektronów, a więc ilości
O powinowactwie do elektronów, a więc ilości
uwalnianej energii decydują głównie elementy
uwalnianej energii decydują głównie elementy
niebiałkowe, tkwiące w kompleksach łańcucha
niebiałkowe, tkwiące w kompleksach łańcucha
oddechowego
oddechowego
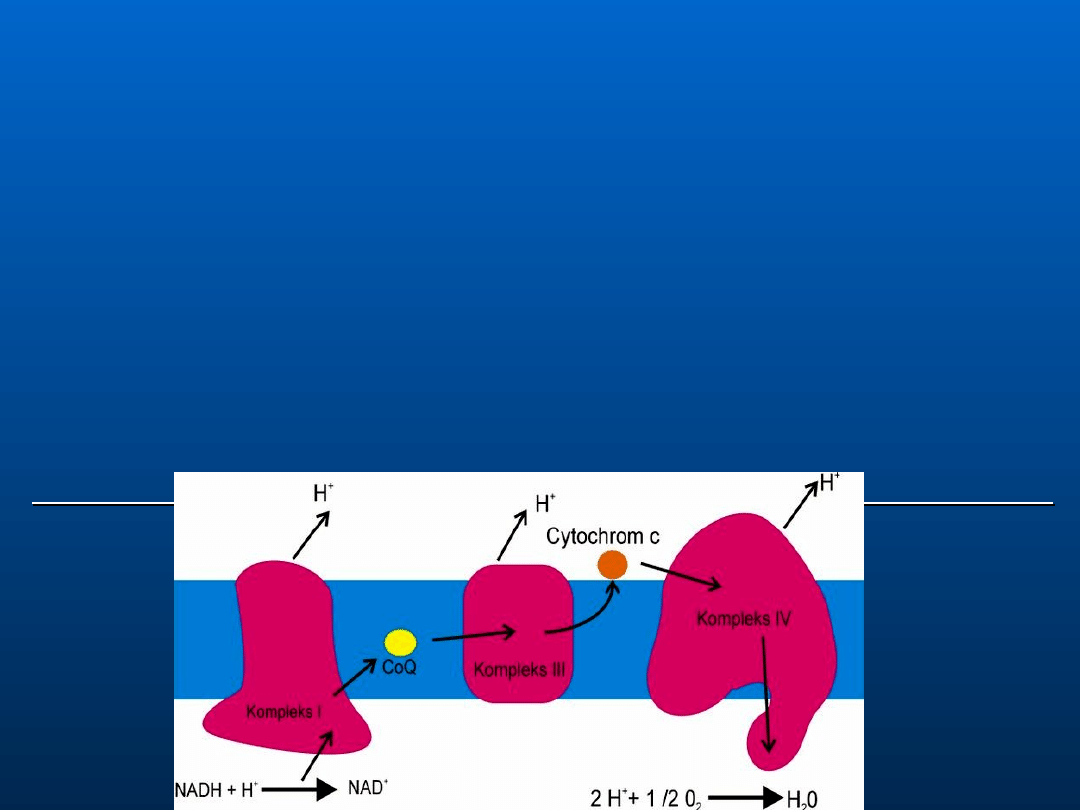
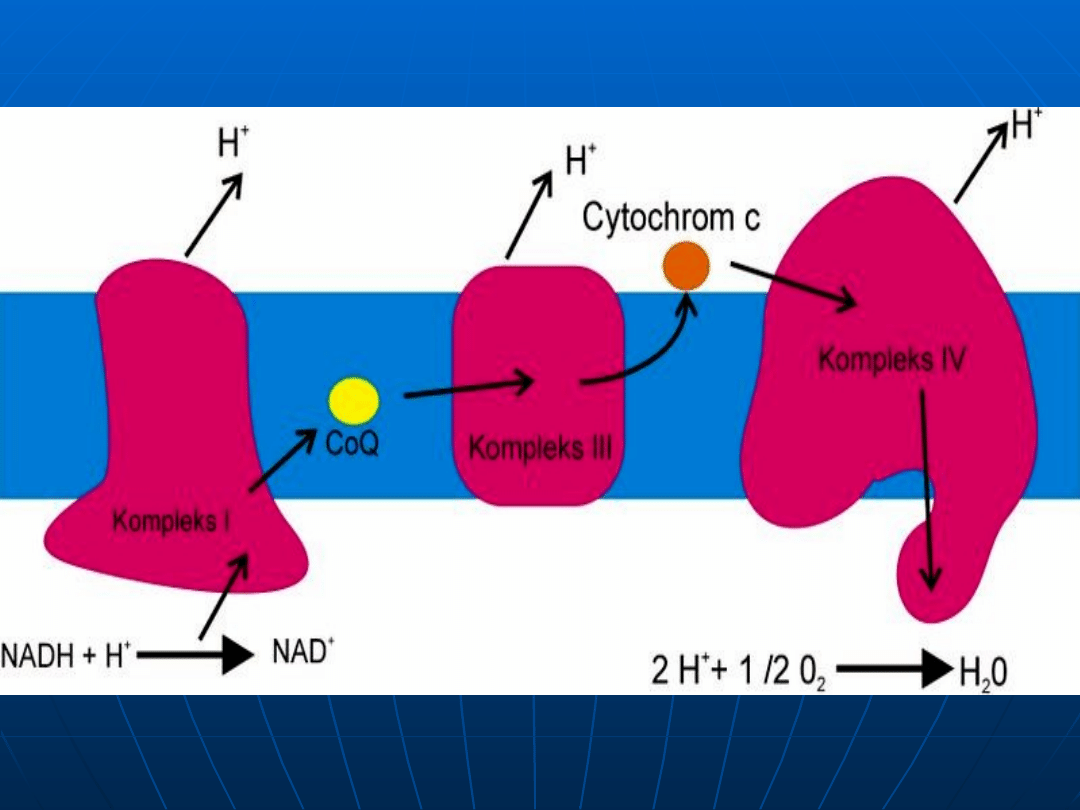
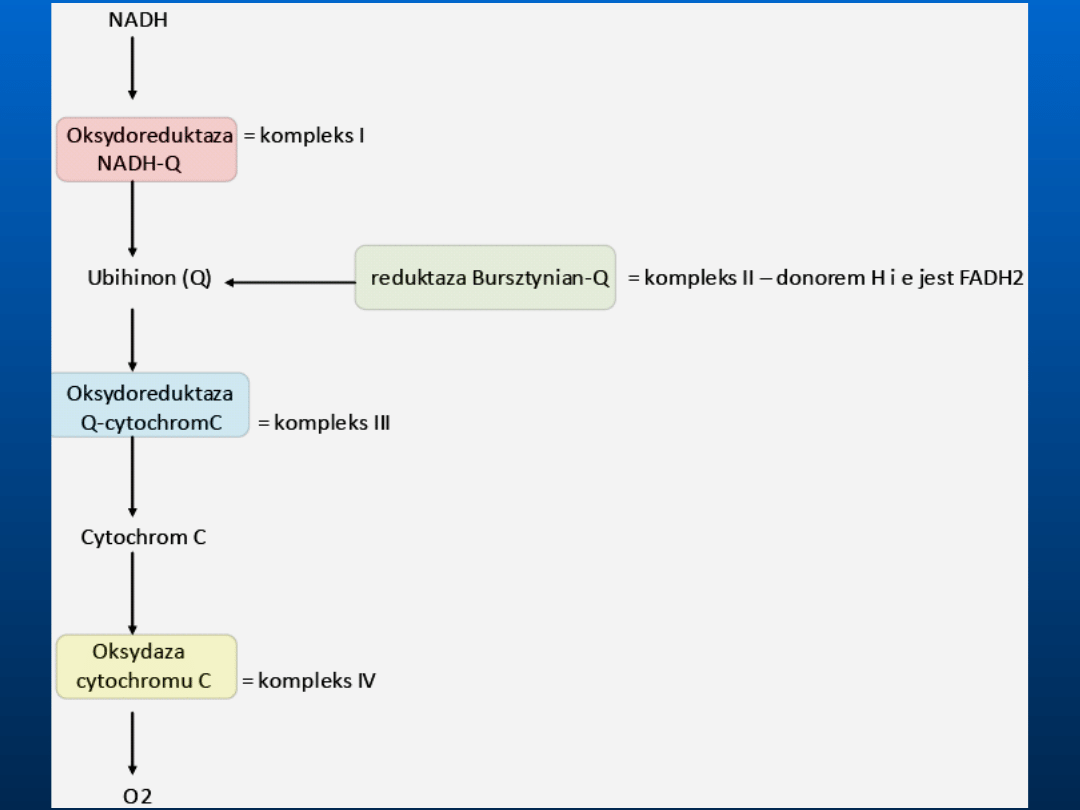
Łańcuch oddechowy składa się z trzech wielkich
Łańcuch oddechowy składa się z trzech wielkich
kompleksów białkowych, które pompują protony
kompleksów białkowych, które pompują protony
podczas przepływu elektronów:
podczas przepływu elektronów:
•
oxydoreduktaza NADH-CoQ,
oxydoreduktaza NADH-CoQ,
•
oxydoreduktaza-bursztynian Q
oxydoreduktaza-bursztynian Q
(
(
nie pompuje
nie pompuje
protonów
protonów
kompleks fizycznie związany z cyklem Krebsa
).
).
•
oxydoreduktaza cytochromowa
oxydoreduktaza cytochromowa
•
oksydaza cytochromowa
oksydaza cytochromowa
•
Te cztery kompleksy noszą nazwy: kompleks I, II, III, IV.
Te cztery kompleksy noszą nazwy: kompleks I, II, III, IV.

Organizacja mitochondrialnego
Organizacja mitochondrialnego
łańcucha oddechowego (1)
łańcucha oddechowego (1)
Kompleks enzymatyczny
Kompleks enzymatyczny
Masa
Masa
(Da)
(Da)
Grupa
Grupa
prostetyczna
prostetyczna
I
I
oksydoreduktaza NADH-CoQ
oksydoreduktaza NADH-CoQ
85000
85000
FMN
FMN
FeS
FeS
II
II
oksydoreduktaza bursztynian-
oksydoreduktaza bursztynian-
CoQ
CoQ
97000
97000
FAD
FAD
FeS
FeS
III
III
oksydoreduktaza CoQH
oksydoreduktaza CoQH
2
2
-
-
cytochrom c
cytochrom c
287000
287000
hem b
hem b
561
561
hem b
hem b
566
566
hem c
hem c
1
1
FeS
FeS
cytochrom c
cytochrom c
13000
13000
hem c
hem c
IV
IV
oksydaza cytochromu c
oksydaza cytochromu c
200000
200000
hem a
hem a
hem a
hem a
3
3
Cu
Cu
a
a
i Cu
i Cu
b
b
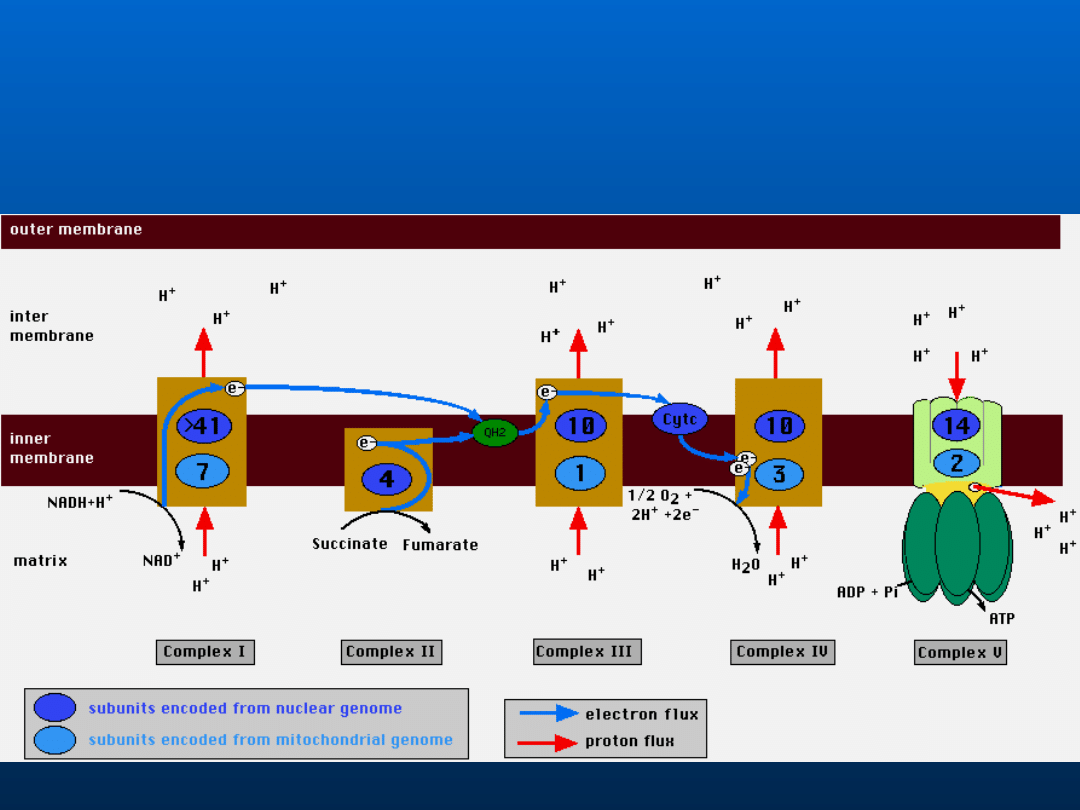
Organizacja mitochondrialnego
Organizacja mitochondrialnego
łańcucha oddechowego (2)
łańcucha oddechowego (2)

•
Elektrony przenoszone są z oxydoreduktazy
Elektrony przenoszone są z oxydoreduktazy
NADH-Q do drugiego kompleksu łańcucha
NADH-Q do drugiego kompleksu łańcucha
(oxydoreduktazy cytochromowej) przez
(oxydoreduktazy cytochromowej) przez
redukowaną formę ubichinonu, nazywanego także
redukowaną formę ubichinonu, nazywanego także
koenzymem Q (skrót CoQ).
koenzymem Q (skrót CoQ).
•
Ubichinon przenosi również elektrony z FADH
Ubichinon przenosi również elektrony z FADH
2
2
do
do
oxydoreduktazy cytochromowej.
oxydoreduktazy cytochromowej.
•
Następnie małe białko cytochrom c transportuje
Następnie małe białko cytochrom c transportuje
elektrony na oksydazę cytochromową, będącą
elektrony na oksydazę cytochromową, będącą
końcowym składnikiem łańcucha.
końcowym składnikiem łańcucha.
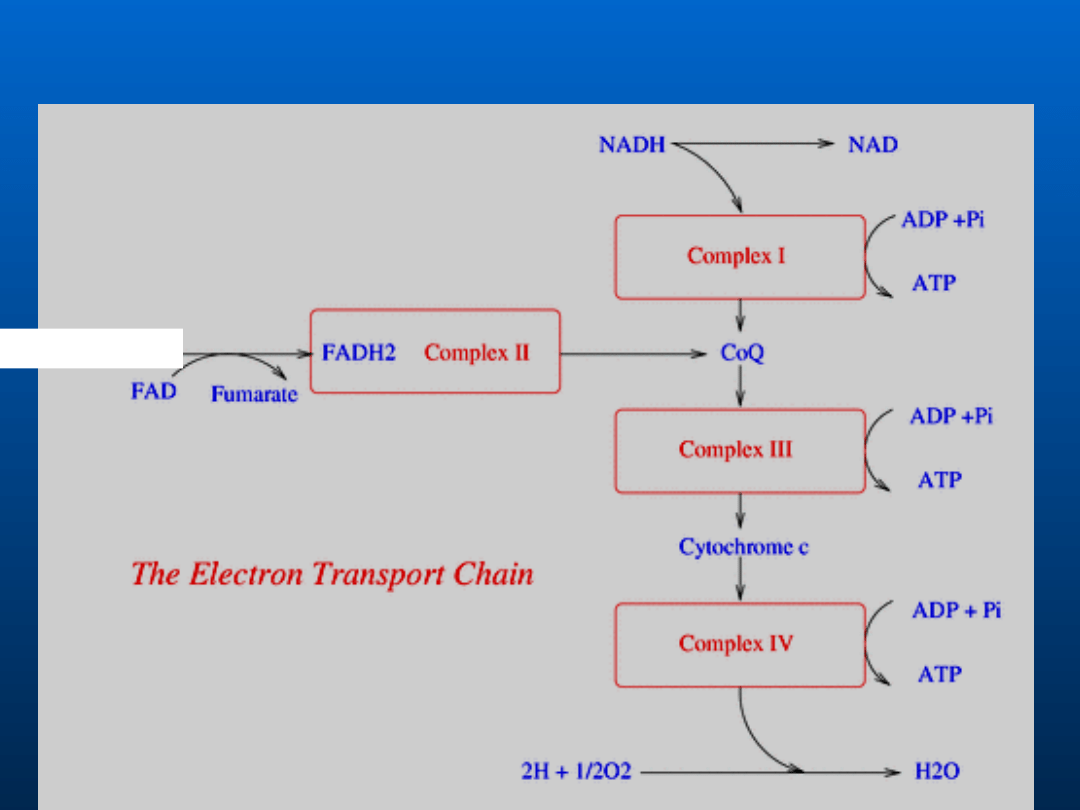
Ogólny schemat łańcucha transportu
elektronów
bursztynian
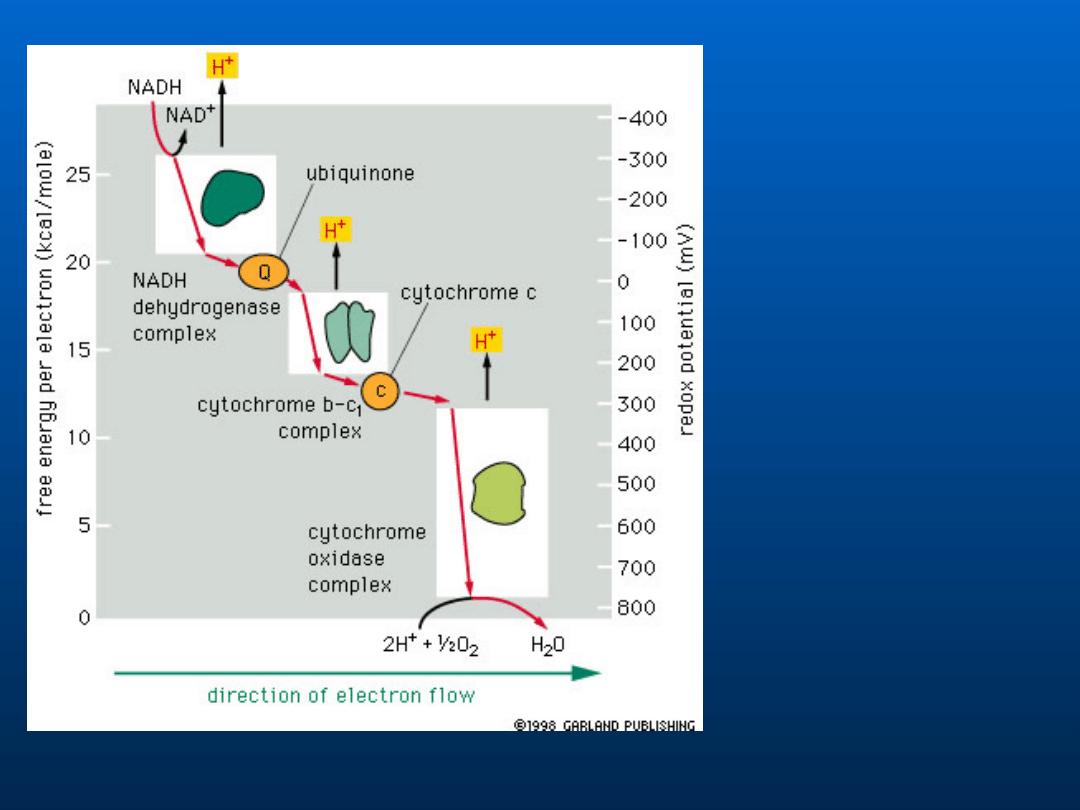
W miejscach, w których
uwalniana jest
wystarczająca ilość
energii dochodzi
do pompowania
protonów

Koenzym Q
pochodna chinonowa z długim ogonem
izoprenowym (liczba jednostek izoprenowych
zależna od gatunku, człowiek ma Q10).
- występuje w 3 stanach utlenienia:
1.
najbardziej utleniona forma Q ma dwie grupy
ketonowe
2.
dołączenie 1 elektronu i 1 protonu powoduje
przejście do semichinonu (QH )
3.
po dołączeniu kolejnego protonu i elektronu
powstaje QH2 - ubichinon
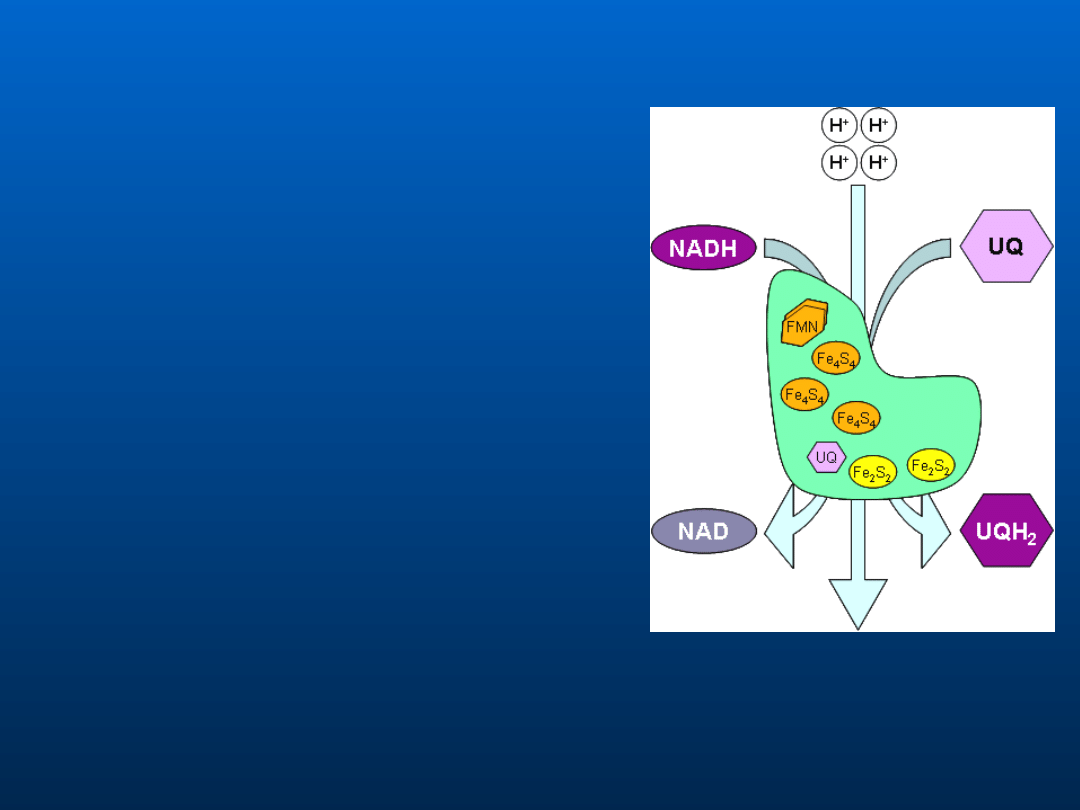
Reduktaza
NADH-Q
(dehydrogenaza NADH)
1.Zawiązanie NADH i przeniesienie
jego dwóch elektronów na
FMN(mononukleotyd flawonowy),
który przechodzi w formę
zredukowaną FMNH
2
NADH + H
+
+ FMN FMNH
2
+
NAD
+
2.Następnie elektrony przekazywane
są na szereg centrów żelazo
siarkowych (Fe-S), w którym elektron
jest przenoszony przez atom Fe
(przechodzi on ze stanu Fe
3+
na Fe
2+
)
3.Dalej elektron jest przyjmowany
przez ubichinon (CoQ), który może
przyjąć aż dwa elektrony i dwa jony
H
+
. W ten sposób ubichinon
przekształca się w ubichinol (CoQH
2
)
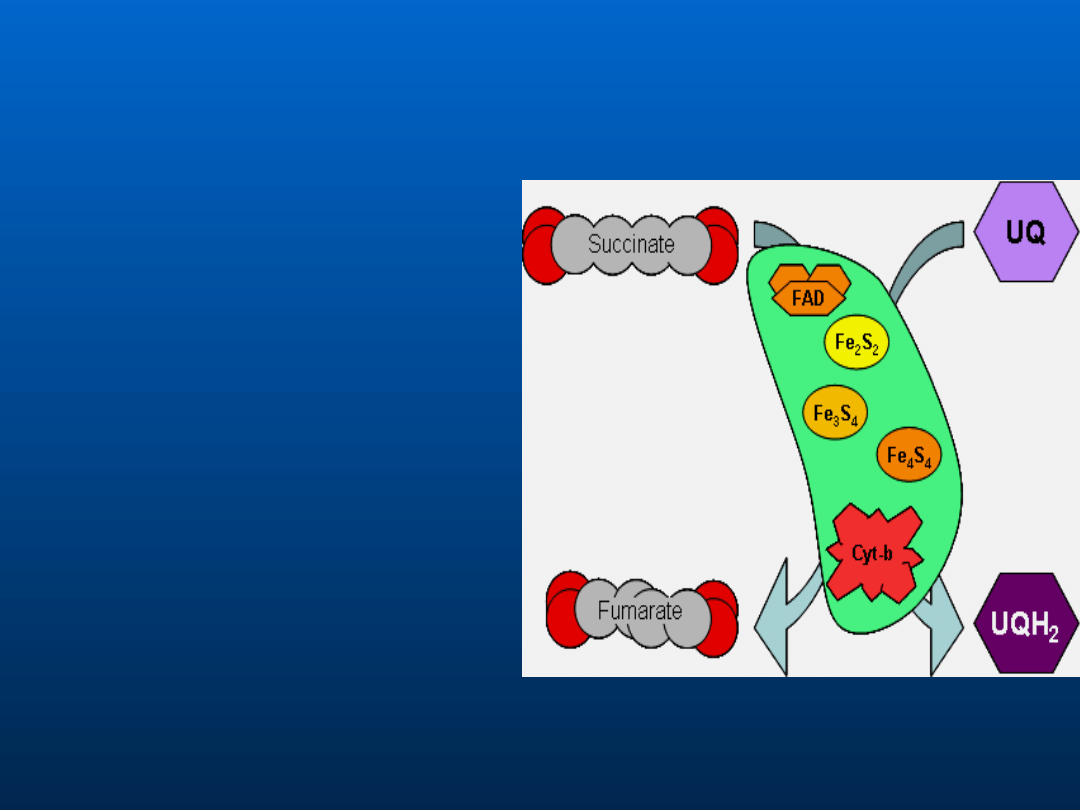
Reduktaza bursztynian-
koenzym Q
Ubichinol jest także
miejscem wejścia dla
elektronów z FADH
2
, który
jest tworzony w cyklu
kwasu cytrynowego
podczas utleniania
bursztynianu do fumaranu
przez dehydrogenazę
bursztynianową.
1.FADH
2
jest utleniany i
podczas tego procesu dwa
elektrony przechodzą do
centrów Fe-S.
2.Dalej przechodzą na
ubichinon,a później
wchodzą do głównego
łańcucha transportu
elektronów.
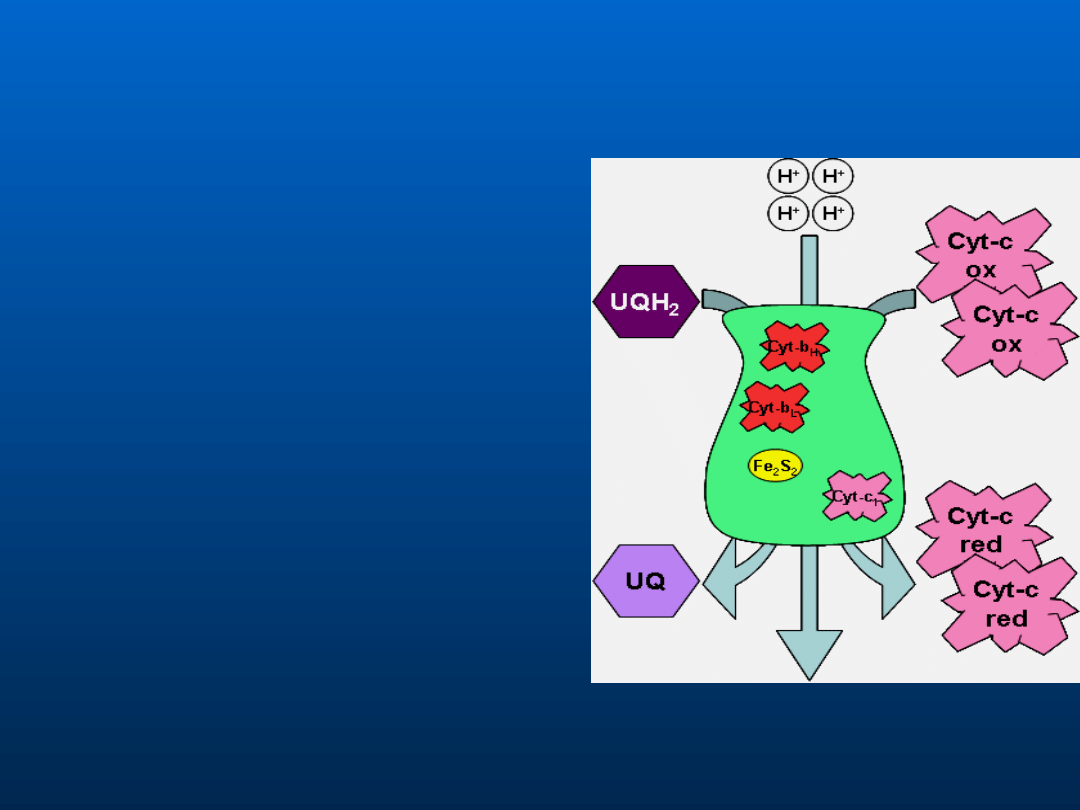
Reduktaza cytochromowa
(kompleks cytochromów b-c
1
)
W reduktazie tej umieszczone
są dwa typy cytochromów b i
c
1
, także białka Fe-S i kilka
innych łańcuchów
polipeptydowych. Cytochromy
są białkami transportującymi
elektrony, które mają grupę
hemową zawierającą atom
żelaza.
Ubichinol jest przenośnikiem
dwuelektronowym, a
cytochromy są przenośnikami
jednoelektronowymi, dlatego
droga transportu elektronów
jest skomplikowana.
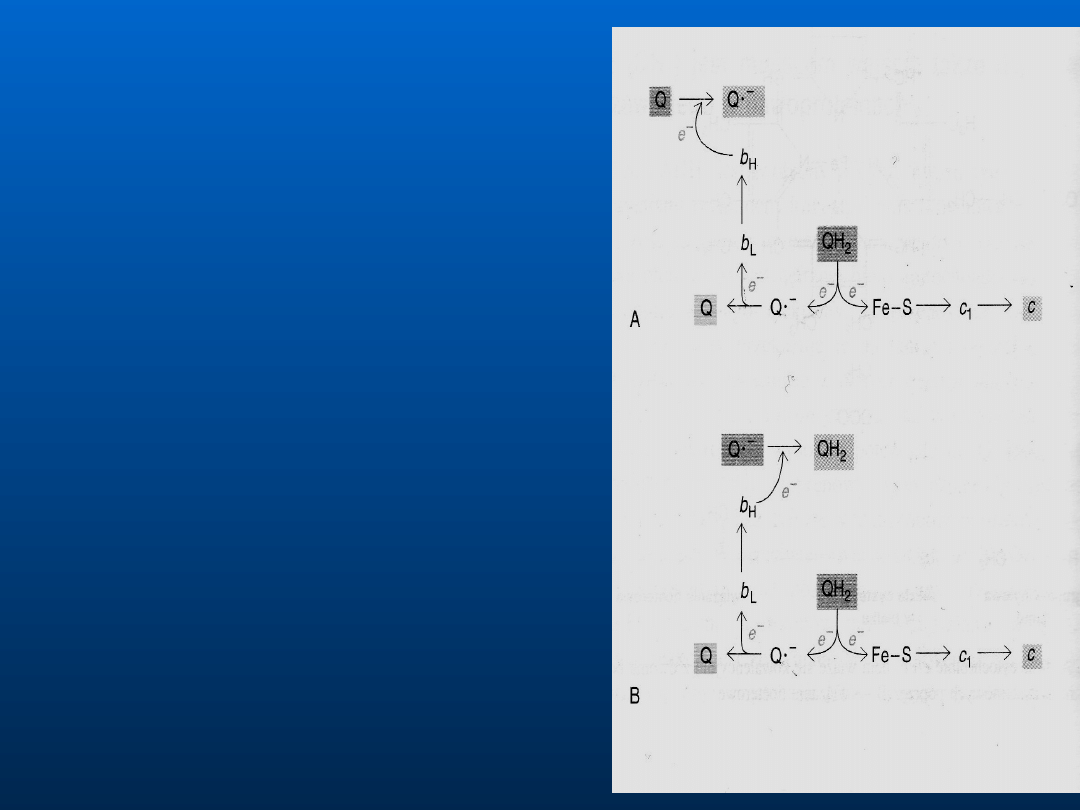
1.Ubichinol uwalnia jeden elektron
i jon H
+
do kompleksu Fe-S, dalej
przechodzi kolejno do cyt-c
1
i cyt-c
(ubchinol przekształca się w anion
semichinionowy (CoQ
. -
)
2. Do transportu elektronów włącza
się cytochrom b, który zawiera
dwie grupy hemowe: hem b
H
i hem
b
L
. CoQ
. -
oddaje swój elektron na
hem b
L
i wraca do postaci CoQ.
3. Hem b
L
redukuje hem b
H
, a ten
redukuje zawiązany CoQ do CoQ
. -
.
Na tym etapie przeprowadzana jest
tylko połowa procesu, gdyż tylko
jeden z dwóch elektronów
oddawanych przez CoQH
2
jest
przenoszony na cyt-c. Drugi czeka
w postaci zwiazanego CoQ
. -

4. Druga cząsteczka
ubichinolu wchodzi w
reakcję z kompleksem w
taki sam sposób jak
pierwsza. Jeden z jej
elektronów przechodzi na
Fe-S, dalej na cyt-c1 i cyt-c.
5. Drugi przechodzi z nowo
utworzonego CoQ
.
-na hem
bL, a następnie na hem bH.
Jednak tym razem hem bH
redukuje związany CoQ . -,
nie CoQ, przez co zamyka
cykl.
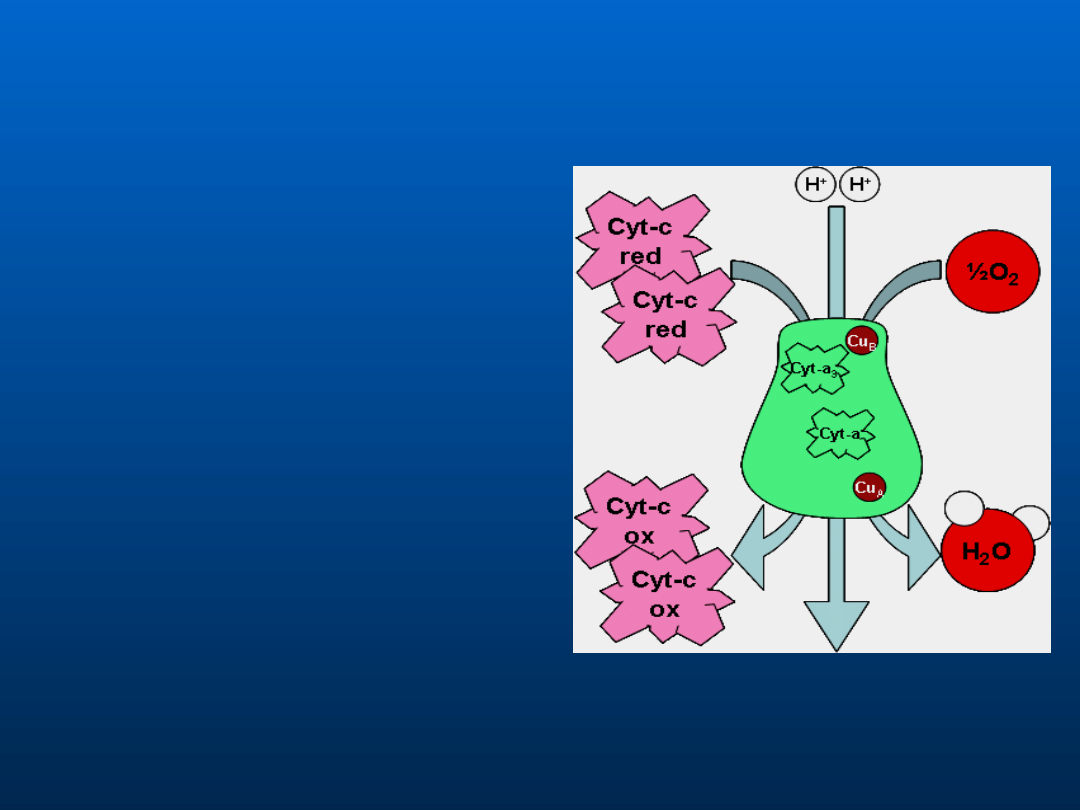
Oksydaza
cytochromowa
Kompleks ten zawiera dwa
cytochromy: cytochrom a i
a
3
. Cytochrom a stanowi
parę z atomem miedzi
Cu
A
, a cytochrom a
3
występuje w parze z
odmiennym atomem
miedzi Cu
B
.
1.Elektron jest przenoszony na
centrum a- Cu
A
2.Dalej przechodzi na centrum
a
3
-Cu
B
3. Następnie O
2
przyjmuje
elektrony, a po przyjęciu
czterech elektronów ulega
redukcji do dwóch cząsteczek
H
2
O.
4 cyt. c (Fe
2+
) + 4 H
+
+ O
2
4 cyt. c (Fe
2+
) +
2H
2
O
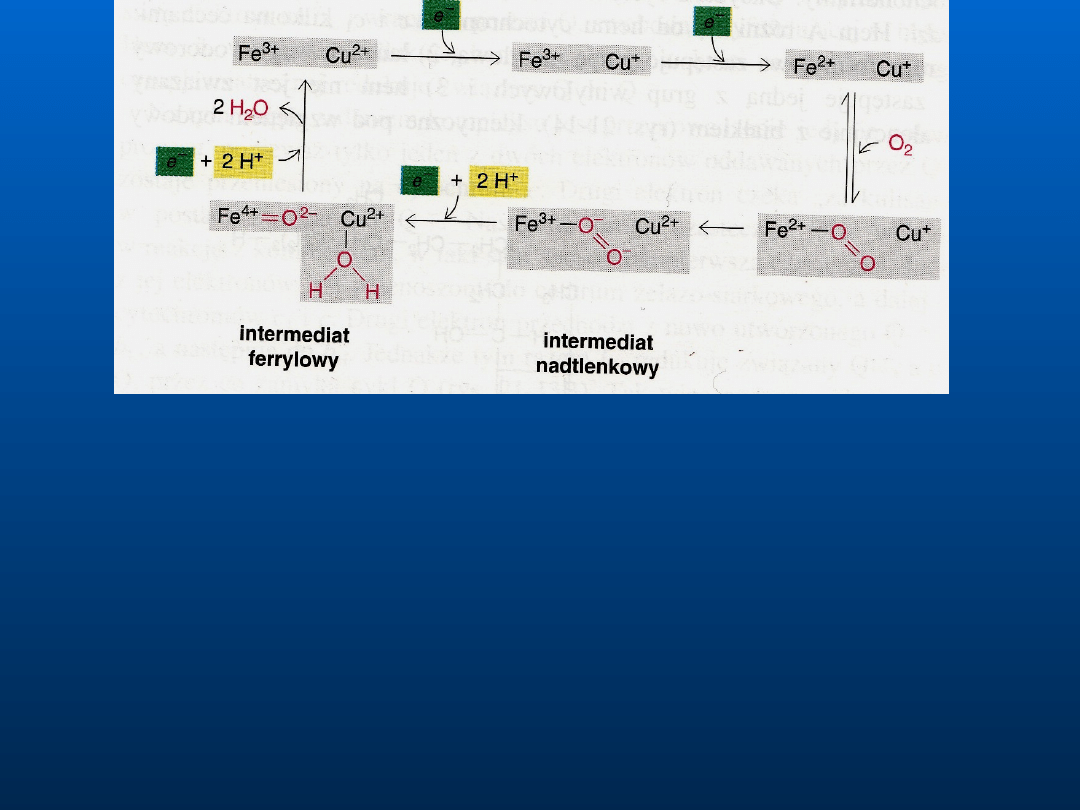
1.Pierwszy pobrany elektron przekazany z cytochromu c redukuje
Cu
2+
, a drugi Fe
3+
.
2.Zredukowany jon Fe
2+
wiąże tlen cząsteczkowy, który usuwa
elektron z każdego z tych jonów i powstaje nadtlenek jako
intermediat.
3.Następnie do reakcji wchodzi drugi elektron i dwa H
+
, co
powoduje rozłożenie nadtlenku. Jeden atom tlenu przyłącza się w
postaci –2 do żelaza i tworzy się stan ferryl +4, a drugi atom łączy
się w postaci H
2
O z Cu
2+
.
4.Wejście czterech elektronów i pobranie kolejnych dwóch H
+
pozwala na uwonienie dwóch cząsteczek H
2
O.
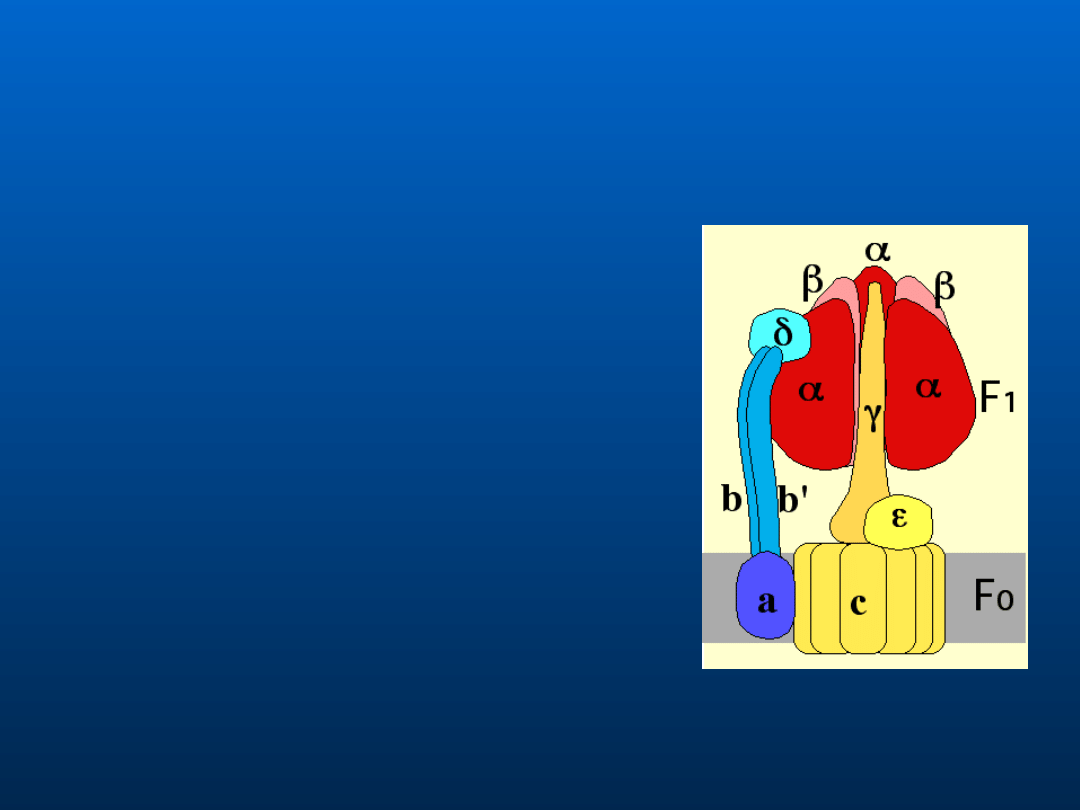
Tworzony przez łańcuch
oddechowy gradient
protonowy zasila syntezę ATP
Zatem, istnieje sprzężenie
między łańcuchem
oddechowym a syntazą ATP
Łańcuch oddechowy: -G
Synteza ATP: + G
Czyli gradient protonowy
pozwala na sprzężenie reakcji
egzoergicznej i
endoergicznej!!
syntaza ATP

Chemiosmotyczna teoria fosforylacji
oksydacyjnej:
1.fosforylacja = synteza ATP
2.fosforylacja oksydacyjna = fosforylacja
zasilana przez utlenianie
3.chemiosmotyczna = siłą napędową
syntezy ATP jest gradient protonowy
tworzony przez łańcuch oddechowy w
wyniku transportu elektronów
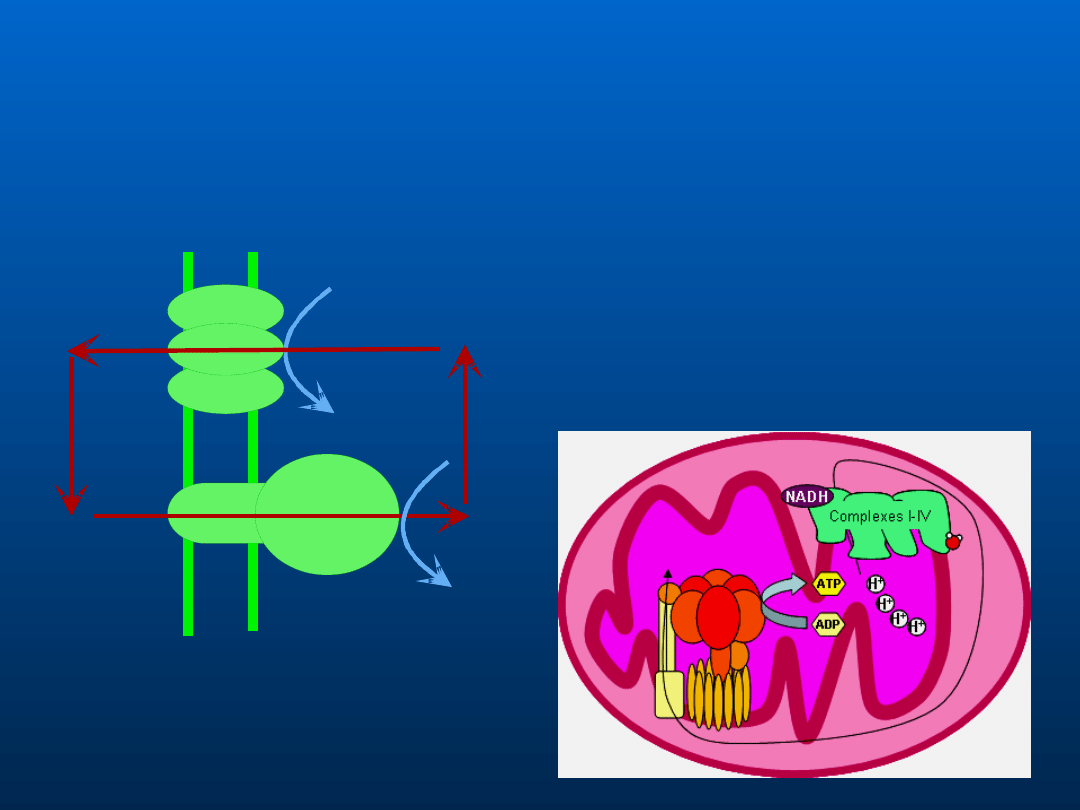
Łańcuch oddechowy jest sprzężony z syntazą ATP
oraz z każdym innym procesem zasilanym
przez gradient protonowy
ATP
O
2

Sprzężenie między łańcuchem oddechowym
a syntazą ATP możemy wyrazić ilościowo
za pomocą kontroli oddechowej (KO).
KO to dopasowanie szybkości pracy łańcucha
oddechowego (zużycia tlenu) do
zapotrzebowania na ATP.
Im intensywniej pracujemy tym więcej ATP
potrzebujemy i tym intensywniej pracują
nasze mitochondria.
• W mitochondriach istnieją białka zdolne do osłabienia
sprzężenia między łańcuchem oddechowym i syntazą
ATP.
• Białka te transportują protony do matriks z
pominięciem syntazy ATP. Są to tzw białka
rozprzęgające

Przekształcenia energetyczne zachodzące w
ramach oddychania komórkowego możemy
wyrazić ilościowo.
Znając liczbę cząsteczek ATP powstających w
wyniku utleniania danej substancji możemy
wyznaczyć jej kaloryczność.
ATP: ok. 0,025 kcal/g
Wydajność, z jaką energia uwalniana podczas utleniania jest
przekształcana w wiązania ATP często przekracza 40%.
Ogromna ilość energii uwalniana podczas utleniania może być
skutecznie wykorzystana tylko w małych porcjach.

Inhibitory
transportu
elektronów
o Rotenon i amylat- hamują transport
elektronów w reduktazie NADH-Q
o Antymycyna A przerywa przepływ
elektronów na poziomie cytochromu b
H
,
znajdującego się w reduktazie
cytochromowej
o Cyjanek (CN
-
), azydek (N
3
-
) i tlenek
węgla (CO) hamują przepływ elektronów
w oksydazie cytochromowej

Podsumowanie
Podsumowanie
DZIĘKI ISTNIENIU ŁAŃCUCHA
DZIĘKI ISTNIENIU ŁAŃCUCHA
ODDECHOWEGO MOŻLIWE JEST
ODDECHOWEGO MOŻLIWE JEST
CAŁKOWITE SPALENIE CZĄSTECZKI
CAŁKOWITE SPALENIE CZĄSTECZKI
GLUKOZY Z WYTWORZENIEM H
GLUKOZY Z WYTWORZENIEM H
2
2
O i CO
O i CO
2
2
EFEKT ENERGETYCZNY TO 38 cz. ATP
EFEKT ENERGETYCZNY TO 38 cz. ATP
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
Wyszukiwarka
Podobne podstrony:
Biochemia wykład 6 Łańcuch oddechowy
lancuch oddechowy, Biomechanika kliniczna
CKT, łańcuch oddechowy(1)
Fizjologia - wyklad 3 - uklad oddechowy, STUDIA
UKŁAD ODDECHOWY wykłady, UKŁAD ODDECHOWY
łańcuch oddechowy
Łańcuch oddechowy
Łańcuch oddechowy, fosforylacja oksydacyjna
lancuch oddechowy
Wykład 8-Układ oddechowy, ratownictwo medyczne, ANATOMIA
2011 09 29, Z, Temat 1 Wyklad 1 Lancuch dostaw, definicje i glowne zalozenia Material do wykladu
5 Wstep do metabolizmu; cykl Krebsa i lancuch oddechowy
Wyklad 14 oddech, Stomatologia, II rok, Mikrobiologia, Wykłady mikrobiologia
inhibitory łańcucha oddechowego
Lancuch oddechowy, Weterynaria Lublin, Weterynaria 1, Biochemia, Biochemia
Materiały, 7 2 ŁAŃCUCH ODDECHOWY
łańcuch oddechowy
więcej podobnych podstron