
Tubercolosi
M.infettiva, di regola contagiosa,
causata da M. tuberculosis
complex. Le manifestazioni
cliniche coinvolgono il polmone ma
possono essere interessati altri
organi e apparati. Esistono anche
forme disseminate

Eziologia
• M.tuberculosis complex: M.tuberculosis,
M.bovis, M.africanum, M.ulcerans, M.microtii
• M.tuberculosis: unico ospite l’uomo
• M.tuberculosis: aerobico, debole gram
positivo, alcol-acido resistente (BAAR),
crescita lenta, colonie non pigmentate,
produce niacina e catalasi termo-sensibile
(eccezione ceppi INH-resistenti), riduce nitrati
• M.bovis: si differenzia per la mancata
produzione di niacina e riduzione dei nitrati.
Infezioni umane rare (aree limitate di
diffusione: San Diego 3% dei casi)
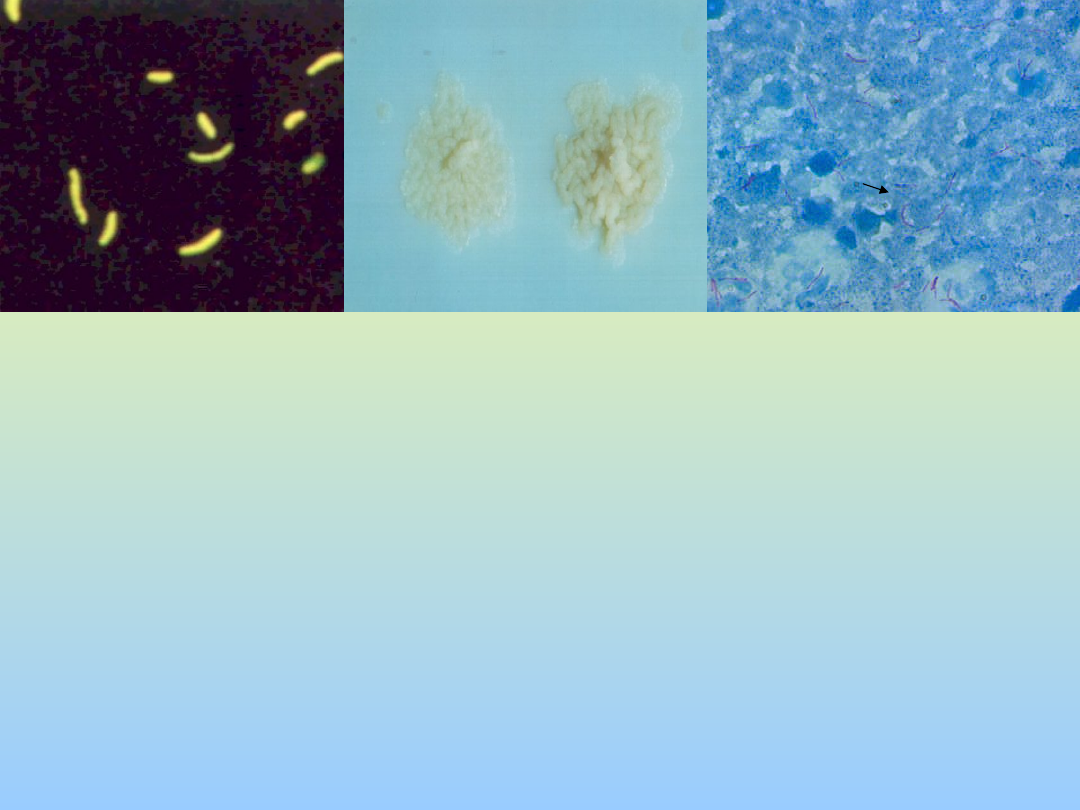
Eziologi
a
• Colorazioni specifiche per dimostrare alcol acido
resistenza (Zhiel-Neelsen Auramina-rodamina)
• Isolamento su terreni solidi (Lowenstain-Jensen o
Middlebrook 7H11) o terreni liquidi (BACTEC, MGIT, e altri)
• Identificazione mediante sonde o prove biochimiche
• Identificazione di M.tubercolosis con PCR su secrezioni
respiratorie
Coltura
Auramina-rodamina
Ziehl-Neelsen

Studio delle resistenze
• Test di sensibilità
• MDR-MT resistenza INI e RIFA
• XDR-MT resistenza INi e RIFA (MDR-
MT) e fluorochinolonici più altre 2
farmaci anti tubercolari di seconda
linea

Epidemiologia
• Affollamento e minore resistenza all’infezione: fattori
principali per la diffusione della TBC
• Rischio annuale stimato di TBC (nuovi casi/anno)
-soggetti non a rischio - USA 0,03%, Italia 0,5%
• Rischio di TBC superiore negli immigrati (pari al paese
di origine), senza tetto, pazienti immunocompromessi,
alcolisti, tossico-dipendenti, altro disagio sociale
• Negli ultimi anni è stato registrato un aumento dei casi
di TBC, legato alla diffusione dell’infezione da HIV
• Rischio di infezione relato all’infettività del caso indice
(superiore se caso indice con esame microscopico
positivo) e al tipo di contatto (ravvicinato e prolungato)


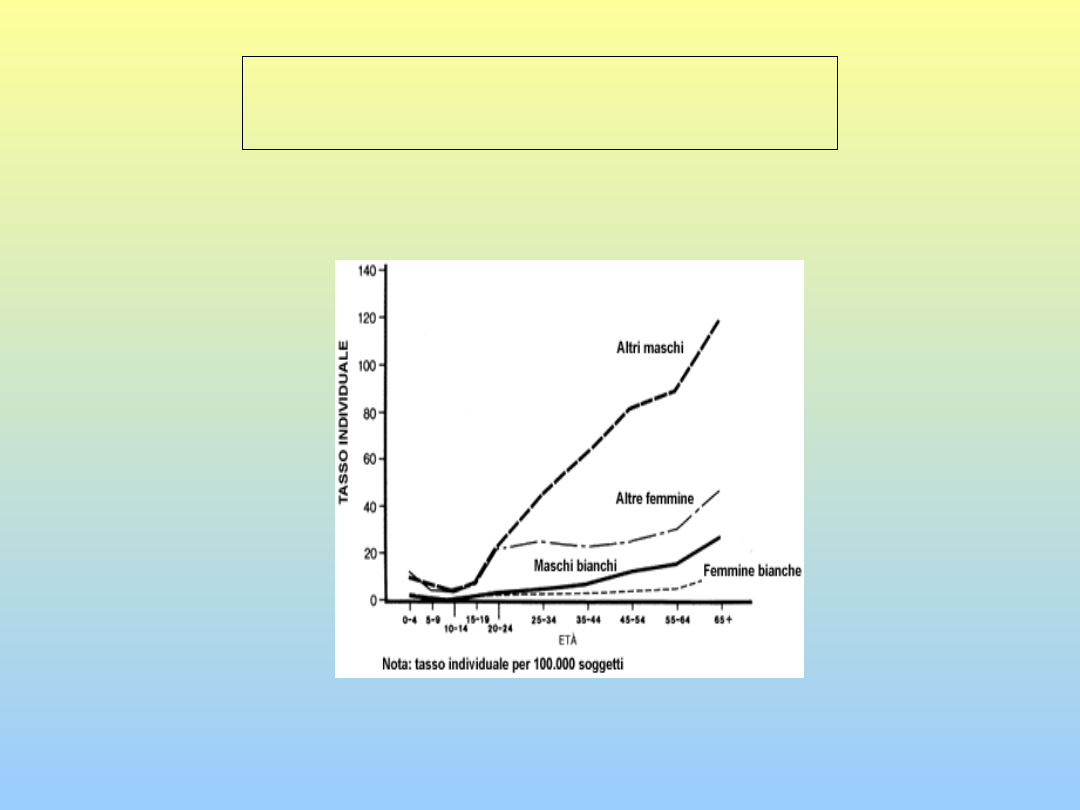
Diffusione della tbc in pazienti
non cucasici, immigrati
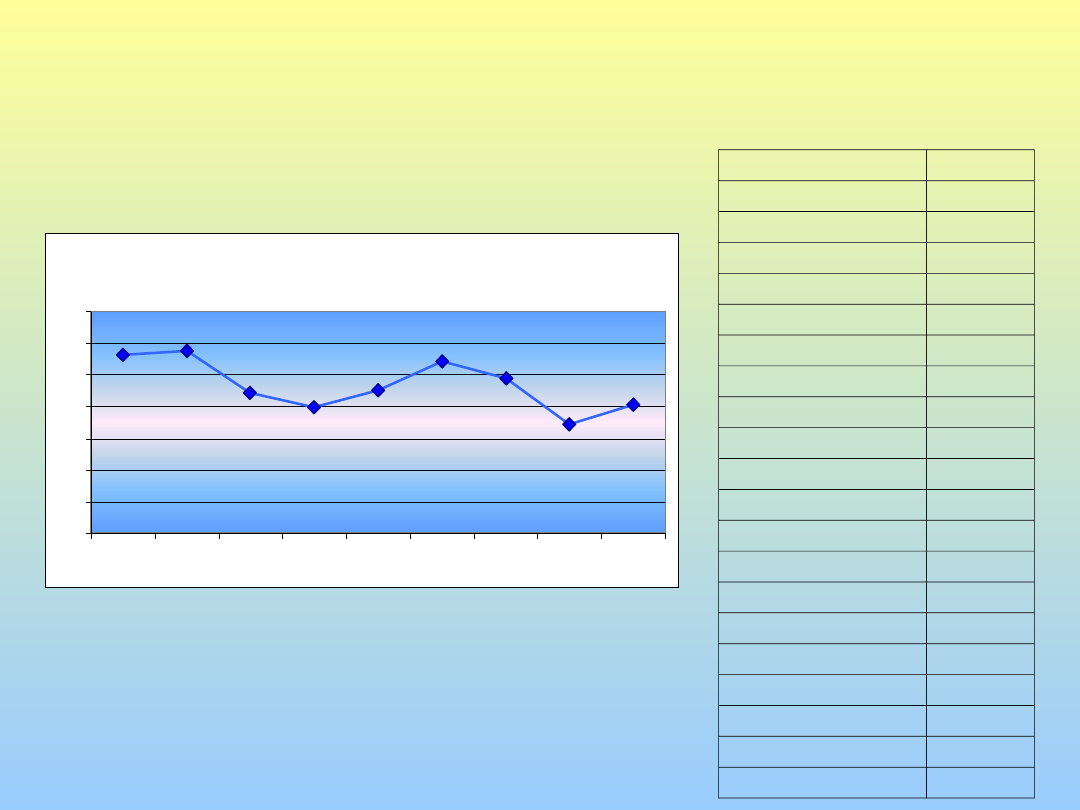
CASI/100.000 ABITANTI PER ANNO
0
2
4
6
8
10
12
14
1995
1996
1997
1998
1999
2000
2001
2002
2003
Tubercolosi in Umbria, 1995-
2003.
OSPEDALE
N° casi
A.O. Perugia
320
A.O. Terni
203
Città di Castello
20
Umbertide
5
Gubbio
11
Castiglione del lago
3
Città della Pieve
8
Passignano sul T.
1
Assisi
5
Marsciano
3
Todi
2
Foligno
58
Gualdo Tadino
11
Spoleto
14
Norcia
1
Cascia
2
Orvieto
24
Narni
8
Amelia
0
TOT.
699
1
29
6
53
29
53
22
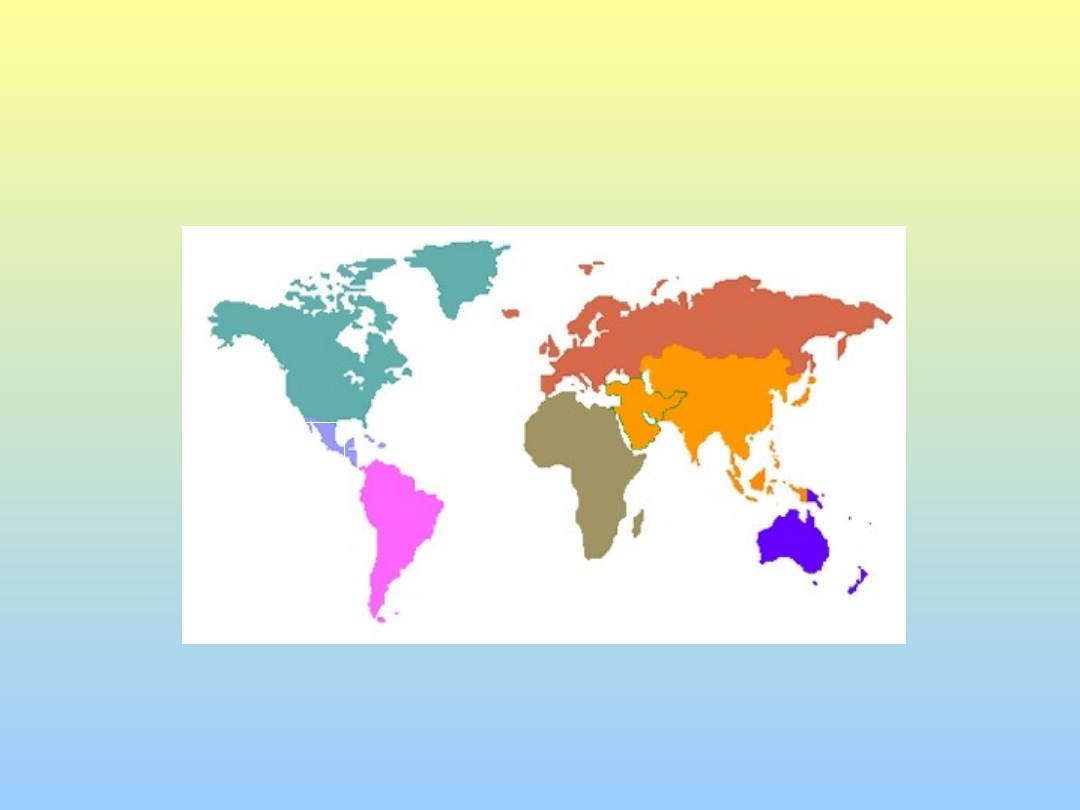
Regione geografica di provenienza dei
pazienti stranieri ricoverati per
tubercolosi in Umbria, 1995-2003.
0
10
20
30
40
50
60
70
80
90
1995
1996
1997
1998
1999
2000
2001
2002
2003
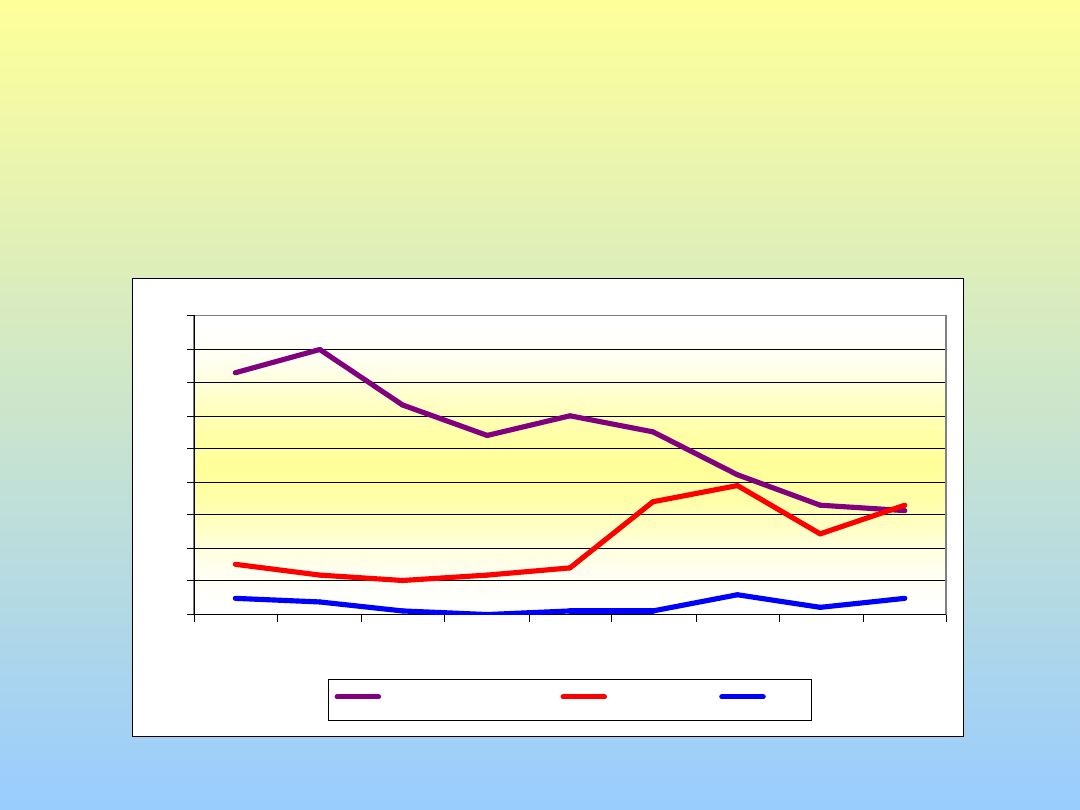
ITALIANI NON HIV
IMMIGRATI
HIV
Distribuzione per anno dei casi di
tubercolosi in italiani HIV-negativi,
immigrati e Hiv positivi, 1995-2003.
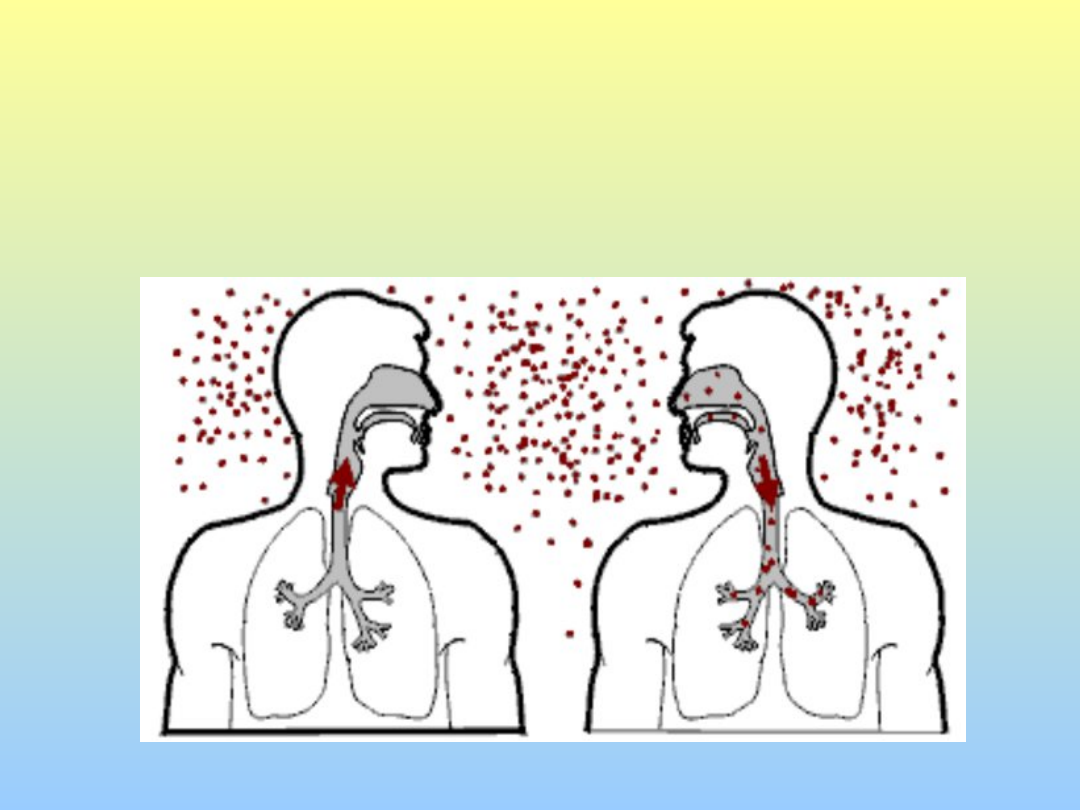
Nella maggior parte dei casi la tubercolosi è
trasmessa per aerosol di particelle, piccole (< 5 μ),
sospese nell’aria che raggiungono gli alveoli
Le particelle si producono con il parlare, tossire,
starnutire, e con i colpi di tosse

Diffusione
• La maggior parte dei casi sono trasmessi per
aerosol di particelle, sufficientemente piccole (<
5 μ), sospese nell’aria che raggiungono gli
alveoli e che si producono con il parlare, tossire,
starnutire, e con i colpi di tosse
• Aerosol che si formano durante la medicazione
di ferite sono anche implicati nella trasmissione
dell’infezione
• Particella di dimensioni > 5 μ non contagianti.
Anche se inalate sono espulse con la tosse
• L’aria della camera del paziente con TBC è
contagiosa anche quando il paziente è assente

Influenza della terapia sulla
diffusione
• Rischio di infezione superiore in casi con esame
microscopico positivo (carica 10.000 BAAR/ml)
• Pazienti adeguatamente trattati diventano
rapidamente non contagiosi (2 settimane nelle
infezioni da M.tuberculosis multi-sensibile)
• In presenza di infezione da M.tuberculosis multi-
resistente (MDR-TB) richiesti 3 espettorati
negativi (esame microscopico), in 3 giorni
consecutivi (> 3 settimane) (CDC 1994)
• L’esame microscopico può persistere positivo
per prolungati periodi dopo l’inizio della terapia
a dispetto della negatività colturale

Rischio di progressione dall’infezione a
tubercolosi
• Infezione primaria → TBC 3-4% dei casi nel 1° anno, e
successivamente 5-15%
• I dati si riferiscono a forti esposizioni e in condizioni di
minore resistenza all’infezione
• Rischio di infezione e progressione superiore per
esposizioni più intense
• Età più suscettibili all’infezione e alla progressione:
bambini, adolescenti 15-25, anziani
• Altri fattori di aumentato rischio: malnutrizione,
alcolismo, disagio sociale, tossicodipendenza, HIV
• Fattori genetici: HLA-DR2, allele DRB1*1501
correlazione con quadri clinici più gravi e fallimenti
terapeutici, allele DRB1*1502 con resistenza
0
10
20
30
40
50
60
70
0
100
200
300
400
500 n° CD4
% TBC
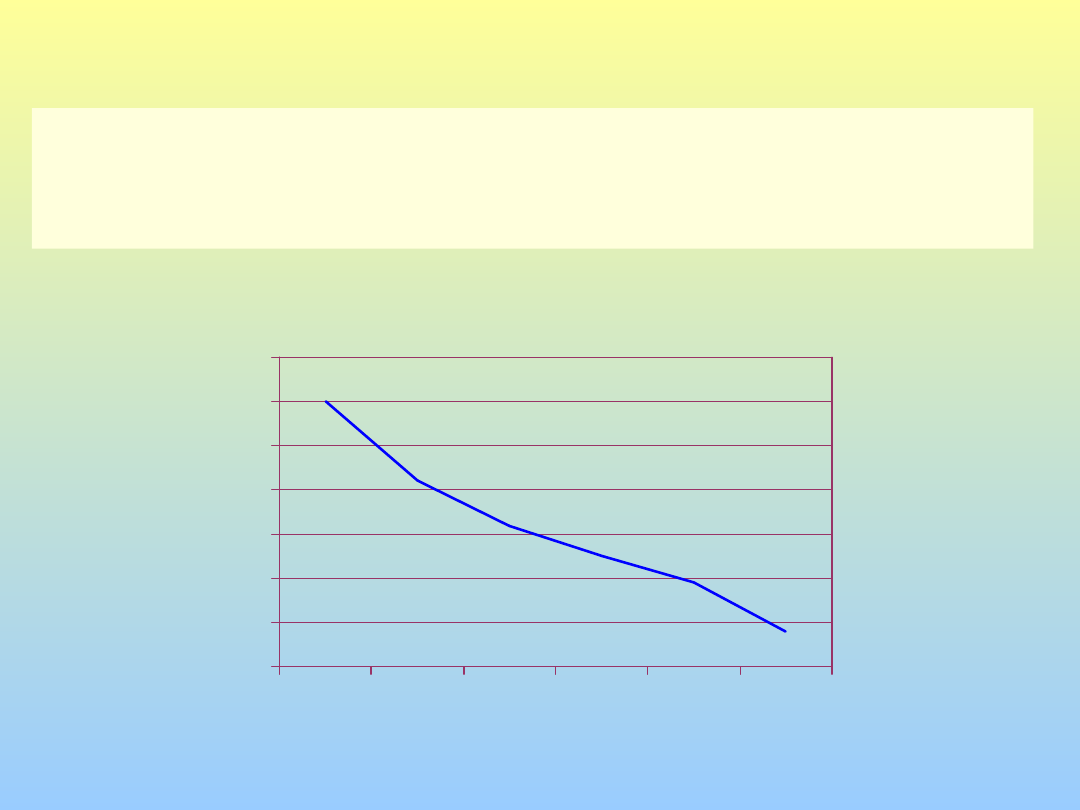
Correlazione tra conta dei linfociti CD4+ e frequenza di
TBC in pazienti con AIDS
(B.Jones. Am.Rev.Respir.Dis.1993,148:1292)

Rischio di TBC in HIV
Association of tuberculosis risk with the degree of tuberculin
reaction in HIV-infected patients.
Arch.Intern.Med.1997;157:797.
Mantoux
- mm
(n.pz)
n.CD4+
(range)
n.pz con
TBC/
n.totale
pz
Incidenz
a di TBC
100- PY*
(95%
C.I.)
Hazar
d
ratio
(95%
C.I.)
P
<2 (802)
-
5/802
0,39
-
-
2-4 (55)
340 (140-
560)
1/55
1,15
2,1
0,5
5-9
(128)
380 (240-
560)
5/128
2,78
5,7
0,07
> 10
(69)
370 (230-
520)
10/69
10,26
23,1
<0,0
1
*PY (persone-anno)
2695 pz HIV+ arruolati, 1054 reattivi (Mantoux e/o CMI)
Considerando solo la risposta alla Mantoux: 802 pz erano negativi, 252 pz
erano positivi
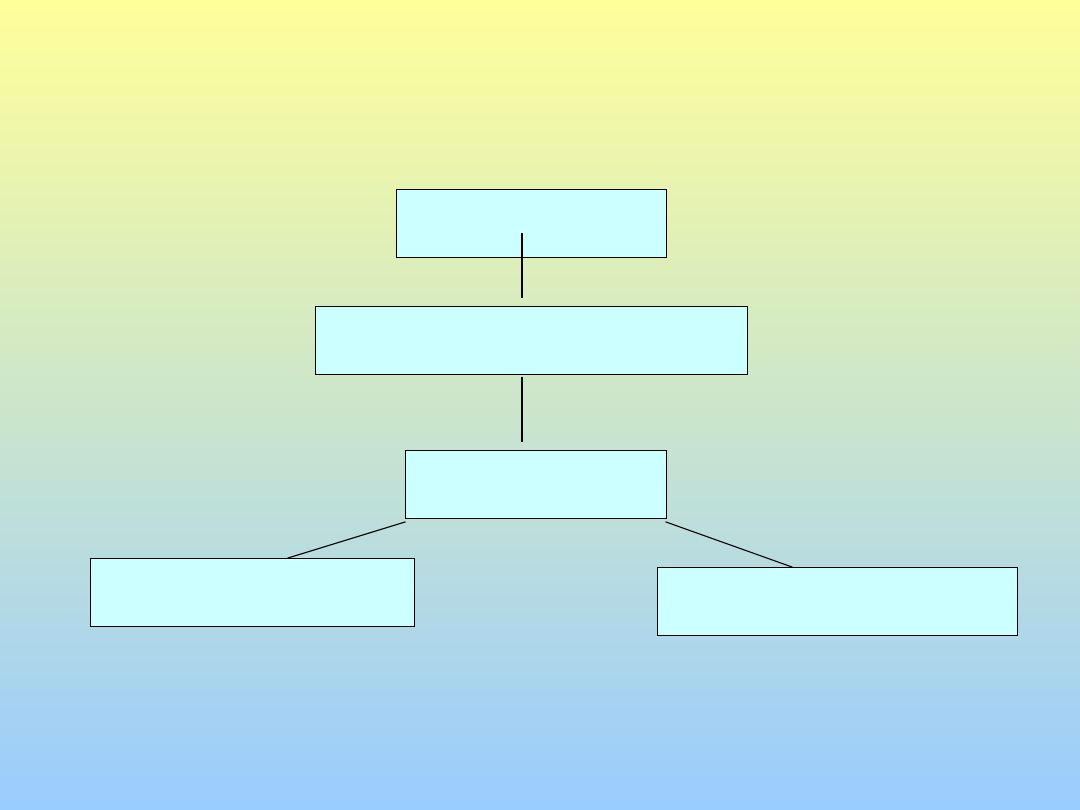
Dinamica della reazione immunologica nella
infezione tubercolare
Macrofago
infettato
Reclutamento/ attivazione
linfociti CD4+, CD8+, T, T
Formazione del
granuloma
Killing intracellulare
dei micobatteri
Lisi dei macrofagi infetti
da cellule citotossiche
IL1, IL2,
TNF
Espressione di
antigeni micobatterici
IL2
INT
INT, Vit D, CD4+, T,
T
IL= Interleukina
T = Linfociti T
T = Linfociti T

Immunologia
• Immunità cellulare (risposta antigene specifica): T
helper Th1 - interleuchina 2, interferone e TNF-β -
attivazione dei macrofagi con batteriocidia
• Reazione di ipersensibilità: fenomeni necrotici e
colliquativi (necrosi di macrofagi non attivati nei quali
i micobatteri si replicano), formazione di granulomi
• Alla necrosi caseosa probabilmente partecipano
anche: linfociti T-citotossici, NK, CD4-T linfociti con
recettori yб, fenomeni coagulativi (anossia), prodotti
intermedi del metabolismo azotato e ossidativo dei
macrofagi
• Immunità umorale: nonostante la produzione di
anticorpi, non sembra abbia un ruolo nel controllo
dell’infezione

Immunologia
• Cellule epiteliodi = macrofagi
fortemente attivati
• Cellule giganti, multinucleate di
Langhans = macrofagi fusi orientati
intorno ad antigeni tubercolari e
nuclei alla periferia

Immunologia
• Quando i macrofagi attivati raggiungono un
certo numero si manifesta la reazione di
ipersensibilità tissutale - reazione cutanea
ritardata alla tubercolina (3-9 settimane).
• Contemporaneamente si è anche sviluppata
l’immunità cellulo mediata.
• Non è ben chiaro se la reazione di ipersensibilità
(fenomeni di necrosi e formazione di granulomi)
e l’immunità cellulo mediata (resistenza
all’infezione) siano espressioni diverse di una
stessa sequenza immunologica e biochimica
oppure il risultato di due processi che dipendono
da diversi antigeni o diverse popolazioni
linfocitarie o entrambi le cose

Immunologia
• Le manifestazioni anatomopatologiche
della tubercolosi sono espressione del
grado di ipersensibilità dell’ospite e della
carica antigenica
• Tubercolosi proliferativa o produttiva
(reazione di ipersensibilità efficiente,
carica antigenica bassa)
• Tubercolosi essudativa (reazione di
ipersensibilità efficiente, carica antigenica
elevata)
• Tubercolosi non reattiva (reazione di
ipersensibilità non efficiente, carica
antigenica elevata)
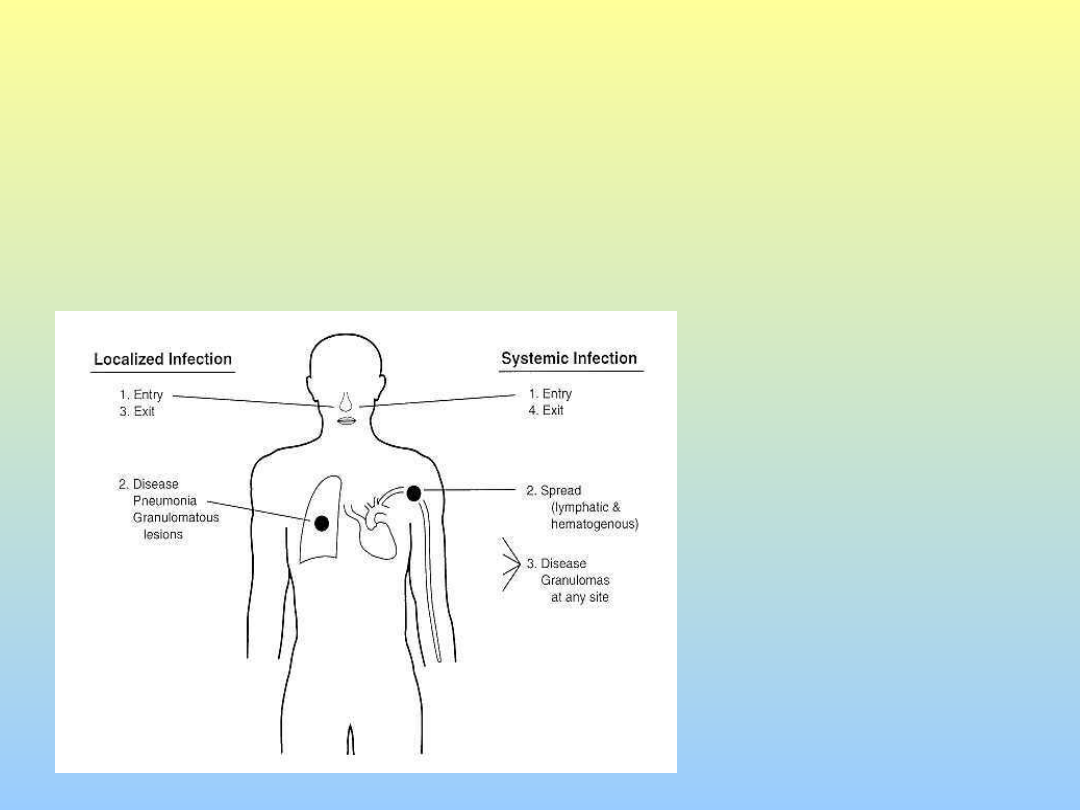
I micobatteri
raggiungo gli alveoli
- lobi inferiori
(maggiore flusso
d’aria) e periferici
(sub-pleurici) -
Focolaio iniziale
generalmente unico
Migrazione di
micobatteri nei
linfonodi regionali.
Alcuni superano il
filtro linfatico e si
localizzano in altre
sedi con 3
possibilità: restare
silenti, replicarsi
(infezione
progressive),
manifestarsi dopo
qualche mese o anni
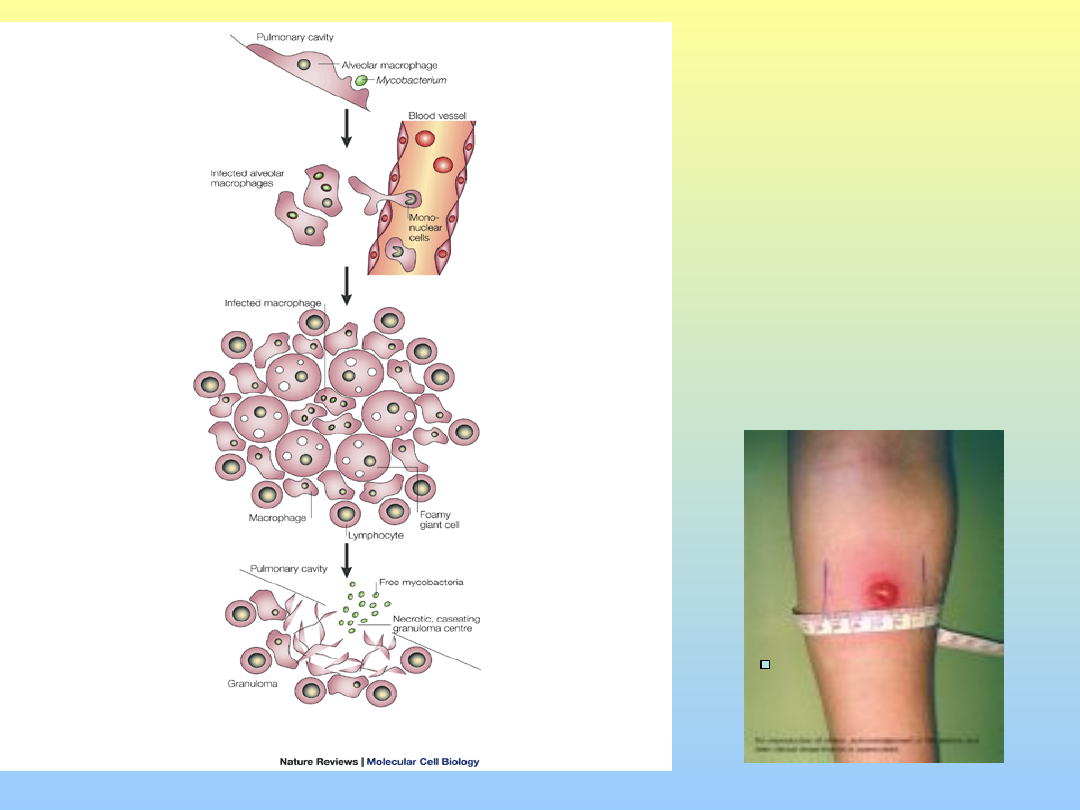
Non è definito se la reazione
di ipersensibilità (fenomeni di
necrosi e formazione di
granulomi) e l’immunità
cellulo mediata (resistenza
all’infezione) siano espressioni
diverse di una stessa
sequenza immunologica e
biochimica oppure il risultato
di due processi che dipendono
da diversi antigeni o diverse
popolazioni linfocitarie o
entrambe le cose
granuloma
Mantoux,
immunità cellulo mediata

Patogenesi
• I micobatteri raggiungo gli alveoli - lobi inferiori
(maggiore flusso d’aria) e periferici (sub-pleurici) -
Focolaio iniziale generalmente unico
• I batteri inglobati dai macrofagi non sono uccisi
• Necrosi dei macrofagi, richiamo di altre cellule
immunitarie
• Focolaio di polmonite localizzata
• migrazione di micobatteri nei linfonodi regionali.
Alcuni superano il filtro linfatico e si localizzano in
altre sedi con 3 possibilità: restare silenti, replicarsi
(infezione progressive), manifestarsi dopo qualche
mese o anni
• Lo sviluppo della immunità e della reazione di
ipersibilità coincide con la cuti-conversione
(positività della Mantoux)

Quadri clinici
• Infezione primaria (complesso
primario)
• Tubercolosi primaria
• Tubercolosi post primaria
• Tubercolosi extra polmonare

Tubercolosi primaria
• Morbigena semplice (manifestazioni sia
polmonari (tenui addensamenti sub
lobari o lobari) che extrapolmonari
(pleurite, cherato congiuntivite
flittenulare), essenzialmente di
carattere allergico
• Adenopatia ilare isolata
• Tisiogena evolutiva
• Miliare primaria

Tubercolosi primaria
•
FOCUS INIZIALE IN CAMPO MEDIO o INFERIORE
Iinfiltrato di Gohn)
•
TENDENZA ALLA LINFOADENITE REGIONALE
ESTENSIVA (anche unico segno Rx grafico)
•
RARAMENTE ERITEMA NODOSO, CONGIUNTIVITE
FLITTENULARE
•
± FEBBRE e ASTENIA
In bambini < 3 anni: disseminazione linfoematogena
progressiva
Tra 3-15 anni: progressione rara, incapsulamento,
calcificazioni, guarigione
In pubertà: interessamento apicale o progressione
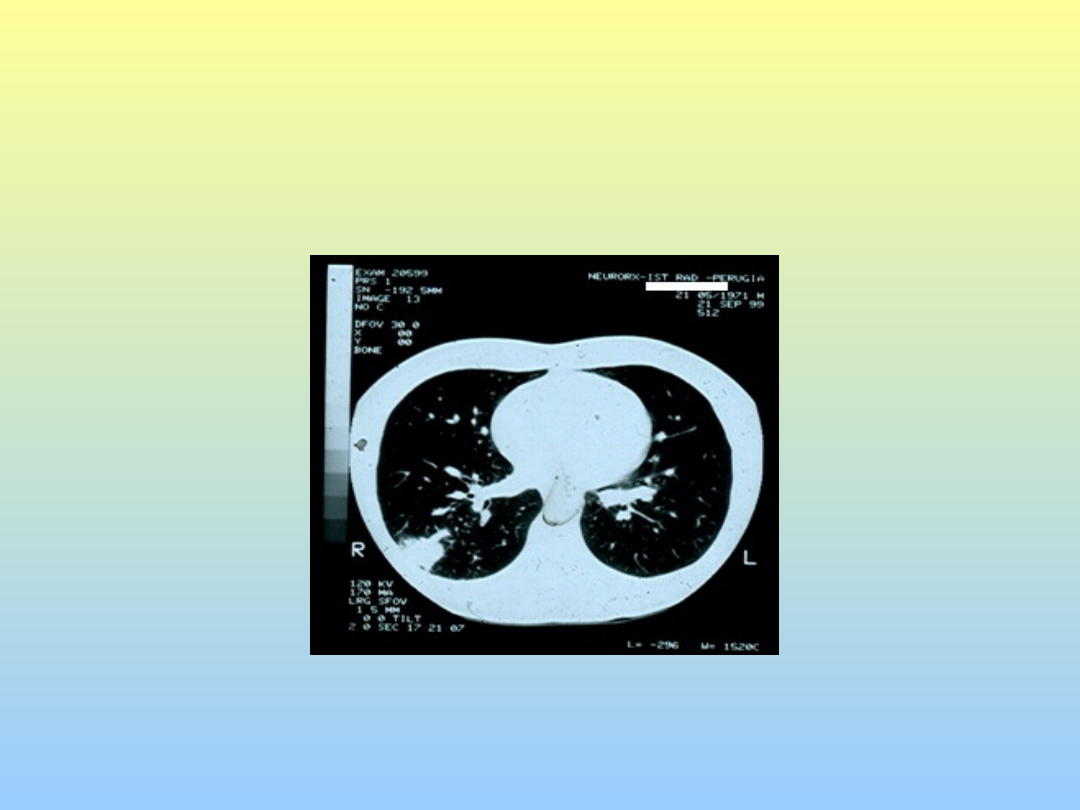
Complesso primario in giovane
immunocompetente

Tubercolosi polmonare post
primaria
• Miliare
• Tubercolosi polmonare essudativa
(infiltrato precoce di Asmann, lobite,
brocopolmonite a focolai disseminati)
• Tubercolosi polmonare cavitaria
cronica

TUBERCOLOSI POLMONARE
SINTOMI
• ANORESSIA, ASTENIA, PERDITA DI PESO, SENSO DI
FREDDO
• FEBBRE POMERIDIANA, SUDORAZIONE NOTTURNA
• ± EMOTTISI , ± DOLORE PLEURICO
• ESAME CLINICO NON SPECIFICO
• ANEMIA NORMOCROMICA, NORMOCITICA,GB
NORMAli
• ± IPER γ GLOBULINEMIA, IPOALBUMINEMIA
• RX TORACE POSITIVO

TUBERCOLOSI POLMONARE
Polmonite lobare inferiore dell’anziano
QUADRI CLINICI SPESSO NON SPECIFICI, A
LENTA RISOLUZIONE O NON RISOLVENTISI.
(disseminazione
endobronchiale da riattivazione apicale !)
Tubercoloma
LESIONI ROTONDE ASINTOMATICHE.
GRANULOMI CASEOSI CIRCONDATI DA STRATI
CONCENTRICI DI FIBROSI, ± CALCIFICAZIONI
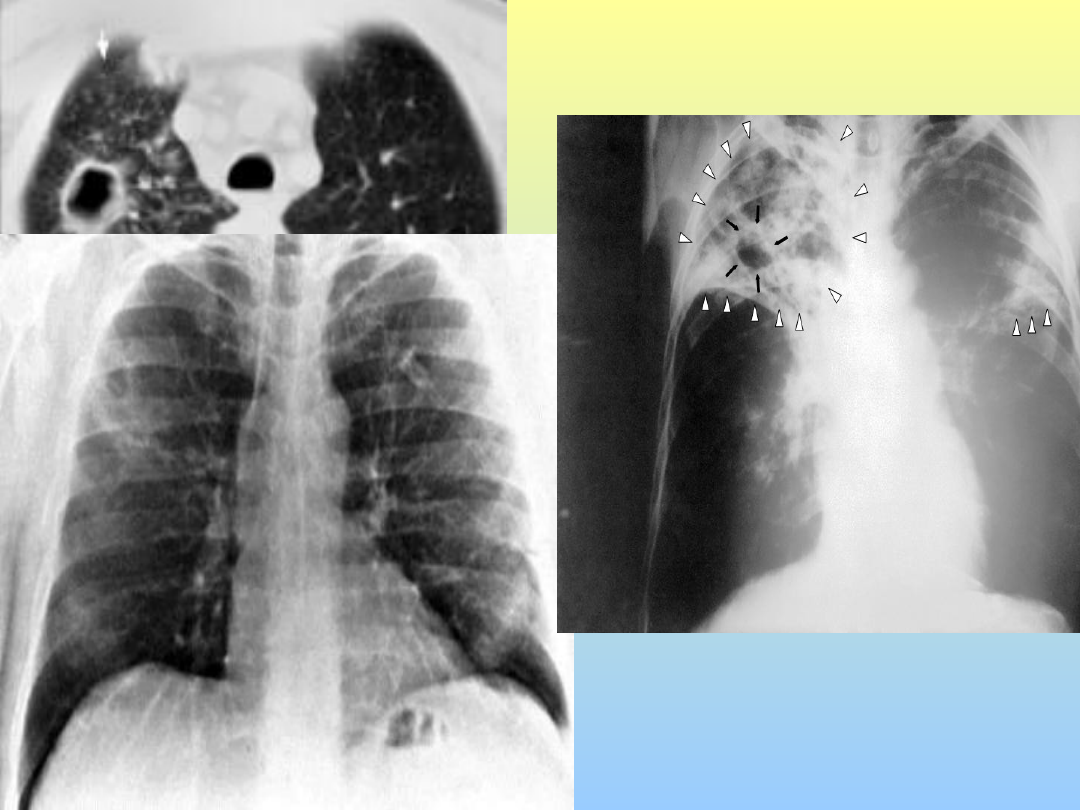
TBC cavitaria apicale dx
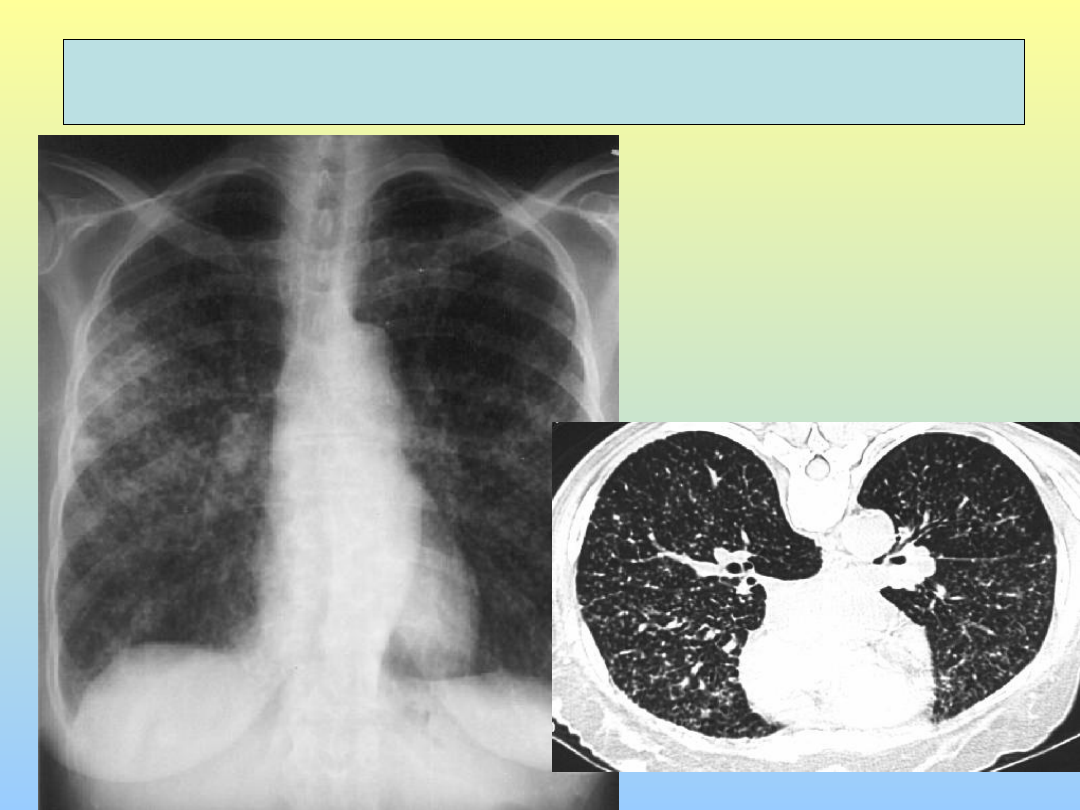
Tubercolosi miliare
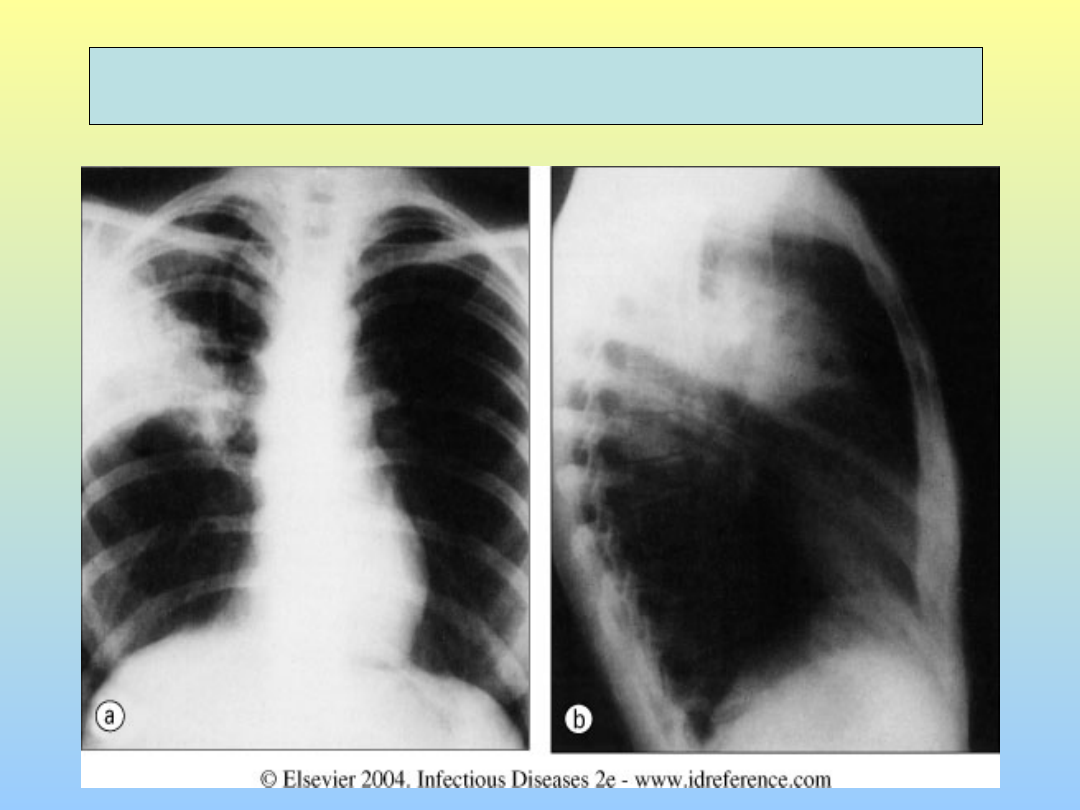
Lobite tubercolare
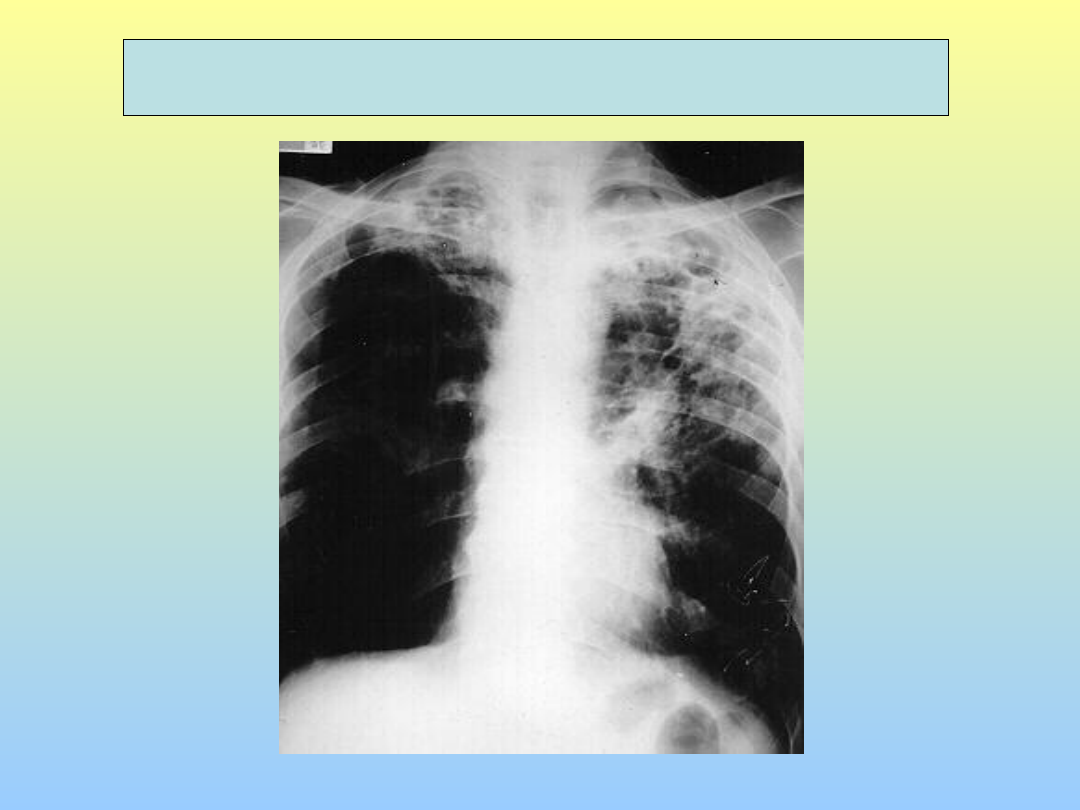
Tubercolosi polmonare cavitaria cronica
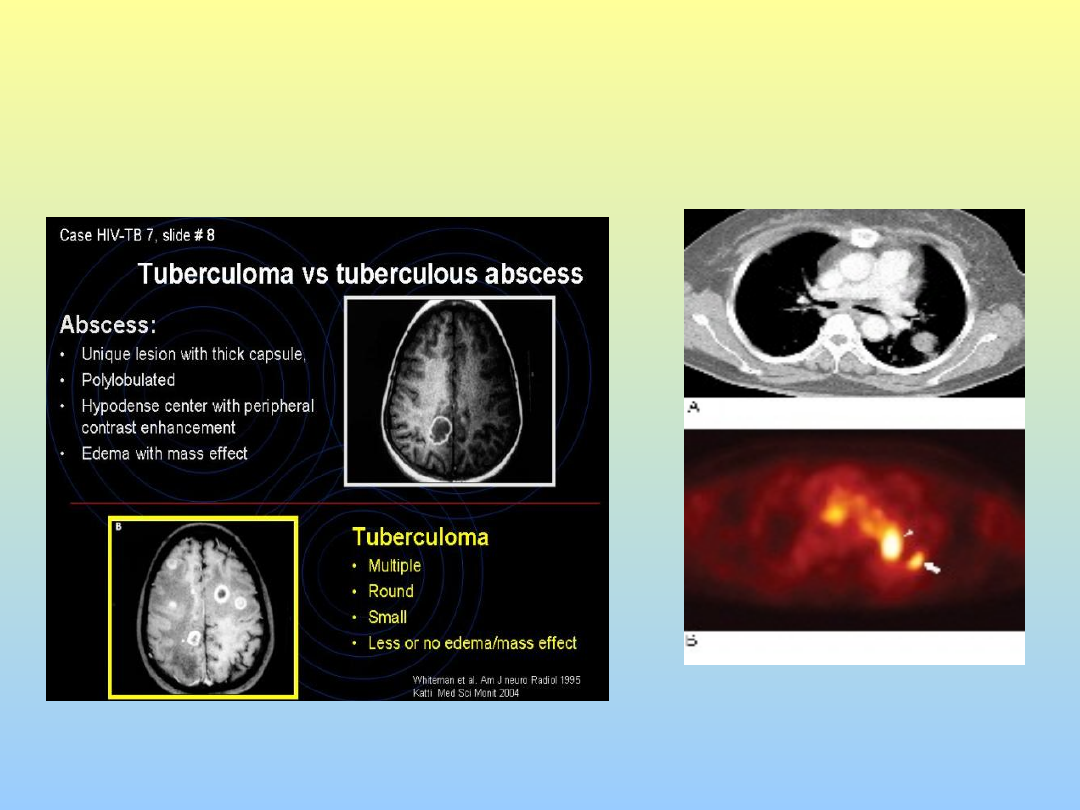
Tubercoloma polmonare
Ascesso tubercolare, tubercolomi cerebrali
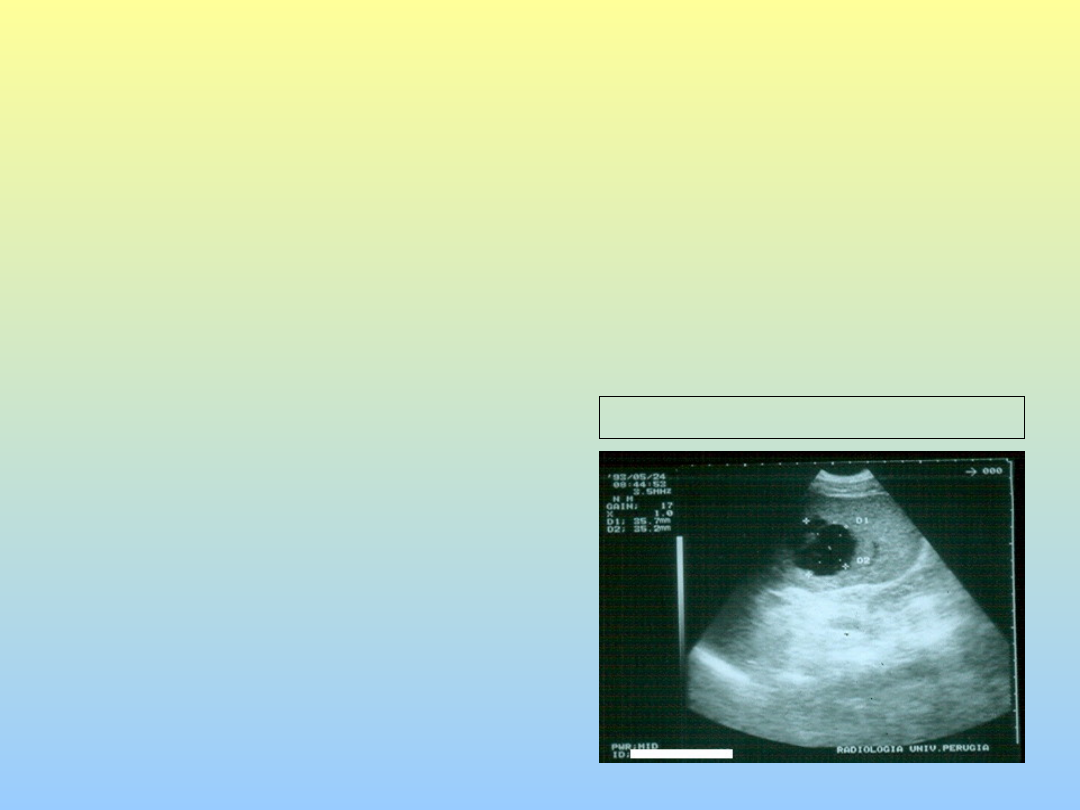
Tubercolosi extra-polmonare
• Miliare disseminata, menigite,
pleurite, pericardite, renale, genitale,
osteo-articolare, laringea, intestinale,
linfonodale, epatite, e altre
Ascesso splenico da M.tuberculosis

TUBERCOLOSI
EXTRAPOLMONARE
TUBERCOLOSI MILIARE
• COMPRENDE TUTTE LE FORME DI DISSEMINAZIONE
EMATOGENA ESTENSIVA. INIZIO E DECORSO
SUBDOLO, NEI BAMBINI FEBBRE INTERMITTENTE
• SUDORAZIONI NOTTURNE
• ANEMIA, GB NORMALI, ± IPONATREMIA
• Rx TORACE SPESSO NEG (noduli miliarici < 1 mm→ TC
polmone)
Nb:
PUO’ CAPITARE IN FORMA ACUTA PRIMA DELLO
SVILUPPO DI IPERSENSIBILITA’,
PUO’ ESSERE DI GRADO MODERATO IN PRESENZA DI
PATOLOGIA
POLMONARE CRONICA,
PUO’ DERIVARE ANCHE DA UN FOCOLAIO EXTRAPOLMONARE

INTRADERMOREAZIONE DI
MANTOUX
• PPD (purified protein derivative). Precipitato proteico
della vecchia tubercolina
• Inoculazione sotto cute, non più profondamente per
evitare il wash out da parte del circolo !!
• VIENE DESCRITTA RICONVERSIONE A CUTINEGATIVO
IN PERCENTUALE PARI A 8% ALL’ANNO
• IN PERSONE CON INFEZIONE ANTICA LA MANTOUX
CON 5 U.tà PUO’ QUINDI RISULTARE NEGATIVA.
UN SUCCESSIVO TEST EFFETTUATO PUO`
RISULTARE POSITIVO (Effetto booster )

Criteri di positività della
Mantoux
• HIV/AIDS, contatti recenti paziente con TBC 5 mm
• Immigrati da paesi ad alta prevalenza di TBC 10 mm
• Immunocompetenti sani 15 mm
• Se il test è positivo può essere indicato eseguire altri
accertamenti (escludere una TBC)
• Se il test è positivo ed è stata esclusa una TBC si
può decidere di trattare l’infezione latente
• Durante i primi giorni dell’infezione primaria e nelle
forme gravi la Mantoux può risultare negativa
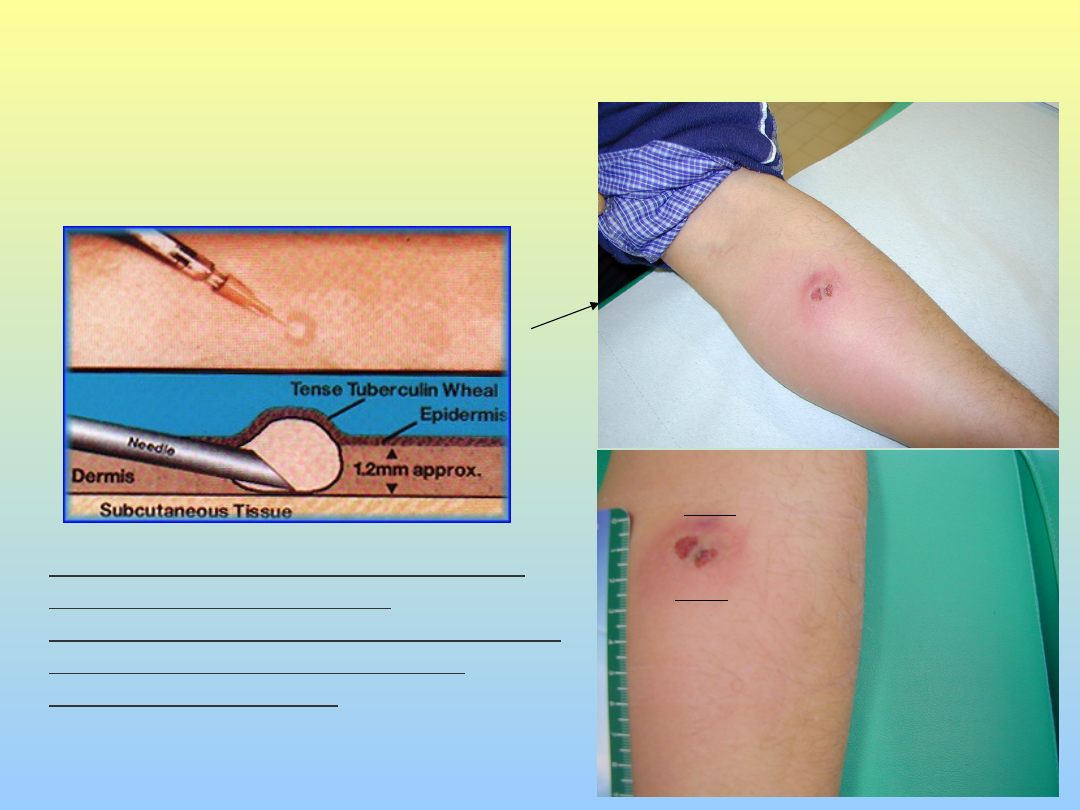
INFEZIONE
TUBERCOLARE
LATENTE
Dosaggio y-interferon
(Quantiferon o Ellispot-TB)
PAZIENTI CUTINEGATIVI VANNO
RITESTATI DOPO UNA
SETTIMANA PER DIFFERENZIARE
L’EFFETTO BOOSTER DALLA
CUTICONVERSIONE
Intradermoreazione di Mantoux

Infezione latente
• Contatto con M.tuberculosis,
controllo della replica batterica,
adeguata risposta immunitaria,
complesso primario, persistenza di
M.tuberculosis con possibilità di
riattivazione, Mantoux positiva
• Terapia

Differenze tra infezione
tubercolare latente e TBC
• Infezione latente
• Assenza sintomi
• Assenza espettorato
• RX torace negativo
• Non contagioso
• Generalmente Mantoux
positiva
• TBC
• Sintomi
• RX torace non sempre
patologico
• Esame microscopico e
coltura non sempre
positivi
• Usualmente Mantoux
positiva
• Contagioso

Diagnosi di TBC
• SOSPETTO CLINO
• Esami microscopici, colturali, PCR
• Secrezioni respiratorie (almeno 10 ml in 3 giorni
consecutivi e processati quanto prima)
• Urine (igiene dei genitali, tutte le urine del
mattino in 3-5 giorni consecutivi, processare
subito o neutralizzare pH)
• Sondaggio gastrico (pazienti che non hanno
espettorazione, bambini, processare subito o
neutralizzare pH)
• Altri campioni (liquor, biopsie, secrezioni)
• Rx torace, TC ad alta risoluzione

Trattamento
• Resistenza primaria: pazienti che non
hanno mai ricevuto terapia.
Incremento dei ceppi INI R dal 3% al
9% dopo il 1997. MDR 2%
• Resistenza secondaria: pazienti che
hanno già assunto farmaci anti-TBC.
Maggiore incidenza degli isolati MDR,
più diffusa in alcune aree geografiche

Farmaci anti-tubercolari e possibili
effetti indesiderati
Farmaco
Dose giornaliera
(adulto)
Isoniazide
5 mg/kg (max 300
mg)
Rifampicina
10 mg/kg (max 600
mg)
Rifabutina
5 mg/kg (max 300
mg)
Pirazinamide
15-50 mg/kg (max
2gr)
Etambutolo
15-25 mg/kg
Sterptomicina
15 mg/kg (max 1 gr)
Farmaci anti-tubercolari e possibili effetti
indesiderati
Farmaco
Effetti indesiderati
Isoniazide
Epatite (1/1000 età < 30 a., 23/1000 età
30-65), neuropatia periferica
Rifampicina Epatite aumenta il rischio di tossicità da
isoniazide, sindrome simil influenzale,
anemia emolitica, piastrinopenia
Rifabutina
Come rifampicina
Pirazinamide Epatite, iperuricemia, gastralgie, artralgie
Etambutolo Neurite ottica, sconsigliato età < 8 anni
Streptomicin
a
Sordità, disturbi vestibolare,
nefrotossicità

Terapia tubercolosi da
M.tuberculosis multi-sensibile
• Schemi di terapia con associazione di
4 farmaci (INI, RIFA, PZA, EBM o STM)
nei primi 2 mesi, proseguire con 2
molecole (INI e RIFA) per altri 4 mesi
se a 2 settimane esame diretto
dell’espettorato negativo o a 2 mesi
coltura negativa altrimenti 7 mesi
• Schemi prolungati nelle forme extra-
polmonari

Terapia tubercolosi
• DOT = directly observed treatment =
terapia supervisionata
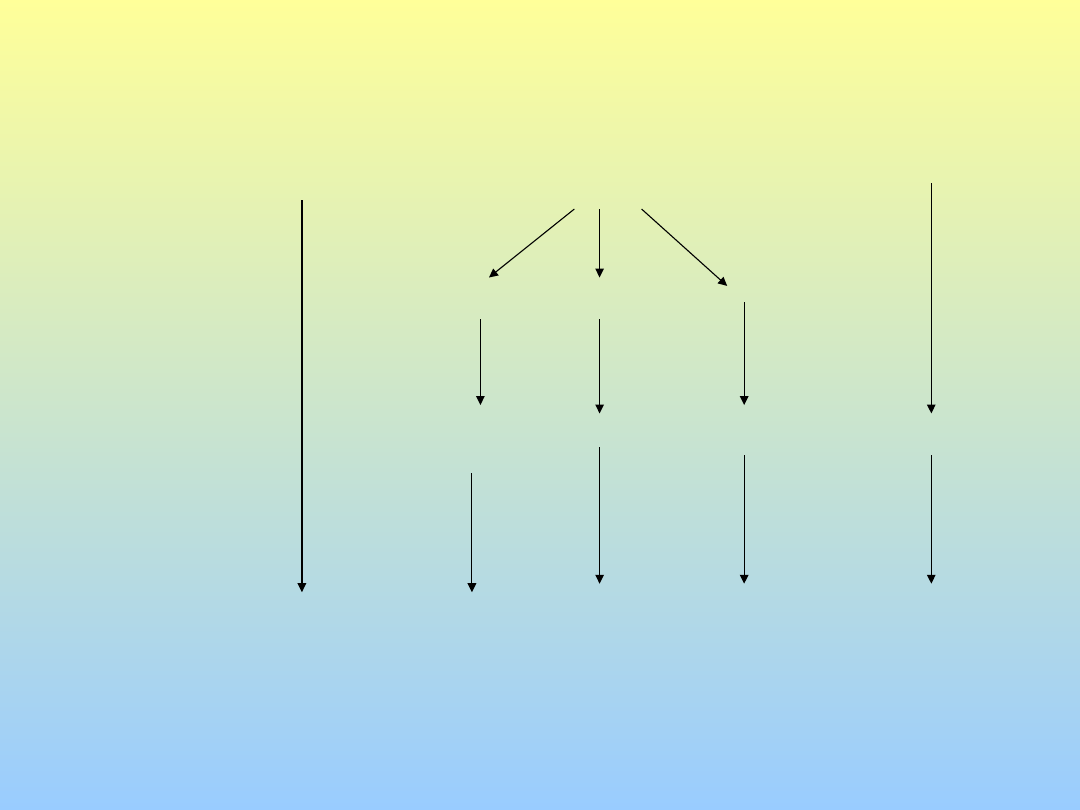
Mantoux
pre-
espos.
Positiva
(10 mm)
Negativa
(< 5 mm)
Non nota
ESPOSIZIONE
Mantoux
post-
esposiz.
Negativa o
5-9 mm
10-14 mm
> 15 mm
> 10 mm
Indicazioni se
RX
negativo
Non
tratt
are
se
non
altri
ment
i
indic
ato
Trattare
solo se
HIV +
Rischio
minimo
Trattamento
Può essere
indicato
Alto
rischio
Trattar
e
Stesse
indicazio
ni della
cuti
conversi
one
Protocollo comportamentale per
esposizione.
Annalas Intern Med, 1995
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
Wyszukiwarka
Podobne podstrony:
Mycobacterium tuberculosis
Tuberculosis 2
Chicken Pox vs Tubercolosis
Tuberculosis
The Differences and Similarities of Pneumonia and Tuberculosi
Mycobakterium tuberculosis, pielęgniarstwo, mikrobiologia i parazytologia
Kaart van de sterfgevallen aan tuberculose in Nederland in de jaren 1901 1908, M van Ravenstijn, ca
Detection and Molecular Characterization of 9000 Year Old Mycobacterium tuberculosis from a Neolithi
Szewczyk, Rafał i inni Rapid method for Mycobacterium tuberculosis identification using electrospra
więcej podobnych podstron