
KOROZJA CHEMICZNA, UTLENIANIE
WYSOKOTEMPERATUROWE I UTLENIANIE
WEWNĘTRZNE
Wykonał : Krzysztof Lewandowski
Prowadzący
Dr inż. Sławomir Szewczyk

PODSTAWY ZJAWISKA KOROZJI
Korozją jest nazywane oddziaływanie fizykochemiczne i
elektrochemiczne między materiałem metalowym a
otaczającym środowiskiem, w wyniku którego następuje
uszkodzenie korozyjne powodujące zmniejszenie własności
materiału.
Zjawisku korozji ulegają różnorodne materiały, nie tylko
metaliczne. Obserwuje się niszczące działanie środowiska na
ceramikę, tworzywa sztuczne, kompozyty. Mechanizm korozji
różnych materiałów zależy od typu przewodności elektrycznej
na granicy faz materiał-środowisko i od rodzaju środowiska.
Dla materiałów o wysokiej przewodności korozja ma charakter
głównie elektrochemiczny. Przy niskiej przewodności lub jej
braku zachodzi jako proces chemiczny lub fizykochemiczny.

PODZIAŁ KOROZJI
Korozja elektrochemiczna – charakteryzuje się występowaniem w
materiałach o wysokiej przewodności elektronowej lub jonowej,
występuje głównie w elektrolitach (np. woda, wodne roztwory
kwasów, wodne roztwory soli, wilgotne gazy),
Korozja chemiczna – polega na niszczeniu materiałów w wyniku
reakcji chemicznych. Środowiskiem występowania są gazy
suche(np. gazy spalinowe, gorące suche powietrze, ropa naftowa i
jej pochodne, substancje organiczne – H
2
S, CO, CO
2
, Cl
2
, NH
3
, H
2
)
Korozja fizykochemiczna - występuje przy niskiej przewodności
materiałów.
Rys. 1. Schemat rozmieszczenia lokalnych ogniw korozyjnych na
powierzchni metalu

KOROZJA CHEMICZNA - GAZOWA
Korozja gazowa w środowisku zawierającym jedynie suchy gaz
np. tlen lub powietrze, azot, siarkę i jej związki, spaliny i pary,
jest najczęstszym przykładem korozji chemicznej. Procesy korozji
chemicznej polegają na niszczeniu materiałów w wyniku reakcji
chemicznych. W odróżnieniu od korozji elektrochemicznej korozja
chemiczna przebiega na sucho, bez udziału elektrolitu.
Jeżeli tworzywo metaliczne zostanie poddane działaniu
środowiska o właściwościach utleniających w podwyższonej
temperaturze, wówczas powstają produkty reakcji, które w
zależności od warunków i składu tworzywa mogą być lotne,
ciekłe lub stałe. Produkty tworzą się przede wszystkim na
powierzchni materiału jako zgorzelina, lecz w pewnych
przypadkach proces utleniania może zachodzić równocześnie lub
nawet wyłącznie w głębi tworzywa metalicznego, w wyniku
dyfuzji utleniacza w głąb materiału (utlenianie wewnętrzne).

KOROZJA GAZOWA - SKUTKI
Korozja gazowa przynosi szczególnie
dotkliwe starty w przemysłach
chemicznym, energetycznym, w
transporcie samochodowym i
lotniczym – wszędzie tam, gdzie
wiele elementów konstrukcyjnych
jest narażonych na działanie
gorących par i gazów. Korozja
gazowa powoduje również znaczne
starty w procesie wytwarzania
metali, głównie wskutek tworzenia
się zgorzeliny podczas obróbki
plastycznej i cieplnej metali i
stopów, zwłaszcza stali, stając się
tym samym przedmiotem
szczególnego zainteresowania
technologów obróbki plastycznej i
cieplnej.
Rys. 2. Połączenie
spawane Niebieski
obszar jest
wynikiem
utleniania się
metalu w wysokich
temperaturach
Rys. 3. Na stali
nierdzewnej tworzy
się szaroczarna
zgorzelina w
procesie
walcowania
Rys. 4.
Powierzchnia
stali nierdzewnej
po usunięciu
zgorzeliny

REAKCJA CHEMICZNA UTLENIANIA
Podstawowym typem reakcji
powodującej korozję gazową przede
wszystkim podczas obróbki plastycznej
i cieplnej jest reakcja chemiczna
utleniania, którą dla najprostszego
przypadku utleniania czystego metalu
dwuwartościowego można przestawić
następująco:
MX
X
M
2
2
1
M - metal
X
2
– utleniacz, np. O
2,
S
2,
N
2

ELEMENTARNE PROCESY CZĄSTKOWE, KTÓRE
SKŁADAJĄ SIĘ NA REAKCJĘ CHEMICZNĄ UTLENIANIA
adsorpcja i chemisorpcja gazu utleniającego na powierzchni ciągłej i cienkiej
warstwy produktu utleniania, powstałej w początkowej fazie procesu,
powstawanie jonów utleniacza na powierzchni adsorbującej warstwy
zgorzeliny i wbudowywanie się ich w sieć krystaliczną zgorzeliny,
dyfuzja jonów metalu z równoważną liczbą elektronów z fazy metalicznej do
zgorzeliny
dyfuzja odrdzeniowa jonów metalu i elektronów od granicy faz rdzeń
metalowy– zgorzelina do powierzchni warstwy przez defekty sieci
krystalicznej w niej występujące,
dyfuzja dordzeniowa jonów utleniacza od granicy faz utleniacz-zgorzelina do
granicy zgorzelina-rdzeń metalowy, połączona z dyfuzją elektronów w
kierunku przeciwnym,
jednoczesna dyfuzja jonów metalu oraz jonów utleniacza w przeciwnych
kierunkach, połączona z odpowiednią dyfuzją elektronów,
dyfuzja metalu, a szczególnie utleniacza – w postaci jonów, atomów lub
cząsteczek– wzdłuż granic ziaren w zgorzelinie oraz metalu.
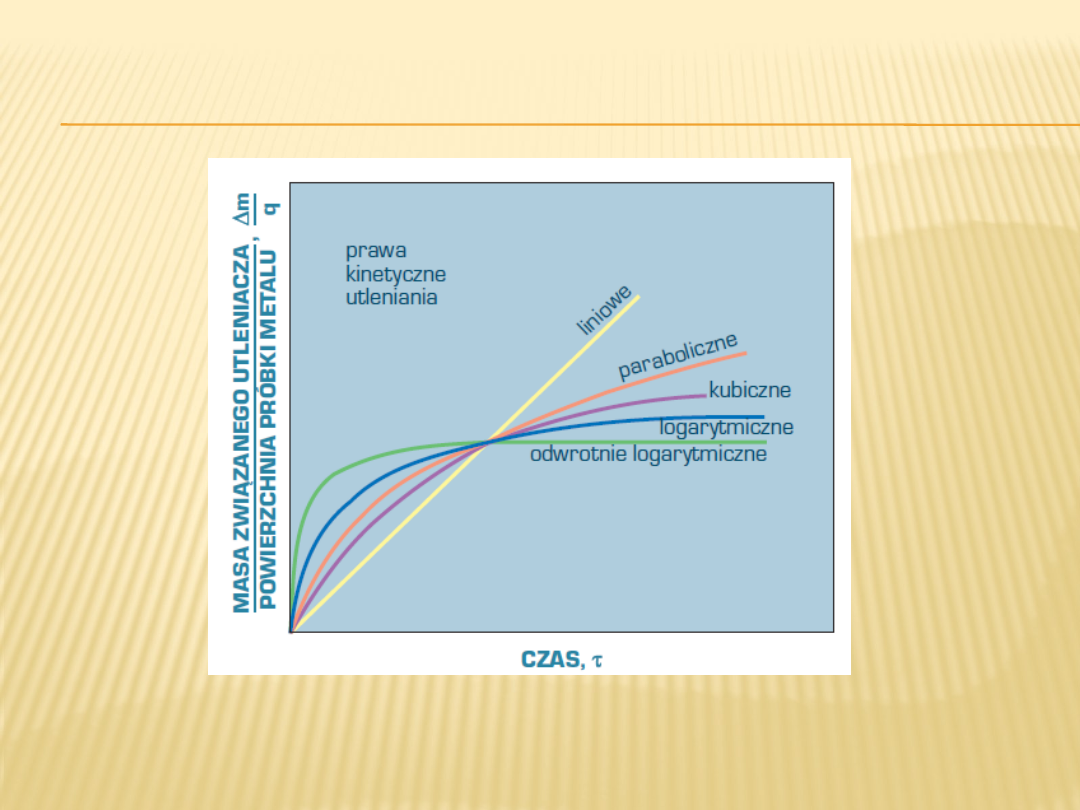
SZYBKOŚĆ UTLENIANIA METALI I
STOPÓW
Rys. 5. Schemat praw kinetycznych utleniania metali

UTLENIANIE
WYSOKOTEMPERATUROWE
Produkty reakcji utleniania metalu zwykle
występują w stanie stałym, rzadko w stanie
ciekłym lub gazowym. Warstwy stałego
produktu reakcji utleniania są nazywane:
zgorzelinami, gdy już po kilku sekundach ich
grubość jest większa od 10 μm,
warstwami nalotowymi, gdy ich grubość jest
mniejsza nawet po bardzo długim czasie.
Warstwy nalotowe są zwykle zwarte i
jednofazowe w całej swej objętości.

ZGORZELINA
Zgorzelina utworzona na powierzchni
czystych metali oraz stopów składa się
przeważnie z dwóch lub trzech warstw,
z których zewnętrzna, granicząca z
utleniaczem, jest najczęściej zwarta,
natomiast wewnętrzna, granicząca z
metalem –porowata
Zgorzeliny mogą być jednofazowe lub
wielofazowe.
ZGORZELINA - ETAP POCZĄTKOWY
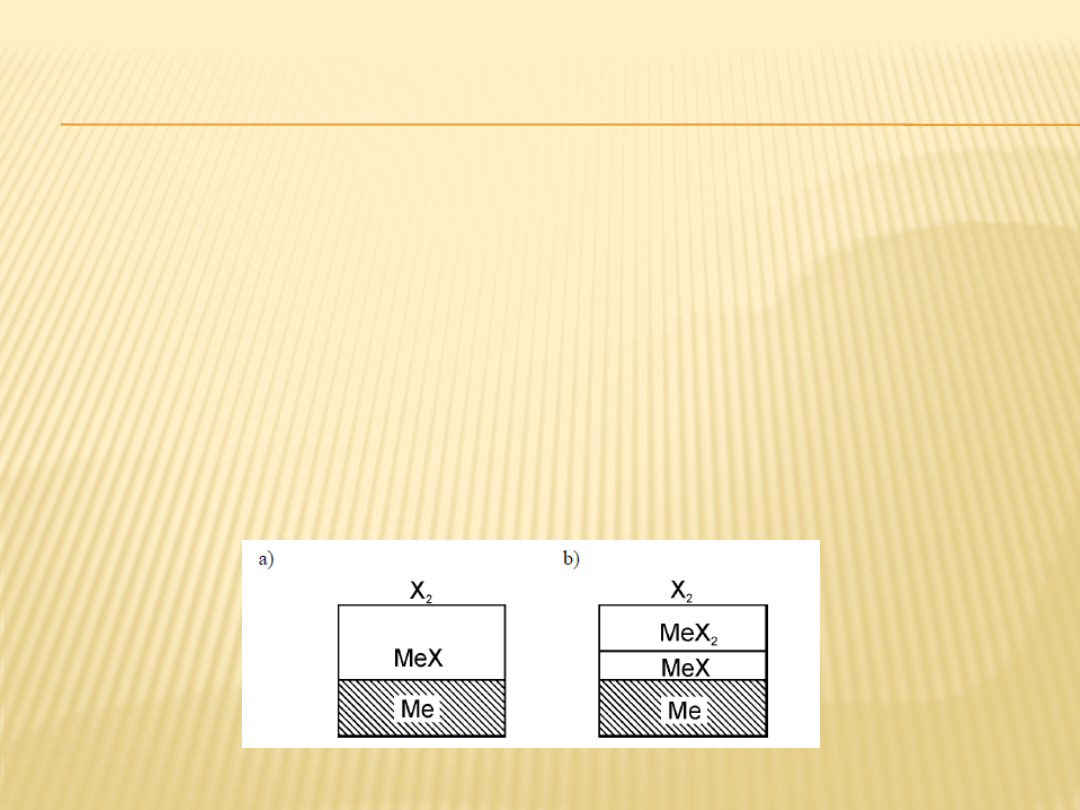
W początkowym procesie reakcji, gdy zgorzelina jest
stosunkowo cienka, na powierzchniach płaskich
utlenianego elementu tworzy się zgorzelina zwarta w
całym swym przekroju, przylegająca ściśle do podłoża
(rys.6 a).
Jeśli metal może tworzyć z utleniaczem w podwyższonej
temperaturze kilka termodynamicznie trwałych związków
(w których metal będzie na różnym stopniu utlenienia), to
powstająca zgorzelina może być wielofazowa (rys.6b).
Rys. 6. Schemat budowy zgorzeliny: a) jednofazowej, b) dwufazowej
(dwuwarstwowej), w początkowym etapie jej powstawania
ZGORZELINA ROZWINIĘTA
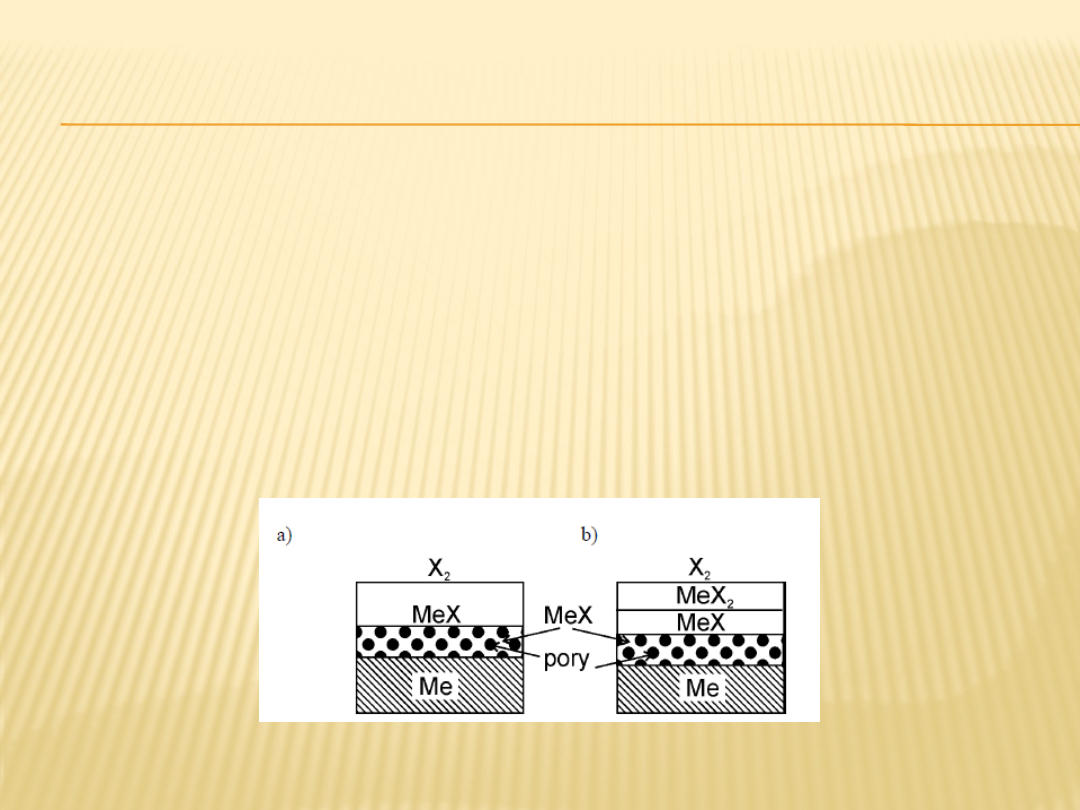
Podczas długotrwałego utleniania pomiędzy
rdzeniem metalicznym i pierwotną zwartą
warstwą zgorzeliny tworzy się z reguły porowata
warstwa wewnętrzna, zbudowana z tej samej
fazy produktu reakcji, z której składa się
warstwa zgorzeliny sąsiadująca bezpośrednio z
metalem w stadium początkowym.
Rys. 7. Schemat budowy zgorzeliny: a) jednofazowej, b) dwufazowej
(wielowarstwowej)
w późniejszym stadium jej powstania
ZGORZELINA – AX I BX Z NIEOGRANICZONA
ROZPUSZCZALNOŚCIĄ
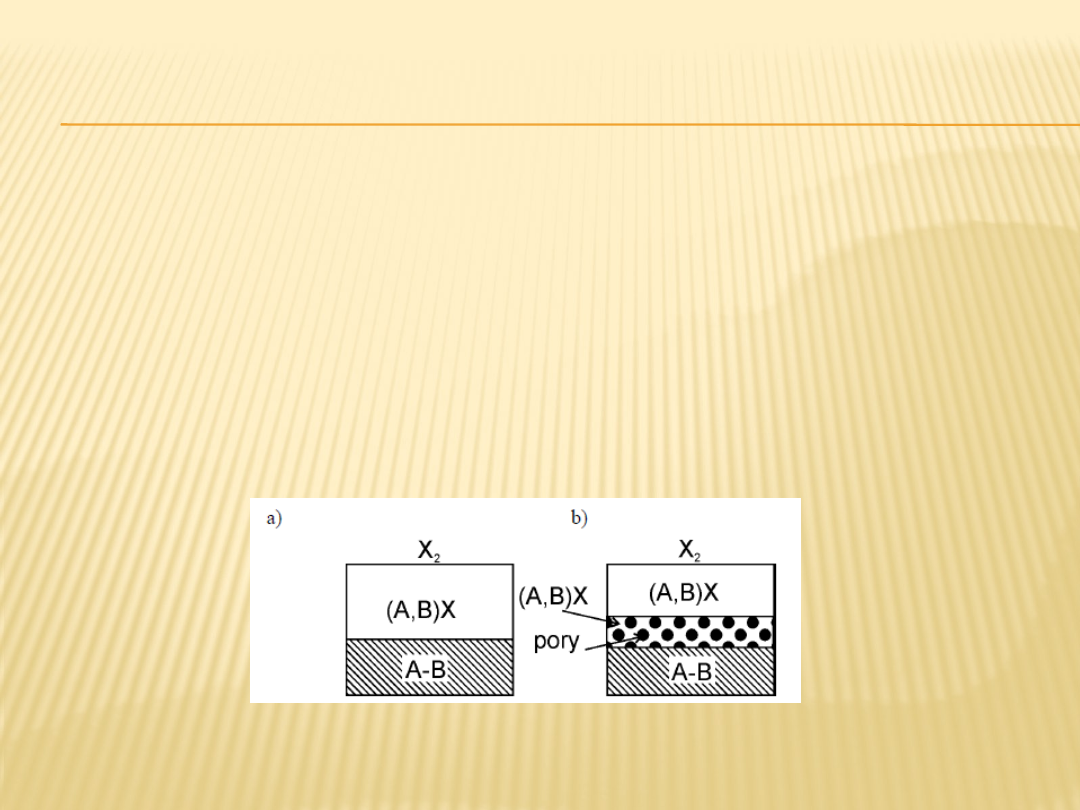
Na stopach dwuskładnikowych, jeżeli oba
składniki A i B mogą tworzyć w warunkach
reakcji związki chemiczne z utleniaczem X, przy
czym wzajemna rozpuszczalność związków AX i
BX jest nieograniczona, niezależnie od składu
stopu powstaje zgorzelina jednofazowa
Rys. 8. Schemat budowy jednofazowej zgorzeliny na stopie
dwuskładnikowym: a) początkowe
stadium reakcji, b) stadium późniejsze; związki AX i BX wykazują
rozpuszczalność
wzajemną nieograniczoną
ZGORZELINA – BRAK ROZPUSZCZALNOŚCI
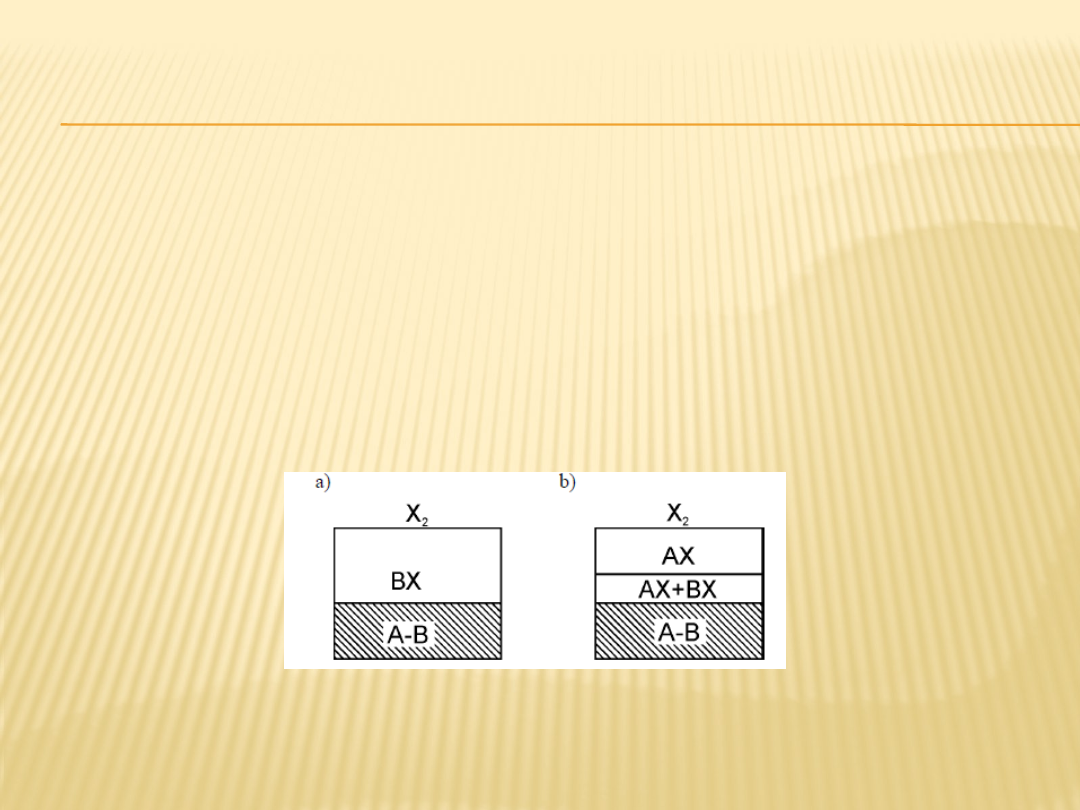
Gdy związki obu metali z utleniaczem nie wykazują żadnej
rozpuszczalności wzajemnej (oraz metale różnią się
powinowactwem chemicznym do utleniacza), wówczas może
powstawać:
zgorzelina homogeniczna zawierająca tylko jeden związek (np. BX, rys.9a)
Zgorzelina dwuwarstwowa heterofazowa, w której warstwę zewnętrzną
tworzy związek metalu podstawowego z utleniaczem (np. AX), a
heterofazową warstwę wewnętrzną mieszanina związków obu składników
stopu z utleniaczem (AX+BX) (rys.9b).
Rys. 9. Schemat budowy zgorzeliny na stopach dwuskładnikowych w przypadku: a) utleniania
selektywnego, gdy stężenie składnika B jest wystarczające do utworzenia warstwy homogenicznej,
b) tworzenia się produktów korozji gazowej wykazujących brak rozpuszczalności wzajemnej, składnik A
jest składnikiem podstawowym o niższym powinowactwie chemicznym do utleniacza niż składnik
stopowy

ZGORZELINA – OGRANICZONA ROZPUSZCZALNOŚĆ
Gdy związki AX i BX wykazują w warunkach reakcji
ograniczoną rozpuszczalność wzajemną, wówczas
tworzyć się może heterofazowa zgorzelina
dwuwarstwowa z ciągłą warstwą wewnętrzną związku
o wyższym powinowactwie chemicznym do utleniacza
(np. BX) nasyconego składnikiem o niższym
powinowactwie chemicznym do utleniacza (w
rozpatrywanym przypadku składnikiem A)
Rys. 10 Schemat budowy heterofazowej zgorzeliny na stopie dwuskładnikowym
w przypadku
ograniczonej rozpuszczalności wzajemnej związków AX i BX; składnik A jest
składnikiem podstawowym o niższym powinowactwie chemicznym do
utleniacza niż składnik stopowy B, (początkowe stadium procesu)
ZGORZELINA A ATMOSFERA
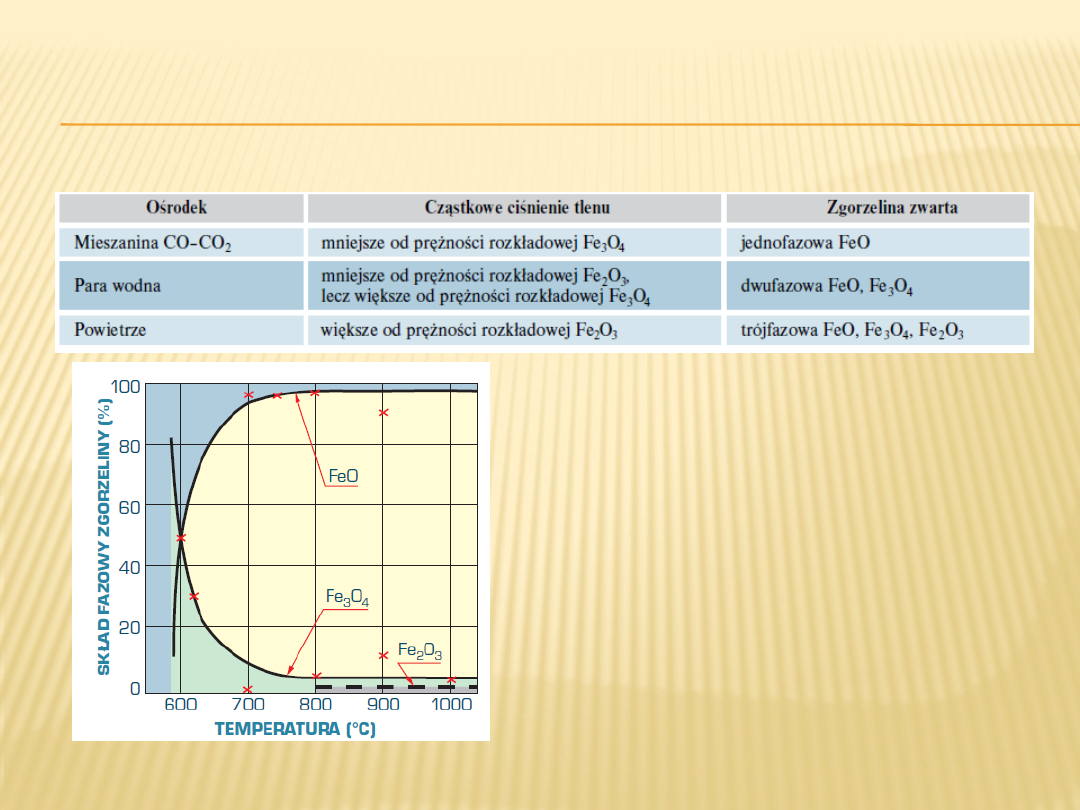
Tablica 1. Typ zgorzeliny tworzącej się w temperaturze 1000C w
zależności od rodzaju atmosfery utleniającej
Z powierzchnią metalu graniczy
zawsze faza, w której metal występuje
w najniższym stopniu
utlenienia (w przypadku żelaza – FeO).
Z atmosferą utleniającą graniczy faza,
w której
metal cechuje się najwyższym
stopniem utlenienia – Fe
2
O
3
Stosunek
grubości faz w zgorzelinie wielofazowej
zwykle nie zależy od czasu reakcji, lecz
zmienia się w sposób istotny wraz z
podwyższeniem temperatury procesu.
Względny udział grubości fazy
wewnętrznej, w której metal
charakteryzuje się najniższym
stopniem utlenienia, rośnie wraz z
podwyższeniem temperatury reakcji.
Rys. 11. Wpływ temperatury na
skład fazowy zgorzeliny tlenkowej
na żelazie
UTLENIANIE WEWNĘTRZNE
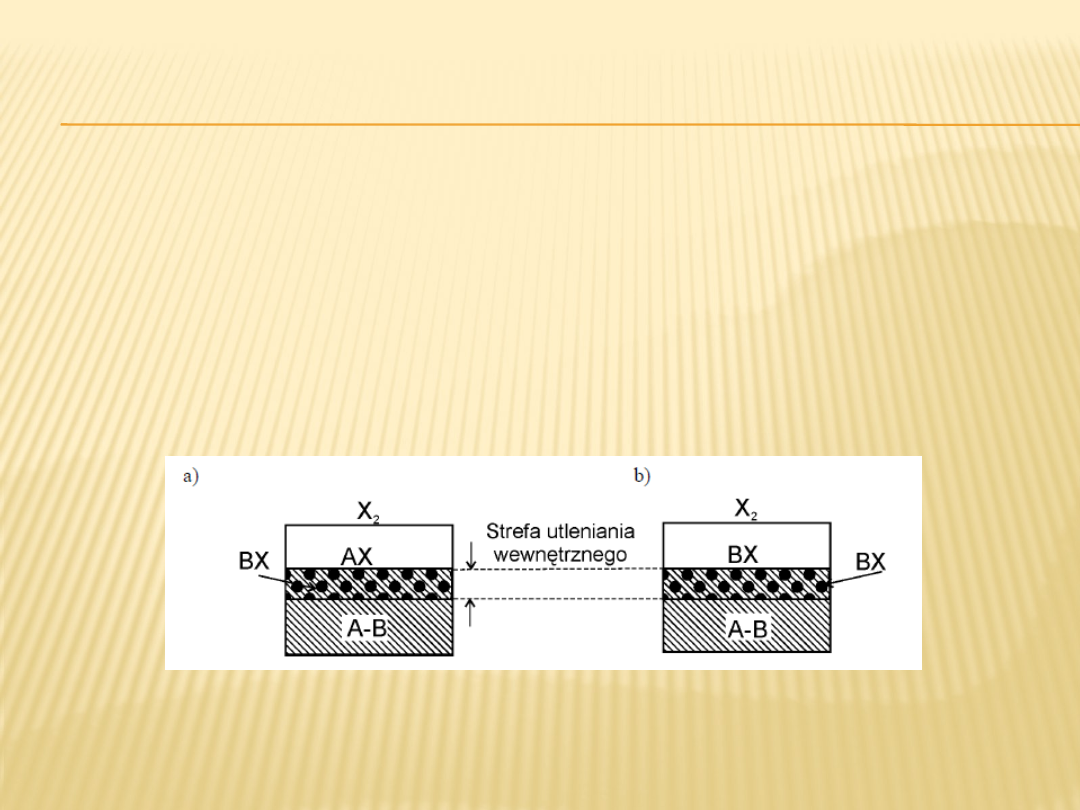
Jeżeli składnik utleniający atmosfery może dyfundować
w głąb stopu i utworzyć związek z metalem o wyższym
powinowactwie chemicznym (np. B) zanim składniki
stopowe zdążą przedyfundować do powierzchni, to na
stopach bogatych w metal A pod warstwą zgorzeliny AX
tworzą się w stopie wysepki związku BX.
Rys. 12. Schemat budowy zgorzeliny i strefy wewnętrznego utleniania w
przypadku tworzenia się jednofazowego produktu reakcji: a – stop bogaty w
metal A, b – stop bogaty w metal B; powinowactwo chemiczne składnika B
wyższe niż składnika A

UTLENIANIE WEWNĘTRZNE
Zjawiska zachodzące wewnątrz materiału
wskutek rozpuszczania się w nim składników
środowiska zewnętrznego można podzielić na
następujące grupy:
tworzenie się roztworów stałych;
przemiany fazowe typu alotropowego;
tworzenie się związków chemicznych lub faz
pośrednich z rozpuszczających się składników
atmosfery i składników materiału, wykazujących do
tych pierwiastków powinowactwo chemiczne (np.
utlenianie wewnętrzne, powstawanie węglików).

UTLENIANIE WEWNĘTRZNE
Proces utleniania wewnętrznego zachodzi wówczas, gdy
utleniacz wnikający do stopu z otaczającej atmosfery
reaguje z jego składnikami, tworząc wydzielenia produktów
reakcji.
Częstą przyczyną tego zjawiska jest małe stężenie tlenu w
otaczającej atmosferze, nie wystarczające do wytworzenia
się warstwy produktu reakcji tlenu z metalem
podstawowym.
Głównymi składnikami powodującymi utlenianie
wewnętrzne są tlen, azot i wodór. Migrują one szybko w
głąb materiału tworząc roztwory międzywęzłowe. Wodór
wnikając do metalu reaguje z węglem tworząc
węglowodorki np. metan, powodując korozję wodorową.

UTLENIANIE WEWNĘTRZNE
Rys. 13. Utlenianie wewnętrzne bez trwałej
zgorzeliny
Rys. 14. Utlenianie wewnętrzne ze zgorzeliną
heterowarstwową

ZAPOBIEGANIE KOROZJI GAZOWEJ
Skład chemiczny stopu i jego zdolność do tworzenia zgorzeliny, która
odgrywa jednocześnie rolę warstwy ochronnej, należy do najistotniejszych
czynników decydujących o przebiegu korozji gazowej. Dobre własności
ochronne wykazuje zgorzelina w postaci ciągłej warstwy jednofazowej
związku – np. BX – utworzona na powierzchni stopu przez dodatek stopowy
o znacznym powinowactwie chemicznym z utleniaczem. Dodatkami takimi
są np. Zn, Al, Si, Cr, Be i Mg. Istotne jest przy tym, by związek BX ściśle
przylegał do metalicznego rdzenia i nie tworzył niskotopliwych eutektyk z
innymi produktami korozji. Warstwa ochronna, której skład fazowy zależy od
rodzaju stopu, nie powinna również wykazywać pęknięć i mikroszczelin,
umożliwiających dyfuzję cząstkową i dysocjacyjny przebieg tworzenia
zgorzelin wielowarstwowych. W niektórych przypadkach skład stopu należy
dobierać tak, aby w wyniku działania tlenu w stopie występowała strefa
utleniania wewnętrznego polepszająca żaroodporność. Jednocześnie liczne
dodatki stopowe sprzyjają przyspieszeniu przebiegu korozji. Przykładem
może być węgiel jako podstawowy składnik stopowy stali, decydujący o
uzyskiwaniu przez te stopy wymaganych własności mechanicznych.
Selektywne utlenianie węgla powoduje odwęglenie, natomiast przewaga
utleniania żelaza wpływa na dodatkowe nawęglenie stali.
Document Outline
- Slide 1
- Podstawy zjawiska korozji
- Podział Korozji
- Korozja Chemiczna - Gazowa
- Korozja Gazowa - Skutki
- Reakcja Chemiczna Utleniania
- Slide 7
- Szybkość Utleniania Metali i stopów
- Utlenianie Wysokotemperaturowe
- Zgorzelina
- Zgorzelina - Etap początkowy
- Zgorzelina Rozwinięta
- Zgorzelina – AX i BX z nieograniczona rozpuszczalnością
- Zgorzelina – Brak rozpuszczalności
- Zgorzelina – Ograniczona Rozpuszczalność
- Zgorzelina a Atmosfera
- Utlenianie Wewnętrzne
- Utlenianie wewnętrzne
- Utlenianie Wewnętrzne
- Utlenianie Wewnętrzne
- Zapobieganie Korozji Gazowej
Wyszukiwarka
Podobne podstrony:
korozja chemiczna i elektrochemiczna metali, Studia, Chemia, chemia od Ines(1)
KOROZJA CHEMICZNA, PWR, chemia
Podstawy technologii chemicznej nowoczesne procesy utleniania
03 Reakcje chemiczne II, utlenianie i redukcja instrukcja
03 Reakcje chemiczne II utlenianie i redukcja instrukcja
Procesy utleniania-utlenianie ksylenów, Uczelnia PWR Technologia Chemiczna, Semestr 5, Technologia C
6 - utlenianie cykloheksanolu, Technologia chemiczna PWR, SEMESTR III, Chemia techniczna organiczna
ćw B Procesy utleniania-utlenianie ksylenów, Uczelnia PWR Technologia Chemiczna, Semestr 5, Technolo
Chemia budowlana - Sprawozdanie 2, Budownictwo S1, Semestr I, Chemia budowlana, Sprawozdania, Redukc
15 Utlenianie chemiczne
Utlenianie i redukcja związków organicznych, Technologia żywności i żywienia człowieka, Inżyneria ch
grochulska segal,systemy odnowy wody, utlenianie chemiczne
Chemia budowlana - Sprawozdanie 3, Budownictwo S1, Semestr I, Chemia budowlana, Sprawozdania, Redukc
Badania utleniania wysokotemperaturowego stopów
15 Utlenianie chemiczne
Utlenianie redukcja Ciepło w reakcjach chemicznych
więcej podobnych podstron