10
aseptyka.
Rok 4. Nr 3/2002
Autor
Higiena
Pozycja kwasu nadoctowego pośród
różnych grup substancji czynnych
Spośród różnych grup substancji
czynnych używanych w dezynfekcji
tylko trzy dysponują rzeczywiście
szeroką skutecznością. Są to aldehy-
dy, chlorowce i ich związki oraz
nadtlenki. Są zasadniczo w stanie
zniszczyć lub inaktywować wszystkie
bakterie łącznie z przetrwalnikami
(Bacillus sp., Clostridinum sp.), grzyby
łącznie z przetrwalnikami grzybów (np.
Aspergillus niger) oraz wirusy łącznie
z najbardziej odpornymi, bezosłono-
wymi wirusami hydrofilowymi (np.
poliowirusem, wirusem zaplenia
wątroby typu A). Te trzy grupy określa-
ne są mianem substancji reaktywnych,
ponieważ pod względem chemicznym
są one silnie reaktywne i niszczą
drobnoustroje w ten sposób, że
wchodzą w reakcje chemiczne z
substancjami zawartymi w komórkach.
Wspomniane trzy grupy substancji reak-
tywnych charakteryzują się różnymi właści-
wościami techniczno-użytkowymi. Obok
skuteczności istotną rolę w wielu dziedzi-
nach zastosowań odgrywa wydajność my-
jąca środków dezynfekcyjnych. Dzięki
znacznej sile utleniającej związki chlorow-
ców (głównie związki z aktywnym chlorem)
wykazują dobre własności myjące. Środki
chlorowo-alkaliczne używane są szeroko na
przykład w przemyśle spożywczym do roz-
wiązywania trudnych problemów związa-
nych z myciem. Z drugiej strony właściwości
te oznaczają stosunkowo silnie występujący
błąd proteinowy w przypadku środków de-
zynfekcyjnych na bazie aktywnego chloru,
ponieważ powstające w trakcie ich działania
rodniki chloru szybko reagują również z każ-
dym obciążeniem organicznym tworząc nie-
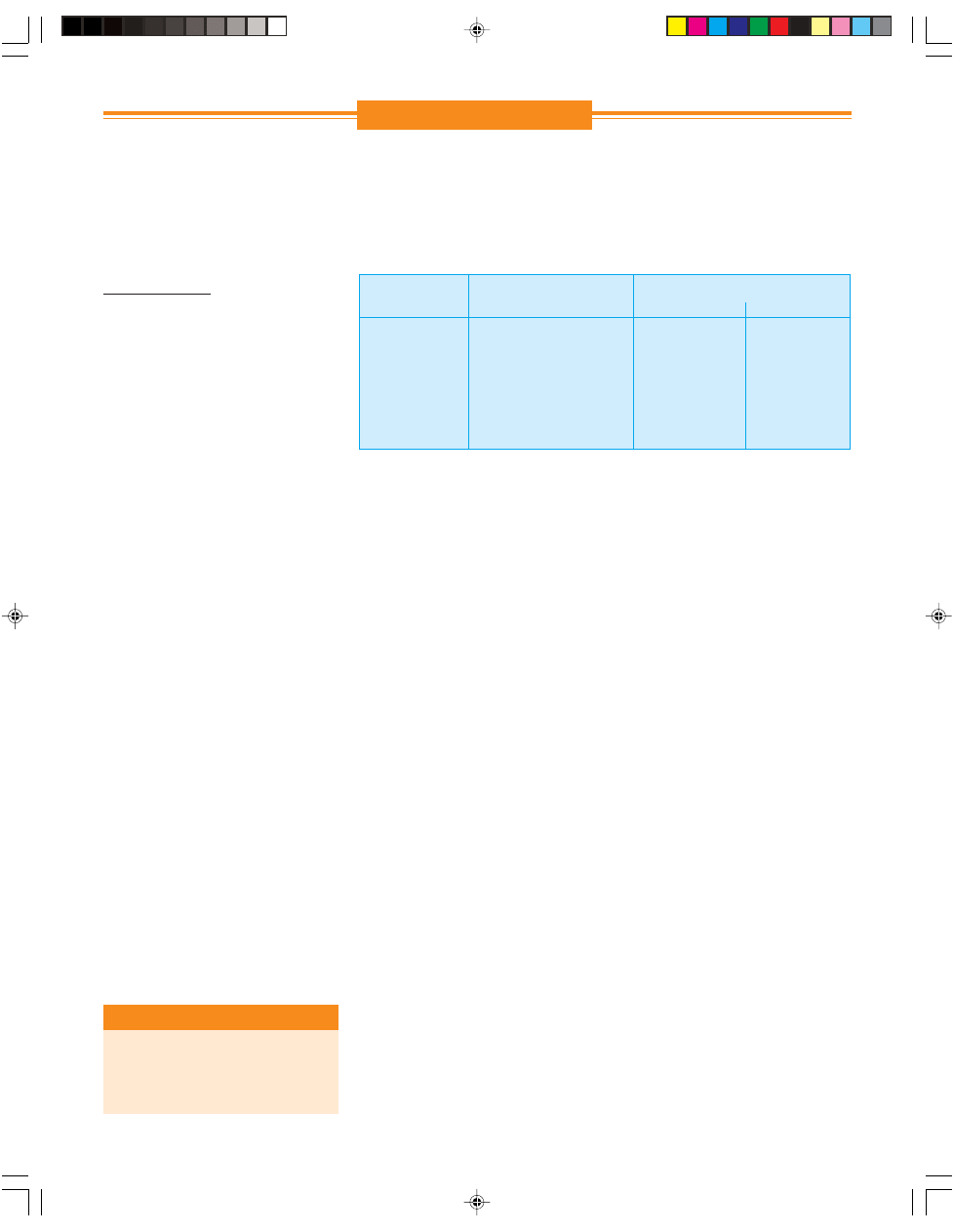
skuteczne związki. Jak pokazuje tabela 1
błąd proteinowy nadtlenków (w naszym
przykładzie kwasu nadoctowego) jest w po-
równaniu z chlorowcami niewielki. Aldehydy,
mimo że np. reagują z wolnymi grupami
amonowymi białek, wykazują stosunkowo
niewielki błąd proteinowy. Przez taką reak-
cję z białkami, która nie niszczy jednak cał-
kowicie ich struktury, aldehydy doprowadza-
ją do ścinania się białek, a tym samym do
ich utrwalania. Środki na bazie aldehydów
mają więc porównawczo gorsze własności
myjące, które można ewentualnie skom-
pensować wzmacniaczem mycia.
W niektórych dziedzinach zastosowań
również zasadniczy wpływ może mieć
temperatura. Podczas gdy zwiększenie
temperatury (np. w chemotermicznych
procesach dezynfekcyjnych) zasadniczo
poprawia skuteczność czynnych substan-
cji dezynfekcyjnych, niższe temperatury
oddziałują na niektóre substancje w spo-
sób zróżnicowany. Aldehydy odznaczają
się stosunkowo poważnym błędem tem-
peraturowym, natomiast w przypadku
związków z aktywnym chlorem i nadtlen-
kami efekt ten jest mniej wyraźny.
Wreszcie również względy ekologiczne
odgrywają pewną rolę przy wyborze sub-
stancji dezynfekcyjnych. Aldehydy i nadtlen-
ki charakteryzują się dobrą biodegradowal-
nością, natomiast przy dezynfekcji wykony-
wanej związkami z aktywnym chlorem na-
wet w niewielkich stężeniach powstają
związki chloroorganiczne, których część z
trudem poddaje się degradacji biologicznej.
Nadtlenki rozpadają się już podczas stoso-
wania lub najpóźniej zaraz potem w ście-
kach, tworząc niegroźne pod względem
ekologicznym produkty rozpadu.
Pozycja kwasu nadoctowego
w porównaniu z innymi nadtlenkami
Najprostszym związkiem pośród nad-
tlenków jest nadtlenek wodoru. Nadtlenek
wodoru ma co prawda dobre działanie wy-
bielające, ale jego mikrobobójcze działanie
jest stosunkowo słabe. Skuteczność przeciw
przetrwalnikom wykazuje dopiero przy wyso-
kich stężeniach lub w wyższych temperatu-
rach. Znacznie lepszą skuteczność mają pe-
roksykwasy organiczne, np. kwas nadocto-
wy, kwas nadbursztynowy i kwas nadftalowy.
Pośród peroksykwasów organicznych stoso-
wanych do dezynfekcji kwas nadoctowy wy-
różnia się tym, że jego roztwory użytkowe
wysychają bez reszty, ponieważ nawet po-
wstający podczas dezynfekcji kwas octowy
odparowuje w całości. Pośród peroksykwa-
sów o prostych łańcuchach (kwas nadmrów-
kowy, nadpropionowy itp.) kwas nadoctowy
jest stosunkowo najmnej uciążliwy pod
względem zapachowym.
11 >
Kwas nadoctowy
jako substancja czynna w dezynfekcji
Drobnoustroje
Drobnoustroje
Drobnoustroje
Drobnoustroje
Drobnoustroje
Substancja
Substancja
Substancja
Substancja
Substancja Czas zniszczenia (min.)
Czas zniszczenia (min.)
Czas zniszczenia (min.)
Czas zniszczenia (min.)
Czas zniszczenia (min.)
testowe
testowe
testowe
testowe
testowe
czynna
czynna
czynna
czynna
czynna
bez obciążenia
bez obciążenia
bez obciążenia
bez obciążenia
bez obciążenia z obciążeniem
z obciążeniem
z obciążeniem
z obciążeniem
z obciążeniem
Staph. aureus
kwas nadoctowy (90 ppm)
5
5
Ps. aeruginosa
kwas nadoctowy (90 ppm)
5
5
E. coli
kwas nadoctowy (90 ppm)
5
5
Staph. aureus
chlor (210 ppm)
5
60
Ps. aeruginosa
chlor (210 ppm)
5
>60
E. coli
chlor (210 ppm)
5
30
Tab.1: Błąd proteinowy aktywnego chloru (chlorowy ług bielący) w porównaniu z kwasem
nadoctowym. Jakościowy test zawiesinowy z obciążeniem białkiem (10% surowicy bydlęcej)
i bez obciążenia. Dane na temat stężenia odnoszą się do substancji aktywnej. W przypadku
aktywnego chloru obciążenie organiczne wymaga znacznego przedłużenia czasu oddziały-
wania, aby osiągnięte zostało całkowite zniszczenie drobnoustrojów testowych.
Dr Bernhard Meyer
Henkel Ecolab GmbH&Co OHG
Postfach 130406
40554 Düsseldorf
B. Meyer
Aseptyka_3_02.p65
2003-02-05, 09:49
10
11
aseptyka.
Rok 4. Nr 3/2002
Higiena
Właściwości użytkowo-techniczne
kwasu nadoctowego
Obok skuteczności (patrz dalej) także
istotne właściwości użytkowo-techniczne
kwasu nadoctowego zależą od pH roztworu
użytkowego. Ponieważ cząsteczki kwasu
nadoctowego wraz z malejącym pH coraz
bardziej objawiają się jako (zdolny do odpa-
rowania) wolny kwas, zatem wraz z maleją-
cym pH wzrasta uciążliwość zapachowa
roztworów o dużym stężeniu. Również tole-
rancja metali względem kwasów jest gorsza
niż względem zasad. Zdolność rozpuszcza-
nia białek wzrasta ze wzrostem pH, zaś
zdolność rozpuszczania wapna występuje
tylko w kwasowym zakresie pH. Stabilność
kwasu nadoctowego maleje wraz ze wzro-
stem pH, ponieważ w środowisku zasado-
wym kwas rozkłada się spontanicznie, po-
dobnie jak wszystkie nadtlenki. Zalecane
jest więc optymalizowanie używania środ-
ków dezynfekcyjnych na bazie kwasu na-
doctowego do specjalnych dziedzin zasto-
sowań o odpowiednim pH.
Kwas nadoctowy można wytwarzać
dwoma zasadniczo różnymi sposobami.
Płynny kwas nadoctowy otrzymywany jest w
drodze prowadzącej do stanu równowagi re-
akcji nadtlenku wodoru z kwasem octowym.
Powstające w ten sposób stężone roztwory
kwasu nadoctowego można stosować bez-
piecznie jedynie w zamkniętych układach,
np. w automatach dezynfekcyjnych lub w
dezynfekcji urządzeń o zamkniętych obie-
gach cieczy, np. aparatów do hemodializy.
Ręczne dozowanie należy wykluczyć, ponie-
waż stężone kwasy są silnie żrące i przy za-
nieczyszczeniu mogą ulec spontanicznemu
rozkładowi, przy czym w sposób wybuchowy
uwalniane są znaczne ilości gazu. Długolet-
nie bezpieczne stosowanie w zamkniętych
układach nie tylko w medycynie, ale również
w branży produkcji napojów i w pralniach
przemysłowych wykazuje, że wykorzystywa-
nie w zamkniętych systemach nie powoduje
nadmiernych zagrożeń.
Do dezynfekcji metodami ręcznymi za-
lecane są systemy, w których kwas nadoc-
towy powstaje dopiero w roztworach użyt-
kowych o odpowiednio niskich stężeniach.
Systemy takie bazują na nadboranie sodo-
wym i TAED (tetracetyloetylenodiamina) i od
wielu lat używane są w proszkach do prania
jako wybielacze. Powstawanie kwasu na-
doctowego na bazie nadboranu i TAED jest
również zależne od pH. Tworzenie się kwa-
su nadoctowego występuje w środowisku
zasadowym silniej, chociaż powstająca
substancja aktywna rozkłada się szybciej
(patrz powyżej). Również tu należy dobierać
optymalną wartość pH.
Mikrobobójcze właściwości
kwasu nadoctowego
Mechanizm działania mikrobobójcze-
go kwasu nadoctowego nie jest całkowi-
cie wyjaśniony. Udowodniono, że rodniki
hydroksylowe odgrywają tutaj decydującą
rolę. Można założyć, że rodniki te powo-
dują nieodwracalne uszkodzenia w zredu-
kowanych grupach funkcjonalnych białek
i tym samym niszczą aparat enzymatycz-
ny i strukturę komórek. To ostatnie zjawi-
sko prowadzi między innymi do nieszczel-
ności błon komórkowych. Kwas nadocto-
wy wykazuje zatem, jak prawie wszystkie
aktywne substancje dezynfekcyjne, sto-
sunkowo niespecyficzny mechanizm dzia-
łania, który w zasadzie uniemożliwia wy-
kształcenie w mikroorganizmach oporno-
ści na tego rodzaju substancje.
Kwas nadoctowy wyróżnia się obok pre-
paratów z aktywnym chlorem najlepszą sku-
tecznością przeciw błonom (filmom) biolo-
gicznym, które często powodują problemy
w układach obiegowych cieczy i innych sys-
temach zamkniętych. Jest to prawdopodob-
nie związane z tym, że zrównoważone pe-
roksykwasy zawsze powodują oderwanie
błony biologicznej od powierzchni przy po-
mocy występującego nadtlenku wodoru.
Przez to ułatwione jest niszczenie przez
kwas nadoctowy komórek drobnoustrojów
zagnieżdżonych w błonie biologicznej.
Skuteczność mikrobobójcza kwasu na-
doctowego zależna jest od pH. Zasadniczo
skuteczność w środowisku kwaśnym jest
lepsza niż w zasadowym. Wynika to z tego,
że tylko w środowisku kwaśnym występują-
cy głównie wolny kwas może przenikać
przez błony komórkowe do wnętrza komó-
rek mikroorganizmów, zaś w środowisku al-
kalicznym występujące przede wszystkim
jony mogą przenikać do komórek dopiero
wtedy, gdy błony komórkowe zostaną już
uszkodzone. Można zatem założyć, że
wspomniane rodniki hydroksylowe powsta-
ją dopiero wewnątrz organizmu docelowe-
go. I tak np. przy pH 3 już 300 ppm kwasu
nadoctowego wykazuje w ciągu 30 minut
skuteczność przeciw przetrwalnikom, zaś
przy pH 8 w tych samych warunkach sku-
teczność jest praktycznie poniżej granicy
mierzalności. Skuteczność przeciw bakte-
riom nie tworzącym przetrwalników (np. wg
EN 1276) osiągana jest przy pH 3 już od
około 50 ppm nawet przy +4°C w ciągu 5
minut. Dla osiągnięcia tej samej skuteczno-
ści bakteriobójczej przy pH 8 konieczne jest
stężenie 300 ppm.
Mimo wszystko kwas nadoctowy wyka-
zuje nawet w środowisku alkalicznym zna-
czącą skuteczność mikrobobójczą. Dlate-
go stosowany jest np. z powodzeniem w
połączeniu z zasadowymi środkami piorą-
cymi w chemotermicznej dezynfekcji bieli-
zny. W celu lepszego wykorzystania roz-
puszczalności białek w środowisku zasa-
dowym opracowano również środki do de-
zynfekcji narzędzi o lekko alkalicznym pH
ze wspomnianymi systemami generujący-
mi kwas nadoctowy. Przy pH 8 potrzeba
około 900 - 1000 ppm kwasu octowego,
aby w temperaturze pokojowej osiągnąć
wystarczającą skuteczność przeciwko
prątkom zgodnie z wytyczną DGHM (Nie-
mieckiego Stowarzyszania ds. Higieny i
Mikrobiologii) dla środków do dezynfekcji
narzędzi. W tych samych warunkach osią-
gana jest wystarczająca skuteczność prze-
ciw poliowirusom zgodnie z wytyczną DVV
(Niemieckiego Zrzeszania ds. Zwalczania
Chorób Wirusowych), a tym samym szero-
ka skuteczność wirusobójcza.
Wykrywanie kwasu nadoctowego
Stężenie kwasu nadoctowego panujące
w roztworze użytkowym w trakcie jego sto-
sowania jest oczywiście decydujące dla od-
powiedniego efektu mikrobobójczego. Za-
leży jednak od otaczających warunków, np.
temperatury, ale przede wszystkim od po-
tencjalnego oddziaływania substancji orga-
nicznych podczas stosowania. Dlatego dla
użytkownika wskazane jest dysponowanie
możliwością skontrolowania zawartości
kwasu nadoctowego w roztworze użytko-
wym. Jako środek utleniający kwas nadoc-
towy można zmierzyć przez stosunkowo
proste do wykonania miareczkowanie. W
tym celu konieczne są jednak różne roztwo-
ry do miareczkowania i pewien zasób do-
świadczenia. Z drugiej strony dla użytkowni-
ka środka dezynfekcyjnego wystarczające
jest sprawdzenie, czy zapewnione jest jesz-
cze minimalne stężenie niezbędne dla okre-
ślonego celu. Oferowane są tu łatwe w uży-
ciu paski testowe, przy pomocy których na
podstawie reakcji barwnej i porównania ze
skalą kolorów możliwa jest ocena roztworu
użytkowego.
Aseptyka_3_02.p65
2003-02-05, 09:49
11
Wyszukiwarka
Podobne podstrony:
Dz U 2002 nr 125 poz 1064
Dz U 2002 nr 199 poz 1673 id Nieznany
Dz U 2002 nr 92 poz 818
Substancje samozapalne 97 2002
Dz-U-2002-Nr-113-poz-984
Dz U 2002 nr 147 poz 1229
Ewidencja zatrudnienia Dz U 2002 Nr 219 poz 1838
Dz U 2002 Nr 199 poz 1673
DU z dnia 11 października 2002 r. Nr 169 Poz. 1386, Studia, STUDIA PRACE ŚCIĄGI SKRYPTY
Dz.U. z 2002 nr 217 poz 1833(1), BHP Ula, Ustawy
DzU 2002 nr 147 poz 1229 o ochronie przeciwpożarowej
Dz U 2002 nr 117 poz 1007 Ustawa o materiałach wybuchowychy
Trucizny jako substancje bezpośrednio zagrażające życiu ludz
Dz U 2002 nr 92 poz 819
Dz U 2002 nr 75 poz 690
NR 24 ANTROPOMOTORYKA 2002, NR 24 ANTROPOMOTORYKA 2002
więcej podobnych podstron