30. Spin elektronu, doświadczenie Sterna-Gerlacha, rozszczepienie linii widmowych. Liczba stanów elektronowych w atomie.
Spin elektronu - spin 
jest nieodłączną cechą elektronu, taka jak jego masa czy też ładunek elektryczny (Spinowy moment pędu (spin) jest wewnętrzną własnością elektronu). Wartość spinu jest skwantowana i zależy od spinowej liczby kwantowej s. Składowa spinu 
zmierzona wzdłuż dowolnej osi jest także skwantowana i zależy od magnetycznej spinowej liczby kwantowej ms, która może przyjmować tylko wartości +1/2 lub -1/2.
Rozszczepienie linii widmowych - pojawienie się w miejscu jednej linii kilku linii wzajemnie rozsuniętych. Powodem rozszczepienia linii widmowych może być zewnętrzne pole magnetyczne (zjawisko Zeemana) lub elektryczne (zjawisko Starka).
Liczba stanów elektronowych w atomie - Wszystkie stany elektronowe o jednakowej liczbie kwantowej „n” tworzą powłokę. Powłokę tworzy 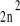
stanów elektronowych. Wszystkie stany o jednakowych wartościach liczb kwantowych „n” i „l” tworzą podpowłokę.
Wszystkie stany tworzące podpowłokę mają niemal jednakową energię (w każdym bądź razie różnicę energii między nimi pomija się przy chociażby ustalaniu elektronowych poziomów energetycznych - czyli przyjmuje się że liczba kwantowa „m” (jak też „ms”) nie mają wpływu na poziom energetyczny). Podpowłokę tworzy 2(2l+1) stanów elektronowych.
31. Zakaz Pauliego, atomy wieloelektronowe, obsadzanie orbitali elektronowych, układ okresowy pierwiastków.
Zakaz Pauliego - zakaz ten mówi, że „żadne dwa elektrony uwięzione w tej samej pułapce nie mogą mieć jednakowych wszystkich liczb kwantowych. Oznacza to, że stany dowolnych dwóch elektronów w atomie muszą się różnić co najmniej jedną liczbą kwantową. Gdyby tak nie było wszystkie elektrony zajęłyby najniższy możliwy poziom energetyczny (czyli spadłyby na podpowłokę 1s), w wyniku czego atom „zapadłby się”. A więc świat w obecnej postaci nie mógłby istnieć.
Atomy wieloelektrodowe - mają więcej niż jeden elektron w atomie; do energii każdego z elektronów wchodzą: energia kinetyczna, energia potencjalna pochodząca od oddziaływania elektron-jądro i energia potencjalna pochodząca od oddziaływania elektron-inne elektrony.
Obsadzanie orbitali elektronowych - w atomach wieloelektrodowych (w odróżnieniu od wodoru) daje się zauważyć różnicę energii pomiędzy orbitalami tej samej powłoki. Odpychanie się elektronów powoduje, że np. energia elektronu z orbitalu 2p jest większa od energii elektronu 2s. Elektrony w danej powłoce obsadzają najpierw orbitale o najniższej energii.
Układ okresowy pierwiastków - jest to zestawienie wszystkich pierwiastków w postaci tabeli, uporządkowanej wg. ich rosnącej liczby atomowej.
32. Promieniowanie rentgenowskie ciągłe i charakterystyczne, prawo Moseley'a.
Promieniowanie rentgenowskie ciągłe: elektron o początkowej energii kinetycznej Eko, który zderza się z jednym z atomów tarczy na która pada traci pewną energię ΔEk, która pojawia się jako energia fotonu rentgenowskiego. Następnie elektron zderza się z innymi atomami aż do chwili zatrzymania się. Emitowane w wyniku tych zderzeń fotony tworzą ciągłą część widma promieniowania rentgenowskiego.
Promieniowanie rentgenowskie charakterystyczne - występuje wówczas, gdy elektron o dużej energii wybija jeden z głębiej leżących elektronów. Wówczas na pozostawioną po wybitym elektronie lukę wskakuje elektron z jednej z powłok o wyższej energii. Podczas tego przejścia elektron atom emituje charakterystyczny foton promieniowania rentgenowskiego.
Prawo Mosley'a - opisuje nam zależność długości fali fotonów promieniowania rentgenowskiego charakterystycznego od liczby atomowej bombardowanego (przez elektrony) pierwiastka.
33. Wiązania chemiczne, wiązania w ciele stałym, porównanie energii wiązania, rozkład elektronów walencyjnych.
Wiązanie jonowe - istotą tego wiązania jest elektrostatyczne oddziaływanie pomiędzy jonami o różnoimiennych ładunkach. Wiązanie to powstaje najczęściej między metalem a niemetalem. Różnica elektroujemności w skali Paulinga jst większa lub równa 1,7. Energia potencjalna wiązania jonowego:

gdzie: pierwszy człon oznacza przyciąganie lub odpychanie elektrostatyczne a drugi odpychanie rdzeni jonowych.
- Dla kryształu: 
gdzie:
Wiązanie kowalencyjne - istotą tego wiązania jest istnienie pary elektronów, które są współdzielone przez oba atomy tworzące to wiązanie. Wiązanie to tworzy się gdy róznica elektroujemności dwóch pierwiastków jest mała lub równa zero.
Orbitale wiążące - w których elektrony posiadają niższą energię niż gdyby przebywały na swoich orbitalach atomowych; orbitale niewiążące - elektrony posiadają taką samą energię jak gdyby przebywały na swoich orbitalach.
Kierunkowość - wiązania kowalencyjne mają charakter kierunkowy. Kierunek wiązania jest wyznaczony przez prostą łączącą jądra sąsiadujących atomów. Kierunkowość decyduje o geometrii cząsteczki.
Hybrydyzacja orbitali - jest to zmieszanie orbitali różnego typu tego samego atomu, w wyniku czego powstaje orbital hybrydyzowany o innym kształcie niż orbitale pierwotne (np. „s” lub „p”).
Wiązanie wodorowe - jest to słabe wiązanie chemiczne (słabsze od jonowego jak również kowalencyjnego) polegające na przyciąganiu elektrostatycznym. Występuje ono pomiędzy kowalentnie związanym atomem wodoru, a elektroujemnymi atomami sąsiedniej cząsteczki. Wiązanie wodorowe pomiędzy cząsteczkami H2O:

- kolorem zielonym zaznaczono wiązanie wodorowe
Wiązanie van der Waalsa - wzajemne oddziaływanie elektrostatyczne pomiędzy dipolami elektrycznymi stałymi albo indukowanymi czy też chwilowymi (zmienny w czasie rozkład ładunku w cząsteczce). Jest to najsłabsze wiązanie.
Potencjał Lennarda-Jonesa - określa oddziaływanie między cząsteczkami w zależności od odległości między nimi. Jeżeli cząsteczki są za blisko siebie to się odpychają, w przeciwnym wypadku się przyciągają.
Wiązanie metaliczne - występuje wówczas, gdy łączą się ze sobą wyłącznie atomy, które łatwo „oddają” elektrony. Oddawane elektrony mogą przemieszczać się pomiędzy atomami pod wpływem np. zewnętrznej różnicy potencjałów jako tzw. „gaz elektronowy”.
![]()
![]()