Obliczenie dokładnych wartości t0, ta, tb i tk
1)
t0 - temperatura początkowa dla τ0=0 [min] - z rownania
t0=24,231 [oC]
2)
ta-pierwsza temperatura okresu głównego dla τa= 5,5 [min]
ta= -0,0055*τa + 22,108 = -0,0055*5,5 + 22,108 ta=22,077 [oC]
tb-ostatnia temperatura okresu głównego dla τb= 16 [min]
tb= -0,0086*τb + 24,294 = -0,0086*16 + 24,294 tb =24,156 [oC]
3)
tk-temperatura końcowa dla τk=28 [min]
tk= -0,0086*τk + 24,294= -0,0086*28+24,294 tk=24,053 [oC]
Obliczenie skorygowanego przyrostu temperatury ΔTgraf metodą graficzną
ΔTgraf =tbk-tak= tb-ta - (l1a1 - l2a2)
l1= 1min a1= -0,0055
l2= 9,4 min a2= -0,0086
ΔTgraf = 24,156 - 22,077 - {1*(-0,0055) - 9,4*(-0,0086) }= 2,00366 [K]
Obliczenie skorygowanego przyrostu temperatury ΔT metodą dokładną
![]()
= 0,5(to + ta) = 22,0925 [oC]
![]()
= 0,5(tb + tk) = 24,1045 [oC]
n = (τb + τa)*2 = 21
![]()
= t6 + t6,5 + .... + t15,5 = 478,43
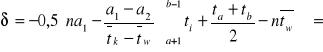
0,119269
ΔT = tb - ta + δ = 2,1982 [K]
Obliczenie ciepła q wydzielonego w procesie spalania
q = Q - qJ - qd Q - ciepło wydzielone w kalorymetrze
qJ - ciepło Joule'a
qd - ciepło spalania drucika
qJ = 10 [J]
qd = 6700*(md-mn) = 6700*(0,0203-0,0126) = 51,59 [J]
Q = (r+mw*Cw) ΔT r = 1478 ± 33 J/K
mw = 2880 g
Cw = 4,188 J/g
a)metoda graficzna:
Q = (r+mw*Cw)ΔTgraf Q = 27128,43 [J]
q = 27128,43 - 10 - 51,59 = 27066,84 [J]
b)metoda dokładna
Q = (r+mw*Cw)ΔT Q = 29746,56
q = 29746,56 - 10 - 51,59 = 29684,97 [J]
c) wartość średnia qsr = 28375,91 [J]
Obliczenie zmiany energii wewnętrznej reagentów ΔUsp
ΔUsp = ![]()
![]()
122 g/mol m = 1,3605 g
a) metoda graficzna
ΔUsp= - 27066,84*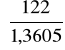
= -2427,16 ![]()
b) metoda dokładna
ΔUsp= -29684,97*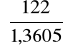
= -2661,93 ![]()
c) wartość średnia
ΔUsp = -2544,54 ![]()
Wyznaczenie ciepła spalania ΔHsp
![]()
![]()
ΔH ![]()
= -2545,72 ![]()
Wyznaczenie standardowego ciepła tworzenia C7H6O2, ΔHtw°
![]()
7C + 3H2 + O2 C7H6O2
![]()
= -![]()
![]()
= -(-2545,72) + 7(-393,51) + 3(-285,84)
![]()
= -1066,37 ![]()
1
Wyszukiwarka
Podobne podstrony:
28fizyczna, inżynieria materiałowa - semestr 4, Inżynieria Materiałowa pwr - semestr 4, Chemia Fizyc
sekuła, inżynieria materiałowa - semestr 4, Inżynieria Materiałowa pwr - semestr 4, Chemia Fizyczna,
sprawko 13, inżynieria materiałowa - semestr 4, Inżynieria Materiałowa pwr - semestr 4, Chemia Fizyc
22fizyczna, inżynieria materiałowa - semestr 4, Inżynieria Materiałowa pwr - semestr 4, Chemia Fizyc
landolt, inżynieria materiałowa - semestr 4, Inżynieria Materiałowa pwr - semestr 4, Chemia Fizyczna
18. SEM ogniw, inżynieria materiałowa - semestr 4, Inżynieria Materiałowa pwr - semestr 4, Chemia Fi
28fizyczna, inżynieria materiałowa - semestr 4, Inżynieria Materiałowa pwr - semestr 4, Chemia Fizyc
chemia fizyczna - zestawy pytan, uniwersytet warmińsko-mazurski, inżynieria chemiczna i procesowa, r
Ćwiczenie 1 - oznaczanie stalej i stopnia dysocjacji, Biotechnologia PWR, Semestr 3, Chemia fizyczna
Ćwiczenie 10 - katalityczny rozpad wody utlenionej, Biotechnologia PWR, Semestr 3, Chemia fizyczna -
Ćwiczenie 2 - liczby przenoszenia i ruchliwosc jonow, Biotechnologia PWR, Semestr 3, Chemia fizyczna
Pomiar ciepła spalania, pwr biotechnologia(I stopień), III semestr, Chemia fizyczna - laboratorium,
Ćwiczenie 6 - diagram fazowy, Biotechnologia PWR, Semestr 3, Chemia fizyczna - Laboratorium, Chemia
Ćwiczenie 4 - destylacja, Technologia INZ PWR, Semestr 3, Chemia Fizyczna, Chemia fizyczna - Laborat
Współczynnik podziału -16 wykres, Biotechnologia PWR, Semestr 3, Chemia fizyczna - Laboratorium, 16.
szybkosc rozpadu jonuw jakis tam ^^, Biotechnologia PWR, Semestr 3, Chemia fizyczna - Laboratorium,
więcej podobnych podstron