ZAKŁAD CHEMII FIZYCZNEJ
URSZULA NAGRABSKA
DARIUSZ WALCZAK
ĆWICZENIE NR 22
TEMAT: WYZNACZANIE STAŁEJ SZYBKOŚCI HYDROLIZY OCTANU ETYLU WODOROTLENKU SODOWYM W ROZTWORZE WODNYM.
Kinetyka zajmuje się zmiennością w czasie reagujących układów chemicznych. Badania kinetyczne dostarczają informacji o przebiegu reakcji chemicznych oraz stanowią podstawę technologicznego projektowania reaktorów.
Wyniki pomiarów kinetycznych opisujemy równaniami, które w większości przypadków wyrażają zależność szybkości reakcji r od stężeń reagentów i od temperatury. Jeśli chcemy znać nie tylko postać równań kinetycznych, lecz rozumieć również ich powiązanie z molekularnym przebiegiem reakcji, musimy poznać mechanizm reakcji. Przez pojęcie „mechanizm reakcji”
Według Boudarta celem podstawowych badań kinetycznych jest:
ustalenie schematu aktów elementarnych,
zaproponowanie sekwencji aktów elementarnych,
wyjaśnienie przebiegu aktu elementarnego.
Szybkość homogenicznej reakcji chemicznej r definiujemy jako zmianę stężenia -c w czasie -t ![]()
i jest ona wielkością intensywną. W przypadku, gdy stężenie -c odnosi się do substratów w równaniu dopisujemy znak (-).
Centralnym problemem kinetyki chemicznej jest znalezienie równania kinetycznego r=f(ci,T) gdzie T jest temperaturą bezwzględną. Po rozdzieleniu zmiennych szybkość nieodwracalnej reakcji chemicznej r wyraża równanie r=k(T)*f(ci), gdzie współczynnik k (T), zwany stałą szybkości reakcji, jest niezależny od stężeń reagentów, zależy natomiast od temperatury. W pewnych przypadkach funkcja f(ci) może też zależeć od temperatury. Funkcja f(ci) ma postać:
![]()
gdzie iloczyn rozciąga się na wszystkie składniki układu. λi jest rzędem reakcji względem składnika i. Rząd reakcji zawarty jest zwykle w granicach -2<λi<2. W szczególnym przypadku może on być równy 0. Szybkość reakcji nie zależy wówczas od stężenia składnika i. Sumę wykładników potęgowych λi, zwaną całkowitym rzędem reakcji, oznaczamy symbolem n. Rząd reakcji jest parametrem równania empirycznego. Rzędów reakcji (λi) nie wolno utożsamiać ze współczynnikami stechiometrycznymi reakcji chemicznych (υi). Doświadczenia wykazały, że w niektórych przypadkach λi jest różne od υi podczas gdy w innych λi=υi. Im mniej skomplikowany jest przebieg reakcji tym bardziej jest prawdopodobne, że rzędy reakcji i współczynniki stechiometryczne będą miały identyczne wartości.
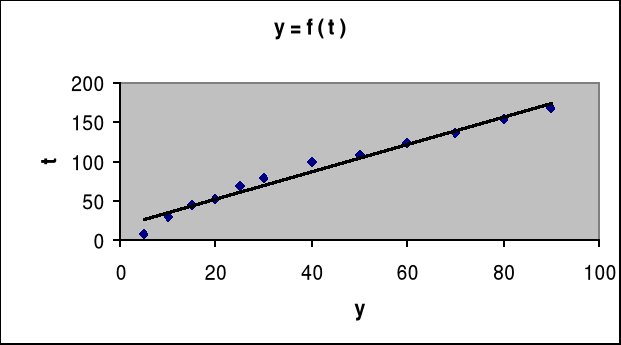
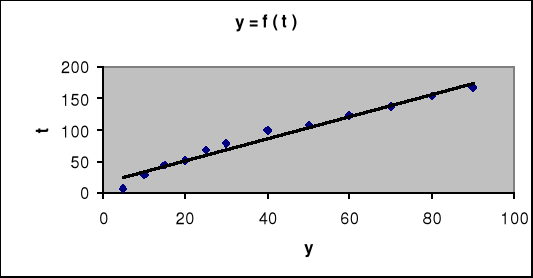
Opracowanie wyników.
Lp. |
t |
t2 |
L [mS] |
L0-L [mS] |
L-L∞ |
|
|
ty |
1 |
5 |
25 |
2,35 |
0,1 |
1,37 |
0,072993 |
7,29927 |
36,49635 |
2 |
10 |
100 |
2,12 |
0,33 |
1,14 |
0,289474 |
28,94737 |
289,4737 |
3 |
15 |
225 |
2 |
0,45 |
1,02 |
0,441176 |
44,11765 |
661,7647 |
4 |
20 |
400 |
1,95 |
0,5 |
0,97 |
0,515464 |
51,54639 |
1030,928 |
5 |
25 |
625 |
1,85 |
0,6 |
0,87 |
0,689655 |
68,96552 |
1724,138 |
6 |
30 |
900 |
1,8 |
0,65 |
0,82 |
0,792683 |
79,26829 |
2378,049 |
7 |
40 |
1600 |
1,72 |
0,73 |
0,74 |
0,986486 |
98,64865 |
3945,946 |
8 |
50 |
2500 |
1,69 |
0,76 |
0,71 |
1,070423 |
107,0423 |
5352,113 |
9 |
60 |
3600 |
1,64 |
0,81 |
0,66 |
1,227273 |
122,7273 |
7363,636 |
10 |
70 |
4900 |
1,6 |
0,85 |
0,62 |
1,370968 |
137,0968 |
9596,774 |
11 |
80 |
6400 |
1,56 |
0,89 |
0,58 |
1,534483 |
153,4483 |
12275,86 |
12 |
90 |
8100 |
1,53 |
0,92 |
0,55 |
1,672727 |
167,2727 |
15054,55 |
|
∑t2 |
|
∑yt |
|||||
|
29375 |
|
59709,73 |
|||||
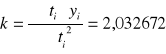
Wyszukiwarka
Podobne podstrony:
LAB22 2
LAB22 01, laser
Lab22(1), Studia, Politechnika
LAB22 , Fizyka laborki, Fizyka (laby i inne), FizLab, fizlab, 022 ST~1
lab22
LAB22
Lab22
lab22
lab22
lab22(1)
lab22
lab22
lab22
LAB22 DOC
więcej podobnych podstron