
Politechnika Śląska
Wydział Górnictwa i Geologii
Rok akademicki 2003/2004
Laboratorium z Hydrogeologii
ANALIZA WODY
1. Sucha pozostałość
Sucha pozostałość jest masą osadu pozostającego po odparowaniu 1 dm3 wody w temperaturze 1050C, wysuszonego do stałej masy.
V - objętość próbki wody = 25 cm3
a1 - masa parownicy z osadem = 74,5507 g
a2 - masa parownicy z osadem = 62,6650 g
b1 - masa parownicy bez osadu = 72,8602 g
b2 - masa parownicy bez osadu = 60,9865 g
![]()
(a - b)1 = 0,3381 g
(a - b)2 = 0,3357 g
(a - b)Śr = 0,3369 g
XŚr = 33,69 [g/dm3] = 3369 [mg/dm3]
2. Oznaczanie twardości węglanowej
Jest to podstawowa własność chemiczna, którą wodzie nadaje objętość rozpuszczonych soli. Oznaczamy miareczkując jony OH, HCO3-, CO32- za pomocą kwasu solnego.
V - objętość zużytego HCl = 0,55 cm3
N - stężenie normalne HCl = 0,1 N
28,04 - gramorównoważnik CaO
R - rozcieńczenie = 20
10 - przelicznik na 0n
![]()
tw = 3,08 [0n]
tw = 1,1 [mval/dm3]
3. Oznaczanie twardości wapniowej
Zasada oznaczania polega na kompleksometrycznym odmiareczkowaniu jonów Ca2+ za pomocą roztworu wersenianu dwusodowego po uprzednim wytrąceniu Mg2+ w postaci wodorotlenku w obecności kalcesu.
V - objętość zużytego wersenianu dwusodowego = 3,0 cm3
M - stężenie molowe wersenianu = 0,05 M
56,08 - stężenie mol CaO
R - rozcieńczenie = 100
10 - przelicznik na 0n
![]()
tCa = 84,12 [0n]
tCa = 30,0 [mval/dm3]
4. Twardość ogólna
Oznaczanie polega na kompleksometrycznym odmiareczkowaniu sumy jonów Ca2+ i Mg2+ za pomocą roztworu wersenianu dwusodowego w obecności czerni eriochromowej.
V - objętość zużytego wersenianu dwusodowego = 4,4 cm3
M - stężenie molowe wersenianu = 0,05 M
56,08 - stężenie mol CaO
R - rozcieńczenie = 100
10 - przelicznik na 0n
![]()
tcal = 123,37 [0n]
tcal = 44 [mval/dm3]
5. Twardość magnezowa
Obliczamy z różnicy twardości ogólnej i twardości wapniowej.
tMg = tcal - tCa
tMg = 39,25 [0n]
tMg = 14,0 [mval/dm3]
6. Oznaczanie jonów chlorkowych
Oznaczanie polega na miareczkowaniu strąceniowym, jony chlorkowe miareczkuje się roztworem Ag+ w obecności, jako wskaźnika, CrO42-.
V - objętość zużytego azotanu srebra = 52,85 cm3
N - stężenie azotanu srebra = 0,1 N
35,5 - gramorównoważnik jonu chlorkowego
R - rozcieńczenie = 100
![]()
Cl- = 18761,7 [mg/dm3]
Cl- = 528,5 [mval/dm3]
7. Obliczanie zawartości jonów wapniowych
Obliczamy korzystając z wyników oznaczenia twardości wapniowej.
V - objętość zużytego wersenianu dwusodowego przy oznaczaniu tw. wapniowej = 3,0 cm3
M - stężenie molowe wersenianu = 0,05 M
40,08 - masa jonowa Ca
R - rozcieńczenie = 100
![]()
Ca2+ = 601,2 [mg/dm3]
Ca2+ = 30,0 [mval/dm3]
8. Obliczanie zawartości jonów magnezowych
Zawartość jonów Mg2+ obliczamy korzystając z wyników oznaczeń twardości ogólnej i wapniowej.
V1 - objętość zużytego wersenianu (tw. ogólna) = 4,4 cm3
V2 - objętość zużytego wersenianu (tw. wapniowa) = 3,0 cm3
M - stężenie molowe wersenianu = 0,05 M
24,32 - masa jonowa Mg
R - rozcieńczenie = 100
![]()
Mg2+ = 170,24 [mg/dm3]
Mg2+ = 14,0 [mval/dm3]
9. Obliczanie zawartości jonów HCO3-
Zawartość tych jonów obliczmy na podstawie oznaczenia twardości węglanowej.
![]()
![]()
= 67,1 [mg/dm3]
![]()
= 1,1 [mval/dm3]
10. Oznaczanie jonów siarczanowych
Jony siarczanowe strąca się chlorkiem baru w postaci trudno rozpuszczalnego siarczanu baru i oznacza wagowo otrzymany osad.
![]()
m1(I) - masa pustego tygla = 31,9045 g
m1(II) - masa pustego tygla = 31,4744 g
m2(I) - masa tygla z osadem po wyprażeniu = 31,9673 g
m2(II) - masa tygla z osadem po wyprażeniu = 31,5371 g
0,4114 - przelicznik BaSO4 na SO42-
V - objętość badanej wody = 25 cm3
![]()
SO42- = 1032,9 [mg/dm3]
SO42- = 21,5 [mval/dm3]
11. Zasadowość ogólna zo
Zasadowość ogólna wywołana jest obecnością w wodzie jonów ![]()
.
Zasadowość jest cechą określającą zdolność wody do zobojętniania kwasów mineralnych w określonych warunkach. Ma duże znaczenie w ocenie wody do celów gospodarczych i technologicznych.
![]()
zo=![]()
b- objętość zużytego kwasu solnego przy oznaczaniu twardości węglanowej,
V- objętość badanej wody, cm3.
b=0,55
V=50 cm3
Zo=1,1 [mval/dm3]
12. Zawartość alkaliów Na+ i K+.
![]()
r - miligramorównoważnik, milaval
K - kationy
A - aniony
rK - ilość miligramorównoważników czyli milivali kationów
rA - ilość miligramorównoważników czyli milivali anionów
Cl- = 528,5 [mval/dm3] Cl- = 18761,7 [mg/dm3]
![]()
= 1,1 [mval/dm3] ![]()
= 67,1 [mg/dm3]
SO42- = 21,5 [mval/dm3] SO42- =1032,9 [mg/dm3]
Ca2+ = 30 [mval/dm3] Ca2+ = 601,2 [mg/dm3]
Mg2+ = 14 [mval/dm3] Mg2+ = 170,24 [mg/dm3]
rK =rNa+ + rCa2+ + rMg2+
rA = rCl- + rSO42- + rHCO3-
rA = 551,1 [mval/dm3]
rA = 19861,7 [mg/dm3]
rCa2+ + rMg2+ = 44 [mval/dm3]
rCa2+ + rMg2+ = 771,44 [mg/dm3]
rNa+ = rA - (rCa2+ + rMg2+) = 507,1[mval/dm3]
Na+ + K+ = 11663,3 [mg/dm3]
Tabelaryczne zestawienie analizy wody
Barwa |
Szara |
Mętność |
Mętna |
Zapach |
Bez zapachu |
Smak |
Słony |
pH |
5,5 |
Sucha pozostałość |
33690 mg/dm3 |
Twardość węglanowa |
3,08 0n; 1,1 mval/dm3 |
Twardość wapniowa |
84,12 0n; 30,0 mval/dm3 |
Twardość ogólna |
123,37 0n; 44,0 mval/dm3 |
Twardość magnezowa |
39,25 0n; 14 mval/dm3 |
Zasadowość ogólna |
1,1 mval/dm3 |
Kationy |
mg/dm3 |
mval/ dm3 |
0/0 mval |
Aniony |
mg/dm3 |
mval/ dm3 |
0/0 mval |
wapniowy Ca2+ |
601,2 |
30 |
5,5 |
chlorkowy Cl- |
18761,7 |
528,5 |
96 |
magnezowy Mg2+ |
170,24 |
14 |
2,5 |
siarczanowy SO42- |
1032,9 |
21,5 |
4 |
alkalia Na+ + K+ |
11663,3 |
507,1 |
92 |
Wodoro-węglanowy HCO3- |
67,1 |
1,1 |
śl.
|
|
12434,74 |
551,1 |
100 |
|
19861,7 |
551,1 |
100 |
Wzór Kryłowa
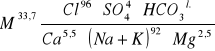
Klasyfikacja wody
Klasyfikacja wg. Sztelaka
Badana woda należy do wód III typu, czyli do wód o wysokiej zawartości chlorków (wody słone i solanki). Wody te występują w strefie izolowanej od wód atmosferycznych. Są to głównie wody reliktowe o zawartości chlorków powyżej 10 g/dm3. Występują poniżej 600m.
Klasyfikacja wg. Szczukariewa - Prikłońskiego
Analizowana woda jest wodą dwujonową. Jest to woda klasy I nazywana chlorkowo-sodową, gdyż anion Cl- i kation Na+ stanowią ponad 20 0/0 mval sumy anionów i kationów.
Klasyfikacja wg. Pazdry
Nasza woda jest silnie zmineralizowana albo słona, gdyż sucha pozostałość mieści się w przedziale 10 -35 g/dm3 i wynosi 33,69 g/dm3. Głównymi składnikami takiej wody są chlorki sodu i wapnia.
Klasyfikacja wg. Marchacza i Malinowskiego
Zbadana woda jest wodą kopalnianą. Należy do II grupy, czyli do wód przemysłowych. Typ II B - wody mineralne o dużej mineralizacji ogólnej, większej od 10000 mg/dm3. Badana woda należy do klasy II B 1, gdyż jest wodą słoną o suchej pozostałości w granicach od 10000 do 50000 mg/dm3.
Zagospodarowanie wody.
Ze względu na coraz większy deficyt wody pitnej na obszarach górniczych, wynika konieczność używania dla celów przemysłowych wód kopalnianych typu II i III
(wg. klasyfikacji Sztelaka). Nasza woda o wysokiej mineralizacji może być użyta do płukania węgla, do podsadzki hydraulicznej i innych procesów przemysłowych, które nie wymagają wody dobrej jakości. Natomiast, aby ją odprowadzić do cieku powierzchniowego należy ją oczyścić z zanieczyszczeń lub rozcieńczyć, gdyż jest ona wodą pozaklasową i stanowi zagrożenie dla odbiornika, gdyż normy są przekroczone.
Woda ta jest solanką chlorkowo-sodową, więc może być również wykorzystana do produkcji soli w zakładach odsalania wód dołowych (np. przy dawnej kopalni Dębieńsko), a wodę po demineralizacji (np. metodą odwróconej osmozy) można stosować jako wodę pitną.
Wyszukiwarka
Podobne podstrony:
Agresywność wody, Uczelnia - Politechnika Slaska, Hydrologia
Agresywność wody 1, Uczelnia - Politechnika Slaska, Hydrologia
k-met.sitową, Uczelnia - Politechnika Slaska, Hydrologia
mapa, Uczelnia - Politechnika Slaska, Hydrologia
k-met.lab, Uczelnia - Politechnika Slaska, Hydrologia
sem 9 cw 6, Uczelnia - Politechnika Slaska, Hydrologia
teoria, Uczelnia - Politechnika Slaska, Hydrologia
sprawozdanie hydro 2, Uczelnia - Politechnika Slaska, Hydro
Stopień zagęszczenia, Uczelnia - Politechnika Slaska, Hydrologia
Sprawozdanie hydro 3, Uczelnia - Politechnika Slaska, Hydro
hydra-laska-poprawione, Uczelnia - Politechnika Slaska, Hydrologia
k-met.porozymetryczną, Uczelnia - Politechnika Slaska, Hydrologia
Juwenilne hizw wyk 2011, Uczelnia - Politechnika Slaska, Hydro
Sprawozdanie hydro porozymetr, Uczelnia - Politechnika Slaska, Hydro
hydra naftową, Uczelnia - Politechnika Slaska, Hydro
Hydro sprawozdanie agresywność, Uczelnia - Politechnika Slaska, Hydro
więcej podobnych podstron