Renara Sobierańska
Wpływ stężenia kwasu na szybkość hydrolizy estru
Proces hydrolizy octanu etylu w środowisku kwaśnym przebiega według następującej reakcji:
H+
CH3COOC2H5 + H2O CH3COOH + C2H5OH
Reakcja ta, zachodząca w środowisku wodnym, katalizowana przez jony wodorowe, jest reakcją pierwszego rzędu. O jej rzędowości decyduje wyłącznie stężenie estru, ponieważ można przyjąć, że stężenie wody nie ulega zmianie, gdyż jest ona w nadmiarze do ilości drugiego substratu.
Szybkość omawianej reakcji określa równanie:
dx/dt =k(a-x)
Gdzie:
A - stężenie początkowe estru
X - stężenie produktu tj. kwasu octowego w danej chwili t
K -stała szybkości reakcji
Przekształcając i całkując ostateczne równanie w granicach czasu od 0 i t i w granicach stężeń od 0 do x znajdujemy następujące wyrażenie na stała szybkości reakcji:
K=1/t ln (a/(a-x))
Obliczanie stałej k wymaga znajomości stężenia początkowego estru a i stężenia estru w danej chwili ( a - x). Kinetykę omawianej reakcji, katalizowanej przez jony wodorowe pochodzące z kwasu solnego, wygodnie jest badać poprzez oznaczenie stężenia produktu. Łączną zawartość kwasu solnego i powstającego kwasu octowego można znaleźć poprzez miareczkowanie roztworu zasadą sodową. Zgodnie z podstawową zależnością analizy miareczkowej ilość kwasu jest proporcjonalna do ilości zasady sodowej potrzebnej do całkowitego zobojętnienia roztworu
(CHCl + x) = Vt (Cz / Vr)
Gdzie:
CHCl - stężenie kwasu solnego
X stężenie powstającego kwasu octowego
Cz stężenie zasady sodowej użytej do miareczkowania
Vr objętość roztworu pobranego do miareczkowania
Vt objętość zasady sodowej potrzebna do zobojętnienia kwasów zawartych w roztworze w danej chwili
W warunkach doświadczenia, stosunek stężenia zasady sodowej i objętości roztworu pobranego do miareczkowania jest wielkością stałą. Łączną zawartość kwasu octowego i kwasu solnego wyraża równanie:
(CHCl + x) = A Vt
Jeżeli przez V0 oznaczymy objętość zasady sodowej, która zobojętnia stała ilość kwasu solnego, co odpowiada pomiarowi w chwili t = 0, a przez V∞ - objętość zasady sodowej potrzebną do zobojętnienia mieszaniny kwasów zawartej w roztworze po zakończeniu procesu hydrolizy octanu etylu, tj. dla t =∞, to prawdziwe są zależności:
CHCl = AV0
(6)
(CHCl + a) = AV∞
(7)
Zatem, stężenie początkowe estru a można obliczyć stosując równanie:
A = A(V∞ - V0)
(8)
Zaś stężenie estru w dowolnej chwili określa wzór:
(a-x) = A (V∞ - Vt)
(9)
Po podstawieniu wyrażeń (8) i (9) do równania (3) otrzymujemy zależność między stałą szybkości hydrolizy octanu etylu k a uzyskanymi wartościami objętości zasady sodowej V0, Vt, V∞
![]()
(10)
Kwas solny c = 0,5 mol dm3
czas min |
czas sek |
Vt |
ln |
Kobl |
Ksr |
kgr |
knum |
0 |
0 |
11,1 |
0 |
0 |
|
|
|
20 |
1200 |
13,5 |
0,4608 |
0,00038400 |
|
|
|
40 |
2400 |
11,6 |
0,08 |
0,00003333 |
0,00011013 |
5,00E-05 |
1,40E-05 |
60 |
3600 |
12,1 |
0,167 |
0,00004639 |
|
|
|
80 |
4800 |
12,4 |
0,2231 |
0,00004648 |
|
|
|
100 |
6000 |
12,5 |
0,2426 |
0,00004043 |
|
|
|
|
|
17,6 |
0 |
|
|
|
|
Kwas solny C =1,5 mol dm3
czas min |
czas sek |
Vt |
ln |
Kobl |
Ksr |
kgr |
knum |
|
|
|
|
|
|
|
|
0 |
0 |
31,9 |
0 |
0 |
|
|
|
20 |
1200 |
34,5 |
0,3502 |
0,00029183 |
0,00014781 |
1,00E-04 |
7,17E-05 |
40 |
2400 |
34,4 |
0,3342 |
0,00013925 |
|
|
|
60 |
3600 |
35,1 |
0,4519 |
0,00012553 |
|
|
|
80 |
4800 |
35,2 |
0,47 |
0,00009792 |
|
|
|
100 |
6000 |
35,4 |
0,507 |
0,00008450 |
|
|
|
|
|
40,7 |
0 |
|
|
|
|
Obliczenia dla Kwasu solnego o C=0,5 mol/l
Czas t [s]
T1 =0
T2=1200
T3=2400
T4=3600
T5=4800
T6=6000
Objętość V [cm3]
V0 =11.1
V1=13,5
V2 = 11,6
V3 =12.1
V4 =12,4
V5= 12,5
V∞ =17,6
![]()
Dla V2
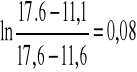
Dla V3
![]()
![]()
Dla V2
![]()
Dla V3
![]()
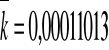
![]()
Obliczenia dla Kwasu solnego o C=1,5 mol/l
]
Czas t [s]
T1 =0
T2=1200
T3=2400
T4=3600
T5=4800
T6=6000
Objętość V [cm3]
V0 31,9
V1 34,5
V2 34,4
V3 35,1
V4 35,2
V5 35,4
V∞ 40,7
![]()
Dla V1
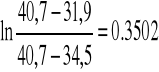
Dla V3
![]()
![]()
Dla V1
![]()
Dla V2
![]()
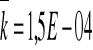
Zależność miedzy czasem miareczkowania octanu etylu a objętościami zasady sodowej ( katalizator HCl o C= 0,5 mol/l)
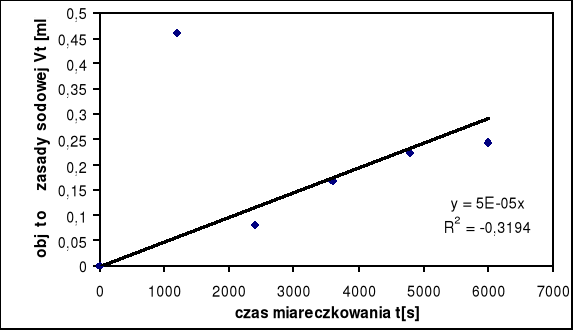
Zależność miedzy czasem miareczkowania octanu etylu a objętościami zasady sodowej ( katalizator HCl o C= 1,5 mol/l)
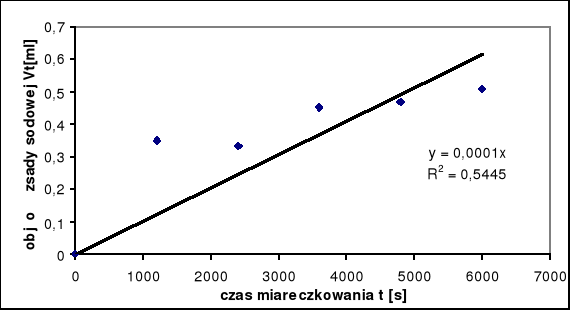
Wnioski:
Stała szybkości reakcji w środowisku kwasu solnego o C=0,5 mol/l jest mniejsza niż stała szybkości w środowisku kwasu o C=1,5 mol/l . Wynika z tego, że im większe stężenie kwasu czyli stężenie jonów wodorowych tym większa stała szybkości reakcji. Reakcja opisana w tym doświadczeniu przebiega szybciej im jest większe stężenie kwasu. Jony wodorowe są katalizatorem i powodują wzrost szybkości tej reakcji.
Wyszukiwarka
Podobne podstrony:
poprawa II 25, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna
poprawa 25, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł
iza 24 dobrze, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna
iza 7, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł, Che
Fizyczna27m, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna u
Sprawozdanie damiana nr 1, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i
Chfizyczna5, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna u
moje 4, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł, Ch
wfizyczna9, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł
chemia fizyczna-ćwiczenie 22, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczn
fizyczna 20, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna u
fizyczna25, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł
Wstęp teoretyczny, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i anality
poprawa, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł, C
fIZYCZNA5, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna uł,
13 fiza word, chemia w nauce i gospodarce Uł, semestr V, sprawozdania chemia fizyczna i analityczna
więcej podobnych podstron