I. Prawo Lamberta Berra
Absorbancja promieniowania przechodzącego przez ośrodek jednorodny jest zależna od rodzaju roztworu i proporcjonalna od jego stężenia (e) oraz grubości warstwy absorbującej tego roztworu (b)
It = Io⋅e-abc
A = abc = lg I0/It
gdzie:
absorbancja
grubość warstwy
stężenie substancji
współczynnik absorpcji.
Długość fali:
λ= C/V [nm]
Liczba falowa:
u=1/λ [cm-1]
Absorbancja:
A=lg⋅I0/It
Transmitancja:
T=It/I0
II. Wynki i obliczenia.
Do otrzymanego roztworu o nieznanym stężeniu Mno4- dodajemy kolejno kwasy wodę, kwasy H2SO4, HNO3 i H3PO4 oraz KJO4. Jony manganu (II) są utleniane przez nadjodany w środowisku kwaśnym do fioletowo zabarwionych jonów manganu (III). Proces przebiega powoli, więc badany roztwór ogrzewa się (nie do wrzenia). Trwała fioletowa barwa roztworu świadczy o zachodzącej reakcji utleniania manganu (II).
5JO4- + 2 Mn2+ + 3 H2O + → 5 JO3- + 2MnO4- + 6H+
Na podstawie pomiarów absorbancji promieniowania świetlnego przy długości fali λ=528nm wykonywanych w pierwszej części ćwiczenia wykreślamy krzywą wzorcową w układzie A=f(c). W tym celu obliczamy stężenia manganu w każdej z próbek korzystając ze wzoru
Cn= (VKMnO4* CKMnO4)/V
gdzie:
VKMnO4 - wzrastające objetości roztworu podstawowego [ml]
CKMnO4 - steżenie roztworu podstaowego manganu (VII);
V- ojętość kolbki z przeniesieniem ilościowo roztworem; 0,05 dm3
Obliczamy stężenie roztworu podstawowego manganu (VII):
MKMnO4 = 0,2873 g
V r-ru = 1dm3
MKMnO4 = 158 g/mol
1 mol KMnO4 - 158 KMnO4
x - 0, 2873 g
__________________________________
x = (1 mol ⋅ 0,2873 g)/ 158 g
x =1,82⋅10-3mol KMnO4 w 1 dm3 r-ru
x = 1,82⋅10-6mol KMnO4 w 1 ml r-ru
Obliczamy stężenia roztworu manganu w poszczególnych próbkach:
V[ml] |
T[%] |
A |
Stężenie molowe roztworu: |
1 |
87 |
0,06 |
0,36*10-4 |
3 |
63 |
0,22 |
1,09*10-4 |
5 |
45 |
0,35 |
1,82*10-4 |
7 |
32 |
0,49 |
2,55*10-4 |
10 |
18 |
0,74 |
3,64*10-4 |
![]()
![]()
![]()
![]()
![]()
WYNIKI DRUGIEJ CZĘŚCI ĆWICZENIA
Nr próbki |
Transmitancja T[%] |
Absorbancja A |
1 |
86 |
0,07 |
2 |
87 |
0,06 |
3 |
86,5 |
0,045 |
4 |
87 |
0,06 |
5 |
87 |
0,06 |
Tśr = 86,7 Aśr = 0,059
Odczytujemy stężenie manganu z krzywej wzorcowej:
Cx = 0,06*10-4 ml/dm3
Obliczmy z krzywej wzorcowej ilość Mn(II) w badanym roztworze:
Cx = 0,06*10-4 mol/dm3
Obliczamy ilość moli MnO4- w 50 ml:
0,06*10-4 mol MnO4 - 1dm3 r-ru
x - 0,05 dm3
----------------------------------------------
x = 0,03*10-5 mol w 50 ml
Obliczamy zawartość MnO4- w 50 ml
MMnO4 = 119 g/mol
1mol MnO4 - 119g KMnO4
3*10-7mol - x
-----------------------------------------------
x = 3,57*10-5 g MnO4
Zawartość Mn w 50 ml
MMn = 54,9 g/mol
119 g MnO4 - 54,9 g Mn
3,57*10-5 g - x
----------------------------------------------
x = 1,6*10-5 mg Mn * 10=1,6*10-6 mg Mn
Zawartość Mn w molach:
1mol Mn _ 54,9 g Mn
x - 1,6*10-4 g Mn
--------------------------------------------
x = 3*10-6 mola Mn
_____________________________________________________
1 mol MnO4 - 1 mol Mn
3*10-6 MnO4 - x
------------------------------------
x=3*10-6 mola Mn w 50 ml
Zawartość Mn w próbce:
X= 3*10-6 2 = 6*10-6 mola Mn
Przeprowadzamy dyskusje wyników:
Średnia arytmetyczna :
![]()
![]()
Odchylenie standardowe:
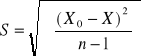
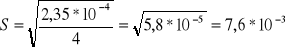
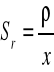
![]()
Względne odchylenie standardowe:
![]()
Katarzyna Pruciak
Anna Pilch
Ochrona Środowiska
Sem III/ Gr 4
Ćwiczenie nr 2
Temat:
Oznaczanie manganu w postaci MnO 4-
![]()
![]()
![]()
![]()
![]()
![]()
![]()
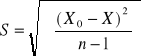
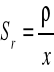
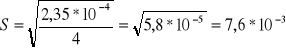
![]()
![]()
Wyszukiwarka
Podobne podstrony:
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
MASZYN~8, PŚk, Maszyny elektryczne
więcej podobnych podstron