BIAŁKA
Zad.1
Opisz przedstawione struktury. Wymień wiązania, które je stabilizują. Gdzie może występować struktura „spinki do włosów”? Napisz co wiesz na ten temat :D
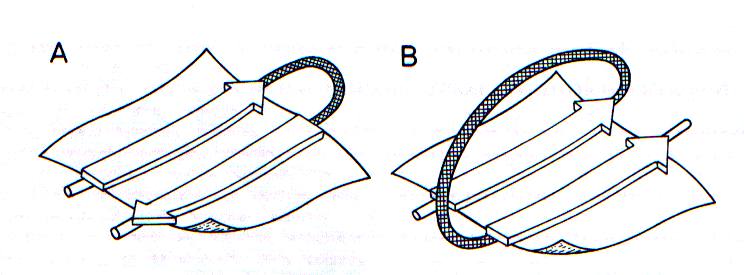
Zad.2
Ludzka, bydlęca, psa, owcza insuliny wykazują podobieństwo, ale nie są identyczne.
a) Opisz strukturę hormonu. Napisz czym różni się insulina zwierzęca od ludzkiej.
beta-fruktora wiązania glikozydowe-1,2 ??????????? jak w sacharozie
b) Jaka jest funkcja insuliny?
Zad. 3
Mioglobina (uzupełnij)
Bierze udział w transporcie i magazynowaniu ……tlenu…………………………………….
W mioglobinie hem wiąże się do globiny niekowalencyjnie przez reszty …histydyny…………..
Wiązanie tlenu zależy od obecności jonu ……fe2+………..
Czy jest protomerem hemoglobiny? …tak………… ???????????????????
Czy ma 4-rzędową strukturę? ……nie………
Wyższe powinowactwo od tlenu do jonu zawartego w mioglobinie wykazują toksyczne cząsteczki (wymień) ……………NO, CO, H2S………………………………………..
Zad.4
Glikacja i glikozylacja.
a) Opisz te dwa procesy, wskaż różnice. Jakie wiązania powstają w ich wyniku?
b) Kiedy w organizmie zachodzi glikacja? w cukrzycy
c) Jak powstają O- i N-glikozydy? Podaj przykłady i reakcje.
Zad. 5
Kolagen (zakreśl prawidłowe stwierdzenia).
a) Występuje w tkance łącznej, kościach, zębach, ścięgnach, skórze, macierzy zewnątrzkomórkowej. TAK
b) Natywny kolagen jest nierozpuszczalnym białkiem włókienkowym. TAK
c) Kolagen zawiera lizynę, która rzadko występuje w innych białkach. NIE bo hydroksylizynę
d) Jest białkiem globularnym. NIE
e) Superhelisa tropokolagenu ułożona jest w taki sposób, że reszty Pro skierowane są do wnętrza spirali i kontaktują się ze sobą a reszty Gly na zewnątrz. NIE
f) Połączenie hydroksyapatytu z kolagenem tworzy twardy i sprężysty materiał. TAK
g) Degradację kolagenu obserwuje się w chorobach: Paget'a, reumatoidalnym zapaleniu stawów, dziąseł. TAK
Uzupełnij.
Najczęściej występujące aminokwasy w kolagenie to: ……………………………………
W awitaminozie…C…… zahamowany jest proces hydroksylacji proliny. Enzym uczestniczący w reakcji wymaga obecności tej witaminy.
Zad. 6
Wymień sposoby zakotwiczania białek w błonie komórkowej.
???????????????? GPI, wiązaniem hydrofobowym; białka peryferyjne i integralne
Zad. 7
Opisz czwartorzędową strukturę białek.
Wymień wiązania stabilizujące IV-rzędową strukturę białek.
Podaj przykłady białek posiadających 4-rzędową strukturę. hemoglobina, chlorofil,
d) Co to jest protomer?
składowa struktury IV rzędowej o strukturze III-rzędowej
e) Co to jest konformacja zamknięta i otwarta?
Zad. 8
Zakreśl prawidłową odpowiedź.
Fibroina jest białkiem włókienkowym o strukturze alfa helisy. NIE
Fibrylarne białka składają się głównie z niepolarnych aminokwasów. TAK
Glicyna uczestniczy w krzyżowych wiązaniach z desmozyną, występujących w elastynie. TAK
α -Keratyna jest podstawowym białkiem włosów i paznokci oraz składnikiem skóry zwierzęcej. TAK
CUKRY
Zad. 9
Zakreśl prawidłowe stwierdzenia.
W wyniku redukcji monosacharydów powstają kwasy aldonowe i uronowe.NIE
Kwas glukonowy ma tendencję do wewnętrznej estryfikacji i tworzy laktony. TAK
Wit. C łatwo ulega utlenieniu, ale nie może ulec ponownej redukcji. NIE - hydroliza
Inwersja przy C5 i epimeryzacja kwasu β-D- glukuronowego (GlcUA) prowadzi do powstania kwasu L-iduronowego. TAK
Szkorbut jest wynikiem przedłużającego się niedoboru witaminy B12. NIE
Podczas wstrząsu hiperglikemicznego, w wyniku nasilonej redukcji glukozy powstaje sorbitol. NIE ???
D-rybitol jest składnikiem ryboflawiny, wit. B6, koenzymów flawinowych. TAK
Wit. C powstaje jako lakton w wyniku wewnętrznej estryfikacji kwasu glukonowego. TAK ????
Zad. 10
Kwas glukuronowy.
a) Co to są glukuronidy?
b) Jaką rolę w organizmie pełni kwas glukuronowy?
Wydalanie z moczem niektórych zwiazków np. kwasu salicylowego ???
c) Narysuj wzór glukuronidu kwasu salicylowego.
Zad. 11
Glikany i pochodne cukrowe pełnią zasadniczą rolę w antygenach grup krwi ABO. N-acetylogalaktozamina dla A, D-Galaktoza dla B, brak tych związkow dla 0
Jaki cukier znajduje się na błonie erytrocytów grupy krwi:
A ……………………………………… B……………………………………….
Zad. 12
Glikozaminoglikany.
Podaj nazwę odpowiedniego GAGu oraz skład jednostki disacharydowej
W przeciwieństwie do pozostałych GAGów nie jest składnikiem tkanki łącznej.
Produkowana przez (podaj nazwę komórek)…………tuczne?…………………Stosowana jako lek przeciwzakrzepowy. heparyna
……………………………………………………………………………………
Jako jedyny GAG nie występuje w postaci usiarczanowanej. Pełni funkcję smaru biologicznego.
………………………kwas hialuronowy……………………………………………………………
Jest ważnym składnikiem chrząstki i tkanki łącznej. W zależności do rodzaju może być usiarczanowana w pozycji C4 lub C6.
………………………………siarczan chondroityny……………………………………………………
Jego nazwa wiąże się z powszechnym występowaniem tego GAGu w skórze.
…………………………………siarczan dermatanu………………………………………………….
Zad. 13
Narysuj jednostkę disacharydową dowolnie wybranego GAGu. Podaj jego nazwę.
Zad. 14
Glikozydy (zaznacz prawidłową odpowiedź).
Podlegają mutarotacji. NIE
Łatwo ulegają hydrolizie. TAK
Są obecne w tkankach zwierzęcych w postaci glukuronidów. TAK
Wiązanie glikozydowe może przyjąć jedynie konfigurację α. NIE
Wymień glikozydy roślinne używane w lecznictwie:
Zad. 15
Co to jest agar? Do czego jest wykorzystywany?
ekstrakt polisacharydowy o właściwościach żelujących otrzymywany z krasnorostów; elektrofereza
Zad. 16
a) Główną pochodną kwasu neuraminowgo jest kwas 5-acetyloneuraminowy należący do
rodziny (podaj nazwę grupy związków)…………… ..…aminocukier???………………........................
c) Gdzie występuje kwas 5-acetyloneuraminowy? ???????/
kwas sjalowy???? mucyny
b) Narysuj wzór liniowy kwasu 5-acetyloneuraminowego. Podaj jego nazwę systematyczną.
??????
TŁUSZCZE
Zad. 17
Do jakiej grupy związków należy kwas fosfatydowy?
Co oznacza określenie „związek amfipatyczny”?
Narysuj wzór kwasu fosfatydowego. Zaznacz fragmenty hydrofobowe i
hydrofilowe.
Zad. 18
a) Związki będące pochodnymi polienowych kwasów tłuszczowych o 20 atomach węgla to
…eikazanoidy…………………………………………………………………………………………….
b) Ich prekursorem jest ……. .20 węglowe polienowe wasy tłuszczowe np. kwas arachidonowy………………………………………………………………
c) Narysuj wzór związku z poprzedniego podpunktu.
d) Do jakiej rodziny kwasów omega jest on zaliczany i dlaczego? ???????
e) Czy jest on niezbędnym kwasem tłuszczowym? Co rozumiemy pod tym pojęciem? TAK wiele produktow z niego powstaje, nie mozemy go produkować
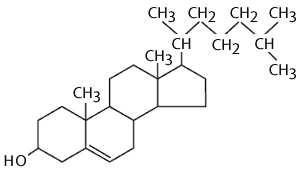
Zad. 19
a) Podaj nazwę narysowanego związku. cholesterol
Napisz w jakiej formie jest on transportowany
we krwi.
HDL, VLDL, LDL w postaci wolnej lub zestryfikowanej
Gdzie występuje ten związek? Podaj 3 przykłady. ściany komórkowe, VLDL, HDL , .fd.???
d) Podaj 4 przykłady związków, będących jego pochodnymi.
hormony płciowe, kwasy żółciowe, mineralokortykoidy, cośtam jeszce kurwa mać
Zad. 20
a) Narysuj dowolny kwas żółciowy i podaj jego nazwę.
b) Jakie właściwości mają sole kwasów żółciowych i co za nie odpowiada?
amfipatyczne?? -OH i pierścienie sterocośtam kurwa
ZWIĄZKI HETEROCYKLICZNE
Zad. 21
Uzupełnij tabelki podając nazwy lub wzory odpowiednich związków.
zasady pirymidynowe występujące w |
pochodna pirymidynowa |
pochodna kwasu barbiturowego |
witamina, której niedobór |
|||
DNA |
RNA |
stosowana w chemioterapii |
stosowana jako lek nasenny |
powoduje pelagrę |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
zasady purynowe występujące w |
końcowy produkt |
analog purynowy stosowany |
pochodna puryny występująca |
|||
DNA |
RNA |
utleniania puryn |
w chemioterapii |
w nasionach kakaowca |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Zad. 22
Podaj nazwę przedstawionego związku:
Nazwij, zaznaczając na wzorze, wiązania oraz podjednostki, z których się składa.
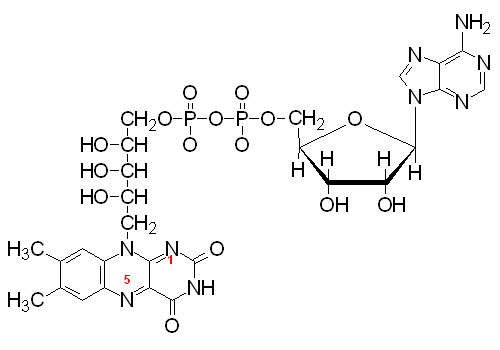
Adenina, deoksyryboza, i co to kurwa trzecie? ja pierdole glicyna z czymś połączona
W jakich formach może występować przedstawiony związek?
W jakich reakcjach bierze on udział?
Zad. 23
Na dowolnym przykładzie omów różnicę pomiędzy nukleotydem a nukleozydem. Narysuj wzory.
Zad. 24
Zakreśl prawidłową odpowiedź.
Hem jest zbudowany z 4 pierścieni pirolowych połączonych mostkami siarczkowymi. NIE metinowymi czy jakoś tak
Nukleotydy absorbują światło w zakresie ultrafioletu. TAK
Pomiędzy zasadami azotowymi: adeniną i tyminą występuje wiązanie podwójne. TAK
Bilirubina jest czerwonopomarańczowym barwnikiem żółciowym powstającym w wyniku rozpadu cząsteczek hemu. TAK
PAPS ma zastosowanie jako aktywny donor grup metylowych. ???
Zasady azotowe są cząsteczkami planarnymi, aromatycznymi i heterocyklicznymi. TAK
Hem stanowi grupę prostetyczną hemoglobiny, mioglobiny, cytochromów i chlorofili. ??? TAK???
ZADANIA OBLICZENIOWE
Zad. 25
Zalecana dawka leku o stężeniu 0,01% wynosi 15mg/kg. Oblicz ile cm3 kroplówki należy podać dziecku o masie 20 kg. Podaj stężenie leku w mmol/l. Mleku = 250g.
Zad. 26
Rozpuszczono 25 mg białka w 75 mg buforu uzyskując roztwór o stężeniu 0,002M/l i gęstości równej 1g/cm3. Oblicz masę cząsteczkową białka w kDa. Podaj stężenie białka w mg/ml.
Zad. 27
Pobrano 200 µl roztworu białka. Następnie uzupełniono zawartość probówki do 1 ml. Absorbancja wynosiła 0,2 przy λ=540.
a) Odczytaj z wykresu stężenie białka i oblicz jego stężenie początkowe podając wynik w
g/ml, µg/ml i mg%.
Obliczenia:
Stężenie początkowe: g/ml = ……………. µg/ml = ……………… mg% = ……………….
b) Co to jest absorbancja? Podaj wzór umożliwiający jej obliczenie.
c) Co odpowiada za właściwości spektrofotometryczne białek?
d) Czy zanieczyszczenie próbki białka kwasami nukleinowymi może wpłynąć na wyniki
pomiaru stężenia roztworu? Odpowiedź uzasadnij.
Wyszukiwarka
Podobne podstrony:
biochemia reaktywacja 2008, medycyna, biochemia, egz
przedtermin biochemia 2011, medycyna, biochemia, egz
Biochem Przedtermin 2010, medycyna, biochemia, egz
AD 2010 Biochemia, medycyna, biochemia, egz
2008 wl2, medycyna, Biochemia
Chemia – przedtermin, Prywatne, biochemia, biochemia 1, biochemia, chemia medyczna, chemia egz
Egz. biochemia 2008, materiały medycyna SUM, biochemia, EGZAMIN, teoretyczny
chemia zywności wykłady, Zachomikowane, Naukowe, Medycyna, Biochemia, Skrypty
BIOCHEMIA PRZEDTERMIN 2005, Medycyna, Biochemia
chirugia- egz 2008-09, MEDYCYNA!, Szczekówka i Stomatologiczna
2 termin biochemia 2008, materiały medycyna SUM, biochemia, EGZAMIN, teoretyczny
Sprawozdanie nr. 2, MEDYCYNA, Biochemia
Śpiączka, MEDYCYNA, Biochemia
EGZAMIN Z FIZJO 2008, materiały medycyna SUM, fizjologia, Fizjologia, test
pytania biochemia - egz, UR, Biochemia, biochemia semestr 2, biochemia semestr 2
Wstrząs, MEDYCYNA, Biochemia
więcej podobnych podstron