Numer ćwiczenia: 9 |
Temat ćwiczenia: Szybkość inwersji sacharozy |
Data wykonania ćwiczenia: 17.12.2013r. |
|
|
Data oddania sprawozdania: 07.01.2014r. |
Grupa: A2 |
Góralik Monika |
Nazwisko sprawdzającego: dr Tomasz Uchacz |
Uwagi: |
Ocena: |
|
1. Cel ćwiczenia.
Celem ćwiczenia było wyznaczenie stałych szybkości inwersji sacharozy do glukozy i fruktozy oraz zbadanie, jaki wpływ na szybkość tej reakcji miało wpływ stężenie katalizatora (HCl).
2. Wykonanie.
Sporządzono 20% roztwór sacharozy poprzez odważenie 20 g tego cukru, przeniesienie go do kolby na 100 cm3 i dolanie wody destylowanej do kreski
Do rurek dwóch polarymetrów (Optical Activity AA-65 i Atago AP-300) wlano roztwór sacharozy i zmierzono jego kąt skręcenia na obu urządzeniach
W zlewkach zmieszano ze sobą po 12 cm3 roztworu sacharozy i 12 cm3 kwasu solnego
o stężeniach 1 i 2M, następnie wlano je do rurek polarymetrów i odczytywano co 10 minut kąt skręcenia światła (czas pomiaru - 1 godzina, czas zerowy - zmieszanie roztworów)Po dokonaniu pomiarów dla niższych stężeń HCl dokonano pomiarów dla wyższych stężeń -
w zlewkach zmieszano ze sobą po 12 cm3 roztworów sacharozy i kwasu solnego o stężeniach
3 i 4 M, wlano mieszaniny do rurek polarymetrów i odczytywano co 5 minut kąt skręcenia światła (czas pomiaru - 0,5 godziny)
3. Wyniki.
Tabela1.: wyniki pomiarów dla katalizatora o stężeniu 1 M
t [min] |
αt [°] |
αt-α∞[°] |
ln(αt-α∞) |
0 |
13,48 |
17,87448 |
2,88337 |
10 |
12,32 |
16,71448 |
2,81628 |
20 |
11,70 |
16,09448 |
2,77848 |
30 |
11,01 |
15,40448 |
2,73466 |
40 |
10,27 |
14,66448 |
2,68543 |
50 |
9,51 |
13,90448 |
2,63221 |
60 |
8,73 |
13,12448 |
2,57448 |
Urządzenie pomiarowe: polarymetr Optical Activity AA-65
Tabela2.: wyniki pomiarów dla katalizatora o stężeniu 2 M
t [min] |
αt [°] |
αt-α∞[°] |
ln(αt-α∞) |
0 |
13,23 |
17,54298 |
2,86465 |
10 |
10,11 |
14,42298 |
2,66882 |
20 |
8,03 |
12,34298 |
2,51309 |
30 |
6,25 |
10,56298 |
2,35736 |
40 |
4,73 |
9,04298 |
2,20199 |
50 |
3,41 |
7,72298 |
2,04420 |
60 |
2,24 |
6,55298 |
1,87992 |
Urządzenie pomiarowe: polarymetr Atago AP-300
Tabela3.: wyniki pomiarów dla katalizatora o stężeniu 3 M
t [min] |
αt [°] |
αt-α∞[°] |
ln(αt-α∞) |
0 |
13,48 |
17,87448 |
2,88337 |
5 |
11,11 |
15,50448 |
2,74113 |
10 |
9,19 |
13,58448 |
2,60893 |
15 |
7,26 |
11,65448 |
2,45569 |
20 |
5,51 |
9,90448 |
2,29299 |
25 |
3,92 |
8,31448 |
2,11800 |
30 |
2,73 |
7,12448 |
1,96354 |
Urządzenie pomiarowe: polarymetr Optical Activity AA-65
Tabela4.: wyniki pomiarów dla katalizatora o stężeniu 4 M
t [min] |
αt [°] |
αt-α∞[°] |
ln(αt-α∞) |
0 |
13,23 |
17,54298 |
2,86465 |
5 |
9,31 |
13,62298 |
2,61176 |
10 |
6,39 |
10,70298 |
2,37052 |
15 |
3,98 |
8,29298 |
2,11541 |
20 |
2,10 |
6,41298 |
1,85832 |
25 |
0,57 |
4,88298 |
1,58576 |
30 |
-0,60 |
3,71298 |
1,31183 |
Urządzenie pomiarowe: polarymetr Atago AP-300
Temperatura pomiaru: 22,8 °C
Odczyty wartości z polarymetrów dla niezinwertowanego cukru równały się dwukrotności α0 - badane roztwory zostały podwójnie rozcieńczone roztworami HCl.
4. Opracowanie wyników
-Kąt skręcenia cukru zinwertowanego - został on obliczony za pomocą wzoru:
α∞=-α0*(0,44-0,005*tc)
gdzie:
α0 - kąt skręcenia (dla t=0 min)
tc - temperatura pomiaru [°C]
Wartości:
α∞=-13,48*(0,44-0,005*22,8)=-4,39448 (dla pomiaru urządzeniem Optical Activity AA-65)
α∞=-13,23*(0,44-0,005*22,8)=-4,31298 (dla pomiaru urządzeniem Atago AP-300)
-Stała szybkości inwersji sacharozy - ta reakcja przebiega według wzoru:
HCl
C12H22O11 + H2O → C6H12O6 + C6H12O6
sacharoza glukoza fruktoza
i można ją uznać na reakcję pierwszego rzędu pomimo tego, że biorą w niej udział dwa rodzaje cząsteczek - stężenie wody jest na tyle wysokie, że można je uznać za stałe. Sacharoza jest prawoskrętna, gdy w formie zinwertowanej (równomolowa mieszanina fruktozy i glukozy) jest lewoskrętna. Kąt skręcenia roztworu podczas powyższej reakcji zmienia się zgodnie z zależnością:
gdzie:
αt - kąt skręcania w danym czasie t
α0 - kąt skręcania sacharozy
α∞ -Kąt skręcania zinwertowanego cukru
c0 - początkowe stężenie sacharozy
c - stężenie sacharozy po czasie t
Te równanie można przekształcić do postaci:
Wstawiając otrzymany wzór do równania kinetycznego reakcji pierwszego rzędu (scałkowanego
w granicach od t=0 do t i c=c0 do c):
można otrzymać:
Te równanie można przekształcić do postaci:
ln(αt-α∞)=ln(α0-α∞)-kt
Powyższemu równaniu, będącym równaniem liniowym, odpowiadają równania umieszczonych poniżej wykresów ln(αt-α∞)=f(t), gdzie współczynnik kierunkowy odpowiada liczbie przeciwnej do wartości stałej k (a=-k).
Wykres1.: zależność ln(αt-α∞) od czasu (dla Ckatalizatora=1 M)
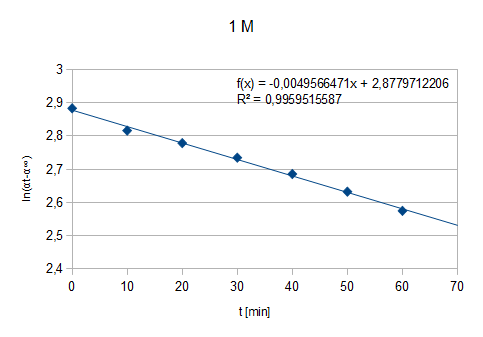
f(t)=-0,00496t+2,87797
a=-0,004957
b=2,877971
k=0,00496 min-1
Wykres2.: zal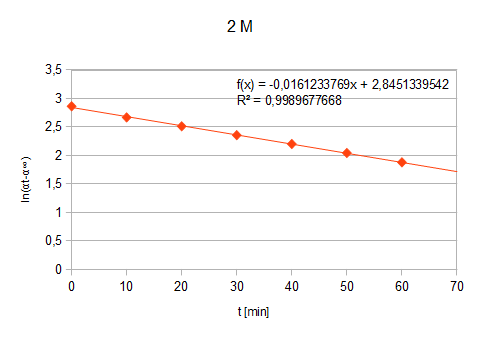
eżność ln(αt-α∞) od czasu (dla Ckatalizatora=2 M)
f(t)=-0,01612t+2,84513
a=-0,01612
b=2,84513
k=0,01612 min-1
Wykres3.: zależność ln(αt-α∞) od czasu (dla Ckatalizatora=3 M)
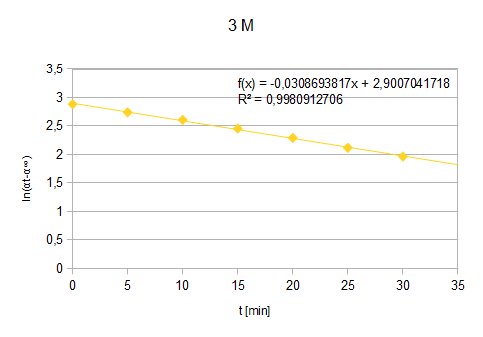
f(t)=-0,03087t+2,90070
a=-0,03087
b=2,90070
k=0,03087 min-1
Wykres4.: zależność ln(αt-α∞) od czasu (dla Ckatalizatora=4 M)
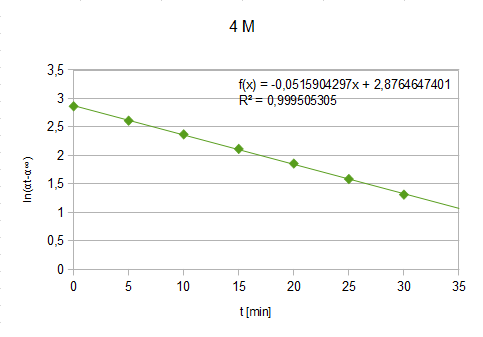
f(t)=-0,05159t+2,87646
a=-0,05159
b=2,87646
k=0,05159 min-1
Tabela5.: stałe szybkości reakcji dla poszczególnych stężeń katalizatora (HCl)
CHCl [mol/dm3] |
k [min-1] |
1 |
0,00496 |
2 |
0,01612 |
3 |
0,03087 |
4 |
0,05159 |
-Wpływ stężenia katalizatora na stałą szybkości inwersji cukru - katalizatorem w tej reakcji jest kwas solny, a właściwie jony H+, pochodzące z jego hydrolizy. Stała szybkości reakcji w obecności katalizatora jest wg Ostwalda liniową zależnością od stężenia katalizatora i jest dana równaniem:
k=k1+k2ckatalizatora
gdzie k1 i k2 to stałe (stała k1 odpowiada wyrazowi b, stała k2 - współczynnikowi kierunkowemu a).
Wykres5.: zależność stałej szybkości reakcji inwersji sacharozy od stężenia katalizatora
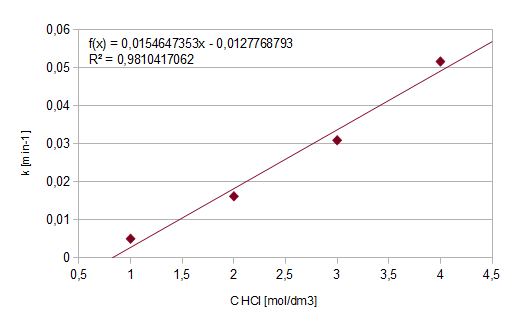
f(c)=0,015465c-0,01278
k1=b=-0,01278
k2=a=0,015465
5. Wnioski.
Podczas tego ćwiczenia zbadano, jak szybko sacharoza ulega inwersji do glukozy i fruktozy podczas hydrolizy katalizowanej kwasem solnym za pomocą polarymetrów. Zauważono, że wraz z postępem reakcji kąt załamania światła w roztworze zmniejszał się - spowodowane jest to tym, że podczas inwersji zmniejsza się stężenie prawoskrętnej D-sacharozy ([α]D=+66.47°), a zwiększa równomolowej mieszaniny prawoskrętnej D-glukozy i silnie lewoskrętnej D-fruktozy (D-glukoza: [α]D=+52.5°,
D-fruktoza: [α]D=−92.4°, stąd dla mieszaniny [α]D=-39,9°*). Na podstawie wykresu zależności wartości stałej szybkości reakcji od stężenia katalizatora (będącego funkcją liniową) dostrzeżono, że im wyższe jest stężenie katalizatora, tym ta reakcja zachodzi szybciej, a co za tym idzie, stała szybkości reakcji jest większa. Na błędy pomiarowe mogły wpłynąć takie czynniki, jak niedokładność odczytu kąta załamania światła przez polarymetry, różniące się od siebie wartości α0 niezinwertowanego cukru (odczyt dla polarymetru Optical Activity AA-65 był nieco wyższy niż dla polarymetru Atago AP-300) oraz dość długi czas odczytu drugiego urządzenia (aktualną wartość w danej chwili pomiaru wskazywało dopiero po ok. pół minuty od rozpoczęcia odczytu po wciśnięciu odpowiedniego przycisku).
*wartości skręcalności właściwej cukrów - za: http://en.wikipedia.org/wiki/Specific_rotation
Wyszukiwarka
Podobne podstrony:
5498
5498, W7 - inżynierii środowiska
5498
5498
5498
więcej podobnych podstron