ĆWICZENIE K-3
Konduktometryczne oznaczanie zawartości kwasu solnego i octowego w mieszaninie
1. Cel i zakres ćwiczenia
Konduktometryczne oznaczanie równocześnie występujących dwóch kwasów jest możliwe tylko wówczas, gdy różnią się one dość znacznie wartościami stałych dysocjacji (mają różną moc).
2. Czynniki i aparatura
wodorotlenek sodowy o natężeniu 0,1 mol/dm3
konduktometr
3. Wykonanie ćwiczenia
otrzymany roztwór kwasu solnego i kwasu octowego o nieznanym stężeniu rozcieńczyć wodą destylowaną w kolbie miarowej do 100 cm3. Następnie pobrać do zlewki 20 cm3 tak przygotowanego roztworu i dodać 80 cm3 wody destylowanej
zlewkę z tak przygotowaną próbką umieścić na mieszadle magnetycznym i zmierzyć przewodnictwo
dodawać z biurety po 1 cm3 wodorotlenku sodowego o stężeniu 0,1 mol/dm3, mieszając po dodaniu każdej porcji i odczytać wartość przewodnictwa. Przed odczytaniem należy trzykrotnie wyjąć sondę pomiarową
miareczkowanie prowadzić do 6 - 7 punktów po przekroczeniu punktu końcowego (PK2!)
miareczkowanie wykonać dla kilku prób (najlepiej 5)
4. Wyniki pomiarów:
Jak widać z wykresów, pierwszy punkt końcowy (PK1) oznaczający koniec miareczkowania mocnego kwasu solnego (HCl) leży na pierwszym załamaniu krzywej miareczkowania. Ilość zużytego NaOH wynosi odpowiednio:
I 7,9 cm3
II 7,5cm3
III 7,5cm3
Drugi punkt końcowy (PK2) oznacza koniec miareczkowania kwasu octowego (CH3COOH). Ilość zużytego NaOH wynosi odpowiednio:
I 15 cm3
II 14,7 cm3
III 14,7 cm3
Dyskusja wyników:
PK1
Średnia arytmetyczna zbiorowości próbnej:
![]()
![]()
Wariacja zbiorowości próbnej
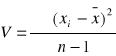
; n -1= k - liczba stopni swobody
![]()
Odchylenie standardowe pojedynczego wyniku
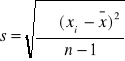
![]()
Odchylenie standardowe średniej arytmetycznej
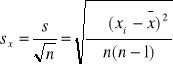
![]()
Względne odchylenie standardowe, charakteryzuje wielkość rozrzutu wyników
![]()
![]()
Przedział ufności:
95% dla k = 2 t-Studenta = 4,303
![]()
[ ]
![]()
[cm3]
PK2
Średnia arytmetyczna zbiorowości próbnej:
![]()
![]()
Wariacja zbiorowości próbnej
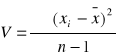
; n -1= k - liczba stopni swobody
![]()
Odchylenie standardowe pojedynczego wyniku
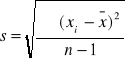
![]()
Odchylenie standardowe średniej arytmetycznej
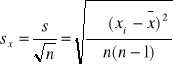
![]()
Względne odchylenie standardowe, charakteryzuje wielkość rozrzutu wyników
![]()
![]()
Przedział ufności:
95% dla k = 2 t-Studenta = 4,303
![]()
[ ]
![]()
[cm3]
Obliczam zawartość obu kwasów w mieszaninie:
NaOH + HCl → NaCl + H2O
NaOH + CH3COOH → CH3COONa + H2O
NaOH reaguje z obydwoma kwasami w stosunku 1 : 1, więc:
![]()
![]()
gdzie:
![]()
więc:
![]()
![]()
MHCl = 36,5 g/mol
![]()
= 60,0g/mol
CNaOH = 0,1 mol/dm3
VNaOH (PK1) = 7,633±0,572cm3
VNaOH (PK2) = 14,8±0,043 cm3
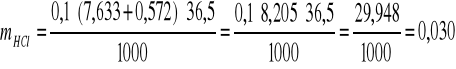
![]()
![]()
![]()
W badanej mieszaninie znajdowało się od 26 do 30 mg czystego HCl, oraz od 40 do 46 mg czystego CH3COOH.
1
Wyszukiwarka
Podobne podstrony:
chemia10, NAUKA, chemia, lab
miareczkownie, NAUKA, chemia, lab
Równowaga w roztworach elektrolitów, NAUKA, chemia, lab
pat sciąga chemia zerówka, NAUKA, chemia, lab
Masa atomowa i cząsteczkowa, NAUKA, chemia, lab
Na ciała poruszające się w cieczy, NAUKA, chemia, lab
Oznaczenie miedzi, NAUKA, chemia, lab
grupy pierwsiatkow chemia, NAUKA, chemia, lab
adsorp, NAUKA, chemia, lab
chemia7, NAUKA, chemia, lab
chemia2, NAUKA, chemia, lab
Spektrofotometria S-3, NAUKA, chemia, lab
E -4, NAUKA, chemia, lab
Politechnika Białostocka, NAUKA, chemia, lab
chemia tabelki 3, NAUKA, chemia, lab
Konduktometriaaa, NAUKA, chemia, lab
więcej podobnych podstron