Tomasz Seliwiorstow
Wydział Biotechnologii i Nauk o Żywności
Kierunek: biotechnologia
Grupa B2
Ćwiczenie nr 53
Tytuł ćwiczenia : Miareczkowanie pehametryczne
Data wykonania ćwiczenia....................
Data oddania sprawozdania..................
Data zwrotu sprawozdania....................
Data ponownego oddania sprawozdania..............
Wstęp:
Miareczkowanie pehametryczne polega na pomiarze pH miareczkowanego roztworu po dodaniu kolejnych porcji titranta (odczynnika miareczkującego). pH jest to ujemny logarytm z aktywności jonów wodorowych, aH+: pH = - log aH,
Wykres zależności pH roztworu miareczkowanego od ilości dodanego titranta nosi nazwę krzywej miareczkowania pehametrycznego.
Miareczkowanie mocnego kwasu mocna zasadą, np. kwasu solnego ługiem sodowym:
HCI(aq) + NaOH(aq) = NaCI (aq) + H2O(c)
Początkowo zmiany pH roztworu miareczkowanego są. małe. W miarę dodawania roztworu ługu stopniowo ubywa jonów wodorowych, H*, które są zastępowane jonami Na*. W pobliżu punktu stechiometrycznego następuje gwałtowna zmiana pH. W tym punkcie stężenie jonów wodorowych jest takie jak w czystej wodzie, a odpowiadające temu stężeniu pH = 7. Po przekroczeniu punktu równoważnikowego dodatek zasady prowadzi do dalszego wzrostu pH roztworu, ze względu na przyrost stężenia jonów OH".
Miareczkowanie słabego kwasu mocna zasadą
W czasie miareczkowania słabego kwasu, np. kwasu octowego mocną zasadą, np. NaOH stężenie jonów H+ w roztworze zależy od stopnia dysocjacji tego kwasu. Dodanie titranta przeprowadza część kwasu w sól (czyli według teorii Bronsteda sprzężoną z nim zasadę) zgodnie z reakcją:
CH3COOH(aq) + OH-(aq) = CH3COO-(aq) + H20
W każdym punkcie miareczkowania ustala się stan równowagi opisanej stałą równowagi Ka:
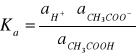
Jeśli pominiemy niewielki ubytek stężenia CH3COOH spowodowany jego dysocjacją oraz założymy, że aktywność niezdysocjowanego kwasu, aCH3COOH, jest równa jego stężeniu w roztworze, [kwas], a ponadto, że współczynnik aktywności jonów octanowych w roztworze jest zbliżony do 1, to możemy napisać, że aktywność, aCH3COO, jest w przybliżeniu równa stężeniu jonów octanowych w roztworze, [sól]. Stąd mamy:
![]()
![]()
Logarytmując ostatnie równanie i zmieniając znak po obu stronach dochodzimy do równania Hendersona-Haselbacha
![]()
![]()
W połowie drogi miareczkowania, gdy zobojętniona jest połowa wyjściowej ilości kwasu, stężenia kwasu i zasady są sobie równe, wtedy pH ≈ pKa. W punkcie równoważnikowym ilość dodanej zasady odpowiada wyjściowej ilości kwasu. W punkcie tym roztwór ma odczyn zasadowy. Dodanie następnych porcji zasady powoduje dalszy wzrost pH roztworu badanego. Położenie punktu równoważnikowego wyznacza się określając punkt przegięcia na krzywej miareczkowania, w którym przyrost pH jest najszybszy. Dokładniej punkt ten można wyznaczyć rysując krzywą pochodną
![]()
której maksimum określa równowagową objętość dodanego ługu, (VNaOH)równ-
Zasada pomiaru pH. Do pomiarów pH wykorzystuje się ogniwo zbudowane z elektrody pomiarowej, którą jest elektroda szklana i elektrody odniesienia, którą jest elektroda kalomelową. Elektrody zanurzone są w roztworze badanym o nieznanym stężeniu jonów wodorowych. Potencjał elektrody szklanej wyrażony wzorem:
![]()
jest liniową funkcją aktywności jonów wodorowych, a potencjał elektrody odniesienia jest stały, niezależny od pH roztworu. Siła elektromotoryczna takiego ogniwa wynosi:
![]()
ponieważ w temperaturze 25°C iloraz 2,3 ![]()
= 0,059, jeśli przyjmiemy ponadto, że: ![]()
; to: ![]()
Zgodnie z powyższym równaniem E jest liniową funkcją pH. Zmiana pH o jednostkę wywoła zmianę SEM tego ogniwa o 0,059 V. Przyrządy używane do pomiarów pH nazywane pehametrami są bezpośrednio wyskałowane w jednostkach pH. Ze względu na to, że parametr A we wzorze na potencjał elektrody szklanej zależy od jej budowy, a także zmienia się w czasie, konieczne jest kalibrowanie pehametru przy pomocy roztworów-buforowych, do tego celu może być stosowany np. 0,05 M kwaśny ftalan potasu, który w temp. 25°C ma pH = 4,00.
Tabela wyników
Mocny kwas |
|
VNaOH [ml] |
pH |
0 |
1,86 |
0,5 |
1,87 |
1 |
1,92 |
1,5 |
1,95 |
2 |
2,00 |
2,5 |
2,08 |
3 |
2,16 |
3,5 |
2,28 |
4 |
2,45 |
4,5 |
2,63 |
4,7 |
3,38 |
4,9 |
3,42 |
5,0 |
3,46 |
5,2 |
6,67 |
5,3 |
8,79 |
5,4 |
9,86 |
5,5 |
10,26 |
5,6 |
10,50 |
5,7 |
10,70 |
5,8 |
10,88 |
5,9 |
10,96 |
6,0 |
11,13 |
6,1 |
11,20 |
6,3 |
11,25 |
6,5 |
11,39 |
6,7 |
11,41 |
7,0 |
11,48 |
7,5 |
11,55 |
8,0 |
11,62 |
8,5 |
11,68 |
9,0 |
11,72 |
9,5 |
11,76 |
10,0 |
11,80 |
10,5 |
11,81 |
11,0 |
11,82 |
11,5 |
11,83 |
12,0 |
11,85 |
12,5 |
11,87 |
Słaby kwas |
|
VNaOH [ml] |
pH |
0 |
1,90 |
0,5 |
1,92 |
1 |
1,95 |
1,5 |
1,99 |
2 |
2,03 |
2,5 |
2,08 |
3 |
2,13 |
3,5 |
2,20 |
3,7 |
2,23 |
3,9 |
2,26 |
4,1 |
2,30 |
4,3 |
2,34 |
4,5 |
2,37 |
4,7 |
2,41 |
4,9 |
2,47 |
5,1 |
2,53 |
5,3 |
2,60 |
5,6 |
2,73 |
5,8 |
2,83 |
6 |
2,99 |
6,2 |
3,37 |
6,4 |
3,56 |
6,6 |
3,95 |
6,8 |
4,16 |
7 |
4,31 |
7,2 |
4,43 |
7,4 |
4,52 |
7,6 |
4,61 |
7,8 |
4,68 |
8,1 |
4,75 |
8,6 |
4,88 |
9,1 |
5,00 |
9,6 |
5,13 |
10,1 |
5,23 |
10,6 |
5,36 |
11,1 |
5,48 |
11,6 |
5,60 |
12,1 |
5,75 |
12,6 |
5,96 |
13,1 |
6,33 |
13,5 |
6,75 |
13,7 |
8,27 |
13,8 |
9,32 |
13,9 |
10,09 |
14,0 |
10,30 |
14,2 |
10,63 |
14,4 |
10,83 |
14,9 |
11,11 |
15,4 |
11,31 |
15,9 |
11,39 |
16,4 |
11,47 |
Wykres zmiany pH od objętości zasady
Wykres pochodnej krzywej miareczkowania od objętości dodanej zasady
Obliczam liczbę moli mocnego kwasu i stężenie molowe roztworu wyjściowego
Wykres zmiany pH podczas miareczkowania mocnego i słabego kwasu od objętości zasady
Wykres pochodnej krzywej miareczkowania od objętości dodanej zasady
Obliczam liczbę moli obu kwasów oraz stężenie molowe wyjściowe roztworów kwasów
Uwagi i wnioski
Metodą miareczkowania pehametrycznego wyznaczyć można zarówno stężenie pojedynczego kwasu, jak również stężenie kwasów słabego i mocnego w mieszaninie W przypadku miareczkowania mieszaniny słabego i mocnego kwasu konieczne jest dodanie acetonu, ze względu na istnienie zjawiska rozdziału słabego kwasu organicznego między fazę wody i acetonu. Ma to na celu częściowy rozdział mieszaniny kwasów, w wyniku, czego można wyznaczyć dwa punkty równoważnikowe
0
2
4
6
8
10
12
0,5
2
3,5
4,1
4,7
5,3
6
6,6
7,2
7,8
9,1
10,6
12,1
13,5
13,9
14,4
Serie1