Ekosystem i jego struktura: podłoże (siedlisko), producenci, konsumenci, konsumenci destruenci
Ekosystem - różnej wielkości funkcjonalny układ łączący przyrodę ożywioną i nieożywioną - organizmy żywe z ich środowiskiem abiotycznym.
Podłoże - Stanowi oparcie mechaniczne. Koniecznym składnikiem ekosystemu jest woda. Jej udział może być różny. Jest źródłem jonów prostych związków mineralnych, służących za pokarm dla producentów (roślin).
Producenci - Organizmy samożywne, które stanowią początek łańcucha pokarmowego i syntetyzują związki organiczne z prostych związków nieorganicznych przy użyciu energii słonecznej na drodze fotosyntezy. Na lądzie - drzewa, trawy itd. W wodach - sinice, okrzemki (fitoplankton). Chemoautotrofy (bakterie) - wytwarzają substancje organiczne w mniejszych ilościach.
Konsumenci - Organizmy cudzożywne. Odżywiają się materią organiczną wytworzoną przez producentów lub pochodzącą z innych konsumentów (drapieżnictwo). W ekosystemie więcej materii organicznej jest konsumowanej w postaci martwej.
Destruenci - Bakterie, grzyby - odżywiają się martwą materią, rozkładając materię organiczną z powrotem do prostych związków mineralnych. Aktywność destruentów decyduje o żyzności gleb. W ekosystemach o niskich temperaturach lub w gorących i suchych występuje niska żyzność m.in. , bo są to niedogodne warunki do funkcjonowania destruentów, w wyniku czego nie mogą one efektywnie rozkładać materii organicznej i producenci nie mają źródła substancji, które mogliby wykorzystać.
Łańcuchy troficzne
Łańcuchy pokarmowe - Organizmy należące do różnych grup uzależnionych od siebie na zasadzie jedzący-zjadany, np. trawa - sarna - wilk. Proste łańcuchy są rzadkie, bo drapieżca zwykle może zjeść więcej niż jeden rodzaj ofiary. W sieci pokarmowej występuje drapieżca szczytowy, którego nikt nie zjada.
Wyjaśnić na czym polega przepływ materii i energii w ekosystemie
Producent -> Konsument I rzędu (roślinożerca) -> konsument II rzędu (drapieżnik) -> …
-> Destruent -> Producent…
Powyższy schemat obrazuje, że współistnienie producentów, konsumentów i destruentów zapewnia obieg materii i równowagę systemu.
W obiegu energii i materii występują straty (wypromieniowywanie energii cieplnej w wyniku procesów oddychania).
Im niższy poziom troficzny (im krótsze ogniwo w łańcuchu) tym organizm może więcej przetworzyć pożywienia na masę własną i tym więcej ma skumulowanej energii. W każdym ogniwie kumuluje się energia, która jest pożywieniem dla ogniwa wyższego.
Wydajność ekologiczna ekosystemu
Wydajność ekosystemu (WE) określa stosunek asymilacji poziomu troficznego (B) do asymilacji poziomu poprzedniego (A) w łańcuchu pokarmowego.
WE=B/A*100%
Wartość WE jest zawsze bardzo mała.
Piramida ekologiczna (piramida energii)
Produktywność ciała ludzkiego 3,4*104kJ
Produkcja cieląt 1,5*106kJ
Produkcja lucerny 6,3*107kJ
Produkcja energii świetlnej 2,6*1010kJ
Wyjaśnić na czym polega krążenie azotu, węgla, wody w przyrodzie
Obieg wody - Parowanie wody z powierzchni zbiorników wodnych, lądów i organizmów lądowych (transpiracja) -> Opady atmosferyczne -> retencja wody w lądowych zbiornikach wodnych + wsiąkanie w glebę -> spływ powierzchniowy + odpływ podziemny + odpływ rzeczny -> morza i oceany
Bilans wodny: przychody + parowanie
3 przypadki:
1) Opady > parowanie - dużo wody odpływa z ekosystemu - następuje wypłukiwanie wielu miogenów (substancji „rodzących życie”), uwalnianych z rozkładu materii organicznej. Przykłady: puszcze tropikalne.
2) Opady = parowanie - Biogeny pozostają w ekosystemie do dyspozycji roślin. Przykłady: żyzne gleby Ukrainy i prerii USA.
3) Opady < Parowanie
Obieg azotu - Zbiornikiem azotu jest powietrze (78%), ale w tej postaci jest prawie zupełnie niedostępny, co wynika z właściwości cząsteczki azotu, która jest obojętna i potrzeba dużo energii, aby ją rozerwać.
Drogi wiązania azotu atmosferycznego w zw. przyswajalne dla organizmu:
1) Błyskawice - uwolnione atomy azotu wiążą się w tlenki, a następnie z wodą, tworząc azotany - źródło azotu dla roślin (około 5% zasobów azotu który dociera do świata roślinnego)
2) Organizmy wiążące azot - w wodach sinice (przyswajają węgiel i azot), w glebach - bakterie azotowe (azot przyswojony wchodzi do obiegu wraz z martwą materią), bakterie korzeniowe (rośliny motylkowe)
3) Azot zawarty w białkach i aminokwasach - wykorzystywany przez zwierzęta. Szczątki organizmów ulegają rozkładowi i azot zostaje uwolniony w postaci kationów amonowych.
Obieg węgla - Krążenie węgla w przyrodzie możemy utożsamiać z krążeniem materii organicznej, która jest oparta na węglu.
Zbiorniki:
Atmosfera - odbiór węgla przez fotosyntezę, dopływ przez oddychanie, spalanie, wypalanie wapna, przepływ dwukierunkowy CO2 między atmosferą i wodami oceanów
Woda oceanów - ekosystem, w którym są producenci wiążący węgiel. Gdy wody są zatrute, może nastąpić większe wydzielanie niż wiązanie węgla.
Biomasa roślin i zwierząt - równowaga -> rośliny wiążą węgiel, zwierzęta je zjadają, oddychanie
Martwa materia organiczna - Występuje w każdym ekosystemie. Obecnie niewielkie ilości węgla są na stałe wyłączone z obiegu (osady denne, pokłady torfu)
Paliwa kopalne
Skały węglanowe - głównie wytwór zwierząt i pierwotniaków (skorupy, muszle zamienione w skały). Węgiel do ich budowy pochodzi z wód morskich, w których zawartość CO2 była w stanie dynamicznej równowagi z atmosferą.
Wyjaśnij pojęcia: „Paliwo umowne” i „Para umowna”
Paliwo umowne (Qu) - jest to wartość opałowa substancji wyrażona jako energia w postaci ciepła, jaką możemy uzyskać z jednostki masy danego paliwa.
Przeliczanie paliwa rzeczywistego na umowne: Pu= (Prz*Qrz)/Qu
Para umowna -oznacza parę suchą o ciśnieniu 1 at., temperaturze 100°C i entalpii (cieplika) 2680 kJ/kg (640 4,18kJ/kg=2680 kJ/kg). Pojęcie to jest równoznaczne z rozpowszechnionym pojęciem pary normalnej. Przyjęta jednostka wagowa 1 tona.
Przeliczanie masy pary na parę umowną: Du= Drz*irz/iu
Podaj sposób określania wskaźnika sumarycznego zużycia energii w paliwie pierwotnym
Wskaźnik sumarycznego zużycia energii w paliwie pierwotnym określamy sumując zużycie energii w zakładzie w różnych postaciach (cieplna, elektryczna, przetworzone paliwo). Przed zsumowaniem energie te powinny być przeliczone na energię pierwotną przy uwzględnieniu sprawności przemian energetycznych. Dla energii elektrycznej sprawność wynosi 0,3, a dla energii cieplnej 0,7.
Energia zawarta w paliwie pierwotnym wynosi odpowiednio:
dla energii elektrycznej: Ep (energia pierwotna paliwa)= Ee (elektryczna)/sprawność (0,3)
dla energii cieplnej: Ep= Ec/ 0,7
Ep wyrażamy w Dżulach.
Wyjaśnij co to jest energochłonność ciągniona
Energochłonność ciągniona może być prowadzona w różnym zakresie. Może dotyczyć procesu, zakładu, branży.
W każdym przypadku wyniki mają charakter kompleksowy i obrazują nie tylko zużycie energii, ale również możliwość zmian tego zużycia.
W zakładzie energia zużywana jest na cele:
produkcyjne (zużycie główne)
poza produkcyjne (zużycie uboczne)
Zużycie energii na cele produkcyjne zależy od wielu czynników, które można podzielić na kilka grup:
czynniki surowcowe,
czynniki technologiczno - techniczne
czynniki organizacyjne
W każdej z tych grup występuje wiele uwarunkowań, które w określony sposób wpływają na zużycie energii w zakładzie produkcyjnym.
Na wyprodukowanie 400 kg suchej substancji koncentratu soku zużyto 3GJ energii cieplnej wytwarzanej w kotle parowym o sprawności 60% i 20 kWh energii elektrycznej z sieci krajowej. Podać energochłonność procesu w MJ energii pierwotnej na 1 kg suchej substancji koncentratu. Obliczenia uzasadnij
m=400kg Ec= 3GJ=3000MJ Ee= 20kWh=72000kJ=72MJ
(ni)c=0,6 (ni)e= 0,3
Ep=?
Ep(Ec/0,6+Ee/0,3)/400=13,1MJ/kg produktu
Na wyprodukowanie 400 kg suchej substancji koncentratu soku zużyto 2,8GJ energii cieplnej i 50 kWh energii elektrycznej z sieci krajowej. Podać energochłonność procesu w MJ energii pierwotnej na 1 kg suchej substancji koncentratu. Obliczenia uzasadnij.
Ep=(2800/0,7+180/0,3)/400=11,5
Zadanie jak powyżej.
Paliwem w kotle parowym jest 100% alkohol metylowy spalany w ilości 200 kg/h przy współczynniku nadmiaru powietrza λ = 1,25. Obliczyć strumień doprowadzanego powietrza w m3/h
2CH3OH+3O2->2CO2+4H2O
64kg - 96kg
200kg - x x=300kg/h
300/32=9,375kmol tlenu/h
1kmol - 22,4m3
9,375 - x2 x2= 210m3 tlenu/h
lamba= Lrz (strumień rzeczywisty)/Lt (teoretyczny)
Lrz= lambda*Lt= 1,25*210= 262,5 m3/h
262,5 - 0,21 (bo tlen w powietrzu to 21%)
x3 - 1 x3= 1250 m3/h
Paliwem w kotle parowym jest 100% alkohol etylowy spalany w ilości 200 kg/h przy współczynniku nadmiaru powietrza λ = 1,25. Obliczyć strumień doprowadzanego powietrza w m3/h
Analogicznie do powyższego.
Wyjaśnij dlaczego oszczędność energii w przemyśle spożywczym przyczynia się do zmniejszenia oddziaływania tego przemysłu na środowisko
Energia powstaje najczęściej w wyniku spalania paliw zawierających węgiel, siarkę, azot i inne pierwiastki. W wyniku spalania powstają tlenki tych pierwiastków, które mają niekorzystny wpływ na środowisko (CO2 dopiero w nadmiarze). Im mniej zużywamy energii (jeśli oszczędzamy), tym mniej paliw trzeba wykorzystać, a zatem tym mniejsza będzie emisja szkodliwych tlenków i pyłów do atmosfery, w której żyjemy.
Spalanie paliw a ochrona środowiska
Wpływ spalania energetycznego paliw na emisję dwutlenku węgla i efekt cieplarniany
Efekt cieplarniany - podwyższenie temperatury powierzchni ziemi spowodowana istnieniem atmosfery ziemskiej. Atmosfera ziemska przepuszcza w kierunku powierzchni ziemi znaczną część promieniowania słonecznego (promieniowanie krótkofalowe). Promieniowanie to jest pochłaniane przez powierzchnię ziemi i zamieniane na ciepło. Niewielka część promieniowania zostaje odbita, a ogrzana powierzchnia ziemi emituje promieniowanie długofalowe, w dużym stopniu pochłaniane przez atmosferę. Energia pochłaniana przez atmosferę jest poprzez nią wypromieniowywana głównie z powrotem w kierunku powierzchni ziemi (tzw. promieniowanie zwrotne - podstawowa przyczyna występowania efektu cieplarnianego) a częściowo w przestrzeń kosmiczną.
Do substancji absorbujących długofalowe promieniowanie ziemskie oprócz CO2 należą:
metan
podtlenek azotu N2O
ozon (znajdujący się w warstwie przypowierzchniowej ziemi)
freony i in.
Największe znaczenie ma CO2.
Wraz ze wzrostem CO2 w atmosferze następuje ocieplenie ziemi i mogą wystąpić bardzo negatywne zjawiska, takie jak: topnienie lodowców i kurczenie się linii wiecznych śniegów w górach oraz wzrost poziomu mórz i oceanów.
Prognozy: podwojenie koncentracji CO2 z 0,03 do 0,06% spowoduje wzrost średniej temperatury powietrza o ponad 2oC, co spowoduje topnienie lodowców i wzrost poziomu wód o 60-75 m.
Najprostszym (teoretycznie) sposobem ograniczenia efektu cieplarnianego jest ograniczenie emisji CO2 przez redukcję spalania paliw. Najpierw możemy zastąpić węgiel innymi paliwami. Następnie poprawić sprawność urządzeń energetycznych poprawiając izolację cieplną budynków, wprowadzając nowe technologie do przemysłu.
Emisja CO2 w kilogramach na jednostkę energii cieplnej uzyskanej z paliwa zależy od ilości węgla zwartej w paliwie. Jeżeli stosunek H:C w węglu kamiennym wynosi 0,5:1, to w oleju opałowym zbliża się do 2:1, a w gazie ziemnym 4:1.
Im wyższa zawartość węgla w paliwie tym wyższa jest emisja CO2. Wśród paliw w gazie ziemnym jest najniższa zawartość węgla, a co za tym idzie gaz ziemny powoduje najniższą emisję CO2.
Emisję CO2 można obniżyć przez konsekwentną redukcję zużycia paliwa i bardzo ekonomiczne jego wykorzystanie, czyli zwiększenie sprawności urządzeń kotłowych.
Emisję CO2 w określonym czasie można obliczyć z iloczynu emisji właściwej (CO2 wł) zużycia paliwa w tym czasie (B) i jego wartości opałowej (Qw):
![]()
Sprawność (ή) urządzenia kotłowego obliczana jest jako stosunek ciepła wykorzystanego do produkcji pary (Q) do ciepła wprowadzonego z paliwem (B×Qw):
![]()
Przekształcając otrzymujemy:
![]()
Im niższa jest sprawność urządzenia kotłowego tym wyższa emisja CO2, czyli w miarę wzrostu sprawności spada emisja CO2.
Tlenek węgla
Tlenek węgla jest produktem niezupełnego spalania (zachodzi w sytuacji, gdy substancja nie może utlenić się do końca):
![]()
Nagromadzenie CO w powietrzu jest szczególnie niebezpieczne, ponieważ nie jest wyczuwalny przez zmysły człowieka. Działanie toksyczne polega na wiązaniu się CO z hemoglobiną krwi Hb i powstaniu hemoglobiny tlenkowęglowej COHb:
![]()
,
przy czym CO wykazuje od 250 do 300 razy większe powinowactwo do hemoglobiny niż tlen. COHb jest trwalsza i 10 razy wolniej hydrolizuje od oksyhemoglobiny, tworzącej się podczas normalnego utleniania hemoglobiny w procesie oddychania.
Podczas dłuższego działania małych dawek tlenku węgla następuje uszkodzenie ośrodkowego układu nerwowego, wydłuża się czas reakcji na bodźce.
Tlenek węgla usuwany jest z atmosfery w procesach samooczyszczania się atmosfery. Istotą jest utlenienie CO do CO2:
![]()
Oraz asymilacja CO przez niektóre grzyby glebowe.
Węglowodory
W normalnych warunkach temperatury i ciśnienia są gazami lub cieczami o dużej lotności, pochodzącymi z emisji niespalonych paliw, pochodnych ropy naftowej. Źródłem są też rozpuszczalniki, pestycydy - z tlenkami azotu tworzącymi tzw. wtórne zanieczyszczenia powietrza, będące głównymi utleniaczami fotochemicznymi (np. wolne rodniki i azotany V nadtlenków organicznych) powstałymi w zanieczyszczonym powietrzu pod wpływem promieni UV i są zdolne do utleniania materiałów nieutlenionych przez tlen atmosferyczny.
Węglowodory są jednym ze składników smogu fotochemicznego tzw. smogu typu Los Angeles.
Wpływ spalania energetycznego paliw na emisję tlenków azotu
Tlenki azotu NOx
Tlenki azotu to głównie toksyczne gazy:
bezbarwny i bez zapachu tlenek azotu (II) NO
brunatny, o ostrej duszącej woni tlenek azotu (IV) NO2
Powstają one w czasie wysokotemperaturowego spalania paliw. W konwencjonalnej instalacji spalającej paliwo powstaje prawie wyłącznie NO:
![]()
Już w kotle ustala się on w 5-10% do NO2:
![]()
Pozostałe części reagują w atmosferze z tlenem powietrza do NO2.
NO2 łatwo rozpuszcza się w wodzie, gdzie tworzy kwas azotowy (V) i (III):
![]()
Kwas azotowy jest jednym ze składników kwaśnego deszczu, uważanego za jedną z przyczyn wymierania lasów. Działanie 1 ppm NO2 przez 2 doby powoduje całkowite obumarcie roślin. U zwierząt 5 ppm NO2 w ciągu 10 min powoduje trudności w oddychaniu, a 100 ppm obrzęk płuc i śmierć już po 5 h.
Mechanizm toksycznego działania NO2 jest następujący: na skutek braku odruchów obronnych NO2 wnika do głębszych partii dróg oddechowych, gdzie z wodą tworzy kwasy, które w wyniku zobojętnienia zasad ustrojowych dają silnie toksyczne sole. Sole te utleniają Fe2+ hemoglobiny do Fe3+, tworząc methemoglobinę i częściowo nitrozohemoglobinę, co powoduje zablokowanie przenoszenia tlenu. Żelazowe przemiany chemiczne w organizmie powodują opóźnienia w występowaniu objawów zatrucia. NO2 rozszerza naczynia krwionośne, co daje spadek ciśnienia krwi, zawroty i bóle głowy.
Tlenki azotu są bezpośrednimi prekursorami powstających w glebie rakotwórczych i mutagennych nitrozoamin, a z węglowodorowymi skażeniami powietrza tworzą bardzo toksyczne utleniacze fotochemiczne, jakim jest np. azotan (V) nadtlenoacetylowy, będący wtórnym zanieczyszczeniem powietrza. Jest on 1000 razy bardziej toksyczny od NO2 i 100 razy bardziej toksyczny od ozonu.
Wtórne zanieczyszczenia powietrza powstają na skutek przekroczenia stężeń progowych zanieczyszczeń pierwotnych i pod wpływem promieniowania UV. Powstają one zwykle wtedy, gdy zawodzą mechanizmy autoregulujące atmosfery, takie jak np. cykl fotolityczny NO2, utrzymujący na stałym poziomie stężenie ozonu i tlenków azotu.
Cykl fotolityczny NO2 w powietrzu jest bardzo ważnym mechanizmem samooczyszczania się atmosfery. Zaburzeniem tego procesu może być spowodowane wysokim nasłonecznieniem i obecnością wolnych rodników powstałych z niespalonych węglowodorów organicznych. Węglowodory znajdujące się w spalinach, szczególnie cukry, reagują z tlenem wytwarzając aldehydy i wolne rodniki. Prowadzi to do powstania bardzo aktywnych rodników nadtlenoacetylowych, a z kolei z NO2 dają niezwykle toksyczne azotany (V) nadtlenoacetylowe (w skrócie PAN).
W analogicznych warunkach, tzn. przy dużym nasłonecznieniu i dużym zanieczyszczeniu powietrza, tworzy się smog fotochemiczny tzw. smog typu Los Angeles.
Emisja CO2, CO, tlenków siarki, tlenków azotu, węglowodorów i ich wpływ na środowisko
Emisja CO2 w kilogramach na jednostkę energii cieplnej uzyskanej z paliwa zależy od ilości węgla zawartej w paliwie. Jeżeli stosunek H:C w węglu kamiennym wynosi 0,5:1, to w oleju opałowym zbliża się do 2:1, a w gazie ziemnym 4:1.
Im wyższa zawartość węgla w paliwie tym wyższa jest emisja CO2. Wśród paliw w gazie ziemnym jest najniższa zawartość węgla, a co za tym idzie gaz ziemny powoduje najniższą emisję CO2.
Emisję CO2 można obniżyć przez konsekwentną redukcję zużycia paliwa i bardzo ekonomiczne jego wykorzystanie, czyli zwiększenie sprawności urządzeń kotłowych.
Emisję CO2 w określonym czasie można obliczyć z iloczynu emisji właściwej (CO2 wł) zużycia paliwa w tym czasie (B) i jego wartości opałowej (Qw):
![]()
Sprawność (ή) urządzenia kotłowego obliczana jest jako stosunek ciepła wykorzystanego do produkcji pary (Q) do ciepła wprowadzonego z paliwem (B×Qw):
![]()
Przekształcając otrzymujemy:
![]()
Im niższa jest sprawność urządzenia kotłowego tym wyższa emisja CO2, czyli w miarę wzrostu sprawności spada emisja CO2.
Tlenek węgla
Tlenek węgla jest produktem niezupełnego spalania (zachodzi w sytuacji, gdy substancja nie może utlenić się do końca):
![]()
Nagromadzenie CO w powietrzu jest szczególnie niebezpieczne, ponieważ nie jest wyczuwalny przez zmysły człowieka. Działanie toksyczne polega na wiązaniu się CO z hemoglobiną krwi Hb i powstaniu hemoglobiny tlenkowęglowej COHb:
![]()
,
przy czym CO wykazuje od 250 do 300 razy większe powinowactwo do hemoglobiny niż tlen. COHb jest trwalsza i 10 razy wolniej hydrolizuje od oksyhemoglobiny, tworzącej się podczas normalnego utleniania hemoglobiny w procesie oddychania.
Podczas dłuższego działania małych dawek tlenku węgla następuje uszkodzenie ośrodkowego układu nerwowego, wydłuża się czas reakcji na bodźce.
Tlenek węgla usuwany jest z atmosfery w procesach samooczyszczania się atmosfery. Istotą jest utlenienie CO do CO2:
![]()
Oraz asymilacja CO przez niektóre grzyby glebowe.
Węglowodory
W normalnych warunkach temperatury i ciśnienia są gazami lub cieczami o dużej lotności, pochodzącymi z emisji niespalonych paliw, pochodnych ropy naftowej. Źródłem są też rozpuszczalniki, pestycydy - z tlenkami azotu tworzącymi tzw. wtórne zanieczyszczenia powietrza, będące głównymi utleniaczami fotochemicznymi (np. wolne rodniki i azotany V nadtlenków organicznych) powstałymi w zanieczyszczonym powietrzu pod wpływem promieni UV i są zdolne do utleniania materiałów nieutlenionych przez tlen atmosferyczny.
Węglowodory są jednym ze składników smogu fotochemicznego tzw. smogu typu Los Angeles.
Tlenki azotu NOx
Tlenki azotu to głównie toksyczne gazy:
bezbarwny i bez zapachu tlenek azotu (II) NO
brunatny, o ostrej duszącej woni tlenek azotu (IV) NO2
Powstają one w czasie wysokotemperaturowego spalania paliw. W konwencjonalnej instalacji spalającej paliwo powstaje prawie wyłącznie NO:
![]()
Już w kotle ustala się on w 5-10% do NO2:
![]()
Pozostałe części reagują w atmosferze z tlenem powietrza do NO2.
NO2 łatwo rozpuszcza się w wodzie, gdzie tworzy kwas azotowy (V) i (III):
![]()
Kwas azotowy jest jednym ze składników kwaśnego deszczu, uważanego za jedną z przyczyn wymierania lasów. Działanie 1 ppm NO2 przez 2 doby powoduje całkowite obumarcie roślin. U zwierząt 5 ppm NO2 w ciągu 10 min powoduje trudności w oddychaniu, a 100 ppm obrzęk płuc i śmierć już po 5 h.
Mechanizm toksycznego działania NO2 jest następujący: na skutek braku odruchów obronnych NO2 wnika do głębszych partii dróg oddechowych, gdzie z wodą tworzy kwasy, które w wyniku zobojętnienia zasad ustrojowych dają silnie toksyczne sole. Sole te utleniają Fe2+ hemoglobiny do Fe3+, tworząc methemoglobinę i częściowo nitrozohemoglobinę, co powoduje zablokowanie przenoszenia tlenu. Żelazowe przemiany chemiczne w organizmie powodują opóźnienia w występowaniu objawów zatrucia. NO2 rozszerza naczynia krwionośne, co daje spadek ciśnienia krwi, zawroty i bóle głowy.
Tlenki azotu są bezpośrednimi prekursorami powstających w glebie rakotwórczych i mutagennych nitrozoamin, a z węglowodorowymi skażeniami powietrza tworzą bardzo toksyczne utleniacze fotochemiczne, jakim jest np. azotan (V) nadtlenoacetylowy, będący wtórnym zanieczyszczeniem powietrza. Jest on 1000 razy bardziej toksyczny od NO2 i 100 razy bardziej toksyczny od ozonu.
Wtórne zanieczyszczenia powietrza powstają na skutek przekroczenia stężeń progowych zanieczyszczeń pierwotnych i pod wpływem promieniowania UV. Powstają one zwykle wtedy, gdy zawodzą mechanizmy autoregulujące atmosfery, takie jak np. cykl fotolityczny NO2, utrzymujący na stałym poziomie stężenie ozonu i tlenków azotu.
Cykl fotolityczny NO2 w powietrzu jest bardzo ważnym mechanizmem samooczyszczania się atmosfery. Zaburzeniem tego procesu może być spowodowane wysokim nasłonecznieniem i obecnością wolnych rodników powstałych z niespalonych węglowodorów organicznych. Węglowodory znajdujące się w spalinach, szczególnie cukry, reagują z tlenem wytwarzając aldehydy i wolne rodniki. Prowadzi to do powstania bardzo aktywnych rodników nadtlenoacetylowych, a z kolei z NO2 dają niezwykle toksyczne azotany (V) nadtlenoacetylowe (w skrócie PAN).
W analogicznych warunkach, tzn. przy dużym nasłonecznieniu i dużym zanieczyszczeniu powietrza, tworzy się smog fotochemiczny tzw. smog typu Los Angeles.
Odsiarczanie spalin
Przyczyny prowadzenia odkwaszania:
bezbarwny gaz
1-2 ppmszkodliwy dla organizmu
roślinygorzej rosną w wyniku czego obniża się liczba plonów
większa szkodliwość na materiały
korozja
niszczy skórę i papier
osłabia wytrzymałość włókien roślinnych
powoduje zakwaszenie akwenów
kwaśne deszcze
Metody odsiarczania:
Mokre
Suche
Półsuche
Regeneracyjne
Metod na mokro
Najczęściej spotykana
Najdroższa
Skuteczna w 90 %
Pochodzące z odsiarczania spalin przy użyciu metody na mokro odpady powstają jako osad w absorberze. Jest to zasadniczo mieszanina siarczynów oraz siarczanów wapnia. Stanowi ona silnie uwodniony materiał (tak zwaną pulpę gipsową), którą ciężko jest odwodnić, ale w takiej postaci nie nadaje się ona do składowania. Dlatego też należy poddać ją intensywnemu natlenianiu, dzięki któremu siarczyny zostają zamienione do postaci siarczanów wapnia, a te, po przeprowadzeniu ich odwodnienia do wilgotności mniejszej niż10%, mogą przyjąć postać dwuwodnego gipsu. Produkt ten z kolei można zużyć jako surowiec służący do produkcji gipsowego spoiwa, czyli gipsu budowlanego. Naturalny gipsowy kamień, którego złoża w znacznych ilościach występują w Polsce, to odpowiednik tego otrzymywanego sztucznie gipsu.
Metoda na sucho
W metodzie tej do spalin wdmuchiwany jest kamień wapienny (drobno zmielony) lub mączka wapienna. W kotle, w paleniskowej komorze panuje wysoka temperatura, dlatego kamień wapienny rozkłada się i powstaje tlenek wapnia CaO oraz dwutlenek węgla CO2. Tlenki siarki (SO2, SO3) wiązane są przez tlenek wapnia, dając siarczyny oraz siarczany wapnia. Przebiega to według następujących reakcji:
CaO + SO2 = CaSO3
CaO + SO3 = CaSO4
Powstające produkty łącznie z zanieczyszczeniami wapiennego kamienia lub mączki, zostają usunięte z odpylacza wraz z lotnym popiołem. Proces ten ma różną skuteczność odsiarczania. Zależy to od poziomu rozdrobnienia addytywu, a także sposobu oraz miejsca wprowadzania go do paleniskowej komory, jak również od czasu trwania całej reakcji. Znaczenie ma również stosunek wapnia do siarki (Ca/S), czyli nadmiar wapnia, który jest do spalin wprowadzany, w odniesieniu do niezbędnej jego ilości potrzebnej do związania występującej w spalinach siarki. Dodanie wapiennego kamienia do węglowych młynów, w których zostanie on zmielony razem z węglem, a następnie dostarczony do kotła, jest najprostszym sposobem zastosowania tej metody. Skuteczność procesu suchego odsiarczania, zależnie od stosunku wapnia do siarki.
Metoda półsucha
Przy użyciu jednego reaktora fluidalnego realizowane jest tu zarówno odsiarczanie, jak i odpylanie oraz granulacja. Ziarna spryskiwane są wapniowym reagentem, w wyniku czego dochodzi do wiązania SO2 we fluidalnej warstwie. Powstają siarczyny oraz siarczany tworzące warstwę "lepiku" na ziarnach. Potrafi on zatrzymywać przenoszony przez spaliny pył, dlatego też dochodzi również do jego odpylania oraz granulacji. Do odpylania spalin (ostatecznego), a także wychwytywania drobnoziarnistych produktów (powstających w trakcie procesu odsiarczania) oraz niezbędnego wapna dochodzi już za fluidalnym reaktorem, w końcowym odpylaczu.
Metoda ta jest skuteczna w odsiarczaniu w zakresie od 40 do 80%. Elektrociepłownie korzystające z metody półsuchego odsiarczania spalin wytwarzają tylko jeden typ odpadu, a mianowicie mieszaninę popiołu z produktami odsiarczania. Odpady te pojawiają się pod postacią paleniskowych odpadów (jest to popiół pochodzący z elektrofiltrów oraz żużel powstający pod kotłem), bądź w postaci odpadu suchego, pochodzącego z absorbera (jest to mieszanina siarczynu i siarczanu wapnia z popiołem).
Wpływ spalania energetycznego paliw na emisję tlenków azotu
Bardzo groźne są również inwersje temperatury przy dużym stężeniu SO2, CO2 i pyłu węglowego w wilgotnym powietrzu, co prowadzi do wytworzenia smogu kwaśnego typu londyńskiego, zwanego mgłą przemysłową.
Mechanizmy powstawania NOx:
szybki
opałowy
termiczny
Szybkie NOx powstaje we froncie płomienia. Ich stężenie zależy w małym stopniu od temperatury, a w dużym od współczynnika nadmiaru powietrza (dzięki wolnemu O2).
Opałowy NOx powstaje podczas reakcji azotu organicznego w paliwie z tlenem z powietrza w temperaturze spalania co najmniej 1000oC. Opałowy NOx powstaje podczas spalania oleju opałowego i węgla. Gaz ziemny nie zawiera związków organicznych azotu.
Termiczny NOx ma największe znaczenie zarówno przy opalaniu węglem, olejem opałowym jak też gazem. Przy powstawaniu termicznego NOx decydujące jest stężenie tleniu podczas spalania i czas przebywania powietrza w strefie płomienia o temperaturze powyżej 1200oC.
Najczęściej stosowane sposoby zmniejszenia emisji tlenków azotu:
obniżenie temperatury spalania (np. stosowanie specjalnych palników - odprowadzenie ciepła w postaci promieniowej)
kontrolowanie procesu mieszania paliwa z powietrzem (zmniejszenie współczynnika nadmiaru powietrza, recyrkulacja splain)
Ubocznym efektem działań redukujących emisję tlenków azotu może być zwiększona emisja CO.
Odpylanie spalin
Wszystkie paliwa cechują się przeciwstawnymi właściwościami pod względem wytwarzania NOx i CO.
Do usuwania popiołów z gazów spalinowych stosuje się odpylacze mechaniczne:
cyklony czy multicyklony (przemysł spożywczy)
elektrofiltry
filtry workowe
Stałe odpady paleniskowe
Spalanie węgla powoduje również powstawanie stałych produktów spalania: popiołu i żużlu, zwanych odpadami paleniskowymi. Ilość tych odpadów zależy od:
ilości użytego węgla, jego jakości (zawartość popiołu)
rodzaju i konstrukcji paleniska
skuteczności zastosowanych urządzeń odpylających (rodzaj ma również wpływ na skład granulometryczny popiołów).
Naszkicować, opisać i scharakteryzować dowolny kocioł parowy płomiennorurowy
Zależnie od tego czy spaliny omywają powierzchnie ogrzewalną parownika po stronie wewnętrznej czy zewnętrznej, kotły dzielą się na:
- płomiennorurowe
- płomienicowe (rura o dużej średnicy)
- płomieniówkowe (rura o małej średnicy)
- płomienicowo - płomieniówkowe
- opłomkowe (rury o małej średnicy) - spaliny omywają z zewnątrz rury wypełnione wodą, parą, mieszaniną wody i pary
Kocioł płomienicowy - zbudowany jest z zewnętrznego płata (walczaka) zamkniętego drzwiami, w których jest zamocowana jedna lub dwie płomienice (rura o dużej średnicy)
Płomienica może być wykonana z blachy falistej, co zwiększa powierzchnię wymiany ciepła.
W przedniej części płomienicy znajduje się palenisko (palnik). Spaliny po wyjściu z płomienicy mogą być wykorzystywane do przegrzewania pary (przepływają przez przegrzewacz pary).
Rys. Schemat kotła płomienicowego ????????
Kotły płomienicowe mają szereg zalet, charakteryzują się:
dużą pojemnością wodną co powoduje ich małą wrażliwość na zmiany obciążenia;
mają prostą budowę co zapewnia ich długi żywot i pewność działania;
mogą być zasilane wodą o gorszych parametrach;
Do wad należą:
mała wydajność;
długi czas rozruchu;
duże zapotrzebowanie miejsca;
niska sprawność w granicach 50%
Wykład 4.6-5.2 (wykład.strona)
Naszkicować, opisać i scharakteryzować kocioł parowy opłomkowy
Kocioł opłomkowy: zakłady przemysłu spożywczego o dużej skali produkcji eksploatują kotły parowe opłomkowe nazywane również wodnorurkowymi. Są to kotły o małej pojemności wodnej, najczęściej opalane są węglem kamiennym.
W kotle opłomkowym powierzchnię ogrzewaną stanowią rury o małej średnicy zwanej opłomkami, które wypełnione są wodą, parą lub mieszaniną wody i pary.
W kotłach opłomkowych odparowanie wody zachodzi w opłomkach, natomiast oddzielanie wody od pary w walcach lub walczakach. Kotły opłomkowe charakteryzują się dużą wydajnością i wysokim ciśnieniem roboczym, mają wysoką sprawność (1,6 - 1,8 MPa)
Wśród wielu rozwiązań kotłów opłomkowych w przemyśle spożywczym eksploatowane są kotły stromorurkowe opromieniowane oznaczane symbolem „ O” lub opromieniowane z dodatkowym pękiem rur gdzie ciepło przejmowane jest na drodze konwekcji oznaczanej symbolem OKR - 5. Dodatkowy symbol „ R” oznacza, że jest to kocioł rusztowy, cyfra 5 - informuje o wydajności - 5 ton na godzinę.
W pokazanym na rysunku kotle walczaki połączone są trzema pękami opłomek.
Spaliny z komory paleniskowej kierowane są za pomocą ścianki (kierownicy) wzdłuż przedniego pęku opłomek następnie ku dołowi przez przegrzane pary, z kolei ku górze wzdłuż pierwszego zespołu opłomek pionowego pęku a następnie ku dołowi wzdłuż drugiego zespołu opłomek tego pęku. W końcu przepływają przez podgrzewacz wody i podgrzewacz powietrza do czopucha.
Woda z walczaka głównego opada opłomkami pęku pionowego do walczaka dolnego a wznosi się pękiem przednim i częściowo najbardziej ogrzewanymi opłomkami pęka pionowego. Górne walczaki połączone są dolnymi rurami wodnymi wyrównującym poziom wody i górnymi parowymi odprowadzającymi parę z przedniego walczaka górnego do walczaka głównego.
Wykład 5.1
Oblicz na podstawie posiadanych wiadomości ile kg węgla zużyje dodatkowo w ciągu roku kocioł parowy OKR-5 pracujący przez 11 miesięcy w roku z nominalną wydajnością do którego wraca tylko 4 tony skroplin na godzinę. Obliczenia uzasadnij
Prawdopodobnie źle (myślę, że opis, że mamy kocioł parowy OKR-5 ma tu znaczenie):
t=11 mies.= 330 dni= 7920 h
mpary= 5t=5000kg wart. opał.=20kJ/kg
r= 2500kJ/kg
Qdostarczone= mpary.*r= 5000*2500= 1,25*107kJ/h
mwęgla= Qdostarczone/wart.opałowa= 1,25*107/20=625 000kg/h=625t/h
Należy jeszcze uwzględnić sprawność kotła, której nie znam.
Wpływ ilości i sposobu doprowadzania powietrza na efekt energetyczny spalania węgla w palenisku kotła parowego.
Nadmiar powietrza:
- zwiększone powstawanie szybkiego i termicznego NOx
- zwiększone zużycie energii na podgrzanie powietrza i jego wpompowanie
- całkowite spalenie węgla do CO2
Za małe napowietrzenie:
- wzrost strat niepełnego spalania węgla do CO2 (wzrost zawartości CO o 1% powoduje wzrost strat ciepła o 4-6%)
- wzrost emisji CO
Temperatura wprowadzanego powietrza ma wpływ na kontrolowanie spalinowych strat ciepła. Zmiana temperatury powietrza o 1 stopień powoduje zmianę temperatury spalin o 0,5 stopnia.
Aby optymalnie napowietrzać ruszt stosuje się napowietrzanie strefowe. Inną formą optymalizacji spalania przez odpowiednie napowietrzanie jest stosowanie spalania w złożu fluidalnym. Odbywa się to w kotłach pionowych, które na dnie posiadają zespół dysz nadmuchujących powietrze. Powietrze utrzymuje w stanie fluidalnym zasypywany miał węglowy.
Wyjaśnij co to jest współczynnik nadmiaru powietrza oraz podaj jego wpływ na efekt energetyczny spalania paliw
Współczynnik nadmiaru powietrza jest to stosunek rzeczywistego zapotrzebowania na powietrze do jego teoretycznego zapotrzebowania.
(lamba)=Lrz/Lteor
Teoretyczne zapotrzebowanie zakłada, że każda cząsteczka tlenu zawarta w powietrzu wchodzi w reakcję ze spalanym związkiem. W rzeczywistości tak się nie dzieje i dlatego musimy doprowadzić do palnika i rusztu większą ilość powietrza zawierającego tlen. Niedostateczne zaopatrzenie w tlen z powietrza (zbyt niski wsp. nadmiaru powietrza) powoduje niecałkowite spalenie (np. węgla) w wyniku czego nie otrzymujemy tyle ciepła, ile byśmy mogli przy pełnym spaleniu. Prowadzi to do wzrostu strat ciepła na drodze niecałkowitego spalenia i emisji szkodliwych gazów, które są produktami niecałkowitego spalania (CO). Straty ciepła powodują, że musimy zużyć więcej paliwa, aby pokryć zapotrzebowanie.
Odzysk ciepła w przemyśle spożywczym, przykłady i ograniczenia.
Wskaźnik określający stopień wykorzystania ciepła odparowanego nazywamy współczynnikiem odzysku (regeneracji) ciepła i definiowany jest jako stosunek ciepła odzyskanego przez gorący produkt do całej ilości ciepła potrzebnego do ogrzewania produktu od temperatury początkowej do temperatury pasteryzacji zgodnie ze schematem:
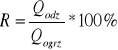
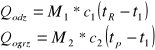
M1 = M2 - strumień masowy produktu
![]()
ciepło właściwe obrabianego produktu
t1 - temperatura początkowa produktu
tR - temperatura po sekcji regeneracji (przed pasteryzacją)
tp - temperatura pasteryzacji
Po skróceniu otrzymujemy:
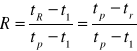
Stosowanie regeneracji przynosi oprócz oszczędności cieplnej również oszczędność wody niezbędnej do chłodzenia produktu do założonej temperatury końcowej, ponieważ im większy współczynnik regeneracji tym niższa temperatura produktu wychodzącego z sekcji regeneracji. Im więcej ciepła chcemy odzyskać, tym musimy zastosować większą powierzchnię wymiany ciepła w sekcji regeneracji.
Nie jest możliwe odzyskanie całej ilości ciepła odpadowego w procesie pasteryzacji. Wraz ze wzrostem strumienia (R) maleje zużycie ciepła do przeprowadzenia procesu, a wiec obniżają się koszty eksploatacji wymiennika, lecz musi wzrosnąć powierzchnia wymiany ciepła, a wiec i cena wzrasta.
Wielkość powierzchni wymiany ciepła w funkcji współczynnika regeneracji podziału.
Przykład:
Niższy współczynnik regeneracji stosowany jest przy pasteryzacji mleka do produkcji sera, ponieważ temperatura końcowa mleka nie powinna być niższa od temperatury optymalnej działalności podpuszczki.
W wymienniku płytowym o wydajności 100 ton/dobę pasteryzuje się ciecz o cieple właściwym 4 kJ/kgK przy zastosowaniu pary jako nośnika ciepła. Temperatura pasteryzacji wynosi 95oC, temperatura wejściowa cieczy 5oC. Współczynnik regeneracji R=50%. Ile kg paliwa o wartości opałowej 20000 kJ/kg zaoszczędzi się w kotle parowym o sprawności 60% w ciągu doby, jeżeli współczynnik regeneracji zwiększy się do 80%
M=100t/doba cw= 4MJ/t*K t2= 95oC t1= 5oC
R1=0,5 R2= 0,8 wart.opał.= 20 000MJ/t (ni)=0,6
Ciepło, które jest potrzebne do pasteryzacji (Q1):
Q1= 100* 4*(95-5)= 36000[MJ/doba]
Ciepło, które odzyskujemy:
R=QR/Q1=> QR= Q1*R=18000[MJ/doba]
Ciepło, które po regeneracji musimy „uzupełnić”:
Q2= 36000-18000=18000[MJ/doba]
Ponieważ sprawność kotła wynosi 0,6 musimy dostarczyć z paliwem ciepło Q3:
18000/0,6= 30000[MJ/doba]
Q3= wart.opał.* B1(strumień masowy) stąd
B1= Q3/wart.opał.= 30000/20000=1,5[t/doba]
Jeżeli R2 wynosi 0,8, to:
QR'= 36000*0,8= 28800 [MJ/doba]
Stąd trzeba uzupełnić:
Q2'=36000-28800= 7200[MJ/doba]
Stąd wynika, że potrzebujemy ciepła z paliwa:
Q3'= 7200/0,6= 12000[MJ/doba]
A paliwa potrzebujemy:
B2= Q3'/wart.opał.= 12000/20000=0,6[t/doba]
(delta)B= B1-B2= 1,5-0,6=0,9[t/doba]
Odp. Jeśli R wzrośnie do 0,8, to dobowo będziemy zużywać o 0,9t węgla mniej.
Zasobniki pary (ciepła) - budowa, działanie, zastosowanie.
W sytuacji gdy nie można zapewnić równomiernego obciążenia kotłów parowych, co ma miejsce w zakładach o różnorodnej produkcji gdzie mogą występować krótkotrwałe szczyty obciążenia, instaluje się przy kotłach parowych zasobniki pary (zasobniki ciepła).
Dzięki zastosowaniu zasobnika można w pewnych okresach czasu zmniejszyć liczbę pracujących kotłów parowych lub przy prawidłowym zbilansowaniu można zmniejszyć liczbę instalowanych kotłów.
Zasobniki ciepła wykonane są jako ciśnieniowe zbiorniki o dużej pojemności wodnej. W przemyśle spożywczym instalowane są zasobniki typu Ruthsa. Jest to izolowany walczak wypełniony w 90% wodą do którego doprowadza się parę za pomocą specjalnych dysz, co powoduje intensywne mieszanie i krążenie wody w zasobniku.
W okresie zbyt dużej produkcji pary w stosunku do zapotrzebowania działów produkcyjnych, zamiast zmniejszenia obciążenia kotła lub wyłączaniu go z ruchu nadmiar pary wtłaczany jest do zasobnika. Para skraplając się oddaje ciepło skraplania wody w zasobniku. Entalpia wody zwiększa się przy tym do wartości odpowiadającej ciśnieniu (p1) pary zasilającej. Jest to okres ładowania zasobnika. Podczas zwiększonego zapotrzebowania na parę, obniża się ciśnienie w zasobniku do ciśnienia (p2) odpowiadającego ciśnieniu pary pobieranej z zasobnika. Część wody w zasobniku odparowuje kosztem różnicy entalpii wody przy ciśnieniach (p1, p2). Jest to okres rozładowania zasobnika. Zasobnik pracuje przy różnicy ciśnień miedzy ciśnieniem (p1) w określonym gromadzeniu ciepła (ładowania), a ciśnieniem (p2) w okresie oddawania ciepła (rozładowania).
Schemat wiązania zasobnika ciepła do układu wytworzenia pary w przemyśle spożywczym.
Zainstalowanie zasobnika pary pozwala w dużym stopniu zwiększyć zdolność akumulacyjne wytwarzania pary i umożliwia pracę kotłów przy prawie stałym obciążeniu, przy maksymalnej zdolności.
Zdolności akumulacyjne zasobnika pary zależą od pojemności wodnej oraz dopuszczalnego spadku ciśnienia.
Korzyści wynikające z zastosowanie zasobników pary:
- równomierność w obciążeniu kotłów parowych, przez co mogą one pracować przy obciążeniu najbardziej ekonomicznym (przy którym sprawność jest najwyższa). Nie występują chwilowe przeciążenia kotłów
- zmniejszenie ilości czynnych kotłów parowych. Gdy nie ma zasobnika pary zwiększone zapotrzebowanie pary musi być pokrywane przez uruchomienie dodatkowego kotła, co pociąga za sobą określone straty ciepła
- możliwość pracy kotłów przy niższym ciśnieniu, wynika ze zwiększonych zdolność zdolności akumulacyjnych wytwarzania pary, ponieważ oprócz akumulacji ciepła w samym kotle dochodzi akumulacja ciepła w zasobniku pary
- wielka elastyczność pary układu wytwarzania pary
Opisać jak przebiega w praktyce i przedstawić na wykresie I-S proces zmiany parametrów pary wodnej w celu dostosowania ich do danych warunków pracy
Dostosowanie parametrów pary do innych odbiorników przeprowadza się w następujący sposób:
W wybranych miejscach głównego rurociągu parowego prowadzi się odgałęzienia, na którym redukuje się ciśnienie pary do wybranej wielkości. Redukcję ciśnienia (rozprężanie)przeprowadza się przy zastosowaniu reguł zawartych w termodynamice dławieniem.
W warunkach procesu odwracalnego, w idealnych dyszach proces rozprężania przebiega przy stałej entropii (s= const.) Na wykresie i-s proces rozprężania od ciśnienia p1 do p2 przebiega po prostej AB.
AB- proces teoretyczny(stała entropii)
AD- proces rzeczywisty (dławienie izentalpowe i= const)
Przy występowaniu tarcia proces musi stać się nieodwracalny, a więc rozprężanie będzie przebiegało za wzrostem entropii. W granicznym przypadku, przy wysokim tarciu, entalpie gazu przed i po rozprężeniu będą sobie równe i proces przebiega wzdłuż odcinka AD. Procesy redukcji ciśnienia pary wodnej (dławione) są procesami przebiegającymi według zasady i1 = i2 ,a więc na wykresie wzdłuż linii poziomych (rys 2).
Dławienie przebiega w odpowiednich zaworach. Instaluje się dwa zawory szeregowo (jeżeli chce się uzyskać duże obniżenie ciśnienia). Każdy zawór redukuje ciśnienie 1:6.
W warunkach przemysłu spożywczego często redukuje się ciśnienie do punktu D. W punkcie A para ma ciśnienie 1,0 MPa, jest lekko wilgotna (x=0,98) i ma temperaturę 179,90C. Parę redukujemy do ciśnienia 0,1 MPa, a więc prowadzimy z punktu A prostą poziomą do punktu D. W tych warunkach para w punkcie D ma temperaturę ok. 1370C i znajduje się powyżej krzywej granicznej x=1, a więc jest w strefie pary przegrzanej, co łatwo zauważyć z liczb, ponieważ para nasycona, tzn. x=1, ma pod ciśnieniem 0,1 MPa i temp. 99,60C.
Zwykle w rurociągach parowych do kontroli parametrów pary stosowane są tylko manometry. Odczytując zatem bezpośrednio redukcyjne ciśnienie 0,1 MPa, możemy łatwo popełnić błąd przypisując parze temperaturę odpowiadającą stanowi nasycenie tj. ok. 1000C, podczas gdy w rzeczywistości jest ok. 1370C. Jeśli redukcję przeprowadza się w pobliżu aparatu, to wprowadzimy ją do wymiennika ciepła. Przeciwdziałanie tym niekorzystnym zjawiskom sprowadza się w praktyce zakładów przemysłu spożywczego do umieszczania reduktora pary w odległości kilku metrów od odbiornika i nie izolowania ostatniego odcinka rurociągu za reduktorem. Następuje wtedy ochłodzenie pary, obniżenie entalpii i związane z nim w tych warunkach obniżenie temperatury i osiągnięcie punktu na krzywej granicznej x=1 tj. stanu nasycenia.
Wyjaśnij zasadę pracy odwadniacza zwężkowego, termodynamicznego, termostatycznego, pływakowego
Odwadniacz zwężkowy
Zasada działania odwadniacza zwężkowego (dławiącego) polega na przepuszczeniu skroplin przez tak dobrany otwór zwężki, aby przepływały przez niego tylko skropliny a tylko w minimalnym stopniu para wodna. Odwadniacze zwężkowe mają budowę podobną do zwężki pomiarowej z tym, że często mają wymienne płytki z kalibrowanym otworem o różnych średnicach. Idea zastosowania zwężki jako odwadniacza opiera się na znanej zależności od obliczania strumienia cieczy lub pary przepływu przez zwężkę.
![]()
M- strumień masowy płynu (cieczy lub pary)
α0 - teoretyczna liczba przepływu
Ponieważ występuje bardzo duża różnica w gęstości pary i cieczy, przy tych samych parametrach pozostałych, strumień masowy pary przepływającej przez zwężkę jest minimalny w stosunku do przepływu cieczy (skroplin) stąd i straty pary są niewielkie.
Przykład:
Przy ciśnieniu pary grzejnej 0,1 MPa gęstość pary wynosi 0,57 kg/m3, gęstość wody (skroplin) wynosi 1000 kg/m3. Stąd stosunek strumienia przepływającej przez odwadniacz zwężkowy pary do strumienia cieczy wynosi ok. 0,02 czyli ok. 2%
Odwadniacze zwężkowe pracują dobrze przy niewielkich wahaniach strumienia skroplin są powszechnie stosowane w stacjach wyparnych do odprowadzania skroplin z wyparek.
Odwadniacze pływakowe z pływakiem zamkniętym są mechanicznymi regulatorami pomiarowymi o działaniu ciągłym.
Gdy wzrasta poziom kondensatu pływak podnosi się i otwiera zawór.
Dzisiejsza penetracja odwadniaczy pływakowych ma dodatkowo wbudowany termostatyczny odpowietrzacz w celu usunięcia powietrza z układu w czasie rozruchu. ………………………
Odwadniacz pływakowy dzwonowy
Odwadniacz dzwonowy działa na zasadzie różnicy wyporności dzwonu wypełnionego parą lub kondensatem. Wewnętrzny zawór jest otwierany lub zamykany dzięki ruchowi dzwona (zamknięcia). Ruch ten w górnej części odwadniacza powoduje, że nie zbierają się w nim zanieczyszczenia.
Zawór wewnętrzny jest zawsze zanurzony w kondensacie, do niego nie dochodzi para. Tak więc nie występuje erozyjne niszczenie gniazda zaworu, stąd jego trwałość.
Dzwon wykonuje ruch w dół i w górę zawór jest zanurzony w kondensacie, dzięki czemu ten typ odwadniacza pracuje bez jakichkolwiek strat pary. Otworek w dzwonie przez który przechodzi powietrze, dwutlenek węgla, itd. jest samoczynnie czyszczona przy pomocy cienkiego druku(?).
Odwadniacz nie wymaga regulacji ani częstego czyszczenia ponieważ większy osad zbiera się w dolnej części obudowy.
Dopływająca pod dzwon para i powietrze powoduje, że wzrasta jego wyporność. Dzwon unosi się do góry i zamyka zawór (zamknięcia).
Odwadniacz pływakowy dzwonowy. Normalna praca.
Dzwon pod wpływem własnej masy opada na dół. Zawór (zamknięcie) jest otwarte. Kondensat bez przeszkód odpływa. Dopływająca pod dzwon para powoduje, że wzrasta jego wyporność. Dzwon unosi się do góry i zamyka zawór (zamknięcie).
Odwadniacze termostatyczne
Zasada działania opiera się na pewnym przechłodzeniu kondensatu. Mogą mieć różną konstrukcję.
Elementem sterującym może być konstrukcja płytek bimetalowych (dwa metale o różnej rozszerzalności cieplnej ze sobą sprasowane)
Zasada działania odwadniacz jest otwarty
Podczas rozruchu instalacji:
odprowadza powietrze zimny kondensat
Podczas odstawienia instalacji :
usuwanie powstałego kondensatu.
Odwadniacz zamknięty:
Przy wzroście temperatury kondensatu płytki bimetalowe wyginają się i przesuwają grzyb iglicowy w kierunku zamykania gniazda dyszowego.
Odwadniacz termodynamiczny
Działanie odwadniacza opiera się na paradoksie hydrodynamicznym.
Elementem sterującym jest metalowa płytka
Strumień mieszaniny parowo-wodnej wpływającej do odwadniacza uderzając w swobodnie umieszczoną ruchomą płytkę nie przesuwającą się w kierunku przepływu wtedy przyciska ją do gniazda.
Zjawisko takie występuje ponieważ w szczelinie między płytką a gniazdami para rozpręża się uzyskując znaczną prędkość a jej ciśnienie dynamiczne wzrasta, a ciśnienie statyczne maleje. Część pary przepływa nad płytką, jej prędkość i ciśnienie dynamiczne obniża się, wzrasta ciśnienie statyczne. Ciśnienie statyczne działając na powierzchnię płytki przyciska ją do gniazda i uniemożliwia przepływ pary. Jeżeli przez odwadniacz płyną skropliny, to płytka pozostaje uniesiona i skropliny bez przeszkód przepływają do gniazda i dalej do rurociągu skroplin.
a) odwadniacz całkowicie otwarty. Odprowadzany jest znany kondensat.
b) odwadniacz zaczyna się zamykać
c) odwadniacz całkowicie zamknięty. Ciśnienie nad płytką w połączeniu z dużą powierzchnia utrzymuje odwadniacz zamknięty
Czy przeponowy wymiennik ciepła ogrzewany parą może pracować bez odwadniacza, odpowiedź uzasadnij
Czy wymiennik ciepła może pracować bez odwadniacza?
Tak, ale jak najkrócej, bo są straty.
Obejście umożliwia ciągłą pracę wymiennika podczas konserwacji czy wymiany odwadniacza. Obejście podczas normalnej pracy nie jest wykorzystywany. Króciec do badania jakości skroplin jak również sprawdzanie ich czystości do jednego odwadniacza mogą być odprowadzone skropliny z kilku wymienników pod warunkiem takich samych parametrów pracy.
Wyjaśnij na czym polega, jak jest realizowana w przemyśle spożywczym i jakie korzyści przynosi skojarzona gospodarka energetyczna.
Skojarzona (równoczesne wytworzenie energii cieplnej i elektrycznej) gospodarka energetyczna.
Sprawność procesu przemiany energii cieplnej zawartej w paliwie w energię elektryczną jako sprawność ogólną obliczona jest ze wzoru:
![]()
η- sprawność ogólna wytwarzania energii elektrycznej
Br - zużycie paliwa kg/kWh
Qr - wartość opałowa spalanego paliwa kJ/kg
1kWh = 3600 kJ
W odniesieniu do paliwa umownego wzór ma postać:
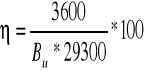
Bu - zużycie paliwa umowne kg/kWh
29300 - wartość umowna kJ/kg
1kWh = 3600 kJ
Maksymalna sprawność przemiany energii zawartej w paliwie w energie elektryczną co zawodowych elektrowniach dochodzi do 40%, wartość średnia jest znacznie niższa i wynosi ok. 30%.
Wniosek:
Jeżeli jedynym celem zakładu elektrycznego jest produkcja energii elektrycznej ponosi się bardzo duże straty.
Wszędzie tam, gdzie do celów produkcyjnych potrzebna jest energia elektryczna i para technologiczna istnieją możliwości bardziej racjonalnej gospodarki energetycznej można zastosować skojarzoną gospodarkę energetyczną.
Istotą gospodarki skojarzonej jest równoczesne wytwarzanie w zakładzie pary grzejnej i energii elektrycznej.
W skojarzonej gospodarce wytwarzamy w kotle parę wodną o bardzo wysokich parametrach. Para kierowana do turbin przeciwprężnych. Turbina jest skojarzona z prądnicą. Z turbiny wypływa para o niższych parametrach, która jest wykorzystywana jako para technologiczna.
Wykorzystanie paliwa 90%
Wytworzona w opisany sposób energia elektryczna ma charakter energii opadowej (produkowanej przy okazji).
Zużycie ciepła na wytworzenie w ten sposób 1 kWh jest 3-5 krotnie mniejsze niż w siłownikach zawodowych (kondensacyjnych).
Gdzie jest wykorzystana gospodarka skojarzona?
Skojarzona gospodarka energetyczna prowadzona jest w cukrowniach. W kotłach parowych kosztem ciepła spalanego wytworzona jest para wodna przegrzana o ciśnieniu 2-8 MPa i temperaturze 300-5000C
Para ta kierowana jest bezpośrednio do turbogeneratorów, w których wytwarzana jest energia elektryczna. Im wzrost ciśnienia i wzrost temperatury pary przegrzanej na wlocie do turbiny, a zarazem im niższe jest ciśnienie pary przeciwprężnej, tym samym więcej energii elektrycznej można uzyskać z dysponującej ilości pary.
Granicą praktyczną jest ciśnienie 8 MPa i temperatura 5000C. Rozprężona w turbinie para wodna ma ciśnienie ok. 0,4 MPa i niewielkie przegrzanie. Para ta służy jako czynnik grzejny, np. w wyparkach. Dzięki gospodarce skojarzonej wykorzystanie energii zawartej w paliwie sięga 90%.
W pomieszczeniu zamkniętym idealnie izolowanym znajduje się pracujące urządzenie chłodnicze sprężarkowe (sprężarka z silnikiem elektrycznym, skraplacz chłodzony powietrzem, zawór redukcyjny, parownik). Wyjaśnić przy pomocy wykresu T-S czy temperatura w tym pomieszczeniu będzie wzrastać, obniżać się, czy pozostanie na stałym poziomie
Wg cyklu Carnota w takim pomieszczeniu temperatura będzie rosnąć, ponieważ ciepło oddane jest większe od ciepła pobranego, a różnica jest wyrównywana przez wykonanie pracy przez sprężarkę. (Wykład 8, strona 2 lub 3).
Przedstawić na wykresie T-S i opisać skutki energetyczne i eksploatacyjne sprężania dwustopniowego z dochładzaniem w stosunku do jednostopniowego bez dochładzania w obiegu chłodniczym w tym samym zakresie temperatur
Wg podręcznika do maszynoznawstwa-ćwiczenie 10
Obieg dwustopniowy z dochładzaniem umożliwia nam uzyskanie niższych temperatur czynnika chłodniczego, oraz pobranie większej ilości ciepła ze środowiska chłodzonego, co skutkuje większą wydajnością chłodniczą obiegu. Umożliwia to również szybsze osiągnięcie założonej temperatury w porównaniu do obiegu jednostopniowego bez dochładzania.
Uzdatnianie wody do celów technologicznych
Uzdatnianie wody do celów technologicznych
Dezynfekcja wody jest to proces, którego zadaniem jest zniszczenie lub inaktywacja żywych i przetrwalnikowych form drobnoustrojów, organizmów patogennych.
Do całkowitej mineralizacji mikroorganizmów stosowane są metody:
Fizyczne
Chemiczne
Metody chemiczne polegają na wprowadzaniu silnych utleniaczy:
Chlor
Podchloryny
Dwutlenek chloru
Chloraminy
Ozon
Najbardziej rozpowszechnioną i najtańszą metodą dezynfekcji wody jest jej chlorowanie.
Dezynfekcja wody
Dezynfekcja wody jest to proces, którego zadaniem jest zniszczenie lub inaktywacja żywych i przetrwalnikowych form drobnoustrojów, organizmów patogennych.
Do całkowitej mineralizacji mikroorganizmów stosowane są metody:
Fizyczne
Chemiczne
Metody chemiczne polegają na wprowadzaniu silnych utleniaczy:
Chlor
Podchloryny
Dwutlenek chloru
Chloraminy
Ozon
Najbardziej rozpowszechnioną i najtańszą metodą dezynfekcji wody jest jej chlorowanie.
Chlor gazowy stosowany w technologii wody do celów spożywczych jest szkodliwy dla zdrowia i środowiska naturalnego. Głównym zagrożeniem są trójchlorometany (THM) oraz inne chlorowce organiczne, które powstają w procesach wstępnego lub wtórnego chlorowania wody.
Bardziej bezpieczną metodą dezynfekcji wody (od stosowania chloru gazowego) jest zastosowanie dwutlenku chloru (ClO2).
Przy zastosowaniu ClO2 substancje organiczne zawarte w wodzie ulegają głównie utlenianiu, a nie chlorowaniu. Wadą stosowania ClO2 jest konieczność jego wytwarzania w stacji uzdatniania ze względu na właściwości wybuchowe oraz możliwość powstawania w wodzie chlorynów i chloranów.
Dezynfekcja ozonem polega na przepuszczeniu przez wodę powietrza nasyconego O3 (tlenem trójatomowym), który jest zarówno silnym utleniaczem jak i dezynfektantem. Ozon podobnie jak dwutlenek chloru wytwarzany jest w miejscu dawkowania.
Przemysłowa metoda produkcji ozonu oparta jest na zasadzie cichego, elektrycznego wyładowania w zmiennym polu wysokiego napięcia, które oddziałuje na strumień czystego, suchego tlenu lub powietrza.
Istotna wada ozonu jako dezynfektanta jest jego mała trwałość, stąd niebezpieczeństwo wtórnego zakażenia wody.
Metody fizyczne polegają na użyciu:
Obróbki termicznej
Naświetlania promieniami ultradźwiękowymi
Zastosowanie ultradźwięków
Promieniowanie gamma
Ultrafiltracji
Obróbka termiczna jest metodą drogą, ale najlepszą. Nie jest stosowana na wysoką skalę. Może być stosowana w niektórych technologiach.
W dezynfekcji wody promieniami ultrafioletowymi (UV) które niszczą mikroorganizmy, źródłem promieniowania UV są specjalne lampy rtęciowe - kwarcowe, lub argonowe, które emitują promieniowanie UV o długości fali od 100 do 400 nm. Maksymalne oddziaływanie UV na drobnoustroje wykazują fale o długości 265 nm. Drobnoustroje wykazują różną odporność na działanie ultrafioletu. Dezynfekowana woda musi być całkowicie klarowna, ponieważ obecność nawet niewielkich ilości zawiesin powoduje rozproszenie promieni i zmniejszenie skuteczności dezynfekcji.
Wadą dezynfekcji wody promieniami UV jest to, że działanie dezynfekujące występuje tylko w czasie naświetlania wody. Nie zapobiega więc wtórnemu rozwojowi bakterii w sieci wodociągowej. Koszty dezynfekcji wody lampami UV są wyższe od kosztów dezynfekcji wody przy użyciu środków chemicznych.
Zaletą metody jest to, że nie zmienia składu fizyko-chemicznego wody.
Z aktualnych, znanych metod dezynfekcji wody, metoda dezynfekcji promieniami UV uważana jest za najbardziej skuteczną, szybką i pewną oraz w najmniejszym stopniu zanieczyszczającą środowisko.
Zastosowanie ultradźwięków do dezynfekcji wody nie jest szeroko stosowane. Obecnie jest to metoda wspomagająca inne procesy dezynfekcji. Skuteczność dezynfekcji ultradźwiękami zależy od natężenia dźwięku, częstotliwości, czasu działania ultradźwięków oraz rodzaju i liczby niszczonych mikroorganizmów. Ultradźwięki, podobnie jak promieniowanie UV nie zabezpieczają wody przed wtórnym rozwojem mikroorganizmów w sieci wodociągowej. Zastosowanie ultradźwięków do dezynfekcji wody do celów spożywczych nie wyszło poza sferę badań laboratoryjnych i półtechnicznych.
Promieniowanie gamma w Polsce niestosowane, ale niesie niebezpieczeństwo zanieczyszczenia wody.
Uzdatnianie wody do celów technicznych (zasilania kotłów parowych)
Woda do zasilania kotłów parowych stanowi zwykle uzupełnienie strat kondensatu w obiegu parowo-wodnym kotłowni.
Uzdatnianie wody do zasilania kotłów:
Zapobiega wytrącaniu osadów i powstawaniu kamienia kotłowego oraz mułu, powodujących dodatkowy opór cieplny na powierzchniach wymiany ciepła
Zmniejsza szybkość korozji urządzenia kotłowego oraz zapobiega pienieniu wody.
Wyjaśnić zasadę użytkowania wody w obiegu zamkniętym. Narysować schemat, podać zalety i wady takiego systemu.
Obieg zamknięty polega na tym, że woda krąży w obiegu. Woda jest czynnikiem pośredniczącym w wymiarze ciepła w skraplaczu, następnie trafia do chłodnicy. Woda częściowo odparowuje pobierając ciepło parowania. W obiegu zamkniętym zawsze mamy wodę do uzupełnienia.
SCHEMAT ŚCIĄGNĄĆ Z INTERNETU
Zalety:
Mniej wody zużywanej ze studni
Wady:
Musimy mieć urządzenie chłodnicze
Wyjaśnić na czym polega proces usuwania żelaza z wody w warunkach przemysłowych
Odżelazianie wody
W wodach głębinowych żelazo najczęściej występuje w postaci jonów dwuwartościowych, których związki są rozpuszczalne w wodzie, np. żelazo (HCO3) lub FeSO4.
W wodach powierzchniowych często znajduje się na najwyższym stopniu utlenienia i występuje w postaci Fe(OH)3.
W wodzie zawierającej duże ilości kwasów humusowych.
Istota odżelaziania wody polega na utlenieniu jonów Fe(II) do Fe(III), a następnie usunięciu wytrąconych związków Fe(OH)3 z uzdatnianej wody w procesach sedymentacji i filtracji.
W warunkach przemysłowych mamy wiele modyfikacji technicznych:
Filtracja
Napowietrzanie i filtracja
Napowietrzanie, sedymentacja i filtracja
Alkalizacja, napowietrzanie, sedymentacja i filtracja
Chemiczne utlenianie i filtracja
Koagulacja i filtracja
![]()
Stosowane jest do odżelaziania wody zawierającej dwuwartościowe żelazo w postaci Fe(HCO3)2. Występuje hydroliza i utlenianie.
Fe (HCO3)2 ulega hydrolizacji.
![]()
Operacja alkalizacji wprowadzana jest dodatkowo, jeżeli w uzdatnianej wodzie żelazo występuje również w postaci FeSO4. Do uzdatnianej wody dodawane jest wapno, węglan lub wodorotlenek sodu.
![]()
Stosowane jest wówczas, gdy skuteczność utleniania żelaza tlenem rozpuszczonym w wodzie jest utrudniona a zastosowanie utleniania nie prowadzi do powstania produktów bardziej szkodliwych niż substraty utleniania.
![]()
Stosowanie sedymentacji uzależnione jest od zawartości żelaza w uzdatnianej wodzie i konstrukcji złoża filtracyjnego. Proces ten zalecany jest, gdy stężenie żelaza w uzdatnianej wodzie jest duże i wynosi 5-10 g/m3.
W przemyśle spożywczym do filtrowania wody w procesie odżelaziania najczęściej stosowane są złoża filtracyjne piaskowe lub piaskowo- antracytowe wpracowane w sposób naturalny. Stosowane są również materiały filtracyjne mające właściwości złóż wpracowanych, co podnosi efektywność procesu odżelaziania, ponieważ oprócz działania typowo filtracyjnego mają one właściwości aktywnego oddziaływania poprzez reakcje chemiczne zachodzące na powierzchni złoża.
![]()
Metoda ta stosowana jest w tych przypadkach, gdy żelazo występuje w połączeniu ze związkami organicznymi a napowietrzanie i utlenianie chemiczne nie przynosi pożądanych efektów odżelaziania lub stwarza niebezpieczeństwo pogorszenia jakości wody.
Stosowanie do utleniania żelaza np. chloru może spowodować powstanie toksycznych chlorowanych związków organicznych w tym trihalometanu (THM).
Proces koagulacji wykorzystywany jest przy oczyszczaniu większości wód powierzchniowych, rzadziej podziemnych. W wyniku koagulacji usuwane są z wody cząstki trudno opadające oraz koloidalne decydujące o mętności wody lub intensywności jej barwy. Najczęściej stosowanymi koagulantami są sole glinu oraz wapno.
Wyjaśnić na czym polega proces usuwania manganu z wody w warunkach przemysłowych
Odmanganianie wody
Proces usuwania manganu z wody jest podobny do procesu odżelaziania. Często w praktyce przemysłowej oba te procesy prowadzone są równocześnie.
Odmanganianie wody polega na hydrolizie i utlenianiu jonów Mn (II) do Mn (IV) i wytrąceniu ich w postaci MnO2* xH2O.
Odmanganianie wody można przeprowadzić stosując:
Napowietrzanie i filtrację
Alkalizację, napowietrzanie i filtrację
Napowietrzanie i filtrację przez wpracowane złoże filtracyjne
Chemiczne utlenianie i filtrację
Koagulację i filtrację
Filtrowanie przez kationit manganowy
Utlenianie w warstwie wodonośnej - metoda VYREDOX (HYDROX).
Związki Mn (II) obecne w uzdatnianej wodzie są bardziej trwałe i nie ulegają hydrolizie jak sole żelaza. Stąd też nie wszystkie wymienione metody usuwania manganu z wody w warunkach przemysłowych mogą być przeprowadzone.
![]()
Skuteczne utlenianie manganu tlenem z powietrza wymaga stosowania wysokiego pH, powyżej 8,5. w praktyce przemysłowej można to osiągnąć dozując do napowietrzaniej wody wodorotlenek wapnia. Proces odmanganiania przebiega zgodnie z równaniami:
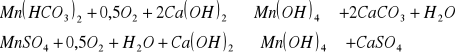
Wytrącający się wodorotlenek manganowy przechodzi następnie w uwodniony dwutlenek manganu, który jest usuwany z wody w drodze filtracji:
![]()
Zmiękczanie wody
Zmiękczanie wody
Polega na usunięciu z niej jonów powodujących twardość tj. głównie kationów wapnia (Ca2+) i magnezu (Mg2+).
Ze względu na rodzaj stosowanych procesów wyróżnia się następujące metody:
Strąceniowe
Jonowe
Membranowe
Metody strąceniowe stosujemy:
Metodę termiczną usuwania twardości węglanowej
Metoda wapniowo- sodowa
Zmiękczanie ługu sodowego i sodą
Zmiękczanie fosforanami
Metody polegają na wytrąceniu z wody związków wapnia i magnezu w postaci trudno rozpuszczalnych osadów.
Usuwanie gazów, odtlenianie wody
Usuwanie gazów
W wodzie znajdują się zawsze rozpuszczone gazy, głównie tlen, azot, dwutlenek węgla, siarkowodór i inne.
Z wody przeznaczonej do zasilania kotłów parowych gazy te powinny być usunięte, szczególnie tlen i dwutlenek węgla, ze względu na możliwość powstawania ogniw korozyjnych w kotle.
Do usuwania gazów z wody w warunkach przemysłowych stosuje się:
Odgazowanie fizyczne
Chemiczne wiązanie gazów (wiązanie chemiczne dotyczy praktycznie tylko tlenu)
Fizyczne odgazowanie wody polega na zmniejszeniu rozpuszczalności gazów w wodzie np. przez podwyższenie temperatury. Podczas odgazowania wody następuje wówczas częściowy rozkład kwaśnego węglanu sodu i tym samym zmniejsza się w wodzie zawartość dwutlenku węgla związanego chemicznie.
![]()
Chemiczne odtlenianie polega na dawkowaniu do wody silnych reduktorów wiążących tlen.
Środkami odtleniającymi stosowanymi w praktyce przemysłowej są:
Siarczyn sodowy (Na2SO3)
Związki hydrazyny (N2H2)
Odtlenianie wody bez wzrostu zasolenia umożliwia dozowanie hydrazyny, wodzianu hydrazyny lub siarczanu hydrazyny. Wiązanie tlenu hydrazyną przebiega zgodnie z reakcją:
![]()
Powstający azot ulatnia się z parą wodną. Hydrazyna i jej wodzian są związkami żrącymi, stąd wada tej metody. Najbardziej bezpieczny jest siarczan hydrazyny, ale dawkowany w postaci wolnego roztworu zawierającego NaOH zwiększa zasolenie wody. W zależności od pH wody powstaje NaHSO4 lub Na2SO4.
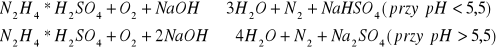
Wyjaśnić symbole BZT, BZT5, ChZT, RLM
Tlenowy i beztlenowy rozkład substancji organicznych
Zasadnicza różnica między tlenowym (aerobowym) i beztlenowym (anaerobowym) procesem rozkładu
Proces aerobowy - następuje szybkie i intensywne namnażanie bakterii przy niewielkiej ilości produktu rozpadu,
Proces anaerobowy - powstanie nowych komórek bakterii jest wolniejsze przy równocześnie znacznej ilości produktu rozpadu
Wyjaśnić, co to jest samooczyszczanie się wód oraz podać, jakie warunki muszą być spełnione by proces taki przebiegał
Samooczyszczanie mineralizacja związków organicznych KOSZTEM TLENU rozpuszczonego w wodzie, powstają dwutlenek węgla, siarczany, azotany, fosforany.
Powstałe związki są usuwane ze środowiska przez glony i rośliny wyższe szczególną rolę odgrywają tu glony- asymilują dwutlenek węgla i wydzielają tlen,
Organizmy zwierzęce takie jak skorupiaki regulują liczebność i strukturę zespołów bakterii uczestniczących w procesach rozkładu,
Skorupiaki i wrotki działają w podobny sposób żerując na glonach i pierwotniakach,
Drobne organizmy zwierzęce są pokarmem np. dla ryb
Ryby są pożywieniem dla człowieka
Brak tlenu zamiast mikroorganizmów tlenowych rozwijają się mikroorganizmy beztlenowe. Powstają takie związki jak: siarkowodór, metan, dwutlenek węgla. Rozmnażanie bakterii trwa tak długo, aż nastąpi całkowite zużycie substancji odżywczych. W wyniku tzw. głodu następuje wymieranie bakterii.
Metody oczyszczania ścieków (mechaniczne, biologiczne, fizyko-chemiczne)
Stosowane metody oczyszczania ścieków zależą od:
Właściwości ścieków
Konicznego stosowania oczyszczania ścieków ze względu na obowiązujące przepisy prawne
Główne problemy związane z oczyszczaniem ścieków w zakładach przemysłu spożywczego:
Zmienna ilość ścieków w czasie
Konieczność wyrównywania przepływu i ładunku zanieczyszczeń
Sezonowość produkcji
Zagrożenie ze strony szkodliwej mikroflory i fauny
W przemyśle spożywczym do oczyszczania ścieków stosuje się:
Metody mechaniczne
Metody biologiczne: sztuczne i naturalne
Metody fizyko-chemiczne
Metody mechaniczne (I etap) oczyszczanie ścieków polega na usunięciu ze ścieków:
Zawiesin
Substancji nierozpuszczalnych
Cząstek pływających
Przy mechanicznym oczyszczaniu ścieków poddawane są one procesom:
Cedzenia
Filtracji
Sedymentacji
Wzbogacaniu (flotacji)
Przy mechanicznym oczyszczaniu ścieków wykorzystuje się następujące urządzenia:
Kraty
Sita
Piaskownik
Osadniki
Odłuszczacze
W oczyszczalni biologicznej (II stopień oczyszczania) wykorzystywane są procesy podobne do tych które zachodzą w sposób naturalny w przyrodzie przy współudziale mikroorganizmów w trakcie samooczyszczania się wód.
Biologiczne oczyszczanie ścieków prowadzone może być w warunkach:
Tlenowych
Niedotlenienia
Beztlenowych (dotyczy zwykle ścieków o dużym ładunku zanieczyszczeń osadów ściekowych).
Wyjaśnić, na czym polega oczyszczanie ścieków z wykorzystaniem złóż biologicznych
Ogólna charakterystyka
Oczyszczanie ścieków materiału osadu czynnego jest jedną z najpowszechniej obecnie stosowanych metod biologicznego oczyszczania ścieków
Oczyszczanie ścieków osadem czynnym jest w zasadzie identyczny z procesem samooczyszczania się wód w rzekach czy jeziorach
Różnica polega tylko na znacznym przyśpieszeniu tego procesu w warunkach sztucznej oczyszczalni, dzięki zgromadzeniu w małej objętości ścieków bardzo dużej ilości mikroorganizmów
Osad czynny - zespół mikroorganizmów tlenowych tworzy się samorzutnie w postaci kłaczkowatej zawiesiny podczas długotrwałego napowietrzania ścieków.
W skład osadu czynnego wchodzą bakterie heterotroficzne, pierwotniaki, grzyby oraz mniejsze ilości wrotków, nicieni itd.
Głównym gatunkiem umożliwiającym tworzenie się kłaczkowatej struktury osadu jest bakteria Zooglea ramigera.
W porównaniu z oczyszczaniem ścieków na złożach biologicznych, osad czynny może zapewniać zawsze wyższy stopień oczyszczania, jest pozbawiony uciążliwości zapachowej i rozwoju muszek, a jej sprawność zimą i latem jest prawie jednakowa.
Oczyszczanie ścieków metodą osadu czynnego odbywa się w:
Różnego rodzaju komorach,
Rowach cyrkulacyjnych,
Zarówno komory jak i rowy cyrkulacyjne są intensywnie napowietrzane.
W oczyszczaniu ścieków metodą osadu czynnego stosowane są różne rozwiązania techniczne. Typowy schemat technologiczny oczyszczania ścieków z wykorzystaniem osadu czynnego przedstawiono na rysunku:
Odmianą komór osadu czynnego są otwarte stawy fakultatywne (bakterie fakultatywne). Są to zbiorniki podobne do naturalnych, gdzie oczyszczanie ścieków odbywa się przez sedymentację zawiesin i ich beztlenowy przerób przez bakterie fakultatywne.
W górnej, aerobowej części stawu mineralizacja substancji organicznych następuje przy współudziale bakterii tlenowych.
Wyjaśnić zasadę oczyszczania ścieków metodą osadu czynnego, podać rozwiązania techniczne w przemyśle
Złoża biologiczne - urządzenie do biologicznego oczyszczania ścieków w warunkach tlenowych, pracujące na zasadzie przekraczania ścieków przez materiał wypełniający złoże, gdzie do oczyszczania ścieków wykorzystuje się mikroorganizmy osiadłe tworzące na wypełnieniu złoża tzw. błonę biologiczną. Złoże biologiczne jest odpowiednikiem naturalnego filtru glebowego. Podstawowa częścią każdego złoża biologicznego jest wypełnienie, w postaci kamieni polnych, tłucznia granitowego, żużla lub innego materiału na którym rośnie błona biologiczna. Złoże jest ułożone na ruszcie tak, aby do złoża możliwy był swobodny dostęp powietrza. Złoża zrasza się od góry ściekami za pomocą obrotowego zraszacza.
Elementy tworzące wypełnienie złoża po kilku tygodniach wpracowywania (zraszania) pokrywają się śluzowatą warstwą, w której przebiega proces oczyszczania. Warstwa ta zwana błoną biologiczną zasiedlana jest przez bakterie, grzyby, glony, pierwotniaki (wiciowce, orzęski), wrotki, nicienie i inne. Organizmy te absorbują zawarte w ściekach i następnie rozkładają je.
Błona osiąga grubość 2-3 mm, gdyż głębiej nie przenika tlen z powietrza.
Ogólna charakterystyka wypełnienia:
Powinno zapewniać wystarczająco dużą powierzchnię do rozwoju błony biologicznej,
Powierzchnia materiału wypełniającego zależy od jego wymiarów i wzrasta, jeśli uziarnienie wypełnienia maleje 1 cm3 kruszywa o granulacji w przedziale 4-8 cm ma około 95 m2 powierzchni.
Przy zmniejszeniu wymiarów kruszywa o połowę powierzchnia wzrasta dwukrotnie.
Drobniejsze kruszywo:
Zapewnia korzystne warunki rozwoju błony biologicznej
Niekorzystne bo tlen nie dochodzi
Obecnie stosowane wypełnienia:
kształtki w postaci cylindrów o wymiarach kilku centymetrów średnicy i wysokości, np. 1 m3 wypełnienia z pierścieni Flexriga ma powierzchnię taką jak kruszywo naturalne, ok. 92 m2/m3, ale zawiera aż 97% wolnych przestrzeni do przepływu ścieków i powietrza i waży zaledwie około 30 kg.
bloki z tworzywa sztucznego o rozwiniętej falistej powierzchni. Produkowane w Polsce wypełnienie złoża o nazwie Terramix pozwala uzyskać powierzchnię około 200 m2/m3 wypełnienia.
Wysokość złoża i rodzaj wypełnienia decydują o:
Możliwości napowietrzenia złoża,
W czasie przepływu ścieków przez złoże czyli czasie kontaktu ścieków z mikroorganizmami tworzą błonę biologiczną Obciążenie hydrauliczne złóż utrzymuje się w przedziale:
dla złóż niskoobciążonych 0,05 - 0,15 m3/m2*h
dla złóż spłukiwanych powyżej 0,8, zazwyczaj do 1,5 m3/m2*h
W czasie oczyszczania ścieków w złożu biologicznym:
Substancje organiczne są częściowo bezpośrednio utleniane do prostych związków mineralnych, wody, dwutlenku węgla i azotanów
Część materii organicznej przetwarzana jest na energię
Część na budowę nowych komórek (przyrost biomasy),
Mikroorganizmy tworzące błonę biologiczną w sposób naturalny starzeją się i obumierają. Martwa część błony biologicznej może być albo bezpośrednio w złożu utleniana (autooksydacja) lub unoszona wraz z odpływającymi ściekami.
Proporcje między utlenianiem substancji a przyrostem błony mówimy o złożach:
Niskoobciążonych - złoża zraszane
Średnioobciążonych - złoża na przemian pracujące
Wysokoobciążonych - złoża spłukiwane
Bardzo wysokoobciążonych, np. złoża wieżowe
Ścieki kierowane na złoża muszą być poddane wcześniej oczyszczaniu mechanicznemu. Oczyszczanie mechaniczne obniża stężenie ścieków dopływających, wyrażone w BZT5.
Zalecane jest, aby ścieki dopływające do złoża miały BZT5 poniżej 20 mg tlenu/ l.
Jeśli stężenie ścieków przekroczy 200 mg tlenu/ l
Recyrkulacja ścieków na złoże, oprócz rozcieńczenia ścieków dopływających, może spełniać jeszcze inne pozytywne funkcje:
zapewnić bardziej równomierne obciążenie hydrauliczne
wzbogacić strumień ścieków w tlen i azotany
Wadami recyrkulacji są:
wyższy nakład energii na pompowanie ścieków
konieczność zwiększenia wymiarów złoża
Oprócz typowych złóż wyróżniamy złoża biologiczne:
Tarczowe
Warstwowe
Oczyszczanie ścieków z wykorzystaniem modułów membranowych
W procesie wykorzystującym technikę membranową reaktor biologiczny np. komora napowietrzania z osadem czynnym zblokowany jest z modułem w taki sposób, że strumień ścieków z komory napowietrzania przepływa w całości przez układ membranowy ultrafiltracyjny. W procesie oczyszczania ścieków wykorzystujemy technikę membranową zasada oczyszczania ścieków jest taka sama jak w oczyszczalniach konwekcyjnych z osadem czynnym, z tym, że instalacja membranowa zastępuje osadnik wtórny.
Z układu odprowadzany jest filtrat - ścieki oczyszczone, natomiast retentat - ścieki z zagęszczonym osadem czynnym wracają do komory napowietrzania. Część retentatu może cyrkulować w obiegu z pominięciem reaktora biologicznego, część odprowadzana jest jako osad nadmierny.
Oczyszczanie ścieków z wykorzystaniem modułu membranowego wykazuje szereg zalet:
Umożliwia oddzielenie całej biomasy od oczyszczanych ścieków pozwalając na znaczne zwiększenie stężenia osadu czynnego w komorze napowietrzania
Zatrzymanie na membranach całej biomasy umożliwia rozwój wolno rozmnażających się bakterii, które w układach klasycznych ulegają wymywaniu
W wyniku zatrzymania w układzie cząstek zawiesiny i długiego czasu zatrzymania substancji trudno ulegających biodegradacji następuje wyraźne większe obniżenie wartości BZT5 w oczyszczanych ściekach
Eutrofizacja i jej skutki
Oczyszczone ścieki zawierające związki azotu i fosforu wprowadzone do rzeki czy jeziora powodują eutrofizację odbiornika i gwałtowny rozwój fitoplanktonu, zwłaszcza glonów.
Skutki eutrofizacji:
Rozwój fitoplanktonu doprowadza do tzw. zakwitu wody,
Biomasa glonów zaczyna stopniowo obumierać, rozpoczyna się ich rozkład,
W krótkim czasie zastaje zużyty cały tlen rozpuszczony w wodzie,
Środowisko staje się beztlenowe
Następuje beztlenowy rozpad martwej substancji organicznej i wszystkie z tym związane uciążliwości.
Aby do tego nie dopuścić konieczne jest usunięcie z oczyszczanych ścieków związków azotu i fosforu.
Wyjaśnić na czym polega biologiczne suwanie azotu ze ścieków
Wszystkie sposoby usuwania związków azotowych są komplikacją dwóch odrębnych procesów.
Nitryfikacji,
Denitryfikacji
Nitryfikacja - jest to biologiczne utlenianie amoniaku oraz soli amonowych do azotanów. Podstawowa rolę w biologicznej nitryfikacji odgrywają bakterie z rodzaju Nitrosomonas i Nitrobacter. Są to bezwzględne tlenowe bakterie autotroficzne zdobywające energię z utleniania amoniaku i azotynów. Źródłem węgla dla tych bakterii jest dwutlenek węgla.
Proces nitryfikacji przebiega w dwóch etapach:
W pierwszym jon amonowy NH4+ jest utleniany (amonifikacja) do jonu azotanowego głównie przez bakterie z rodzaju Nirtosomonas i Nitrococcus.
![]()
W drugim jon azotynowy jest utleniany do jonu azotanowego przez bakterie z rodzaju Nitrobacter
![]()
Usuwanie związków azotowych
Proces nitryfikacji charakteryzuje się znacznym zużyciem tlenu. Na 1 kg azotu amonowego ulegającego nitryfikacji zużywa się 4,6 g tlenu czyli ok. 17 m3 powietrza.
Dla porównania zapotrzebowanie tlenu do utleniania jonów Fe2+ i Mn2+ w procesie odżelaziania i odmanganiania wynosi odpowiednio 0,14 i 0,29 kg/kg.
Tak duże zapotrzebowanie tlenu sprawia, że taki proces odczyszczania ścieków jest bardzo energochłonny, ponieważ główną pozycją w strukturze zużycia energii w procesie oczyszczania ścieków jest ich napowietrzanie.
Denitryfikacja - jest to redukcja utlenionych związków azotu przez bakterie fakultatywne do produktów końcowych, którymi mogą być azot cząsteczkowy (N2) i tlenki azotu (N2O, NO) wywołana przez bakterie denitryfikacyjne (denitryfikatory).
Denitryfikacja przebiega w warunkach beztlenowych, ale w obecności azotanów V i azotanów III jako zewnętrznych akceptorów elektronów (oddychanie azotanowe). Takie warunki, w odróżnieniu od ściśle beztlenowych, w których nie ma zewnętrznych akceptorów elektronów określa się jako anoksyczne (niedotlenienia).
Warunkiem koniecznym do przebiegu procesu denitryfikacji jest:
Obecność utlenionych związków azotu (azotanów),
Nieobecność rozpuszczonego tlenu (warunki anoksyczne niedotlenienia),
Obecność bakterii fakultatywnych,
Obecność łatwo asymilowanego źródła węgla
Jako źródło węgla organicznego w procesie denitryfikacji mogą być wykorzystywane łatwo rozkładalne związki organiczne takie jak: kwas octowy, glukoza, sacharoza. Najczęściej wykorzystywane są substancje zawarte w ściekach surowych doprowadzane do komór oczyszczania ścieków, a także zmagazynowane substancje wewnątrzkomórkowe. Intensywność przebiegu procesu denitryfikacji zależy od temperatury oraz rodzaju dostępnego substratu (źródła węgla organicznego).
W technicznych rozwiązaniach urządzeń nitryfikacji i denitryfikacji uzyskuje się przez:
Zastosowanie odrębnych komór - reduktorów do nitryfikacji i denitryfikacji,
Utworzenie odrębnych stref tlenowych i anoksycznych w jednym urządzeniu,
Za pomocą rozdzielacza procesów nitryfikacji i denitryfikacji w czasie
Wyjaśnić na czym polega biologiczne usuwanie fosforu ze ścieków
Usuwanie związków fosforowych
Fosfor zawarty w ściekach występuje głównie w postaci ortofosforanów i fosforanu organicznego. Fosfor jest główną substancją powodującą eutrofizację wód i dlatego zgodnie z przepisami musi być usuwany ze ścieków do określonego poziomu. Wykorzystane procesów biologicznych do likwidacji drugiego pierwiastka biogennego jakim jest fosfor wprowadzane jest dopiero w ostatnich latach.
Do niedawna jednymi skutecznymi sposobami usuwania związków fosforu ze ścieków były metody fizyko-chemiczne, polegające na wytrąceniu (nierozpuszczalnych) fosforanów V wapnia.
Do usuwania fosforu wykorzystywane były:
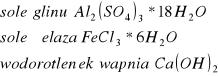
Strącany był CaHPO4 * 2H2O, który przechodził w formę apatytową: Ca3(PO4)2.
W biologicznej metodzie proces defosfatacji polega na wykorzystaniu zjawiska nadmiernej akumulacji fosforanów w specyficznych warunkach przez określone szczepy bakterii z rodzaju Acinetobacterium. Praktyczny sposób wzbogacania biocenozy w bakterie Acinetobacter i inne zdolne do akumulacji polifosforanów to okresowe wytwarzanie środowiska beztlenowego, a następnie warunków tlenowych.
Usuwanie związków fosforowych następuje w dwóch strefach bioreaktora: beztlenowej i tlenowej.
W warunkach beztlenowych przy dużej obfitości składników odżywczych bakterie fosforowe np. Acinetobacter zużywają część nagromadzonych wcześniej polisacharydów jako źródło energii do wchłaniania łatwo rozkładalnych substratów. Dochodzi przy tym do zwrotnego wydzielania fosforu do otoczenia.
W fazie aerobowej mikroorganizmy magazynują polifosforany ze zwiększoną intensywnością w ilości przewyższającej pierwotne ich rozpuszczone formy.
Fosfor zakumulowany w komórkach bakterii w postaci osadu opada na dno osadnika wtórnego, gdzie ścieki są kierowane z bioreaktora. Część osadu jest zwracana do strefy beztlenowej bioreaktora w celu utrzymania wysokiej koncentracji bakterii fosforowych. Pozostała część (osad nadmierny) kierowana jest do dalszej przeróbki w komorach fermentacji beztlenowej.
Osady ściekowe, ich obróbka i zagospodarowanie
Osady oddzielone od ścieków surowych w osadnikach wstępnych oraz osady nadmierne powstające w trakcie biologicznego tlenowego oczyszczania ścieków po wydzieleniu w osadnikach wtórnych przechodzą zwykle dalszą obróbkę na terenie oczyszczalni.
Osady różnią się między sobą znacznie zapachem, wyglądem, zawartością wody, zdolnością do odwadniania, strukturą ciał stałych oraz składem chemicznym. Osady zawierają zwykle ponad 75% wody i są uważane za płynne.
W celu zmniejszenia ilości osadów organicznych i łatwiejszego ich zagospodarowania poddaje się je fermentacji beztlenowej (metanowej). Przefermentowany osad zajmuje dużo mniejszą objętość niż osad świeży. Osad przefermentowany nie gnije, łatwo i stosunkowo szybko wysycha. W oczyszczalniach w przemyśle spożywczym przefermentowany osad często suszony jest na specjalnych poletkach.
Poletko wykonane jest w płytkim wykopie, zdrenowane. Dreny zasypane warstwą żwiru i położone płyty.
Osad - nawóz organiczny nie brudzi, nie ma zapachu. Poletka pokrywane są warstwą przefermentowanego osadu o grubości 20-30 cm.
Osad odwadniany jest i wysycha w ciągu kilkunastu dni. Wysychając osad pęka i przyjmuje strukturę gąbczastą dzięki obecności pęcherzyków gazu znajdującego się w nim w chwili wypuszczenia z komory fermentacyjnej. Odwadnianie osadów ściekowych prowadzi się ponadto za pomocą pas taśmowych, filtrów próżniowych, wirówek i innych urządzeń.
Zagospodarowanie osadów może być różne:
Mogą być bez przeszkód wykorzystywane rolniczo
We własnym zakresie przez zakłady przemysłu spożywczego np. do niwelacji terenu
Wykorzystanie jako paliwo energetyczne
Wykorzystanie jako dodatku porotwórczego do surowcowej keramzytu.
Keramzyt - jest to sztuczne kruszywo lekkie otrzymywane przez wypalanie naturalnego surowca - gliny pęczniejącej w temperaturze 1100 - 12000C. kruszywo to stosowane jest powszechnie do produkcji betonu lekkiego wykorzystywanego m. in. do produkcji pustaków stropowych. Wykorzystywane jest także jako podłoże w uprawach hydroponicznych.
Beztlenowe oczyszczanie ścieków
Beztlenowe oczyszczanie ścieków
W przemyśle spożywczym wykorzystanie beztlenowego rozkładu substancji organicznych w procesie oczyszczania ścieków jest szczególnie uzasadnione przy dużych stężeniach zanieczyszczenia ścieków.
Wydajność fermentacji metanowej w m3 biogazu/ kg substancji fermentowanej
Tłuszcze 1,250
Skrobia 0,825
Inne węglowodany 0,79
Białka 0,704
Pomiędzy procesami rozkładu tlenowego i beztlenowego występuje wiele różnic:
Czas trwania procesu beztlenowego jest wielokrotnie dłuższy
Możliwy do uzyskania stopień rozkładu substancji organicznych w warunkach beztlenowych jest znacznie niższy, co oznacza, że np. ścieki oczyszczone w procesie beztlenowym nie spełniają warunków rozporządzenia o odprowadzeniu ścieków do odbiornika
Produkty rozpadu beztlenowego mają bardzo uciążliwy nieprzyjemny zapach, co narzuca konieczność prowadzenia procesu w urządzeniach zamkniętych . Uciążliwość ta nie występuje przy rozkładzie tlenowym.
Wyszukiwarka
Podobne podstrony:
ekologia i zarządzenie środowiskowe plśl opracowane pytania
EKOLOGIA MIROSŁAWSKI OPRACOWANE PYTANIA
Ekologia - opracowane pytania, SGGW - Technologia żywnosci, VI SEEMSTR, Semestr VI, ekologia
Ekologia opracowane pytania
Pytania na ekologie - opracowane, OPRACOWANE PYTANIA NA EKOLOGIĘ
elologia opracowane pytania, Studia SGGW, WNoŻ Inżynierskie 2008-2012, Sem VI, ekologia
Marketing Opracowane Pytania Egzaminacyjne 2009 Furtak (46)
testy spalanie, Politechnika Wrocławska Energetyka, IV semestr, Spalanie i paliwa, spalanie i paliwa
opracowane pytania z I egz 2009 1, Studia, III rok, Gospodarka Nieruchomosciami, testy GN
Logistyka globalna i transportowa opracowane pytania! 06 2009
KOLO KONWERSJA PYTANIA opracowane, PWr W9 Energetyka stopień inż, V Semestr, Konwersja energii, WYKŁ
teoria Sportu - Opracowane Pytania Egzaminacyjne 3 rok 2008-2009, Teoria sportu
ściąga alfabetycznie, PWr W9 Energetyka stopień inż, III Semestr, Spalanie i paliwa, Opracowane pyta
Marketing Opracowane Pytania Egzaminacyjne 2009 Furtak (46)
haran egzamin opracowane pytania
Opracowane pytania BiUD
prawo opracowane pytania egzamin id 3
więcej podobnych podstron