skanuj0004
60
II. Chemiczne i fizykochemiczne metody rozdzielania
V
/
6. Neutralizacja
61
dopływ
odpływ
CO,
|
—1 0 0 0 0 |
/O"" —_____ 6 flr-----; — — | |
|
i |
Li \ |
oooo |
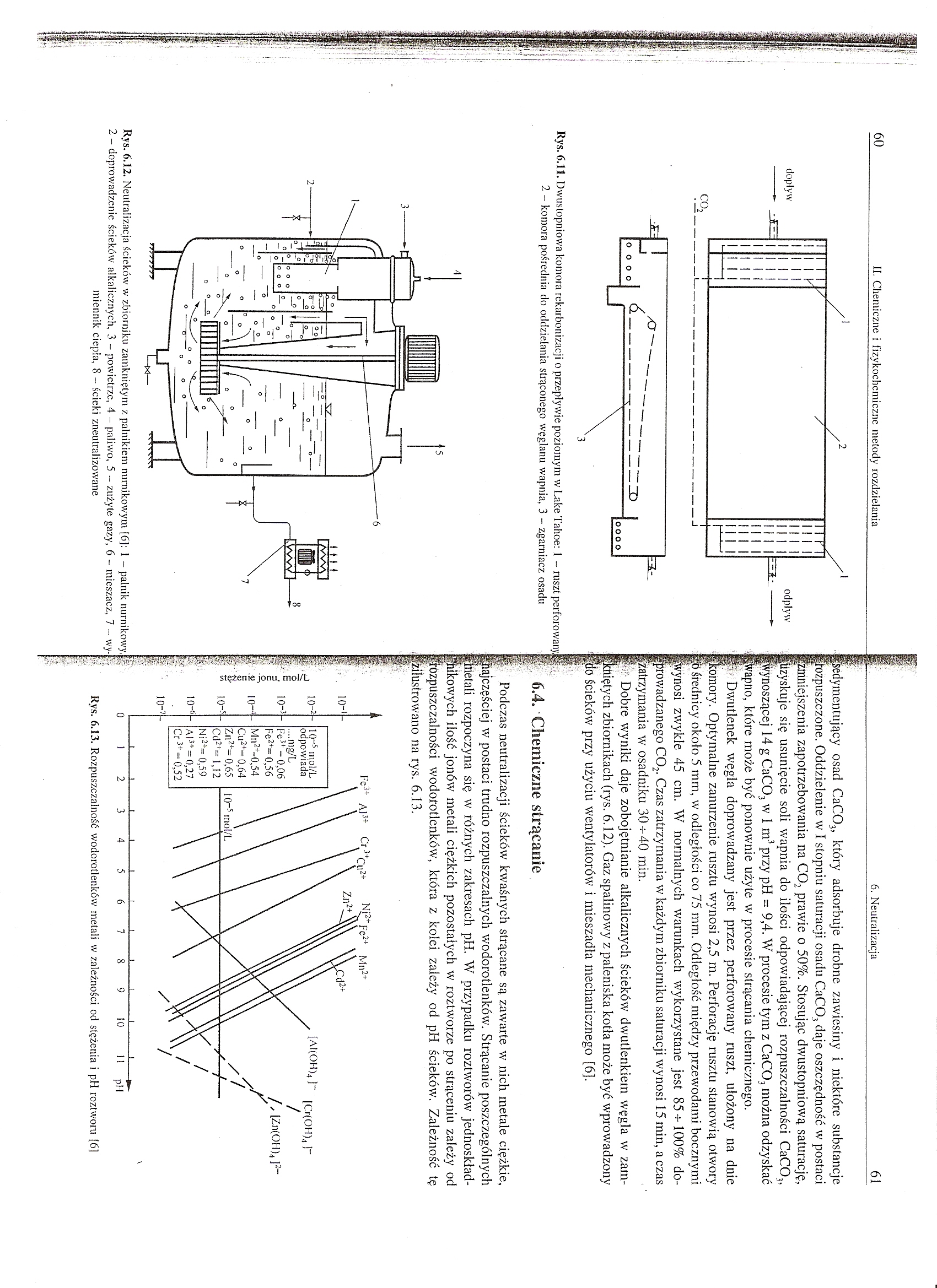
Rys. 6.11. Dwustopniowa komora rekarbonizacji o przepływie poziomym w Lakę Tahoe: 1 - ruszt perforowany] 2 - komora pośrednia do oddzielania strąconego węglanu wapnia, 3 - zgarniacz osadu
sćdymentujący osad CaC03, który adsorbuje drobne zawiesiny i niektóre substancje Rozpuszczone. Oddzielenie w I stopniu saturacji osadu CaC03 daje oszczędność w postaci itiiniejszenia zapotrzebowania na C02 prawie o 50%. Stosując dwustopniową saturację, jiżyskuje się usunięcie soli wapnia do ilości odpowiadającej rozpuszczalności CaC03, wynoszącej 14 g CaC03 w 1 m3 przy pH = 9,4. W procesie tym z CaC03 można odzyskać Wapno, które może być ponownie użyte w procesie strącania chemicznego.
|> Dwutlenek węgla doprowadzany jest przez perforowany ruszt, ułożony na dnie jtomory. Optymalne zanurzenie rusztu wynosi 2,5 m. Perforację rusztu stanowią otwory p średnicy około 5 mm, w odległości co 75 mm. Odległość między przewodami bocznymi wynosi zwykle 45 cm. W normalnych warunkach wykorzystane jest 85-?-100% doprowadzanego C02. Czas zatrzymania w każdym zbiorniku saturacji wynosi 15 min, a czas zatrzymania w osadniku 30^-40 min.
1 Dobre wyniki daje zobojętnianie alkalicznych ścieków dwutlenkiem węgla w zam-iętych zbiornikach (rys. 6.12). Gaz spalinowy z paleniska koda może być wprowadzony Pd ścieków przy użyciu wentylatorów i mieszadła mechanicznego [6].

Rys. 6.12. Neutralizacja ścieków w zbiorniku zamkniętym z palnikiem nurnikowym 16]: 1 - palnik nurnikowy, 2 - doprowadzenie ścieków alkalicznych, 3 - powietrze, 4 - paliwo, 5 — zużyte gazy, 6 - mieszacz, 7 — wymiennik ciepła, 8 - ścieki zneutralizowane
yyyy
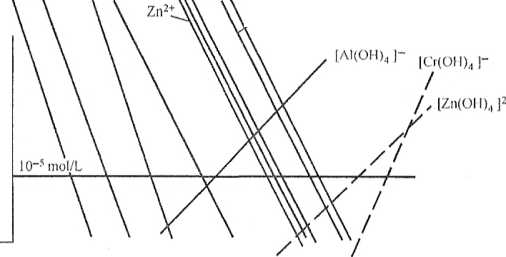
Podczas neutralizacji ścieków kwaśnych strącane są zawarte w nich metale ciężkie, Najczęściej w postaci trudno rozpuszczalnych wodorotlenków. Strącanie poszczególnych iletali rozpoczyna się w różnych zakresach pH. W przypadku roztworów jednoskład-ikowych ilość jonów metali ciężkich pozostałych w roztworze po strąceniu zależy od (rozpuszczalności wodorotlenków, która z kolei zależy od pH ścieków. Zależność tę zilustrowano na rys. 6.13.
Fe3+ Ąl3+ Crt3+C(J2+ N^pe2+ Mn2+
JZ d2+
10“5 moI/L odpowiada ....mg/L Fe3+ = 0,06 Fe2+= 0,56 Mn2+=0,54 Cu2+= 0,64 Zn2+= 0,65 Cd2+= 1,12 Ni2+= 0,59 AI3+ = 0,27 Cr3+ = 0,52
0 1 2 34 5 6789 10 11 pH
Rys. 6.13. Rozpuszczalność wodorotlenków metali w zależności od stężenia i pH roztworu [6]
Wyszukiwarka
Podobne podstrony:
skanuj0002 56 11. Chemiczne i fizykochemiczne metody rozdzielania Rys. 6.8. System automatycznego da
52 II. Chemiczne i fizykochemiczne metody rozdzielania 6. Neutralizacja53 Tabela 6.1. Zużycie reagen
skanuj0002 56 11. Chemiczne i fizykochemiczne metody rozdzielania Rys. 6.8. System automatycznego da
skanuj0003 58 II. Chemiczne i fizykochemiczne melody rozdzielania Złoże magnezytowe, lub z tlenkiem
skanuj0051 (60) Rozdział IV - Elementy składowe dokumentu Gdy chcemy zmienić położenie pola tekstowe
skanuj0001 (507) i ii, i. * d. StcKcczie 16- Które metody sa stosowane u dzieci z
więcej podobnych podstron