skanowanie0025
www.wsip.pl '5 ** -j
|
1 |
2 |
3 |
|
6 |
P |
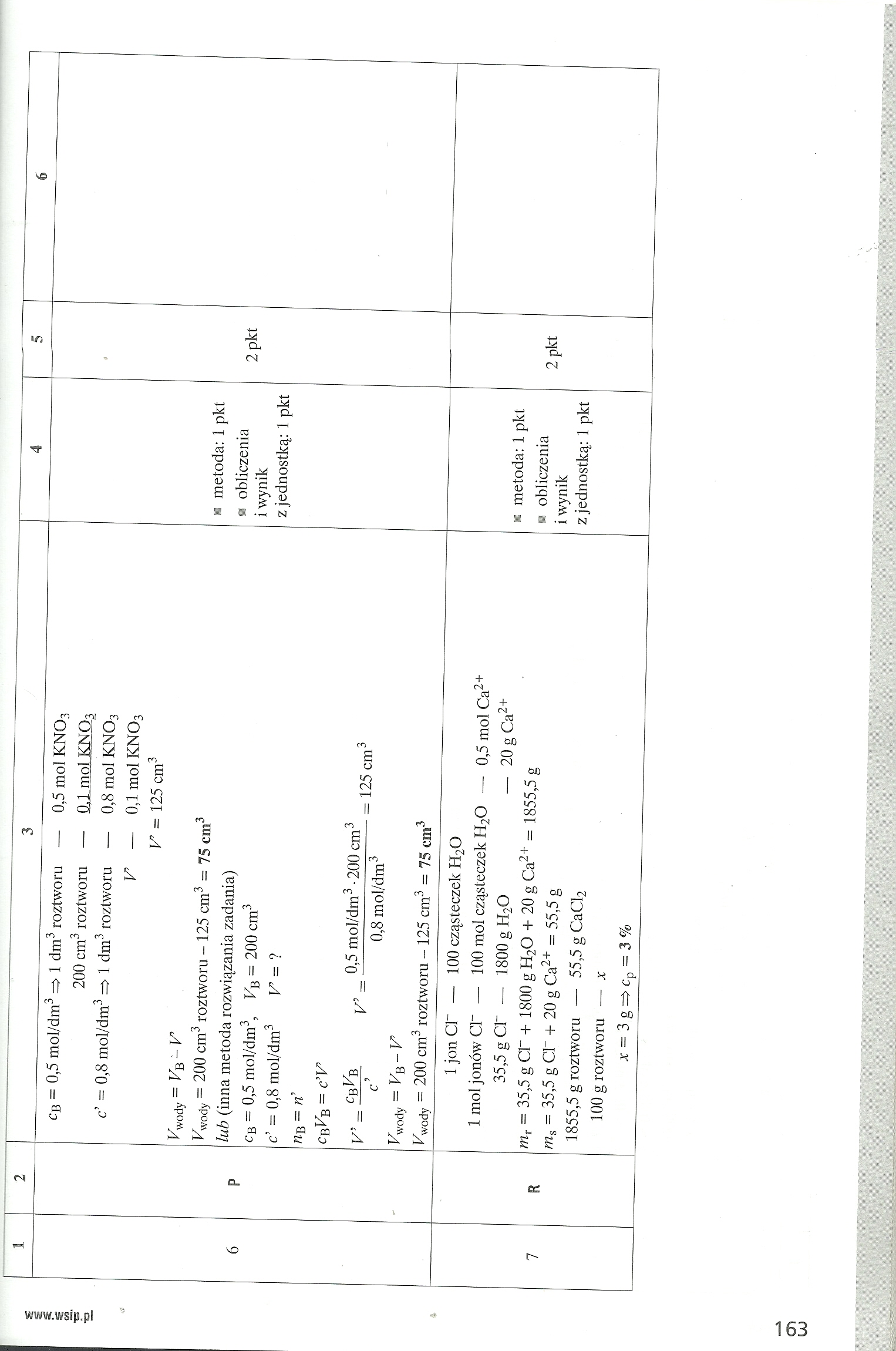
CB ~ 0,5 mol/dm3 => 1 dm3 roztworu — 0,5 mol KN03 200 cm3 roztworu — 0.1 mol c’ = 0,8 mol/dm3 => 1 dm3 roztworu — 0,8 mol KN03 V — 0,1 mol KN03 V = 125 cm3 ^wody “ l^B ~ I'” K/ody = 200 cm3 roztworu -125 cm3 = 75 cm3 lub (inna metoda rozwiązania zadania) cb = 0,5 mol/dm3, VB = 200 cm3 o* = 0,8 mol/dm3 V = ? nB = n’ cBVB m c'V yi __ cBVB v, _ 0,5 mol/dm3 • 200 cm3 ^ ^ c’ 0,8 mol/dm3 ^wody = VB - V ^wody “ 200 cm3 roztworu -125 cm3 = 75 cm3 |
|
7 |
R |
1 jon Cl“ — 100 cząsteczek H2O 1 mol jonów Cl" — 100 mol cząsteczek H2O — 0,5 mol Ca2+ 35,5 g Cl" — 1800 gH20 — 20gCa2+ mt = 35,5 g Q“ + 1800 g H20 + 20 g Ca2+ = 1855,5 g ms = 35,5 g OT + 20 g Ca2+ = 55,5 g 1855,5 g roztworu — 55,5gCaC32 100 g roztworu — x x = 3g=>cp = 3% |
|
4 |
5 |
6 | |
|
■ metoda: 1 pkt ■ obliczenia i wynik z jednostką: 1 pkt |
2 pkt | ||
|
■ metoda: 1 pkt ■ obliczenia i wynik z jednostką: 1 pkt |
2 pkt |
Wyszukiwarka
Podobne podstrony:
skanowanie0024 3 www.wsip.pl 1 2 3 4 5 6 3.1 P lmolHCl — 22,4 dm3 x — 0,314 dm3 x = 0,014 mo
skanowanie0015 www.wsip.pl 1 2 3 25.1 R 2 H20 —► 02 + 4e“ + 4H+ 25.2 R 2 mol e" — 1 mol H2
skanowanie0041 2 1 www.wsip.pl
skanowanie0043 www.wsip.pl 4 5 6 każdy wzór: 1 pkt 3 pkt 1 pkt ■ Reakcja ta będzie zachodzi
skanowanie0014 »ww.wsip.pl l • 3 4 5 6 15.1 R Mn + 2 Ag+ -> 2 Ag + Miir+ 1 pkt 3 pkt *
skanowanie0033(1) www.wsip.pl11.1 barwa bladozielona: Fe2+ barwa brunatna (żółta): Fe3+ 1
skanowanie0024(1) Szlifuj swój angielski - www.ang.pl http://www. ang.pl/future_simpie.
hpqscan0020 a) 10”3(b) A O"11 c) 10 9 d) 10 14 mol/dm3 130. pł^rpztworu wodne
http://www.wsip.com.pl/serwisy/mmm/archiwum/potatol0/test6_2.htm Uczniowie rozwiązują zadania w
33266 skanowanie0028 URSA Polska Sp. z o.o. ul. Armii Krajowej 12 42-520 Dąbrowa Górnicza
SMARTTECH 3D~ www.skaner3d.pl Rysunek 2.1 Proces skanowania Wynikiem pojedynczego skanowania jest ch
www.conrad.pl&NRMJ 1. Źródło - Funkcja pozwala na określenie metody skanowania obrazów. -
Onimo www.conrad.pl[Active Frame Setting] Krok 5 - Skanowanie Wybierz ,Zeskanuj klatkę (Scan Curren
FORUm inTERnETOUJE15 min Uruchom kreskówkę pt. „Forum" z serwisu www.sieciaki.pl
Uruchom kreskówkę pt. Czat http://www.sieciaki.pl/sieciotv/11, kreskówki, 3/id/ 57 Wiemy już, czym j
dr Jarosław Ruszewski dr Piotr Sitniewski www.jawnosc.pl Ustawa o dostęp do
więcej podobnych podstron