Wykład 1 (1)
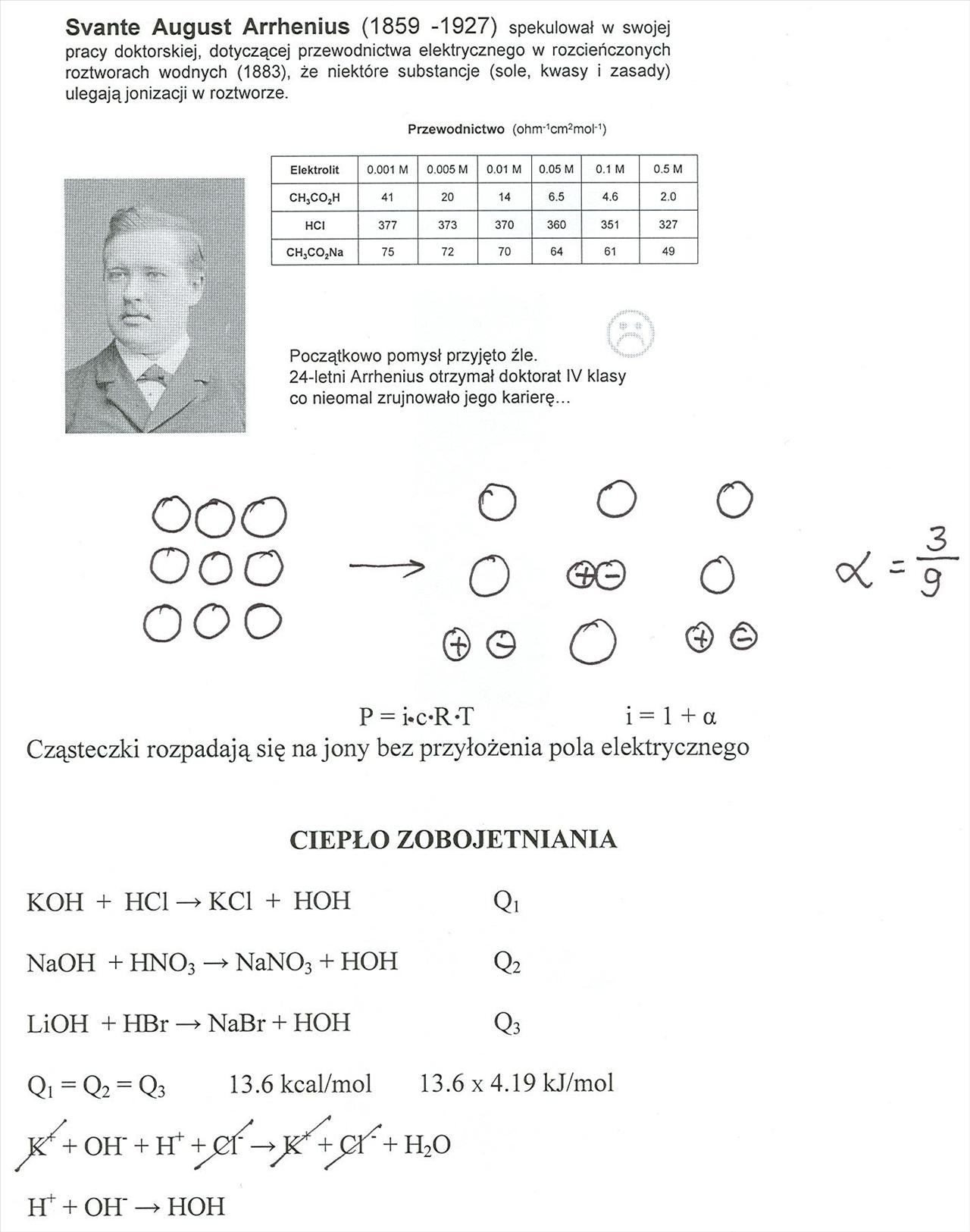
Svante August Arrhenius (1859 -1927) spekulował w swojej
pracy doktorskiej, dotyczącej przewodnictwa elektrycznego w rozcieńczonych roztworach wodnych (1883), że niektóre substancje (sole, kwasy i zasady) ulegają jonizacji w roztworze.
Przewodnictwo (ohnr1cm2mol*1)
|
Elektrolit |
0.001 M |
0.005 M |
0.01 M |
0.05 M |
0.1 M |
0.5 M |
|
ch3co2h |
41 |
20 |
14 |
6.5 |
4.6 |
2.0 |
|
HCI |
377 |
373 |
370 |
360 |
351 |
327 |
|
CH3C02Na |
75 |
72 |
70 |
64 |
61 |
49 |
♦»* 'ft f iii ii i
\ j

Początkowo pomysł przyjęto źle.
24-letni Arrhenius otrzymał doktorat IV klasy co nieomal zrujnowało jego karierę...
|
O |
o |
O |
|
0 |
©0 |
O oC |
|
© © |
o |
© © |
CM
ooo
ooo
ooo
i = 1 + a
P = i-c-R-T
Cząsteczki rozpadają się na jony bez przyłożenia pola elektrycznego
CIEPŁO ZOBOJĘTNIANIA
|
KOH + HCI -> |
KC1 + HOH |
Qi |
|
NaOH + HN03 |
NaN03 + HOH |
q2 |
|
LiOH + HBr -> |
NaBr + HOH |
q3 |
|
Qi = Qź = Qs |
13.6 kcal/mol |
13.6 x 4.19 kJ/mol |
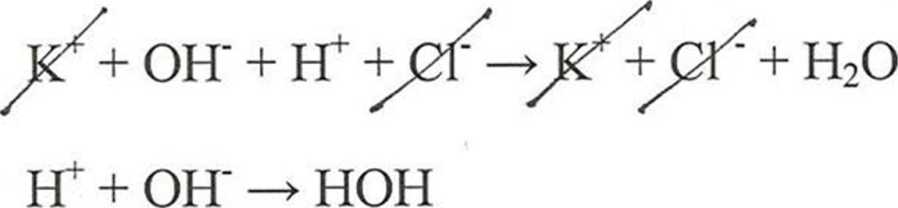
Wyszukiwarka
Podobne podstrony:
DSC01737 Svante August Arrhenius (1859 -1927) spekulował w swojej pracy doktorskiej, dotyczącej prze
Wykład 12 - ELEKTROLITY, KWASY, ZASADY I SOLE Svante August Arrhenius (1859-1927) Nobel 1903 c Praca
Svante August Arrhenius (1859 - 1927)*Kwasy - zasady Niektóre roztwory mają charakterystyczne cechy:
mgr Jerzy Pietraszko - wykładowca matematyki na Politechnice Wrocławskiej, w swojej pracy dokto
Historia myśli psychologicznej wykład 4 Prof. Bobryk str. 2 Kiedy Twardowski miał w swojej pracy wyj
Kiedy Maria rozmyślała nad tematem swojej pracy doktorskiej, Henn/ Becquerel badał dziwne właściwośc
i. Wprowadzenie W swojej pracy doktorskiej zamierzam zająć się całkowicie nowym, powstającym na nasz
więcej podobnych podstron