02 (124)

/~\ Egz_IC_.34.DCX;
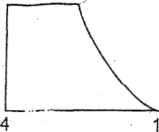
/3. Przy stwierdzeniach, odnoszących się do przedstawionego niżej schematu przemian odwracalnych I mola gazu doskona-Jłego, wpisz, które są prawdziwe, a które fałszywe:
3'/; pkt możliwe do uzyskania: po !A pkt za każdą dobrą odpowiedź, po -Yj pkt ta złą, za brak odpowiedzi 0 pkt.
a) jeśli AH,.2=0 to T3>Tf... P
b) r...££U2...t...T, _
c) 'aŚ,+.u.,>0 * .... P.ft-bSZ..........
d) AHi.2=qi.2 ..........
e) AH2.3=q2.}
0 ah,^3=ah,.2.3 ...PGi^{.E*3....
g) Wi.2-3-i<Wm JS&tdA.........
V
4. \ Wpisz, które stwierdzenia dotyczące termochemii są prawdziwe, a które fałszywe:
2 pkt możliwe do uzyskania: po Yi pkt za każdą dobrą odpowiedź, po -'A pkt za złą, za brak odpowiedzi 0 pkt.
a) standardowe molowe entalpie tworzenia siarki jednoskośnej i siarki rombowej są sobie równe ...ę~ftfck2.-...
b) standardowa entalpia pierwiastka w formie trwałej w temperaturze 298 K pod ciśnieniem standardowym zależy
od masy molowej pierwiastka
c) molowe ciepło reakcji CHł(g) + 02(g) - 2H2(g) + C02(g) pod stałym ciśnieniem jest równe molowemu ciepłu tej
reakcji w warunkach izochorycznych ....frT#Źifc&2...
d) prawo Hessa ma zastosowanie wyłącznie do entalpii standardowych w temperaturze 298K
5. Wpisz, które stwierdzenia dotyczące entropii i II zasady termodynamiki sa prawdziwe, a które fałszywe:
j 2 pkt możliwe do uzyskania: po Y: pkt za każdą dobrą odpowiedź, po -/: pkt za złą, za brak odpowiedzi 0 pkt.
a) entropia jest ekstensywną funkcją stanu
b) ciepło nigdy nie może przepływać od ciała o temperaturze niższej do ciała o temperaturze wyższej
c) entropia układu podczas przebiegającej w nim samorzutnie reakcji chemicznej może maleć ...PMsRffi
d) entropia 1 grama lodu jest mniejsza niż entropia 1 grama wody w tych samych warunkach P i T
6. Wpisz, które stwierdzenia dotyczące termodynamiki sa prawdziwe, a które fałszywe:
2 pkt możliwe do uzyskania: nie ma punktów ujemnych
a) zmiana entropii podczas reakcji CH^g) + 02(g) = 2H2(g) + C02(g) jest dodatnia
b) pojemność cieplna wody podczas topnienia pod stałym ciśnieniem, (óH/5T)p, jest nieskończenie wielka
Sb**. Cg)Wb.r5
.o) jeśli Cp(pary)< Cp(cieczy), to ze wzrostem temperatury ciepło parowania rośnie d) molowa entalpia parowania wody jest większa od molowej entalpii parowania n-pentanu
7. Entalpię (zmianę entalpii) układu często określa się jako ciepło wymieniane przez układ pod stałym ciśnieniem (pochodna (dH/dT)p=Cp). Ćzy oznacza to, że: (napisz PRAWDA lub FAŁSZ)
2 pkt możliwe do uzyskania; Yi pkt za każdą dobrą odpowiedź, —A pkt za złą, za brak odpowiedzi 0 pkt.
a) procesy przebiegające w warunkach stałej objętości nie prowadzą do zmiany entalpii układu .....
b) zmiana entalpii nigdy nie może być równa zmianie energii wewnętrznej ..frJlftfcfrZ....____
c) entalpia zmienia się w każdym procesie (poza izoentalpowymi) lecz jedynie w procesach prowadzonych w warunkach
t izobarycznych można ją utożsamić z wymienianym ciepłem
d) w procesach izoentalpowych nigdy nie dochodzi do zmiany temperatury układu .....
8. Przedstaw najprostszy dowód na konieczność istnienia temperatury zera bezwzględnego:
/ pkt możliwe do uzyskania; nie ma punktów ujemnych
r-^o °
'z&cr O S(oj » o
~5>Lx£} <*4aJbirt -
ggc>u^Q
r\
Wyszukiwarka
Podobne podstrony:
Plik:EGZ_15A_89.doc Przy stwierdzeniach, odnoszących się do przedstawionego niżej schematu przemian
02 (126) Plik I G/ ISA S i i-. 3. Przy stwierdzeniach, odnoszących się do przedsta
skanuj0006 Powodzenia! 1. Przy stwierdzeniach, odnoszących stę do przedstawionego niżej schematu prz
Zadanie 1. (o-i) Oceń prawdziwość poniższych stwierdzeń odnoszących się do przemówienia Włodzimierza
Zadanie 1. (0-1) Oceń prawdziwość poniższych stwierdzeń odnoszących się do przemówienia Włodzimierza
gielda2 str2 2 1. Które ze stwierdzeń odnoszących się do arteria circumflexa humeri anterior jest/są
więcej podobnych podstron