arkusz eII + odpowiedzi0005

O—C.H
P
II
CH,OH
III
H
OH H
H
\
H
C-C
/
C
O—CH,
H OH
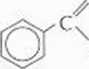
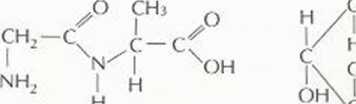
Zaznacz i nazwij występujące w nich charakterystyczne wiązania: P peplydowe, L — estrowe, G — glikozy-dowe.
Zadanie 20. (4 pkt.)
Roztwory słabych kwasów i ich soli / mocnymi zasadami (np. CH.COOH i CH.COONa w porównywalnych ilościach), a także roztwory słabych zasad i ich soli / mocnymi kwasami (np. NH, • HzO i NH4C.'I) nazywamy roztworom i buforowymi.
Roztwory buforowe mają określone stężenie jonów wodorowych, które zależy od stosunku stężeń kwasu i soli (lub zasady i soli) i które praktycznie nie ulega zmianie przy rozcieńczaniu roztworu. Niewielkie zmiany pH następują po dodaniu małych ilości mocnego kwasu lub mocnej zasady.
Bufory odgrywają ważną rolę w procesach biochemicznych zachodzących w organizmach roślinnych i zwierzęcych, są leż wykorzystywane w chemii analitycznej i w wielu procesach technologicznych.
Na przykładzie buforu octanowego, w którym zachodzą reakcjo CH.COOI ł ^OtyCOO + H*
O IjCOONa —- CH ,COO" + Na*
wyjaśnij, w jaki sposób utrzymuje on praktycznie stałe pH |x> wprowadzeniu do roztworu niewielkich ilości: a) kwasu solnego
b) zasady sodowej
Zadanie 21. (5 pkt.)
Do elektrolizera z platynowymi elektrodami wprowadzono wodny roztwór zawierający siarczan(VI) miedzi(ll), siarczan(VI) chromu(lll) i chlorek sodu. Elcktrolizer połączono ze źrórłłem prądu stałego. Określ, jakie produkty i w jakiej kolejności wydzieliły się na:
a) katodzie.................................... b) anodzie........................................
98
Wyszukiwarka
Podobne podstrony:
arkusz cI + odpowiedzi0005 Zadanie 22. (3 pkt.) Podaj nazwy i wzory sumaryczni; reagentów X, Y, Z wy
arkusz eI + odpowiedzi0005 Zadanie 18. (4 pkt.) Podaj nazwy systematyczne 1 związków: II III IV /&g
arkusz dI + odpowiedzi0005 Zadanie 19. (2 pkt.) Uzupełnij podane równania reakcji: -► CU, —CH2 —OH a
arkusz eII + odpowiedzi0003 Zadanie 12. 4 pkt.) Do czterech probówek z wodą wprowadzono następujące
arkusz eII + odpowiedzi0004 Zadanie 15. (2 pkt.) Reakcja jodometanu 7 wodorotlenkiem sodu to reakcja
arkusz bI + odpowiedzi0007 Zadanie 28. (1 pkt) Dane s<] cztery wzory pierścieniowe i łańc uchowe
arkusz aI + odpowiedzi0004 Zadanie 17. (1 pkt) Dany jest wzór sumaryczny związku: C,H,Br.. Podaj wzo
arkusz dI + odpowiedzi0006 Zadanie 23. (4 pkt.) Narysuj wzory strukturalne i podaj nazwy czterech iz
arkusz eII + odpowiedzi0002 Zadanie 7. (2 pkt.) Mieszaninę magnezu z tlenkiem krzemu(IV) podpalono.
więcej podobnych podstron