skanuj0006
REGliŁY DOTYCZĄCE WARTOŚCI IR
Reguła 1.
W szeregu homologicznym indeks retencji zwiększa się o 100 jednostek ze wzrostem łańcucha o jedną grupę CH,
Reguła Z.
Dla izomerów różniących się temperatuią wTzema o 5T„ rozdzielanych na niepolarnej fazie stacjonarnej, różnicę indeksów retencji ól opisuje równanie
6I = 5ÓT..
Reguła 3.
Indeksy retencji substancji niepolarnej są do siebie zbliżone niezależnie od rodzaju fazy stacjonarnej, na której jest rozdzielana Indeksy retencji tych samych substancji na mepolarnych fazach stacjonarnych są do siebie zbliżone
Reguła 4.
Różnica indeksów retencji substancji chiomatografowanej na polarnej i niepolarnej fazie stacjonarnej, tzw dyspersja retencji, jest charakterystyczna dla struktury substancji i można ją przewidzieć.
|
WYKORZYSTANIE REAKCJI CHEMICZNYCH >—[) Reakcja przed rozdziałem chromatograficznym | ||||
|
Na podstawie analizy przesunięć czasów' retencji pioduktów reakcji w stosunku do odpowiednich wartości dla substratów można sądzić o obecności określonych grup funkcyjnych w analizowanych związkach a niekiedy także elementów szkieletu cząsteczki (np stwierdzenie ilości i położenia wiązań wielokrotnych, obecności pierścieni) Jabpla 15.1.Odczynniki stmwanc «5r> ifcT)waD/atii łtcęanic/mch » ctinmu-UĄsrafii gizimc] i akrcr* ich | ||||
|
(łlr-niuL |
Z»iąAi ukMHc: |
/«iąAi pńthkftinc | ||
|
) ki wnet) Uidisila/an ♦ Utfnc<)k*htauMijn |
aliohnk 1- i ll-rrędowi:. fenole, potwi. ckŁją. uLiicm. k*t» karboi-Ą lowc |
odprmiodme lx urn.; • kMiiioav | ||
|
N.i kbb|lrimctyk»-Miili«|jc-.lamid |
jai wyżej. UkA: aminy |
- | ||
|
N-1 linkr.y t>r^bM4«tmb^4 |
alLuKtiac r>m lll-i #płnwv|. kwa>y tafokijink-. cuin. yullukwas;. | |||
|
Cll*l + Af(0 |
aikohfłc l-f/yiiuWC. UKtljpUl,. |
ctoymcnkmc | ||
|
liÓAmcun |
tik.***:, kanie. i* my kaihiA>yki»c |
p>.*ćlu>tlnc mci) Iow C | ||
|
UCHO w ubanoiti NoBJL lab IICOCNI |
amia> i anuł. |
v alków ita mci) bejj jimp | ||
|
Ik/modntl oilmy w pin nic |
akubok. km-k merkaptany. aminy |
pocłaidnc aod* kne | ||
WYKORZYSTANIE REAKCJI CHEMICZNYCH ż—\/ Reakcja po rozdziale chromatograficznym
Gaz nośny po opuszczeniu kolumny przepuszcza się przez roztwór odpowiedniego odczynnika w małej probówce Rezultat reakcji w postaci wytrącania osadu lub zmiany zabarwienia obserwuje się współbieżnie z ukazującymi się na chromatogranue pikami
Tabela 2. Odczynniki stosowane do identyfikacji grup funkcyjnych związków organicznych n eluacie z kolumny
|
ip |
(Kk/snnik • |
Zabarw Umie roztworu |
1yp/wi4/ku wykrywanej! |
|
i |
CtSO, |
ciemno-zółiy |
alkohole |
|
: |
2.4-1 >inilrolcny!»*h\ dra/y na |
jółty osad |
aldehydy i ketony |
|
3 |
AgNOjW etanolu |
biały osad |
halogenki alkilowe |
|
4 |
Odczynnik Schiffa: wodny fuksyn> nasycony SO; |
różowy |
aldehydy |
|
5 |
PbiCHtCOO); |
/ółty osad |
mcrkapiany. siarczki |
|
t* |
Odczynnik Hinshcrga: chlorek knMMKulfomlu w nutwnnt KOH |
pomarańczowy |
aminy 1- i II-rzędowe |
WYKORZYSTANIE POŁĄCZENIA CHROMATOGRAFII GAZOWEJ Z INNYMI METODAMI ANALITYCZNYMI
GC-MS - najbardziej uniwersalna i najczęściej stosowana metoda sprzężona
GC-FTIR - umożliwia jednoznaczną identyfikację, kiedy dysponujemy wzorcem badanej substancji Dostarcza ponadto mformacji o obecności i wzajemnym położeniu charaktery stycznych grup funkcyjnych
GC-FTIR-MS - łączy możliwości obu metod sprzężonych
GC-AES - identyfikacja związków metaloorganicznych,
próby stosowania w analizie elementarnej do wyznaczania wzorów
sumarycznych składników mieszaniny
ZASTOSOWANIE DETEKTORÓW SELEKTYWNYCH
Dw ukanałowy układ detekcji
<c
Kanał A - detektor uniwersalny (nieselektywny). np
* plomieniowo-jonizacyjny (FID)
* ciepliui-przcwodnościowy (TCD)
Kanał B - detektor selektywny, np
* termojomzacyjnv (NPD) - związki fosfóro-i azotoorganiczne
* plonueniowo-fotometryczny (FPD) - związki fosforo- i siarkoorgamcznc
* wychwytu elektronów (EC'D) - związki halogenoorgamczne
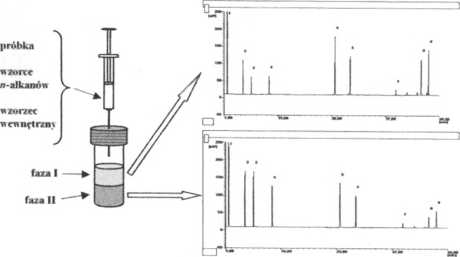
WYKONANIE ANALIZY Z PODZIAŁEM PRZEDKOLUMNOWYM
Chrom a t ogramy warstwy górnej i dolnej
Wyszukiwarka
Podobne podstrony:
73697 skanuj0007 iaz George C. Honians się przez gęstwę jeżyn. Nasze twierdzenie dotyczące wartości
14796 skanuj0052 (14) 1. Funkcje systemu politycznego: 1. Regulacyjna: Dotyczy por
69932 skanuj0005 132 George C. Homans się przez gęstwę jeżyn. Nasze twierdzenie dotyczące wartości r
skanuj0016 (112) Tablica 2: Wartości orientacyjne liniowego współczynnika sprzężenia cieplnego (ciąg
skanuj0017 (103) Tablica 2: Wartości orientacyjne liniowego współczynnika sprzężenia cieplnego (ciąg
skanuj0018 (104) 05Tablica 2: Wartości orientacyjne liniowego współczynnika sprzężenia cieplnego (ci
więcej podobnych podstron