70866 P5190006
|
Politechnika Wrocławska | |||
|
■tli] |
Laboratorium Chemii Fizycznej (1-30) |
28 | |
|
Adsorpcja | |||
|
Data /f.oę./n |
Grupa, zespćf | ||
|
jł/ci | |||
|
KoWttuum |
Kolumna , |
Stanowisko | |
Stężenie NaOH użytego do miareczkowania
A
fNłOH” mol dm 3,
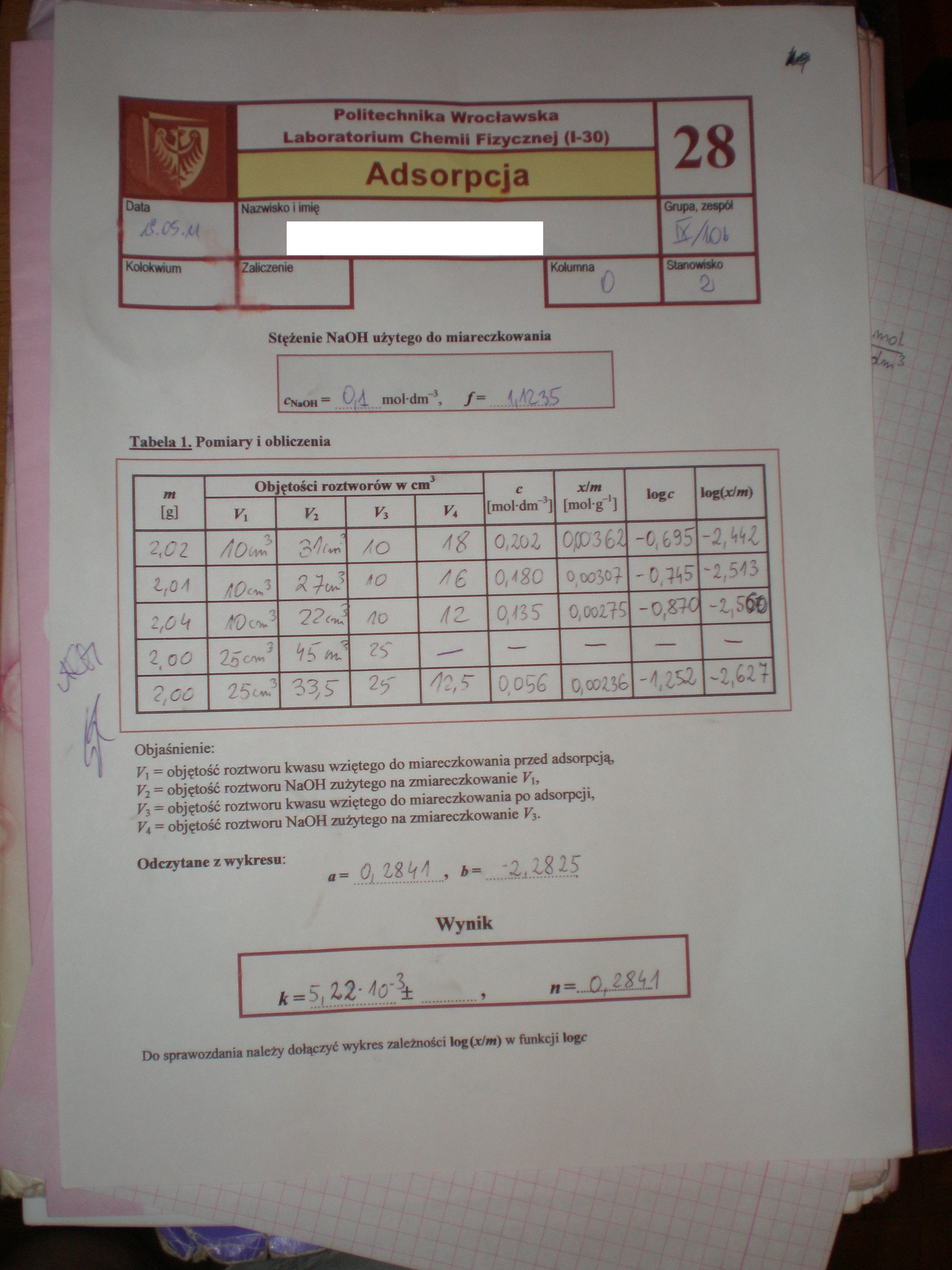
Tabela 1. Pomiary i obliczenia
|
m |
Objętości roztworów w cm3 |
1- |
t~ | |||||
|
[gj |
y,, |
Vi |
Pj |
vĄ |
[moldm 3 |
[mol-g '] |
logc |
log(x/m) |
|
2,CZ |
/tDow |
/o |
tg | |||||
|
1,0 4 |
w |
te |
0,0030? |
-0,745 |
-2,543 | |||
|
2,6 <1 |
,f9cv3 |
40 |
tz |
fopc | ||||
|
2 toO |
2S<^7 |
‘ibfyu |
— |
— |
— |
— |
— | |
|
?,CC |
33, ST |
25T |
0 |
0, oo*& |
-lisi |
( CTN <So | ||
Objaśnienie:
Pi = objętość roztworu kwasu wziętego do miareczkowania przed adsorpcją, Vi — objętość roztworu NaOH zużytego na zmiareczkowanie V,,
P3 * objętość roztworu kwasu wziętego do miareczkowania po adsorpcji,
Vą - objętość roztworu NaOH zużytego na zmiareczkowanie P3.
Odczytane z wykresu: _ _
.= oLmj*=.....
Wynik
k = 5. •
Do sprawozdani, należy dołączyć wykres zależności lot(x/m) w funkcji logc
Wyszukiwarka
Podobne podstrony:
34514 P5170008 BU Politechnika Wrocławska Laboratorium Chemii Fizycznej (1-30) 24 Stalagmometria
P4180001 $ JiOU Politechnika Wrocławska Laboratorium Chemii Fizycznej (1*30) 13 Potencjometryczny
P3240012 Data Politechnika Wrocławska Laboratorium Chemii Fizycznej (1-30)Przewodnictwo mocnych
52019 P3160001 20 20 Nazwisko I imię Zaliczenie Politechnika Wrocławska Laboratorium Chemii Fizyczne
SKRYPTY DLA SZKÓŁ WYŻSZYCH POLITECHNIKA ŁÓDZKAĆWICZENIA LABORATORYJNE Z CHEMII FIZYCZNEJ DLA STUDENT
więcej podobnych podstron